Propriétés/EffetsCode ATC
N06BA04
Mécanisme d'action/Pharmacodynamique
Le chlorhydrate de méthylphénidate est un stimulant du système nerveux central. Son mode d'action thérapeutique sur le TDAH n'est pas connu. On suppose que le méthylphénidate bloque la recapture de la noradrénaline et de la dopamine dans les neurones présynaptiques et renforce la libération de ces monoamines dans l'espace extra-neuronique. Le méthylphénidate est un mélange racémique des isomères d et l, l'isomère d étant plus actif du point de vue pharmacologique que l'isomère l.
Efficacité clinique
Études cliniques
L'efficacité du méthylphénidate dans le traitement du TDAH a été démontrée dans 4 études randomisées, en double aveugle, contrôlées contre placebo menées chez des enfants et des adolescents et dans 2 études en double aveugle, contrôlées contre placebo menées chez des adultes qui présentaient les critères d'un TDAH selon le DSM-IV.
Adultes
Deux études en double aveugle, contrôlées contre placebo, menées chez 627 adultes âgés de 18 à 65 ans ont été réalisées. En ce qui concerne les études contrôlées, il s'agissait d'une étude de titration de la dose avec groupes parallèles, multicentrique, de 7 semaines (étude 02-159) et d'une étude à dose fixe avec groupes parallèles, multicentrique, de 5 semaines (étude 3002) dans lesquelles le méthylphénidate utilisé une fois par jour (36 à 108 mg/jour ou 18, 36 et 72 mg/jour) a été comparé avec un placebo.
Dans l'étude 02-159, la variation du critère d'évaluation principal, l'échelle AISR (Adult ADHD Investigator Rating Scale; échelle destinée à l'évaluation du TDAH par l'investigateur chez l'adulte), a été évaluée à la fin de la semaine 7 chez des adultes âgés de 18 à 65 ans atteints de TDAH. Cette étude a comparé le méthylphénidate à des doses comprises entre 36 mg/jour et 108 mg/jour, et un placebo. Sur les 226 patients inclus dans cette étude de 7 semaines, 110 ont été randomisés dans le groupe traité par méthylphénidate et 116 dans le groupe placebo. La dose initiale était de 36 mg/jour, mais la dose a été augmentée par paliers de 18 mg/jour (36 à 108 mg/jour), en fonction de la survenue de certains critères d'amélioration en présence d'une tolérance acceptable. Lors de l'évaluation par l'investigateur au cours du dernier rendez-vous de l'étude, une réponse significativement meilleure au score moyen de la variation (moyenne des moindres carrés, SEM) de l'échelle AISR a été observée pour les adultes qui avaient pris du méthylphénidate, par rapport aux adultes qui avaient pris le placebo.
L'étude 3002 était une étude dose-réponse multicentrique, en double aveugle, randomisée, contrôlée contre placebo, avec groupes parallèles (durée de 5 semaines) et 3 groupes à dose fixe (18, 36 et 72 mg). Les patients chez qui un TDAH avait été diagnostiqué ont été randomisés pour recevoir soit du méthylphénidate à des doses de 18 mg (n=101), 36 mg (n=102), ou 72 mg/jour (n=102), soit un placebo (n=96). Après 5 semaines, les patients adultes des trois groupes qui avaient reçu du méthylphénidate ont présenté une réponse significativement meilleure au score global de l'échelle CAARS-SS (Conners' Adult ADHD Rating Scale – Self Report – Short Form (échelle de Conners pour l'évaluation du TDAH chez les adultes)), par rapport aux patients qui avaient pris le placebo
Adolescents
Une étude randomisée, en double aveugle, multicentrique, contrôlée contre placebo (étude 01-146) menée chez 177 patients âgés de 13 à 18 ans atteints de TDAH a évalué dans quelle mesure des améliorations peuvent être observées après un traitement par méthylphénidate à des doses allant jusqu'à 72 mg/jour (1,4 mg/kg/jour), en comparaison avec un placebo. Sur 220 patients ayant été inclus dans la phase de titration ouverte de 4 semaines, 177 patients sont passés à une dose individualisée (au maximum 72 mg/jour), selon que certains critères d'amélioration de l'échelle d'évaluation du TDAH étaient ou non satisfaits et qu'une tolérance acceptable était constatée lors de l'évaluation globale de l'efficacité. Les patients qui remplissaient ces critères ont ensuite été randomisés pour recevoir leur dose individualisée de méthylphénidate (18-72 mg/jour, n=87) ou le placebo (n=90) durant une phase en double aveugle de deux semaines. À la fin de cette phase, les scores moyens de l'évaluation par l'investigateur obtenus sur l'échelle de l'évaluation du TDAH présentaient des résultats significativement meilleurs pour les adolescents qui avaient pris du méthylphénidate que pour ceux qui avaient pris le placebo.
Enfants
Trois études en double aveugle, contrôlées contre principe actif et placebo, ont été réalisées chez 416 enfants âgés de 6 à 12 ans. Dans les études contrôlées, le méthylphénidate utilisé une fois par jour (18, 36 ou 54 mg), le méthylphénidate utilisé trois fois par jour sur une période de 12 heures (dose journalière totale: 15, 30 ou 45 mg) et un placebo ont été comparés dans deux études croisées monocentriques de 3 semaines (études C-98-003 et C-97-025) et dans une étude comparative en groupes parallèles, multicentrique, de 4 semaines (étude C-98-005). Les trois études étaient conçues de façon à démontrer une supériorité du méthylphénidate par rapport au placebo.
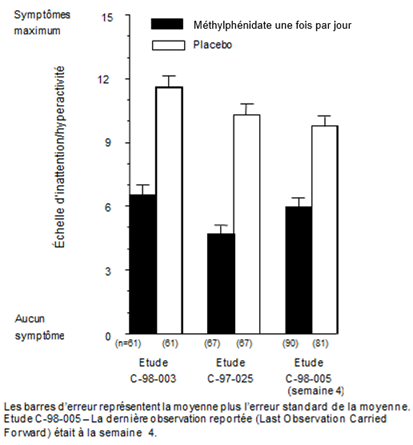
Dans les études C-98-003, C-97-025 et C-98-005, les symptômes de TDAH ont été évalués par les enseignants à l'aide de l'échelle de Conners pour l'inattention/hyperactivité avec agression (IOWA). Dans les trois études contrôlées, les enfants qui avaient reçu du méthylphénidate présentaient unanimement un classement significativement meilleur au niveau de la sous-échelle inattention/hyperactivité en comparaison avec le placebo. Les valeurs pour le méthylphénidate et le placebo des trois études sont illustrées dans la figure 1.
Figure 1. Evaluation moyenne de l'inattention/hyperactivité des enfants par leur enseignant au moyen de l'échelle de Conners pour l'IOWA lors de l'utilisation du méthylphénidate
|
