Propriétés/EffetsCode ATC: J05AX18
Prevymis est un médicament antiviral contre le CMV.
Mécanisme d'action
Le letermovir est un médicament antiviral contre le CMV.
Le letermovir inhibe le complexe terminase de l'ADN du CMV qui indispensable à la réplication virale. Les analyses biochimiques et électromiscroscopiques ont montré que le letermovir affecte la formation d'unités génomiques de longueur adéquate et interfère avec la maturation des virions.
Activité antivirale
Dans un modèle d'infection en culture cellulaire, la CE50 médiane du letermovir contre un ensemble d'isolats du CMV obtenus en clinique a été de 2,1 nM (intervalle 0,7 nM à 6,1 nM; n = 74).
Résistance virale
En culture cellulaire
Les gènes UL56 et UL89 du CMV codent des sous-unités de l'ADN terminase du CMV. Des CMV mutants présentant une sensibilité réduite au letermovir ont été sélectionnés en culture cellulaire. Les mutations correspondent au gène UL56 et affectent les acides aminés situés entre les positions 231 et 369 (V231A, V231L, V236L, V236M, E237D, L241P, T244K, T244R, L257I, F261C, F261L, F261S, Y321C, C325F, C325R, C325Y, M329T, R369G, R369M, R369S). En présence de ces mutations, la CE50 est 13 à 5870 fois plus élevée que pour les virus de référence de type sauvage. Il n'y a pas de mutation de résistance connue au letermovir liée au gène UL89.
Dans les études cliniques
Dans une étude de phase 2b évaluant des doses de letermovir de 60, 120 ou 240 mg/jour vs placebo sur une période allant jusqu'à 84 jours chez 131 receveurs de GCSH, une analyse de la séquence d'ADN d'une région choisie du gène UL56 (acides aminés 231 à 369) a été réalisée sur des échantillons obtenus auprès de 12 patients traités par letermovir. Ces patients avaient été en échec prophylactique et leurs prélèvements étaient disponibles pour analyse. Un participant de l'étude (qui avait reçu 60 mg/jour) a présenté un variant génotypique (VG) résistant au letermovir (V236M).
Dans une étude de phase 3 (P001), une analyse de la séquence d'ADN de l'ensemble des régions codantes des gènes UL56 et UL89 a été réalisée sur des échantillons obtenus auprès de 22 patients traités par letermovir dans la population en full analysis set. Ces patients avaient été en échec prophylactique et leurs prélèvements étaient disponibles pour analyse. Un patient a présenté un VG résistant au letermovir (V236M).
Résistance croisée
Une résistance croisée avec un médicament d'une autre classe est peu probable. Le letermovir est pleinement actif contre les populations virales porteuses de substitutions conférant une résistance aux inhibiteurs de la polymérase de l'ADN du CMV (ganciclovir, cidofovir et foscarnet). Ces inhibiteurs de la polymérase de l'ADN sont pleinement actifs contre les populations virales porteuses de substitutions conférant une résistance au letermovir.
Pharmacogénomique
L'impact de mutations affectant le gène OATP1B1 sur la pharmacocinétique du letermovir a été étudié sur 299 participants des études cliniques. Il s'agit des variants SLCO1B1 (rs4149056, rs2306283, rs4149032) et UGT1A1 (rs4148323 et mutation des répétitions du TA dans le promoteur). Ces variants n'ont pas donné lieu à des effets cliniquement significatifs en termes d'exposition au letermovir.
Électrophysiologie cardiaque
L'effet du letermovir sur l'intervalle QTc à des doses allant jusqu'à 960 mg administrées par voie i.v. a été évalué sur 38 sujets sains dans une étude de durée de QT randomisée, en dose unique, contrôlée versus placebo et comparateur actif (moxifloxacine 400 mg par voie orale), avec essai croisé à quatre séquences. Le letermovir ne provoque pas d'allongement cliniquement significatif de l'intervalle QTc après l'administration d'une dose de 960 mg par voie i.v., ce qui correspond à des concentrations plasmatiques environ 2 fois supérieures à celles de la dose i.v. de 480 mg.
Efficacité clinique et sécurité
Adultes séropositifs au CMV receveurs [R+] d'une greffe allogénique de cellules souches hématopoïétiques
Afin d'évaluer la capacité prophylactique du letermovir dans le cadre d'une stratégie préventive contre l'infection ou la maladie à CMV, l'efficacité du letermovir a été examinée dans une étude de phase 3 (P001) multicentrique en double aveugle, contrôlé versus placebo chez des adultes séropositifs au CMV receveurs [R+] d'une GCSH allogénique. Les sujets ont été randomisés (2:1) pour recevoir soit le letermovir soit le placebo. La randomisation a été stratifiée en fonction du centre d'étude et du risque de réactivation du CMV (élevé versus faible) à l'inclusion. Le letermovir a été initié après la GCSH (jours 0 - 28 post-greffe) et poursuivi jusqu'à la semaine 14 post-greffe. Le letermovir a été administré soit par voie orale soit par voie i.v. Le suivi des patients a été centré sur le critère principal d'efficacité jusqu'à la semaine 24 post-greffe. La surveillance s'est poursuivie en continu ensuite jusqu'à la semaine 48 post-greffe.
Parmi les 565 patients traités, 373 ont reçu le letermovir (dont 99 qui ont reçu au moins une dose i.v.) et 192 ont reçu le placebo (dont 48 qui ont reçu au moins une dose i.v.). Le délai médian avant instauration du letermovir a été de 9 jours après la greffe. Au début de l'étude, 37% des patients présentaient une prise de la greffe (engraftment). L'âge médian était de 54 ans (intervalle de 18 à 78 ans). Au début de l'étude, 50% des patients recevaient un traitement myéloablatif, 52% de la ciclosporine et 42% du tacrolimus. Les motifs de greffe les plus fréquents étaient la leucémie myéloïde aiguë (38%), le syndrome myéloblastique (15%) et le lymphome (13%). Au début de l'étude, 12% des patients étaient positifs à l'ADN du CMV.
Au début de l'étude, 31% des patients étaient à haut risque de réactivation tel que défini par un ou plusieurs des critères suivants: donneur HLA (Human Leukocyte Antigen) apparenté (frère/sœur) avec au moins une incompatibilité sur l'un des trois loci suivants des gènes HLA: donneur HLA-A, B ou DR; donneur haplo-identique; donneur non apparenté avec au moins une incompatibilité sur l'un des quatre loci suivants des gènes HLA: HLA-A, B, C et DRB1; utilisation de sang de cordon ombilical comme source de cellules souches; utilisation de greffons avec cellules T déplétées ex vivo; réaction greffon contre l'hôte (GVHD) de grade 2 ou supérieur nécessitant des corticoïdes systémiques.
Efficacité
Infection à CMV cliniquement significative
Le critère principal d'efficacité de l'étude P001 a été l'apparition d'une infection à CMV cliniquement significative jusqu'à la semaine 24 post-greffe. L'infection à CMV cliniquement significative a été définie comme étant soit la survenue d'une maladie à CMV touchant un organe cible soit l'instauration d'un traitement préemptif anti-CMV (PET) en raison d'une virémie à CMV documentée (utilisation du Roche COBAS AmpliPrep/COBAS TaqMan Assay).
Dans l'analyse du critère principal, le letermovir a démontré une plus grande efficacité que le placebo (voir Tableau 3). La différence estimée de traitement de -23,5% était statistiquement significative (valeur de p unilatérale <0,0001).
Tableau 3: P001: Résultats d'efficacité chez les receveurs de GCSH (approche NC=F, population FAS)
|
|
Letermovir
|
Placebo
| |
|
(N=325)
|
(N=170)
| |
Paramètres
|
n (%)
|
n (%)
| |
Critère principal
(Pourcentage de patients en échec prophylactique)
|
122 (37,5)
|
103 (60,6)
| |
Raisons des échecs†
|
|
| |
Infection au CMV cliniquement significative jusqu'en semaine 24‡
|
57 (17,5)
|
71 (41,8)
| |
Instauration d'un traitement préemptif sur la base d'une virémie à CMV documentée
|
52 (16,0)
|
68 (40,0)
| |
Maladie à CMV d'un organe cible
|
5 (1,5)
|
3 (1,8)
| |
Sortie de l'étude avant la semaine 24
|
56 (17,2)
|
27 (15.9)
| |
Résultat manquant jusqu'à la fenêtre de consultation de la semaine 24
|
9 (2,8)
|
5 (2,9)
| |
Différence de traitement ajustée en fonction de la stratification (letermovir-placebo)§
|
|
| |
Différence (IC 95%)
|
-23,5 (-32,5, -14,6)
|
| |
Valeur de p
|
<0,0001
|
| |
† Les catégories d'échec sont mutuellement exclusives et se basent sur la hiérarchie des catégories dans l'ordre indiqué.
‡ Une infection à CMV cliniquement significative a été définie comme étant soit la survenue d'une maladie à CMV touchant un organe cible soit l'instauration d'un traitement préemptif en raison d'une virémie à CMV documentée et de l'état clinique du patient.
§ Les IC 95% et la valeur de p pour les différences entre traitements en pourcentage de réponse ont été calculés à l'aide de la méthode de Mantel-Haenszel ajustée en fonction des strates, en pondérant la différence en fonction de la moyenne harmonique de la taille de l'échantillon par bras pour chaque strate (risque élevé ou faible). Une valeur de p unilatérale ≤0,0249 a été utilisée pour déterminer la significativité statistique.
Remarque: FAS = population totale d'analyse (full analysis set); cette population inclut les patients randomisés qui ont reçu au moins une dose de médicament à l'étude, et exclut les patients présentant un ADN du CMV détectable en début d'étude. Approche suivie pour le traitement des valeurs manquantes: approche abandon=échec (Non-Completer = Failure; NC = F). Dans l'approche NC = F, l'échec a été défini comme l'ensemble des patients qui ont développé une infection au CMV cliniquement significative ou qui sont sortis prématurément de l'étude, ou ceux pour lesquels aucun résultat n'avait été relevé jusqu'à la fenêtre de consultation de la semaine 24 post-greffe.
N = Nombre de patients dans chaque groupe de traitement.
n (%) = Nombre (pourcentage) de patients dans chaque sous-catégorie.
|
En semaine 24 post-greffe, le taux d'infections à CMV cliniquement significatives (événements Kaplan-Meier, KM) a été de 18,9% dans le groupe letermovir vs 44,3% dans le groupe placebo (valeur de p nominale bidirectionnelle stratifiée du log-rank<0,0001) (voir Fig. 1). Chez les patients traités par le letermovir, les facteurs liés à une infection à CMV cliniquement significative entre les semaines 14 et 24 post-greffe ont été les suivants:
·risque élevé de réactivation du CMV en début d'étude,
·présence d'une GVHD et
·utilisation d'un stéroïde à un moment quelconque après randomisation.
Fig. 1: P001: Courbe de Kaplan-Meier du délai de survenue d'une infection à CMV cliniquement significative jusqu'à la semaine 24 post-greffe chez les receveurs de GCSH (population FAS)
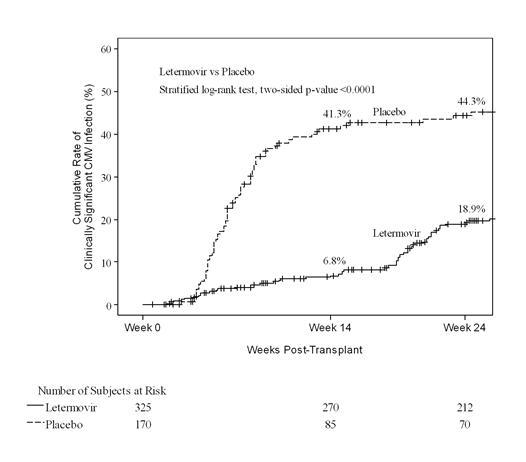
L'efficacité a été nettement supérieure dans tous les sous-groupes du bras letermovir, y compris les suivants:
·risque faible ou élevé de réactivation du CMV,
·traitements de conditionnement, et
·traitements immunosuppresseurs concomitants.
Mortalité
Les taux d'événements de mortalité globale (analyse Kaplan-Meier) a été de 12,1% dans le groupe letermovir vs 17,2% dans le groupe placebo en semaine 24 post-greffe (valeur de p nominale bidirectionnelle stratifiée du log-rank = 0,0401) et 23,8% vs 27,6% en semaine 48 post-greffe (valeur de p nominale bidirectionnelle stratifiée du log-rank = 0,2117). Les taux d'événements de mortalité globale (analyse Kaplan-Meier) selon le sexe (hommes vs femmes) en semaine 24 post-greffe a été de 16,4% vs 6,6% dans le groupe letermovir et de 14,2% vs 25,4% dans le groupe placebo; ces taux d'événements décomposés selon le sexe sont à interpréter avec précaution; en effet, la randomisation n'a pas été stratifiée par sexe, ce qui a donné lieu en baseline à des déséquilibres entre groupes de traitement en termes de risque de mortalité spécifiquement liés au sexe.
|

