Propriétés/EffetsCode ATC
L01XL03
Mécanisme d'action
YESCARTA, un médicament d'immunothérapie constitué de cellules T d'immunothérapie autologues génétiquement modifiées, se lie aux cellules cancéreuses et aux cellules B normales exprimant le CD19. Suite à la liaison des cellules CAR T anti-CD19 avec les cellules cibles exprimant le CD19, les domaines de co-stimulation CD28 et CD3-zéta activent la cascade de signalisation qui conduit dans les cellules T, à l'activation, la prolifération, à l'acquisition de fonctions effectrices et à la sécrétion des cytokines et des chimiokines inflammatoires. Cette cascade d'événements conduit à l'apoptose et à la nécrose des cellules cibles exprimant le CD19.
Pharmacodynamique
Après la perfusion de YESCARTA, la réponse pharmacodynamique a été évaluée en mesurant l'élévation transitoire des cytokines, des chimiokines et d'autres molécules dans le sang à 4 semaines d'intervalle. Les taux de cytokines et de chimiokines telles que les interleukines (IL) IL-6, IL-8, IL-10, IL-15, le TNF-α, l'IFN-γ et sIL2Rα ont été analysés. Un pic d'élévation a été observé au cours des 14 premiers jours après la perfusion et les taux étaient généralement revenus aux valeurs initiales en 28 jours.
En raison de l'effet on-target, off-tumour de YESCARTA, une aplasie de cellules B est attendue sur un certain intervalle après le traitement. Parmi les 73 patients atteints de LDGCB et de LMPGB dans ZUMA-1 pour lesquels des échantillons évaluables étaient disponibles au début de l'étude, 40% présentaient des cellules B détectables; l'aplasie de cellules B observée au début chez la majorité des patients a été attribuée à des traitements antérieurs. Après le traitement par YESCARTA, la proportion de patients présentant des cellules B détectables a diminué: 20% d'entre eux présentaient des cellules B détectables à 3 mois et 22% d'entre eux présentaient des cellules B détectables à 6 mois.
L'initiation d'une régénération des cellules B a été constatée pour la première fois à 9 mois, alors que 56% des patients présentaient des cellules B détectables. Cette tendance de régénération des cellules B s'est poursuivie sur la durée puisque 64% des patients présentaient des cellules B détectables à 18 mois et 77% des patients présentaient des cellules B détectables à 24 mois.
Parmi les 141 patients dans ZUMA-7 avec des échantillons évaluables au début de l'étude, 57% présentaient des cellules B détectables. Après le traitement par YESCARTA, la proportion des patients présentant des cellules B détectables a diminué: 38% présentaient des cellules B détectables au mois 3 et 41% présentaient des cellules B détectables à 6 mois. L'initiation de la régénération des cellules B a été constatée pour la première fois à 9 mois, alors que 58% des patients présentaient des cellules B détectables. Cette tendance de régénération des cellules B s'est poursuivie sur la durée puisque 64% des patients présentaient des cellules B détectables à 18 mois et 85% des patients présentaient des cellules B détectables à 24 mois.
Parmi les 113 patients dans ZUMA-5 atteints de LF ayant des échantillons évaluables à l'inclusion, 75% des patients présentaient des lymphocytes B détectables. Après le traitement par YESCARTA, la proportion des patients présentant des lymphocytes B détectables a diminué: 40% des patients présentaient des lymphocytes B détectables à 3 mois. La restauration des lymphocytes B a été observée au cours du temps, 61% des patients présentant des lymphocytes B détectables à 24 mois.
Il est important de noter que les patients n'ont pas eu besoin d'être suivis après la progression de la maladie; par conséquent, la majorité des patients dont les échantillons étaient évaluables étaient des répondeurs.
Efficacité clinique
Étude clinique ZUMA, phases 1 et 2 (LDGCB récidivant ou réfractaire, LMPCB et LDGCB résultant d'un lymphome folliculaire, après au moins deux lignes de traitement systémique)
Un total de 108 patients (7 patients inclus dans la phase 1 et 101 patients inclus dans la phase 2) atteints de lymphome non Hodgkinien (LNH) à cellules B agressif r/r ont été traités par YESCARTA dans une étude de phase 1/2 en ouvert, multicentrique, monobras.
D'après la classification OMS de 2008, qui était valide au moment de l'étude, l'efficacité a été évaluée sur 101 patients inclus dans la phase 2, y compris des patients atteints de LDGCB (N = 77), de LMPGB (N = 8) et de LDGCB qui résultaient histologiquement d'un lymphome folliculaire (N = 16). D'après la classification actuelle de l'OMS 2016:
Le LDGCB dans ZUMA-1 incluait des patients atteints de LDGCB non spécifiés, d'autres sous-types de LDGCB et de LBHG. Ceci est basé sur l'analyse rétrospective, post-hoc d'une partie des patients par «independent pathology review». Quarante-sept patients étaient évaluables pour le statut MYC, BCL-2, et BCL-6. Trente patients présentaient un LDGCB double expresseur (surexpression des protéines MYC et BCL-2); 5 patients étaient atteints d'un LBHG avec réarrangement des gènes MYC, BCL-2 ou BCL-6 (mutation de 2 gènes (double hit) ou de 3 gènes (triple hit)); 2 patients étaient atteints d'un LBHG non spécifié. En raison du nombre restreint de patients atteints de LBHG, aucune conclusion ne peut être établie par rapport à l'efficacité clinique au sein de cette population de patients. Soixante-six patients étaient évaluables pour la détermination des cellules B d'origine (cellules B germinales [GCB] ou cellules B activées [ABC]). Parmi ces patients, 49 présentaient un type GCB et 17 patients présentaient un type ABC.
Les patients éligibles étaient âgés d'au moins 18 ans et présentaient une maladie réfractaire, définie comme maladie progressive (progressive disease, PD) ou comme maladie stable (stable disease, SD) comme meilleure réponse à la dernière ligne de traitement utilisée ou présentant une progression de la maladie au cours des 12 derniers mois après une greffe de cellules souches [GCS] autologues . Les patients qui sont réfractaires à une chimiothérapie ou en récidive après au moins deux lignes de traitement systémique sont généralement inéligibles à une greffe de cellules souches hématopoïétiques (GSCH).
Les patients devaient avoir reçu au moins un traitement antérieur par des anticorps anti-CD20 ainsi qu'un régime à base d'anthracycline. Les patients présentant un lymphome du SNC, ou ayant fait l'objet d'une greffe de cellules souches hématopoïétiques allogéniques ou d'un traitement antérieur par CAR T anti-CD19 ou un autre traitement à base de cellules T génétiquement modifiées ont été exclus. Les patients ayant des antécédents de troubles du SNC (p.ex. convulsions ou ischémie vasculaire cérébrale), une fraction d'éjection cardiaque inférieure à 50%, ou une saturation en oxygène en air ambiant inférieure à 92% ou une maladie autoimmune nécessitant un traitement immunosuppresseur systémique étaient exclus. La durée médiane du suivi était de 27,1 mois (toujours en cours). La population en ITT était définie comme l'ensemble des patients ayant eu une leucaphérèse, et la population en mITT comme l'ensemble des patients ayant reçu YESCARTA.
Données démographiques de la population intent-to-treat (mITT) modifiée
L'âge médian de la population de l'étude mITT était 58 ans (intervalle: 23 à 76 ans); 67% étaient des hommes, 86% étaient caucasiens, 3% étaient d'origine asiatique et 4% étaient afro-américains. Le statut ECOG au début de l'étude correspondait pour 42% à ECOG 0 et pour 58% à ECOG 1. Le nombre médian de traitements précédents était 3 (intervalle: 1 à 10); pour 76% des patients, la maladie était réfractaire à 2 lignes de traitement précédentes ou plus, et 21% des patients étaient en récidive dans l'année suivant la greffe autologue de cellules souches [GCS] autologues. 46% des patients avaient un indice pronostique international de 3/4, et 85% des patients étaient atteints d'une maladie de stade III/ IV.
Données démographiques de la population intent-to-treat (ITT)
L'âge médian de la population de l'étude ITT était 58 ans (intervalle: 23 à 76 ans); 69% étaient des hommes, 85% étaient caucasiens, 4% étaient d'origine asiatique et 4% étaient afro-américains. Le statut ECOG au début de l'étude correspondait pour 41% à ECOG 0 et pour 59% à ECOG 1. Le nombre médian de traitements précédents était 3 (intervalle: 1 à 10); pour 77% des patients, la maladie était réfractaire à 2 lignes de traitement précédentes ou plus, et 20% des patients étaient en récidive dans l'année suivant la GCSA. 46% des patients avaient un indice pronostique international de 3/4, et 85% des patients étaient atteints d'une maladie de stade III/ IV.
YESCARTA a été administré en une perfusion unique à une dose cible de 2 x 106 cellules CAR T anti-CD19/kg à l'issue d'un schéma de chimiothérapie lymphodéplétive par 500 mg/m2 de cyclophosphamide par voie intraveineuse et 30 mg/m2 de fludarabine par voie intraveineuse; la lymphodéplétion a eu lieu les 5ème, 4ème et 3ème jours avant le traitement par YESCARTA. L'ensemble des 108 patients traités par YESCARTA dans l'étude ZUMA-1 (phases 1 et 2) ont reçu une chimiothérapie lymphodéplétive. Tous les patients avaient un nombre initial de globules blancs ≥1 x 103/μl (à savoir avant la chimiothérapie lymphodéplétive). Seuls les patients présentant un nombre absolu de neutrophiles ≥1000/μl, un nombre absolu de lymphocytes ≥100/μl et un taux de plaquettes ≥75 000/μl au départ ont été inclus dans l'étude. Une chimiothérapie en relais entre la leucaphérèse et la chimiothérapie lymphodéplétive n'était pas autorisée. Tous les patients ont été hospitalisés dans le but de surveiller et prendre en charge des effets indésirables survenant pendant au moins 7 jours après la perfusion de YESCARTA.
Phase 2 de ZUMA-1
Parmi les 111 patients qui ont eu une leucaphérèse, 101 ont reçu YESCARTA. Neuf patients n'ont pas été traités, en raison, principalement, de progression de la maladie ou d'événements indésirables sévères après le recrutement et avant l'administration des cellules. Sur les 111 patients, un patient n'a pas reçu le médicament en raison d'un problème de fabrication. Le délai médian entre la leucaphérèse et la réception du médicament était de 17 jours (intervalle: 14 à 51 jours), et le délai médian entre la leucaphérèse et la perfusion était de 24 jours (intervalle: 16 à 73 jours). La dose médiane était de 2,0 x 106 cellules CAR T anti-CD19/kg.
Le critère de jugement principal était le taux de réponse objective (Objective Response Rate, ORR) évalué par les médecins-investigateurs. Les critères d'évaluation secondaires incluaient le taux de réponse objective (ORR) évalué par un comité d'évaluation indépendant, la durée de la réponse (Duration of Response, DOR), la survie sans progression (PFS), la survie globale (Overall Survival, OS) et la sévérité des effets indésirables. Il était attendu que le ORR devait être testé chez les 92 premiers patients traités et être significativement plus élevé que le taux préspécifié de 20% (p < 0,0001).
Dans l'analyse préliminaire, basée sur la population en intention de traiter modifiée (mITT) (suivi minimum de 6 mois) le ORR a été de 82%, et le taux de réponse complète (Complete Response, CR) était de 54%, selon les médecins-investigateurs (critère de jugement principal). Dans l'analyse actualisée (suivi minimum de 12 mois), le ORR était de 83%, et le taux de CR était de 58% selon les médecins-investigateurs. Dans l'analyse de suivi à 24 mois, le ORR était de 83% et le taux de RC était de 58% selon les médecins-investigateurs. Les résultats d'efficacité sont résumés ci-dessous, dans le tableau 4. La valeur médiane OS au sein de la population en ITT était de 17,4 mois (IC à 95% de 11,6 NE). Les taux de OS à 12 et 24 mois étaient respectivement de 59,5% et 47,7%. La valeur médiane de l'OS n'a pas encore été atteinte au sein de la population en mITT parmi les 50 événements/101 patients observés. Les taux de OS à 12 et 24 mois étaient respectivement de 60,4% et 50,5%. Dans une analyse à 36 mois, la valeur médiane OS au sein de la population en mITT (101 patients) était de 25,8 mois. Dans une analyse à 60 mois, les estimations de Kaplan-Meier des taux de OS à 3 ans, 4 ans et 5 ans étaient de 47%, 44% et 43% respectivement.
Tableau 4: Résumé des résultats d'efficacité pour la phase 2 de ZUMA-1 (analyse à 24 mois)
|
|
Tous les patients ayant eu une leucaphérèse (ITT)
Cohorte 1 + 2
(N = 111)
|
Tous les patients traités
mITT
Cohorte 1 + 2
(N = 101)
| |
|
Évaluation d'une commission d'examen indépendante
|
Évaluation de médecins-investigateurs
|
Évaluation d'une commission d'examen indépendante
|
Évaluation de médecins-investigateurs
| |
ORR (%) [IC à 95%]
|
68 (58, 76)
|
77 (69, 85)
|
74 (65, 82)
|
83 (74, 90)
| |
CR (%)
|
50
|
55
|
54
|
58
| |
PFS (mois) [IC à 95%]
|
9,5 (6,1, 15,4)
|
6,2 (4,0, 12,4)
|
9,1 (5,7, n.e.)
|
5,9 (3,3, 15,0)
| |
DOR,a, médiane (IC à 95%) en mois
|
n.e. (10,9, n.e.)
|
9,0 (3,9, n.e.)
|
n.e. (10,9, n.e.)
|
9,0 (3,9, n.e.)
| |
DOR, CR, médiane (IC à 95%) en mois
|
n.e. (n.e., n.e.)
|
non disponible
|
n.e. (n.e., n.e.)
|
n.e. (12,9, n.e.)
| |
DOR, PR, médiane (IC à 95%) en mois
|
2,1 (1,3, 11,1)
|
non disponible
|
2,1 (1,3, 11,1)
|
1,9 (1,3, 2,1)
| |
Suivi médian (mois)
|
27,1
| |
Suivi minimal (mois)
|
22,9
| |
OS, médiane (mois) [IC à 95%]
|
17,4 (11,6, n.e.)
|
n.e. (12,8, n.e.)
| |
OS à 6 mois (%) [IC à 95%]
|
81,1 (72,5, 87,2)
|
79,2 (69,9; 85,9)
| |
OS à 12 mois (%) [IC à 95%]
|
59,5 (49,7, 67,9)
|
60,4 (50,2, 69,2)
| |
OS à 24 mois (%) [IC à 95%]
|
47,7 (38,2, 56,7)
|
50,5 (40,4, 59,7)
|
IC, intervalle de confiance; CR, réponse complète; DOR, durée de la réponse; ITT, intention de traiter; mITT, intention de traiter modifiée; n.e. = non estimable; ORR, taux de réponse objective; OS, survie globale; PR, réponse partielle.
a La durée de la réponse et la PFS ont été censurées au moment de la GCSH pour les patients ayant reçu une GCSH alors qu'ils continuaient à répondre
Note: la mITT était définie par tous les patients qui recevaient au moins une dose de YESCARTA de 1x106 cellules CAR-T/kg
Étude clinique ZUMA-7, phase 3, (LDGCB r/r et LBHG r/r)
L'efficacité et la sécurité de YESCARTA chez les patients adultes atteints de LDGCB r/r et LBHG r/r ont été démontrées dans une étude de phase 3 randomisée, en ouvert et multicentrique (ZUMA-7). La plupart des patients inclus avaient reçu le diagnostic d'un LDGCB non autrement spécifié/non classifiable davantage (69%) et d'un lymphome B de haut grade (LBHG) (0% à LBHG non autrement spécifié et 16% à réarrangement des gènes MYC / BCL-2 / BCL-6 (y compris double hit ou triple hit)) selon l'évaluation du laboratoire central. 46 patients (13%) ont été catégorisés en tant que «non confirmés» ou «manquants», et 10 patients (3%) ont été catégorisés en tant que «lymphome autre que LDGCB ou LBHG». Les patients ont été encore catégorisés selon les sous-groupes moléculaires (type cellule B de centre germinatif (58%) et type cellule B activée (7%) ainsi que «non classés» (9%)) et le statut d'expression de CD19 «oui» (77%) et «non» (7%) selon l'évaluation du laboratoire central. Tous les patients avaient reçu au préalable un traitement de première ligne avec une thérapie à base d'anthracycline et des anticorps monoclonaux anti-CD20, à moins que la tumeur ait été CD-20-négative. Au total, 359 patients ont été randomisés selon un rapport 1:1 pour recevoir une perfusion unique de YESCARTA ou recevoir le traitement standard (défini par 2 à 3 cycles de chimio-immunothérapie standard [R-ICE, R-DHAP ou R-DHAX, R-ESHAP ou R-GDP] suivie d'un traitement à haute dose [THD] et de greffe de cellules souches [GCS] autologue chez des patients dont la maladie répondait au traitement). La randomisation a été stratifiée 1) selon la réponse au traitement de première ligne (réfractaire primaire vs récidive ≤6 mois vs récidive > 6 et ≤12 mois) et selon l'aaIPP («age-adjusted international prognostic index») 0 / 1 vs 2 / 3. Les raisons de l'exclusion de l'étude étaient le traitement antécédent par greffe autologue de cellules souches hématopoïétiques (CSH), le lymphome primaire au niveau du SNC ou les métastases cérébrales, les cellules malignes détectables dans le liquide céphalorachidien et un indice de performance ECOG (Eastern Cooperative Oncology Group) de 2 ou plus. Les patients présentant des infections actives ou graves ont été exclus, toutefois les patients présentant des infections des voies urinaires simples et une pharyngite bactérienne non compliquée ont été autorisés s'ils répondaient à un traitement actif. Les patients atteints d'infections connues par le virus VIH, de l'hépatite B (HBsAG-positifs) ou de l'hépatite C (anti-VHC-positifs) ont été exclus. L'inclusion de patients après un traitement avec succès de l'hépatite B ou de l'hépatite C dans l'anamnèse était autorisée, si aucune charge virale n'était détectable dans la PCR quantitative et/ou le test d'acide nucléique.
Après une chimiothérapie lymphodéplétive, YESCARTA a été administré en une perfusion intraveineuse unique à une dose cible de 2 x 106 cellules CAR-T anti-CD19/kg (dose maximale: 2 x 108 cellules). Le schéma thérapeutique pour lymphodéplétion consistait en 500 mg/m² de cyclophosphamide par voie intraveineuse et 30 mg/m² de fludarabine par voie intraveineuse, tous deux administrés les 5e, 4e et 3e jours avant YESCARTA. Un traitement de transition d'attente non modificateur de la maladie, qui était limité aux corticostéroïdes, pouvait être administré entre la leucaphérèse et la chimiothérapie lymphodéplétive chez les patients ayant une charge tumorale élevée lors de la sélection.
Sur les 180 patients qui avaient été randomisés pour le traitement par YESCARTA, 178 ont été soumis à la leucaphérèse et 170 ont été traités par YESCARTA. Huit patients (4%) n'ont pas été traités après la leucaphérèse, notamment en raison de progression de la maladie, d'évènements indésirables graves ou de décès. Étant donné qu'une nouvelle administration pour un patient de l'étude clinique a nécessité un deuxième processus de fabrication, 171 charges ont été fabriquées au total. Le délai médian entre la leucaphérèse et la libération du produit était de 13 jours (intervalle: 10 à 24 jours) et le délai médian entre la leucaphérèse et la perfusion de YESCARTA était de 26 jours (intervalle: 16 à 52 jours). La dose médiane était de 2,0 x 106 cellules CAR-T anti-CD19/kg pour les patients ayant un poids corporel de < 100 kg (min: 1,0 x 106 cellules CAR-T anti-CD19/kg; max: 2,1 x 106 cellules CAR-T anti-CD19/kg). Pour les patients ayant un poids corporel de > 100 kg, la dose médiane était de 200 x 106 cellules CAR-T anti-CD19. 60 (33%) des patients traités ont reçu un traitement de transition d'attente par corticostéroïdes. Les 170 patients qui ont reçu YESCARTA ont tous été surveillés dans un établissement de santé pendant au moins 7 jours. Sur les 179 patients qui avaient été randomisés dans le bras de traitement standard de l'étude, 64 patients (36%) ont reçu une THD-GCSA, y compris 2 patients qui ont reçu une GCSA en dehors des spécifications du protocole.
Dans le groupe traitement standard 49 patients (41%) atteints de LDGCB et 9 patients (35%) atteints de LBHG ont reçu une GCSA-HD.
Dans la population globale de l'étude, l'âge médian était de 59 ans (intervalle: 21 à 81 ans); 66% étaient de sexe masculin et 83% étaient blancs. Septante-quatre pour cent des patients étaient atteints de LGCB réfractaire primaire, et 26% des patients étaient en récidive dans les 12 mois du traitement de première ligne. Les patients avaient un score IPI ajusté selon l'âge de 0-1 (55%) ou de 2-3 (45%) et un indice de performance ECOG de 0 (54%) ou de 1 (46%).
La durée réelle médiane de suivi était de 20,07 mois (intervalle: 0,59 à 37,75 mois) dans le groupe YESCARTA et de 18,23 mois (intervalle: 0,03 à 37,26 mois) dans le groupe de traitement standard.
Le critère d'évaluation principal était la survie sans événement (event-free survival, EFS), déterminée par une évaluation centralisée en aveugle. L'EFS était définie comme le temps entre la randomisation et la progression de la maladie selon la classification de Lugano (Cheson et al., 2014), le début d'un nouveau traitement du lymphome ou le décès de cause quelconque, en fonction de ce qui se produisait en premier. L'étude a montré une amélioration statistiquement significative de l'EFS chez les patients randomisés à YESCARTA en comparaison du traitement standard (HR: 0,398 [IC à 95%: 0,308; 0,514]). La survie à 24 mois sans évènement était de 40,5% [IC à 95%: 33,2; 47,7] dans le bras YESCARTA et de 16,3% [IC à 95%: 11,1; 22,2] dans le bras de traitement standard.
Les critères secondaires ORR et CR étaient significativement plus élevés chez les patients traités par YESCARTA, avec une différence d'OR de 33,1% [IC à 95%: 23,2; 42,1) et une différence de CR de 33% dans le bras YESCARTA (Tableau 5). La durée médiane de réponse était de 26,9 mois (intervalle: 0 à 29 mois) dans le bras YESCARTA, comparée à 8,9 mois (intervalle: 0 à 32 mois) dans le bras de traitement standard (HR: 0,736 [IC à 95%: 0,488; 1,108]). Au moment de l'analyse principale de l'EFS, la durée médiane de l'étude était de 24,9 mois.
L'analyse primairede la survie globale (OS), qui était un critère d'évaluation secondaire important, a été réalisée à la date définie dans le protocole d'étude, à savoir cinq ans à compter de l'inclusion du premier patient. Une amélioration statistiquement significative de l'OS avec YESCARTA par rapport au traitement standard a été démontréepar la réduction du risque de décès de 27,4% (HR: 0,726 [IC à 95%: 0,540; 0,977]). Avec des taux de OS à 48 mois estimés de 54,6% et 46,0% respectivement, l'OS médiane dans le bras YESCARTA n'a pas été atteinte comparée à 31,1 mois dans le bras de traitement standard. La durée médiane de l'étude est de 47,2 mois. Cinquante-sept pour cent (57%) des patients ont reçu une immunothérapie cellulaire après une absence de réponse au traitement standard ou après avoir rechuté après la randomisation au traitement standard.
Le résumé des résultats de l'efficacité dans la population globale est indiqué dans le tableau 5. La courbe de Kaplan-Meier de l'OS est illustrée dans la Figure 1.
Tableau 5: Résumé des résultats de l'efficacité pour ZUMA-7
|
|
YESCARTA
N = 180
|
Traitement standard
N = 179
| |
EFSa
| |
Nombre des évènements (%)
|
108 (60)
|
144 (80)
| |
Médiane, mois [IC à 95%]b
|
8,3 [4,5; 15,8]
|
2,0 [1,6; 2,8]
| |
Hazard Ratio stratifié [IC à 95%]
|
0,398 [0,308; 0,514]
| |
Valeur p du log-rank stratifiéec
|
< 0,0001
| |
OSf
| |
Nombre des évènements (%)
|
82 (46)
|
94 (53)
| |
OS médiane, mois [IC à 95%]b
|
Non atteinte (28,6; n. e.)
|
31,1 (17,1; n. e.)
| |
Hazard Ratio stratifié [IC à 95%]
|
0,726 (0,540; 0,977)
| |
Valeur p du log-rank stratifiéec,d
|
0,0168
| |
ORR (%) [IC à 95%]a
|
83 [77,1, 88,5]
|
50 [42,7, 57,8]
| |
Odds Ratio [IC à 95%]
|
5,31 [3,08, 8,90]
| |
Valeur p du test CMH stratifiéec
|
< 0,0001
| |
Taux de la réponse complète (%)
|
65 [57,6, 71,9]
|
32 [25,6, 39,8]
| |
Taux de la réponse partielle (%)
|
18 [13,0, 24,8]
|
18 [12,6, 24,3]
| |
PFSe
| |
Nombre des évènements (%)
|
96 (53)
|
103 (58)
| |
Médiane, mois [IC à 95%]b
|
14,7 [5,4, n. e.]
|
3,7 [2,9, 5,3]
| |
Hazard Ratio stratifié [IC à 95%]
|
|
0,490 [0,368, 0,652]
|
IC, intervalle de confiance; CMH, Cochran-Mantel-Haenszel; EFS, survie sans événement; n.e., non estimable; OS, survie globale; PFS, survie sans progression.
a Définie dans le cadre d'une évaluation centrale au moment de l'analyse principale de l'EFS.
b Méthode de Kaplan-Meier.
c Valeurs p unilatérales. Test du log-rank stratifié ou test CMH stratifié selon la réponse au traitement de première ligne (réfractaire primaire vs récidivant ≤6 mois après le traitement de première ligne vs récidivant > 6 et ≤12 mois après le traitement de première ligne) et ajusté à l'indice pronostique international en fonction de l'âge sur la base du traitement de deuxième ligne (0 à 1 vs 2 à 3).
d La valeur p est comparée à 0,0249, la limite d'efficacité unilatérale (seuil de signification) pour l'analyse principale de l'OS.
e Selon estimation de l'investigateur.
f Après évaluation au moment de l'analyse principale de l'OS (cinq ans à compter de l'inclusion du premier participant).
Une efficacité constante a été observée dans les sous-groupes, y compris réponse au traitement de première ligne, score IPI ajusté selon l'âge dans le traitement de deuxième ligne, indice de performance ECOG, âge, statut à double expression du lymphome, sous-type de maladie LBHG, statut CD19, symptômes B, implication de la rate, charge tumorale élevée et implication de la moelle osseuse.
Figure 1a. Courbe de Kaplan-Meier de la survie globale dans l'étude ZUMA-7 (ensemble complet d'analyses; analyse principale de la survie globale)
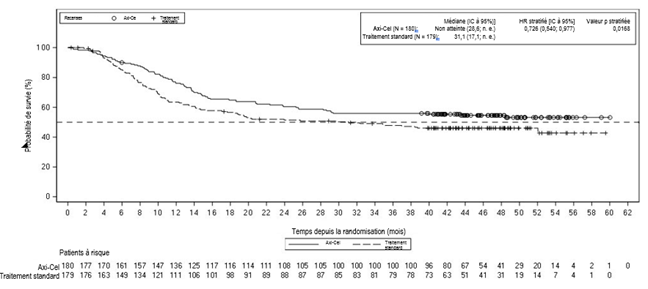
IC, intervalle de confiance; HR, Hazard Ratio; SOCT, traitement standard.
aLes patients qui ne répondaient pas au traitement standard ont pu recevoir, en dehors des spécifications du protocole, un traitement subséquent du lymphome, y compris un traitement par cellules CAR-T anti-CD19.
Traitement répété par YESCARTA
Au moment de l'analyse principale de l'OS, 10 patients (6%) au total ont reçu un traitement répété par YESCARTA. En raison du nombre restreint de patients, il n'est pas possible d'en tirer de conclusion en ce qui concerne l'efficacité et la sécurité.
Traitement subséquent du lymphome
Cinquante-sept pour cent (57%) des patients dans le bras de traitement standard ont reçu ensuite une immunothérapie cellulaire hors protocole (y compris 55% qui ont reçu une thérapie autologue par cellules CAR anti-CD19) après la randomisation.
Huit pour cent (8%) des patients dans le bras YESCARTA ont reçu ensuite une immunothérapie cellulaire hors protocole (y compris 7% qui ont reçu une thérapie autologue par cellules CAR anti-CD19 et y compris les 10 patients (6%) qui ont reçu un traitement répété par YESCARTA).
Greffe subséquente de cellules souches
Quatre pour cent (4%) des patients dans le bras de traitement standard et 7% dans le bras YESCARTA ont reçu ensuite un traitement à haute dose et une greffe autologue de cellules souches [HDT + GCSA], et 4% des patients dans le bras de traitement standard et 8% des patients dans le bras YESCARTA ont reçu ensuite une allogreffe de cellules souches (GCS).
Étude clinique (ZUMA-5), phase 2, LF récidivant ou réfractaire
L'efficacité et la sécurité de YESCARTA chez les patients adultes atteints de LF, ayant été traités par YESCARTA, ont été évaluées dans une étude de phase 2 multicentrique, en ouvert, monobras chez des patients atteints de LF récidivant ou réfractaire d'après la classification de l'OMS de 2016.
Les patients éligibles étaient âgés de ≥18 ans et présentaient une maladie récidivante ou réfractaire après au moins 2 lignes de traitement précédentes.
Le traitement précédent devait avoir inclus un anticorps monoclonal anti-CD20 associé à un agent alkylant (l'anticorps anti-CD20 en monothérapie ne comptait pas comme ligne de traitement). Les patients présentant une MS (sans récidive) > 1 an après la fin du dernier traitement étaient exclus. Les patients présentant un lymphome du SNC, ou ayant déjà fait l'objet d'une GCS allogénique ou ayant reçu un traitement antérieur par cellules CAR T anti-CD19 ou un autre traitement à base de cellules T génétiquement modifiées ont été exclus. Les patients présentant des antécédents de troubles du SNC (tels que convulsions ou ischémie vasculaire cérébrale), une fraction d'éjection cardiaque inférieure à 50%, ou une saturation en oxygène en air ambiant inférieure à 92%, ou une maladie auto-immune nécessitant un traitement immunosuppresseur systémique n'étaient pas éligibles. L'étude excluait les patients présentant des infections actives ou sévères, un lymphome transformé ou une localisation au niveau du SNC.
Au moment de l'analyse principale, un total de 127 patients atteints de LF avaient été inclus dans l'étude, y compris 80 patients qui avaient reçu au moins 3 lignes de traitement précédentes, et tous présentaient une leucaphérèse. Au cours de la période comprise entre la date de clôture des données de l'analyse principale et la date de clôture des données de l'analyse de suivi à 24 mois, aucun autre patient atteint de LF n'a été inclus ou traité par YESCARTA.
La durée réelle du suivi a été de 26,55 mois (intervalle: 0,3 à 44,3 mois, étude toujours en cours). Parmi les 127 patients atteints de FL recrutés, 80 patients avaient reçu au moins 3 lignes de traitement précédentes. Les données démographiques de la population ayant reçu au moins 3 lignes de traitement précédentes étaient conformes à celles de la population globale. Un résumé des données démographiques des patients est fourni dans le Tableau 6.
Tableau 6: Résumé des caractéristiques de la population pour les patients atteints de LF de l'étude ZUMA-5 (analyse à 24 mois)
|
Paramètres
|
Patients ayant eu une leucaphérèse ≥2 lignes de traitement précédentes
(N = 127)
|
Patients ayant eu une leucaphérèse ≥3 lignes de traitement précédentes
(N = 80)
| |
Âge (ans)
| |
Médiane (min, max)
|
60 (34, 79)
|
60.5 (34, 79)
| |
≥65
|
31%
|
33%
| |
Sexe masculin
|
59%
|
61%
| |
Origine ethnique
| |
Caucasien
|
92%
|
93%
| |
Asiatique
|
2%
|
4%
| |
Afro-américain
|
3%
|
3%
| |
Statut ECOG
| |
ECOG 0
|
62%
|
58%
| |
ECOG 1
|
38%
|
43%
| |
Forte masse tumorale, telle que définie par les critères GELF
|
51%
|
56%
| |
Nombre médian de traitements précédents (min; max)
|
3 (1, 10)
|
4 (3, 10)
| |
Patients atteints d'une maladie réfractaire à ≥2 lignes de traitement précédentes
|
29%
|
24%
| |
Patients atteints d'une maladie de stade III/IV
|
86%
|
88%
| |
Traitement antérieur par un inhibiteur de PI3K
|
28%
|
43%
| |
Délai de rechute < 24 mois après le premier traitement par association chimiothérapie et anti-CD20
|
56%
|
54%
|
ECOG, Eastern Cooperative Oncology Group; GELF, Groupe d'Étude des Lymphomes Folliculaires.
YESCARTA a été administré en une perfusion intraveineuse unique à une dose cible de 2 x 106 cellules CAR T anti-CD19/kg après une chimiothérapie lymphodéplétive par cyclophosphamide (500 mg/m² par voie intraveineuse) et fludarabine (30 mg/m2 par voie intraveineuse), tous deux administrés les 5e, 4e et 3e jours avant YESCARTA. Tous les patients ont été hospitalisés dans un but d'observation pendant au moins 7 jours après la perfusion de YESCARTA. L'administration et la surveillance de YESCARTA dans ZUMA-5 sont conformes à la procédure appliquée dans ZUMA-1.
L'analyse principale a été réalisée lorsque 84 patients atteints de LF recrutés consécutivement ont eu un suivi minimum de 12 mois à partir de la première évaluation de la réponse. Le critère d'évaluation principal était le dORR. Les critères d'évaluation secondaires comprenaient le taux de CR, le ORR et la CR chez les patients ayant reçu au moins 3 lignes de traitement précédentes, la DOR, l'OS, la survie sans progression (PFS) et l'incidence des effets indésirables. Trois des 127 patients atteints de LF inclus au moment de l'analyse principale n'ont pas été traités, principalement en raison du non-respect des critères d'inclusion ou du décès avant le traitement. Une analyse de suivi à 24 mois a été réalisée, lorsque 86 patients atteints de LF avaient un suivi minimum de 24 mois après la perfusion.
Lors de l'analyse de suivi à 24 mois, aucun patient supplémentaire n'a eu de leucaphérèse ni n'a été traité par YESCARTA. Le délai médian entre la leucaphérèse et la libération du produit était de 12 jours (intervalle: 10 à 37 jours), le délai médian entre la leucaphérèse et la réception du produit fini était de 17 jours (intervalle: 13 à 72 jours) et le délai médian entre la leucaphérèse et la perfusion de YESCARTA était de 27 jours (intervalle:19 à 330 jours). La dose médiane était de 2,0 × 106 cellules CAR T anti-CD19/kg.
Parmi les 127 patients atteints de LF inclus, 80 avaient reçu au moins 3 lignes de traitement précédentes. Le ORR était de 91% et le taux de CR était de 79%. Le délai médian de réponse était de 0,99 mois (intervalle: 0,8 à 3,1 mois), la DOR médiane était de 38,6 mois et la proportion de répondeurs toujours en réponse était de 55% jusqu'au mois 24. L'analyse des sous-groupes comprenait le ORR chez les patients réfractaires (89%) ainsi que les patients présentant un score FLIPI ≥3 (95%), une charge tumorale élevée (91%), une progression de la maladie dans les 24 mois suivant la première immunothérapie (91%) et un traitement antérieur par un inhibiteur de PI3K (91%). Les principaux résultats d'efficacité pour les patients atteints de LF ayant reçu au moins 3 lignes de traitement précédentes sont résumés dans le Tableau 7. Vingt-neuf des 80 patients atteints de LF qui avaient reçu au moins 3 lignes de traitement précédentes ont initialement obtenu une PR, dont 19 ont ensuite obtenu une CR.
Tableau 7: Résumé des résultats d'efficacité pour l'ensemble des patients atteints de LF inclus dans ZUMA-5 ayant reçu au moins 3 lignes de traitement précédentes (analyse à 24 mois)
|
Paramètres
|
Ensemble des patients ayant eu une leucaphérèse
N = 80
| |
ORRa, (%) [IC à 95%]
|
91% [83, 96]
| |
CR, (%) [IC à 95%]
|
79% [68, 87]
| |
PR, (%) [IC à 95%]
|
13% [6, 22]
| |
DORb, médiane en mois [IC à 95%]
|
38.6
| |
(intervalle)
|
(24.7, NE)
| |
DOR min, max (mois)
|
(0.0, 38,6)
| |
Réponse en cours (n)
|
44
| |
Taux de rémission continuec % (IC à 95%)
|
| |
12 mois
|
78,1 (66,2, 86,2)
| |
18 mois
|
72,8 (60,2, 82,0)
| |
24 mois
|
65,4 (51,2, 76,4)
| |
Survie sans progression, médiane, mois [IC à 95%]
|
40,2 (26,6, NE)
| |
Survie globale, médiane (mois) [IC à 95%]
|
NE (40,2, NE)
| |
Survie globale, % [IC à 95%]
|
| |
12 mois
|
96,2 (88,7, 98,8)
| |
18 mois
|
91,1 (82,2, 95,7)
| |
24 mois
|
85,2 (74,7, 91,5)
|
CR, réponse complète; DOR, durée de réponse; IC, intervalle de confiance; NE, non évaluable; dORR, taux de réponse objective; PR, réponse partielle.
a. Selon la classification de Lugano du groupe de travail international (Cheson 2014), évalué par le comité indépendant d'examen radiologique.
b. Parmi tous les répondeurs, la DOR est mesurée à partir de la date de la première réponse objective jusqu'à la date de la progression ou du décès.
c. Mesuré à partir de la date de la première réponse objective jusqu'à la date de la progression ou du décès.
|

