CompositionPrincipes actifs
Eskétamine (sous forme de chlorhydrate d'eskétamine).
Excipients
Acide citrique monohydraté (E330), édétate de sodium, hydroxyde de sodium, eau pour préparations injectables.
Indications/Possibilités d’emploiSpravato, en association avec un antidépresseur oral, est indiqué pour le traitement des épisodes de dépression majeure résistants au traitement chez les adultes qui n'ont pas répondu à au moins 2 antidépresseurs différents pour le traitement de l'épisode dépressif modéré à sévère actuel.
Spravato, en association avec un traitement antidépresseur oral, est indiqué comme traitement aigu de courte durée pour la réduction rapide des symptômes dépressifs chez les patients adultes présentant un épisode sévère de dépression majeure (sans symptômes psychotiques) lorsque la symptomatologie est évaluée cliniquement comme une urgence psychiatrique.
Spravato doit être uniquement administré dans un endroit où les mesures de sécurité nécessaires peuvent être assurées (y compris des mesures de soins avancés en réanimation cardiopulmonaire) avant, pendant et après l'administration du médicament (voir Posologie/Mode d'emploi et Mises en garde et précautions).
Posologie/Mode d’emploiLa décision de prescrire Spravato doit être prise par un psychiatre. Spravato doit être administré en complément d'un traitement par un antidépresseur (AD) oral. L'administration doit être réalisée par le patient lui-même, sous la supervision directe d'un médecin.
Spravato doit être utilisé dans un lieu de traitement doté d'un équipement de réanimation approprié et d'un personnel médical formé à la réanimation cardiopulmonaire. Cela comprend notamment des mesures de ventilation active et de gestion des crises hypertensives.
Une séance de traitement comprend l'administration nasale de Spravato et une surveillance ultérieure d'au moins 2 heures après l'administration.
Remarques importantes avant et après le traitement
Mesure de la pression artérielle avant et après le traitement
La pression artérielle doit être mesurée avant l'administration de la dose de Spravato (voir Mises en garde et précautions).
Si la pression artérielle est élevée au début du traitement (systolique > 140 mmHg, diastolique > 90 mmHg), le rapport des risques d'augmentation de la pression artérielle et des bénéfices du traitement par Spravato doit être évalué (voir Mises en garde et précautions) et l'utilisation doit, le cas échéant, être reportée. Spravato ne doit pas être utilisé si une augmentation de la pression artérielle ou de la pression intracrânienne représente un risque grave (voir Contre-indications).
Après l'administration de Spravato, la pression artérielle doit être mesurée une nouvelle fois après environ 40 minutes, ainsi que par la suite si cela est indiqué d'un point de vue clinique, et la surveillance du patient doit si nécessaire être poursuivie au-delà de la période d'observation de 2 heures (voir Mises en garde et précautions).
Si la pression artérielle baisse et que le patient semble être cliniquement stable, le patient peut quitter les lieux à la fin de la période d'observation; si ce n'est pas le cas, il doit continuer à être surveillé (voir Mises en garde et précautions).
Consommation d'aliments et de liquide avant l'utilisation de Spravato
Des nausées et des vomissements peuvent survenir après l'administration de Spravato. Les patients ne doivent par conséquent rien manger pendant au moins 2 heures avant l'administration et ne rien boire pendant au moins 30 minutes avant l'administration.
Traitement par corticostéroïdes nasaux et décongestionnants nasaux
Les patients ayant besoin d'un corticostéroïde ou d'un décongestionnant pour instillation nasale le jour du traitement ne doivent pas utiliser ces médicaments dans l'heure précédant l'administration de Spravato. Les instructions concernant la préparation du patient et l'utilisation du spray nasal figurent dans le mode d'emploi.
Posologie usuelle
Spravato doit être utilisé en association avec un antidépresseur oral.
Adultes
Dépression résistante au traitement (DRT)
Les recommandations posologiques pour Spravato lors de DRT sont indiquées dans le tableau 1. Les ajustements de la dose doivent être réalisés en fonction de l'efficacité et de la tolérance de la dose précédente.
Tableau 1: Posologie recommandée de Spravato lors de DRT
|
Phase d'instauration
|
Phase d'entretien
| |
Semaines 1-4:
(deux séances de traitement par semaine):
Début le jour 1, dose*: 56 mg
Doses ultérieures: 56 mg ou 84 mg
Le bénéfice thérapeutique doit être évalué à la fin de la phase d'instauration afin de déterminer la nécessité de poursuivre le traitement.
|
Semaines 5-8:
56 mg ou 84 mg une fois par semaine
À partir de la semaine 9:
56 mg ou 84 mg toutes les 2 semaines ou une fois par semaine**
La nécessité de la poursuite du traitement doit être évaluée à intervalles réguliers.
| |
* Pour les patients de ≥65 ans, la dose initiale recommandée le jour 1 est de 28 mg (voir Instructions posologiques particulières).
** La fréquence d'administration doit être ajustée individuellement à la fréquence la plus basse permettant le maintien d'une rémission/de la réponse thérapeutique.
|
Traitement aigu de courte durée d'une urgence psychiatrique dans le cadre d'une dépression majeure
La posologie recommandée de Spravato est de 84 mg, deux fois par semaine pendant 4 semaines. Une réduction de la dose à 56 mg doit être effectuée en fonction de la tolérance. Le bénéfice thérapeutique doit être évalué après 4 semaines de traitement, afin de déterminer la nécessité de poursuivre le traitement.
Dans cette indication, le traitement au-delà de 4 semaines n'a pas été étudié dans des études contrôlées.
Les patients qui présentent également une DRT doivent être évalués, afin de déterminer si la poursuite du traitement par Spravato au-delà de 4 semaines s'avère nécessaire.
Mode d'administration
Spravato est uniquement destiné à l'administration nasale. Le spray nasal est destiné à une utilisation unique et libère un total de 28 mg d'eskétamine en deux pulvérisations (une pulvérisation par narine). Afin d'éviter une perte de principe actif, le spray nasal ne doit pas être actionné avant utilisation. Il est destiné à être utilisé par le patient lui-même, sous la supervision directe d'un médecin, pour 1 spray nasal (dose de 28 mg), 2 sprays nasaux (dose de 56 mg) ou 3 sprays nasaux (dose de 84 mg), avec une pause de 5 minutes entre chaque utilisation des sprays nasaux.
Observation après l'administration
La pression artérielle doit être contrôlée environ 40 minutes après l'utilisation de Spravato, puis une nouvelle fois selon le jugement clinique (voir Mises en garde et précautions).
En raison de la survenue possible de sédation, de dissociation et d'élévation de la pression artérielle, les patients doivent être surveillés pendant au moins 2 heures sous la supervision d'un médecin, jusqu'à ce que le patient soit assez stable, selon le jugement clinique, pour quitter les lieux (voir Mises en garde et précautions).
Séance(s) de traitement manquée(s)
Si un patient manque une ou plusieurs séances de traitement durant les 4 premières semaines de traitement, le schéma posologique en cours doit être maintenu chez ce patient.
Chez les patients présentant une DRT, qui manquent une ou plusieurs séances de traitement durant la phase d'entretien et dont l'évaluation clinique montre une aggravation des symptômes dépressifs, il faut envisager de revenir au schéma posologique précédent (voir tableau 1).
Instructions posologiques particulières
Patients présentant des troubles de la fonction hépatique
Aucun ajustement de la posologie n'est nécessaire chez les patients présentant une altération de la fonction hépatique légère (stade A de Child-Pugh) ou modérée (stade B de Child-Pugh). Une période d'observation prolongée après l'administration de Spravato peut être nécessaire chez les patients présentant une altération de la fonction hépatique modérée (voir Pharmacocinétique – Cinétique pour certains groupes de patients, Troubles de la fonction hépatique).
Spravato n'a pas été évalué chez les patients présentant une altération de la fonction hépatique sévère (stade C de Child-Pugh). L'utilisation n'est pas recommandée chez ces patients (voir Pharmacocinétique – Cinétique pour certains groupes de patients, Troubles de la fonction hépatique).
Patients présentant des troubles de la fonction rénale
Aucun ajustement de la posologie n'est nécessaire chez les patients présentant une altération de la fonction rénale légère à sévère. Les patients dialysés n'ont pas été étudiés.
Patients âgés
Dépression résistante au traitement (DRT)
Chez les patients âgés de 65 ans ou plus, la dose initiale de Spravato est de 28 mg (jour 1, dose initiale, voir tableau 1). Les doses ultérieures doivent être augmentées par paliers de 28 mg à 56 mg ou 84 mg, selon l'efficacité et la tolérance.
Traitement aigu de courte durée d'une urgence psychiatrique dans le cadre d'une dépression majeure
Aucune donnée n'est disponible pour cette indication chez les patients âgés de 65 ans et plus.
Enfants et adolescents
L'utilisation de Spravato n'est pas indiquée chez les patients de moins de 18 ans. La sécurité et l'efficacité de Spravato n'ont pas été démontrées chez les patients âgés de 17 ans et moins.
Patients japonais et chinois présentant une dépression résistante au traitement
L'efficacité de Spravato chez les patients japonais et chinois atteints de DRT n'a pas été établie (voir Propriétés/Effets – Efficacité clinique).
Contre-indicationsSpravato est contre-indiqué chez les patients:
·lorsqu'une augmentation de la pression artérielle ou de la pression intracrânienne représente un risque grave (voir Mises en garde et précautions – Effet sur la pression artérielle):
·atteints d'une maladie vasculaire anévrismale connue (y compris l'aorte thoracique ou abdominale et les artères intracrâniennes ou périphériques)
·ayant des antécédents connus d'hémorragie intracérébrale
·ayant récemment subi (au cours des 6 dernières semaines) des événements cardiovasculaires, y compris un infarctus du myocarde (IM)
·ayant une hypersensibilité connue à l'eskétamine, la kétamine ou l'un des excipients.
Mises en garde et précautionsSuicide/pensées suicidaires ou aggravation clinique
L'efficacité de Spravato dans la prévention du suicide ou la réduction des pensées ou des comportements suicidaires n'a pas été établie.
L'utilisation de Spravato pour le traitement aigu de courte durée d'une urgence psychiatrique dans le contexte d'une dépression majeure n'exclut pas la nécessité d'une hospitalisation, si celle-ci s'avère cliniquement appropriée, même si les patients présentent une amélioration après avoir reçu une dose initiale de Spravato.
Tous les patients traités par des antidépresseurs, y compris ceux traités par Spravato, doivent être étroitement surveillés de sorte à détecter la survenue d'une aggravation clinique ou de pensées et comportements suicidaires, en particulier au cours des premiers mois du traitement médicamenteux et après une modification de la posologie. Les patients (et les personnes qui les assistent) doivent être informés de la nécessité de surveiller toute détérioration clinique éventuelle, tout comportement suicidaire ou toute pensée suicidaire et tout changement de comportement inhabituel. Ils doivent consulter un médecin dans les plus brefs délais si de tels symptômes se manifestent.
Les troubles dépressifs sont associés à un risque accru de pensées suicidaires, de comportement autodestructeur et de suicide (événements liés au suicide). Ce risque accru existe jusqu'à la survenue d'un soulagement significatif des symptômes ou d'une rémission. Les patients doivent donc faire l'objet d'une surveillance étroite. L'expérience clinique acquise jusqu'à présent montre que le risque de suicide peut augmenter dans les stades précoces de la guérison.
Le risque de pensées suicidaires ou de tentatives de suicide est accru chez les patients ayant des antécédents de comportement suicidaire ou ayant présenté des intentions suicidaires prononcées avant le traitement. Ils doivent donc faire l'objet d'une surveillance particulièrement attentive pendant le traitement.
Dans les études pivots regroupées, menées auprès de patients adultes atteints d'un trouble dépressif majeur (TDM) sévère et présentant des pensées suicidaires actives avec une intention suicidaire, la survenue d'une automutilation intentionnelle (confirmée comme n'étant pas une tentative de suicide) a été rapportée au cours de la phase de traitement en double aveugle chez 3,1% des patients du groupe Spravato plus traitement standard (SOC) et chez 1,3% des patients du groupe placebo plus SOC. Au cours de la phase de surveillance ultérieure, pendant laquelle les patients ne recevaient que le SOC, des tentatives de suicide ont été observées chez respectivement 3,7% et 1,6% des patients précédemment traités par Spravato et par le placebo.
Une méta-analyse d'études cliniques contrôlées contre placebo sur l'administration d'antidépresseurs oraux chez des adultes atteints de troubles psychiatriques a montré, chez les patients de moins de 25 ans prenant des antidépresseurs, un risque accru de comportement suicidaire par rapport au placebo.
Chez les patients dont la dépression s'aggrave de façon persistante ou qui présentent des pensées ou des comportements suicidaires émergents, une modification du schéma posologique, incluant l'arrêt éventuel de Spravato et/ou de l'antidépresseur oral concomitant, doit être envisagée.
Dépression respiratoire
Aucun cas de dépression respiratoire n'a été observé dans les études cliniques sur l'eskétamine en spray nasal (Spravato); de rares cas de sédation profonde ont été signalés. Une dépression respiratoire peut être causée par une injection intraveineuse rapide de fortes doses d'eskétamine ou de kétamine, administrées en tant qu'anesthésique. L'utilisation concomitante de Spravato et de dépresseurs du système nerveux central peut augmenter le risque de sédation (voir Interactions). Pendant la période suivant la mise sur le marché, de rares cas de dépression respiratoire ont été observés. La majorité de ces cas a été rapportée en association avec des dépresseurs du système nerveux central et/ou chez des patients présentant des comorbidités telles qu'une obésité, une anxiété, des maladies cardiovasculaires et respiratoires. Ces événements étaient transitoires et ont disparu après une stimulation verbale/tactile ou un apport supplémentaire d'oxygène. Le patient doit faire l'objet d'une surveillance étroite pour détecter la survenue d'une sédation ou d'une dépression respiratoire.
Effet sur la pression artérielle
Spravato peut causer une augmentation temporaire de la pression artérielle systolique et/ou diastolique, dont l'ampleur est maximale environ 40 minutes après l'administration du médicament et dont la durée peut atteindre environ 1 à 2 heures (voir Effets indésirables). Une augmentation substantielle de la pression artérielle peut survenir au cours de toute séance de traitement. Spravato est contre-indiqué chez les patients pour lesquels une augmentation de la pression artérielle ou de la pression intracrânienne représente un risque grave (voir Contre-indications). Les patients atteints d'autres maladies cardiovasculaires et cérébrovasculaires doivent être soigneusement évalués avant la prescription de Spravato, afin de décider si les bénéfices potentiels de Spravato l'emportent sur les risques.
Chez les patients dont la pression artérielle est élevée avant l'administration de Spravato (directive générale: > 140/90 mmHg chez les patients de < 65 ans et > 150/90 mmHg chez les patients de ≥65 ans), il est recommandé d'envisager de modifier le style de vie et/ou d'adopter un traitement médicamenteux pour diminuer la pression artérielle avant de commencer le traitement par Spravato. La décision de reporter ou non le traitement par Spravato doit tenir compte du rapport bénéfice/risque de chaque patient.
La pression artérielle doit être surveillée après l'administration de Spravato jusqu'à ce qu'elle revienne aux valeurs initiales avant l'administration de Spravato. Si la pression artérielle reste élevée, la nécessité d'un traitement antihypertenseur doit être immédiatement évaluée et il doit, si nécessaire, immédiatement être mis en œuvre.
Dans les études cliniques d'homologation, 8% à 17% des patients traités par Spravato ont présenté une augmentation de la pression artérielle systolique > 40 mmHg et une augmentation de la pression artérielle diastolique > 25 mmHg, contre 1% à 3% sous le placebo.
Les patients âgés de ≥65 ans ont présenté une incidence accrue d'augmentation aiguë de la pression artérielle (pression artérielle systolique ≥180 mmHg ou pression artérielle diastolique ≥110 mmHg) par rapport aux patients âgés de moins de 65 ans (voir Mises en garde et précautions – Patients de ≥65 ans). Un traitement d'urgence doit immédiatement être mis en œuvre chez les patients présentant des symptômes de crise hypertensive.
La pression artérielle des patients traités par des psychostimulants ou des inhibiteurs de monoamine oxydase (IMAO) doit faire l'objet d'une surveillance étroite (voir Interactions).
Patients atteints de maladies cardiovasculaires ou respiratoires cliniquement significatives ou instables
Le traitement des patients atteints de maladies cardiovasculaires ou respiratoires cliniquement significatives ou instables ne peut être initié que si les bénéfices l'emportent sur les risques. Voici quelques exemples d'affections qui devraient être prises en compte, sans toutefois s'y limiter:
·insuffisance respiratoire significative, y compris la BPCO;
·apnée du sommeil avec obésité morbide (IMC ≥35);
·patients présentant une bradycardie ou une tachyarythmie non contrôlée, entraînant une instabilité hémodynamique;
·antécédents connus d'IM. Ces patients doivent être cliniquement stables et exempts de symptômes cardiaques avant l'utilisation;
·cardiopathie valvulaire ou insuffisance cardiaque significatives d'un point de vue hémodynamique (classe III à IV de la NYHA).
Dissociation
Les effets psychologiques les plus fréquents de Spravato étaient des troubles dissociatifs ou des modifications de la perception (y compris une altération de la perception du temps et de l'espace, ainsi que des illusions), la déréalisation et la dépersonnalisation (voir Effets indésirables). Étant donné que Spravato peut provoquer des effets dissociatifs, les patients atteints de psychose doivent être soigneusement évalués avant l'utilisation de Spravato; le traitement ne doit être initié que si les bénéfices l'emportent sur les risques.
En raison du risque de dissociation, les patients doivent être surveillés pendant au moins 2 heures à chaque séance de traitement sous la supervision d'un médecin. Il faut ensuite évaluer quand le patient peut être considéré comme cliniquement stable et en mesure de quitter le cabinet ou la clinique.
Sédation
En raison de la possibilité d'une sédation retardée ou prolongée, les patients doivent être observés pendant au moins 2 heures à chaque séance de traitement sous la surveillance d'un médecin. Il faut ensuite évaluer quand le patient peut être considéré comme cliniquement stable et en mesure de quitter le cabinet ou la clinique.
Lors de l'utilisation concomitante de Spravato et de dépresseurs du système nerveux central, le patient doit être étroitement surveillé pour détecter tout signe de sédation (voir Interactions).
Troubles cognitifs et moteurs
Selon les observations réalisées dans le cadre d'études cliniques, Spravato peut causer une somnolence, une sédation, des symptômes dissociatifs, des troubles de la perception, des vertiges oscillatoires et rotatoires, ainsi que de l'anxiété (voir Effets indésirables). Ces effets peuvent affecter l'attention, la capacité de jugement, la pensée, la vitesse de réaction et les capacités motrices. Les patients doivent faire l'objet d'un suivi et d'une évaluation sous la supervision d'un médecin à chaque séance de traitement afin de déterminer à quel moment le patient est cliniquement stable (voir Posologie/Mode d'emploi – Observation après l'administration).
Une altération à long terme des capacités cognitives et de la mémoire a été signalée lors de l'utilisation à long terme ou l'abus de kétamine. Ces effets n'ont pas augmenté au fil du temps et étaient réversibles après l'arrêt du traitement par la kétamine. Les études cliniques, y compris une étude clinique à long terme avec des patients traités en médiane pendant 45,8 mois (jusqu'à 79 mois), ont évalué l'effet de l'eskétamine en spray nasal sur la fonction cognitive au cours du temps; la performance cognitive est restée stable entre le début et la fin de l'étude.
Patients de ≥65 ans
Les expériences concernant l'efficacité et la sécurité de Spravato chez les patients de ≥65 ans sont limitées et l'utilisation de Spravato chez ces patients, en particulier en présence de comorbidités cardiovasculaires, doit être effectuée avec prudence (voir Études cliniques, Effets indésirables).
Dans les études d'homologation, 194 patients (12%) âgés de ≥65 ans ont été traités par Spravato. Dans le cadre d'une étude de 4 semaines en double aveugle, l'efficacité et la sécurité de Spravato en association avec un AD oral (n = 72) ont été comparées à celles d'un placebo administré par voie intranasale en association avec un AD oral (n = 66). Au cours de cette étude, 11,1% des patients traités par Spravato ont présenté une augmentation aiguë de la pression artérielle (systolique ≥180 mmHg ou diastolique ≥110 mmHg), contre 6,2% dans le groupe témoin. Il n'y avait pas de différence statistiquement significative au niveau du critère d'évaluation principal de l'efficacité (voir Propriétés/Effets – Efficacité clinique et Mises en garde et précautions – Effet sur la pression artérielle).
Effet sur l'aptitude à la conduite
Deux études ont été menées pour évaluer les effets de Spravato sur l'aptitude à la conduite (voir Pharmacodynamique – Effet sur l'aptitude à la conduite). Avant l'administration de Spravato, les patients doivent être informés de ne pas effectuer d'activités potentiellement dangereuses et nécessitant une vigilance et une coordination motrice totales, telles que la conduite d'un véhicule ou l'utilisation de machines, avant le lendemain matin et après un sommeil réparateur (voir Mises en garde et précautions – Troubles cognitifs et moteurs).
Effets sur la vessie
Des cas de cystite interstitielle ont été signalés chez des personnes ayant utilisé la kétamine comme drogue récréative ou à fortes doses et à long terme pour le traitement de douleurs chroniques. Dans les études cliniques menées avec l'eskétamine en spray nasal, les symptômes tels que la cystite, la douleur vésicale et la cystite interstitielle ont été évalués chez les participants. Aucune des études comprenant des traitements durant jusqu'à 79 mois n'a mis en évidence des cas de cystite interstitielle associée à l'eskétamine. Dans les études cliniques menées avec Spravato, les symptômes au niveau des voies urinaires inférieures (pollakiurie, dysurie, urgence mictionnelle, nycturie et cystite) étaient plus fréquents chez les patients traités par Spravato que chez ceux du groupe sous placebo.
Pendant le traitement par Spravato, les patients doivent être surveillés pour détecter tout symptôme éventuel affectant les voies urinaires et la vessie et, si cela est indiqué sur le plan clinique, doivent être adressés à un spécialiste.
Abus médicamenteux et dépendance
Abus
Avant de prescrire Spravato, le risque d'abus ou de mauvaise utilisation doit être déterminé pour chaque patient, et chaque patient qui reçoit Spravato doit être surveillé pendant le traitement pour détecter un éventuel développement de tels comportements ou états, y compris le comportement d'approvisionnement de substances. Les personnes ayant des antécédents d'abus de drogues ou de médicaments ou encore de dépendance peuvent présenter un risque accru d'abus ou de mauvaise utilisation de Spravato. Une évaluation soigneuse du rapport bénéfice/risque doit être réalisée avant de traiter des personnes ayant des antécédents d'abus ou de dépendance à des substances, y compris l'alcool.
Il a été rapporté que la kétamine, le mélange racémique d'arkétamine et d'eskétamine, est utilisée comme drogue d'abus. Dans le cadre d'une étude portant sur le potentiel d'abus chez des consommateurs de drogues récréatives multiples (n = 41), des doses uniques d'eskétamine en spray nasal (84 mg et 112 mg) et de kétamine par voie intraveineuse (perfusion de 0,5 mg/kg en 40 minutes), en tant que témoins positifs, ont entraîné un nombre de points (score) significativement plus élevé que le placebo pour l'évaluation subjective «J'aime cette substance» et pour d'autres indicateurs des effets subjectifs des médicaments et stupéfiants.
Dépendance
Une dépendance et une tolérance ont été signalées lors d'une utilisation à long terme de la kétamine. Les personnes présentant une dépendance à la kétamine ont rapporté des symptômes de sevrage tels qu'une forte envie de consommer la substance, de l'anxiété, des tremblements, des accès de transpiration et des palpitations. Il convient de prêter attention aux signes de dépendance lors du traitement par Spravato.
Insuffisance hépatique sévère
En raison d'une augmentation prévue de l'exposition et de l'absence d'expérience clinique, Spravato n'est pas recommandé chez les patients présentant une insuffisance hépatique classée Child Pugh C (sévère).
Une hépatotoxicité ayant été rapportée en lien avec l'utilisation de kétamine à long terme, la possibilité de cet effet pour une utilisation de Spravato à long terme ne peut pas être exclue.
Autres populations à risque
Spravato doit être utilisé avec prudence chez les patients présentant les tableaux cliniques mentionnés ci-après. Ces patients doivent être soigneusement évalués avant de prescrire Spravato; le traitement ne doit être instauré que si les bénéfices l'emportent sur les risques:
·Psychose (actuelle ou antécédents).
·Manie ou trouble bipolaire (actuels ou antécédents).
·Hyperthyroïdie insuffisamment contrôlée.
·Antécédents de lésion cérébrale, d'encéphalopathie hypertensive, de traitement intrathécal avec shunt ventriculaire ou d'autres symptômes associés à une pression intracrânienne accrue.
Patients n'ayant pas fait l'objet d'études cliniques
L'efficacité et la sécurité de Spravato n'ont pas été établies chez les populations de patients suivantes: patients présentant des antécédents de crises convulsives, patients atteints de maladies neurodégénératives (p.ex. maladie d'Alzheimer, démence vasculaire, maladie de Parkinson avec signes cliniques de déficience cognitive, patients présentant une déficience cognitive légère et patients présentant une hypertension non contrôlée [< 65 ans: PAS/PAD > 140/90 mmHg; ≥65 ans: PAS/PAD ≥150/90 mmHg]).
Grossesse
Sur la base des expérimentations animales réalisées avec la kétamine, la prise de Spravato pendant la grossesse peut être nuisible au fœtus (voir Grossesse, Allaitement).
InteractionsInteractions pharmacodynamiques
Agents dépresseurs du SNC
La sédation peut être renforcée lors d'une utilisation concomitante avec des agents dépresseurs du SNC (p.ex. benzodiazépines, opioïdes, alcool). Les symptômes de sédation doivent faire l'objet d'une surveillance étroite lors d'une utilisation concomitante de Spravato et d'agents dépresseurs du SNC.
Psychostimulants
La pression artérielle peut augmenter en cas d'utilisation concomitante de psychostimulants (p.ex. amphétamines, méthylphénidate, modafinil, armodafinil). La pression artérielle doit être étroitement surveillée lors d'utilisation concomitante de Spravato et de psychostimulants.
Inhibiteurs de monoamine oxydase (inhibiteurs de MAO)
La pression artérielle peut augmenter en cas d'utilisation concomitante d'inhibiteurs de monoamine oxydase [inhibiteurs de MAO] (p.ex. tranylcypromine, sélégiline, phénelzine). La pression artérielle doit être étroitement surveillée en cas d'utilisation concomitante de Spravato et d'inhibiteurs de MAO.
Interactions pharmacocinétiques
L'eskétamine est largement métabolisée dans le foie. La voie métabolique principale de l'eskétamine dans les microsomes hépatiques humains est la N-déméthylation en noreskétamine. Les principales enzymes du système du cytochrome P450 (CYP) pour la N-déméthylation de l'eskétamine sont le CYP2B6 et le CYP3A4 (voir Pharmacocinétique).
Données in vitro
L'eskétamine n'est pas un substrat du transporteur de la glycoprotéine P (P-gp; protéine de multirésistance 1), de la protéine de résistance au cancer du sein (BCRP) ou des transporteurs d'anions organiques (OATP) 1B1 ou OATP1B3. La noreskétamine n'est pas un substrat pour ces transporteurs ou pour les transporteurs d'anions organiques (OAT) 1, OAT3, ou encore les transporteurs de cations 1 ou 2 (OCT1 ou OCT2). L'eskétamine et la noreskétamine n'ont pas d'effet inhibiteur sur la P-gp, la BCRP, la MATE1 (Multidrug and Toxin Extrusion 1), la MATE2-K, l'OAT1 ou l'OAT3. L'eskétamine est un faible inhibiteur de l'OCT2; la pertinence clinique de cette inhibition n'est pas connue. La noreskétamine n'inhibe pas l'OCT2. L'eskétamine et la noreskétamine présentent un faible potentiel d'inhibition réversible ou dépendant du temps des enzymes du CYP (CYP1A2, 2B6, 2C8, 2C9, 2C19, 2D6 et 3A4). L'inhibition du CYP3A4 par la noreskétamine était dépendante du substrat et a été considérée comme étant cliniquement non pertinente. L'eskétamine et la noreskétamine n'inhibent pas les uridine diphosphate glucuronosyltransférases (UGT) 1A1 et 2B7.
Dans les hépatocytes humains, l'eskétamine et ses principaux métabolites circulants n'ont eu aucun effet inducteur sur le CYP1A2. In vitro, certains effets inducteurs de l'eskétamine sur le CYP3A4 et le CYP2B6 ont été observés dans les hépatocytes humains, mais n'ont pas entraîné d'interaction médicamenteuse cliniquement pertinente (voir Effet de Spravato sur d'autres médicaments).
Effet de Spravato sur d'autres médicaments
L'administration nasale de 84 mg d'eskétamine deux fois par semaine pendant 2 semaines a entraîné une diminution d'environ 16% de l'AUC∞ plasmatique moyenne du midazolam oral (dose unique de 6 mg), un substrat du CYP3A4 hépatique.
L'administration nasale de 84 mg d'eskétamine deux fois par semaine pendant 2 semaines n'a eu aucun effet sur l'AUC∞ plasmatique moyenne du bupropion oral (dose unique de 150 mg), un substrat du CYP2B6 hépatique.
Effet d'autres médicaments sur Spravato
Inhibiteurs des enzymes hépatiques
Le prétraitement de sujets sains par de la ticlopidine par voie orale (250 mg deux fois par jour pendant 9 jours avant le jour de l'administration d'eskétamine et le jour même), un inhibiteur de l'activité du CYP2B6 hépatique, n'a eu aucun effet sur le taux plasmatique maximal (Cmax) de l'eskétamine administrée sous forme de spray nasal. L'aire sous la courbe des concentrations plasmatiques d'eskétamine au cours du temps (AUC∞) a augmenté d'environ 29%. La demi-vie terminale de l'eskétamine n'a pas été affectée par le prétraitement par la ticlopidine.
Le prétraitement par la clarithromycine orale (500 mg deux fois par jour pendant 3 jours avant le jour de l'administration d'eskétamine et le jour même), un inhibiteur de l'activité du CYP3A4 hépatique, a entraîné une augmentation de la Cmax moyenne de l'eskétamine administrée par voie nasale d'environ 11% et de l'AUC∞ moyenne d'environ 4%. La demi-vie terminale de l'eskétamine n'a pas été affectée par le prétraitement par la clarithromycine.
Inducteurs des enzymes hépatiques
Le prétraitement par la rifampicine orale (600 mg par jour pendant 5 jours avant l'administration d'eskétamine), un inducteur puissant de l'activité de diverses enzymes CYP hépatiques, telles que le CYP3A4 et le CYP2B6, a réduit la Cmax moyenne et l'AUC∞ moyenne de l'eskétamine administrée en spray nasal d'environ 17% et 28% respectivement.
Autres préparations en spray nasal
L'utilisation de Spravato en association avec d'autres médicaments administrés par voie nasale a été évaluée dans le cadre des études d'interaction pharmacocinétique suivantes. Le prétraitement de sujets ayant des antécédents de rhinite allergique et une exposition antérieure aux pollens de graminées par l'oxymétazoline en spray nasal (2 pulvérisations d'une solution à 0,05%, 1 heure avant l'administration nasale d'eskétamine) a eu un effet mineur sur la pharmacocinétique de l'eskétamine.
Le prétraitement de sujets sains par administration nasale de furoate de mométasone (200 mcg par jour pendant 2 semaines, dernière dose de furoate de mométasone 1 heure avant l'administration nasale d'eskétamine) a eu un effet mineur sur la pharmacocinétique de l'eskétamine.
Grossesse, allaitementGrossesse
Il n'existe pas de données suffisantes concernant l'utilisation chez la femme enceinte.
Dans les expérimentations animales menées avec la kétamine, une tératogénicité et des effets neurotoxiques ont été observés chez les fœtus (voir Données précliniques). Un potentiel d'effets de l'eskétamine sur le développement fœtal ne peut être exclu. Spravato n'est pas recommandé pendant la grossesse et pour les femmes en âge de procréer, qui n'utilisent pas de contraception.
Afin d'éviter une exposition fœtale à l'eskétamine, les femmes en âge de procréer doivent recourir à une méthode de contraception hautement efficace, avant le traitement et jusqu'à 6 semaines après le dernier traitement par Spravato. Si une femme tombe enceinte pendant le traitement par Spravato, il faut interrompre le traitement par l'eskétamine et aviser la patiente le plus tôt possible du risque potentiel pour le fœtus, ainsi que des options cliniques/thérapeutiques.
Allaitement
Les risques de Spravato pendant l'allaitement n'ont pas été étudiés chez l'être humain. Les données issues d'expérimentations animales suggèrent un passage de l'eskétamine dans le lait maternel. Il faut alors décider soit de ne pas procéder au traitement par Spravato pendant l'allaitement, soit d'arrêter l'allaitement au début du traitement par Spravato, en tenant compte des bénéfices du traitement pour la mère et des bénéfices de l'allaitement pour le nourrisson (voir Données précliniques).
Effet sur l’aptitude à la conduite et l’utilisation de machinesSpravato a une influence importante sur l'aptitude à la conduite ou l'utilisation de machines. Dans les études cliniques, il a été rapporté que Spravato causait une somnolence, une sédation, des symptômes dissociatifs, des troubles de la perception, des vertiges oscillatoires et rotatoires et de l'anxiété (voir Effets indésirables). Avant l'administration de Spravato, les patients doivent être informés de ne pas effectuer d'activités potentiellement dangereuses nécessitant une attention et une coordination motrice totales, telles que la conduite d'un véhicule automobile ou l'utilisation de machines, avant le lendemain et après un sommeil réparateur (voir Mises en garde et précautions et Propriétés/Effets – Efficacité clinique).
Effets indésirablesCette section traite des effets indésirables. Les effets indésirables sont des événements indésirables pour lesquels un lien probable avec l'utilisation de l'eskétamine est présumé sur la base d'une évaluation complète des informations disponibles sur les événements indésirables. Un lien de causalité avec l'eskétamine ne peut pas être établi de manière fiable dans les cas individuels. De plus, comme les études cliniques sont menées dans des conditions très différentes, la fréquence des effets indésirables observés dans les études cliniques d'un médicament ne peut être directement comparée à celle observée dans les études cliniques d'un autre médicament et peut ne pas refléter les fréquences observées dans la pratique clinique.
Résumé du profil de sécurité
Effets indésirables observés dans les études lors de DRT
La sécurité de Spravato a été évaluée chez 1709 patients ayant reçu un diagnostic de DRT (patients atteints de trouble dépressif majeur [TDM] et non-répondeurs au traitement par au moins deux AD oraux à une posologie et sur une durée adéquates pendant l'épisode actuel de TDM) dans le cadre de cinq études de phase III (3 à court terme et 2 à long terme) et d'une étude de recherche de dose de phase II. Parmi les patients traités par l'eskétamine dans les études terminées de phase III, 479 (29,9%) ont reçu un traitement pendant au moins 6 mois et 178 (11,1%) pendant au moins 12 mois.
Effets indésirables chez les patients atteints de TDM présentant des pensées ou des comportements suicidaires aigus (indication «Traitement aigu de courte durée d'une urgence psychiatrique dans le cadre d'un TDM»)
La sécurité de Spravato a été évaluée chez 262 patients ayant reçu un diagnostic de TDM et présentant des pensées suicidaires avec intention suicidaire, provenant de deux études de phase 3 et d'une étude de phase 2. Dans l'ensemble, le profil de sécurité de Spravato dans ce programme clinique a été généralement similaire à celui observé dans les études sur la DRT.
Effets indésirables fréquents
Les effets indésirables les plus fréquemment observés chez les patients sous traitement par Spravato plus un AD oral (incidence ≥10% et supérieure à celle observée avec un AD oral plus un placebo en spray nasal) ont été la dissociation, les vertiges oscillatoires, les nausées, la sédation, les céphalées, la dysgueusie, l'hypoesthésie, les vertiges rotatoires, l'anxiété, l'élévation de la pression artérielle et les vomissements. La plupart de ces effets indésirables ont été légers ou moyennement sévères, ont été rapportés le jour de l'administration et ont régressé le jour même.
Effets indésirables cités comme étant une raison de l'arrêt du traitement
Dans les études de courte durée menées auprès de patients adultes de < 65 ans (données résumées tirées de TRD3001/TRD3002) et de ≥65 ans atteints de DRT (TRD3005), la proportion de patients traités par Spravato plus un AD oral ayant interrompu le traitement en raison d'un événement indésirable était de 4,6% chez les adultes de < 64 ans et de 5,6% chez les patients de ≥65 ans, contre 1,4% chez les adultes de < 64 ans et 3,1% chez les patients de ≥65 ans traités par un AD oral et un placebo en spray nasal. Dans une étude à long terme, les taux d'abandon en raison d'événements indésirables ont été semblables chez les patients traités par Spravato plus un AD oral et chez les patients recevant un AD oral plus un placebo en spray nasal, c'est-à-dire respectivement de 2,6% et 2,1%. Dans toutes les études de phase 3, les effets indésirables ayant entraîné l'arrêt du traitement par Spravato chez plus de 2 patients (> 0,1%) ont été les suivants (classés par fréquence): anxiété (1,2%), dépression (0,9%), élévation de la pression artérielle (0,6%), vertiges oscillatoires (0,6%), pensées suicidaires (0,5%), dissociation (0,4%), nausées (0,4%), vomissements (0,4%), céphalées (0,3%), faiblesse musculaire (0,3%), vertiges rotatoires (0,2%), hypertension artérielle (0,2%), crises de panique (0,2%) et sédation (0,2%).
Dans les études combinées de phase 3 SUI3001/SUI3002, des événements indésirables ayant entraîné l'arrêt du traitement sont survenus chez 6,2% (14/227) des patients avec un diagnostic de TDM et présentant des pensées suicidaires avec intention suicidaire (indication «Traitement aigu de courte durée d'une urgence psychiatrique dans le cadre d'une dépression majeure») dans le groupe Spravato + SOC, et chez 3,6% (8/225) des patients dans le groupe placebo + SOC. Les événements indésirables ayant entraîné l'arrêt du traitement chez > 1 participant dans le groupe Spravato + SOC ont été les suivants: dissociation, élévation de la pression artérielle, trouble de la dépersonnalisation/déréalisation et nausées.
Liste des effets indésirables
Les effets indésirables sont présentés par classes de systèmes d'organes MedDRA et par fréquence, selon la convention suivante: très fréquents (≥1/10), fréquents (≥1/100 à < 1/10), occasionnels (≥1/1000 à < 1/100), rares (≥1/10 000 à < 1/1000), très rares (< 1/10 000) et fréquence inconnue (ne peut être estimée sur la base des données disponibles).a
Affections psychiatriques
Très fréquents: dissociation (41,7%)b, anxiété (13,7%)b.
Fréquents: humeur euphorique, tension psychiqueb.
Affections du système nerveux
Très fréquents: dysgueusie (17,8%)b, vertiges oscillatoires (37,9%)b, sédation (25,9%)b, hypoesthésie (16,3%)b, céphalées (23,7%)b.
Fréquents: altération mentaleb, tremblementsb, léthargieb, dysarthrieb.
Occasionnels: nystagmus.
Affections de l'oreille et du labyrinthe
Très fréquents: vertiges rotatoires (16,3%)b.
Affections cardiaques
Fréquents: tachycardieb.
Affections respiratoires, thoraciques et médiastinales
Fréquents: irritation de la gorgeb, affections nasalesb.
Rares: dépression respiratoire.
Affections gastro-intestinales
Très fréquents: nausées (27%), vomissements (10,7%).
Fréquents: sécheresse buccale.
Occasionnels: hypersialorrhée.
Affections de la peau et du tissu sous-cutané
Fréquents: hyperhidroseb.
Affections du rein et des voies urinaires
Fréquents: pollakiurieb, dysurie.
Troubles généraux et anomalies au site d'administration
Fréquents: sensation anormale, sensation d'ivresse, asthénie.
Occasionnels: trouble de la démarche.
Investigations
Très fréquents: pression artérielle élevée (13,1%)b.
Affections vasculaires
Occasionnels: hypotension.
a Aucun effet indésirable ne correspondait aux fréquences «très rares» ou «inconnues».
b Les termes suivants ont été combinés:
La dissociation comprend: dissociation; trouble de la dépersonnalisation/déréalisation; déréalisation; trouble dissociatif; flash-back (revivre des scènes du passé); hallucination; hallucination auditive; hallucination visuelle; illusion; hallucination somatique; hallucinations, mixtes; hyperacousie; acouphènes; diplopie; vision trouble; troubles oculaires; photophobie; altération de la vue; dysesthésie; dysesthésie orale; paresthésie; paresthésie orale; paresthésie pharyngée; perception modifiée du temps; rêveries; perceptions délirantes; sensation de chaleur; sensation de froid; sensation de température corporelle modifiée.
L'anxiété comprend: anxiété; anxiété anticipatoire; trouble anxieux; trouble anxieux généralisé; agitation; peur; nervosité; tension interne; crise de panique; trouble panique; réaction de panique; sensation de nervosité; irritabilité; tremblements psychogènes; hyperactivité psychomotrice.
La tension psychique comprend: tension psychique; pleurs, dysphorie.
Les vertiges oscillatoires comprennent: vertiges oscillatoires; étourdissement positionnel; vertiges liés à la procédure; vertiges liés à l'effort.
La sédation comprend: sédation; somnolence; altération de l'état de conscience; état de conscience atténué; hypersomnie; stupeur.
Les céphalées comprennent: céphalées; céphalées sinusales.
La dysgueusie comprend: dysgueusie; hypogueusie.
L'hypoesthésie comprend: hypoesthésie; hypoesthésie orale; hypoesthésie dentaire; hypoesthésie pharyngée; hypoesthésie intranasale.
La léthargie comprend: léthargie; fatigue; indifférence; retard psychomoteur.
L'altération mentale comprend: altération mentale; état de confusion; trouble de l'attention.
La dysarthrie comprend: dysarthrie; trouble du langage; élocution lente.
Les tremblements comprennent: tremblements; tremblements d'action.
Les sensations vertigineuses (vertiges rotatoires) comprennent: sensations vertigineuses; vertige positionnel.
La tachycardie comprend: tachycardie sinusale; tachycardie; fréquence cardiaque élevée; extrasystoles.
Les affections nasales comprennent: gêne dans le nez; formation de croûtes dans le nez; sécheresse du nez; démangeaisons dans le nez.
L'irritation de la gorge comprend: irritation de la gorge; douleur oropharyngée.
L'hyperhidrose comprend: hyperhidrose; sueurs froides.
La pollakiurie comprend: pollakiurie; trouble de la miction; urgence mictionnelle.
La pression artérielle élevée comprend: pression artérielle élevée; pression artérielle systolique élevée; pression artérielle diastolique élevée; hypertension; cardiopathie hypertensive; crise hypertensive.
Description de certains effets indésirables
Sécurité à long terme
La sécurité de Spravato plus AD oral à long terme a été évaluée dans une étude d'extension de phase 3 multicentrique, en ouvert (TRD3008) menée auprès de 1148 patients adultes présentant une DRT, ce qui correspond à 3777 patients-années d'exposition. En médiane, les patients ont été traités par Spravato pendant 45,8 mois (jusqu'à 79 mois), 63% des patients ayant été traités pendant au moins 3 ans et 28% des patients pendant 5 ans. Le profil de sécurité de l'eskétamine a correspondu au profil de sécurité connu observé dans les études cliniques pivots. Aucun nouveau problème en matière de sécurité n'a été constaté.
Dissociation/altération des perceptions
La dissociation a été l'un des effets psychologiques les plus fréquents de l'eskétamine, y compris une altération de la perception du temps et de l'espace ainsi que des illusions, une déréalisation et une dépersonnalisation. Ces effets indésirables ont été signalés comme étant passagers et spontanément résolutifs et sont survenus le jour de l'administration. La dissociation a été évaluée à l'aide de rapports d'événements indésirables et du questionnaire CADSS (Clinician-Administered Dissociative States Scale, échelle gérée par le clinicien visant à mesurer les états dissociatifs). Un score CADSS total de plus de 4 indique la présence de symptômes dissociatifs et l'augmentation à un score de 4 ou plus est survenue plus fréquemment chez les patients traités par l'eskétamine que dans le groupe sous placebo dans le cadre des études à court terme. L'incidence de la dissociation (score CADSS total > 4) se situait entre 61% et 69% chez les adultes de < 65 ans traités par Spravato, contre 8% dans le groupe témoin. L'incidence de la dissociation (score CADSS total > 4) était de 75% chez les patients de ≥65 ans traités par Spravato, contre 14% dans le groupe témoin. Les symptômes de dissociation ont régressé dans les 2 heures suivant l'administration. L'incidence des dissociations graves était inférieure à 4%.
Sédation/somnolence
Les effets indésirables de type sédation et somnolence ont majoritairement été de sévérité légère ou modérée, sont survenus le jour de l'administration et ont spontanément régressé le jour même. La sédation a été évaluée sur la base de rapports d'événements indésirables et à l'aide de l'échelle MOAA/s (Modified Observer's Alertness/Sedation). Sur l'échelle MOAA/s, 5 signifie «réagit promptement à une stimulation vocale utilisant son nom et un ton normal», et 0 signifie «absence de réaction après une pression douloureuse exercée sur le trapèze». Toute diminution de la valeur sur l'échelle MOAA/s par rapport au niveau observé avant l'administration de la dose a été considérée comme une indication de sédation, et une telle diminution s'est produite dans les études à court terme chez un plus grand nombre de patients sous eskétamine que dans le groupe sous placebo. L'incidence de la sédation (score MOAA/s total < 5) se situait entre 50% et 61% chez les adultes de < 65 ans traités par Spravato et était de 49% chez les patients de ≥65 ans traités par Spravato. Parmi les patients, 0,3% ont perdu connaissance (score MOAA/s total = 0). Les effets sédatifs ont généralement régressé dans l'heure et demie suivant l'administration. La proportion de patients présentant une somnolence est restée relativement stable au cours du temps pendant le traitement à long terme. Dans les cas de sédation, aucun symptôme de détresse respiratoire n'a été observé et les paramètres hémodynamiques (signes vitaux et saturation en oxygène) sont restés dans l'intervalle normal.
Troubles cognitifs
Dans les études à court terme, le traitement par Spravato plus un AD oral chez les patients adultes atteints de DRT n'a eu aucune incidence sur les aspects cognitifs évalués et n'a été associé à aucune modification systématique de la cognition chez les patients âgés. Dans les études à long terme, en accord avec ces observations, la performance dans chacun des tests cognitifs a présenté une légère amélioration ou est restée stable lors de chaque phase de traitement, par rapport à la valeur initiale (valeur de référence).
Les effets cognitifs à long terme de Spravato n'ont pas été évalués au-delà d'une année.
Ralentissement du temps de réaction
Dans le sous-groupe de patients âgés (≥65 ans) de l'étude à long terme ouverte sur la sécurité, un ralentissement du temps de réaction a été observé à partir de la semaine 20 et jusqu'à la fin de l'étude; la performance dans d'autres tests cognitifs est cependant restée stable.
Modifications de la pression artérielle
Spravato entraîne une augmentation de la pression artérielle systolique et/ou diastolique à toutes les posologies recommandées. L'augmentation de la pression artérielle est maximale environ 40 minutes après l'administration de Spravato et dure environ 4 heures. Au cours des quatre premières semaines de traitement, 8% à 17% des patients traités par Spravato, et 1% à 3% des patients traités par le placebo ont présenté une augmentation supérieure à 40 mmHg de la pression artérielle systolique et/ou une augmentation de 25 mmHg de la pression artérielle diastolique dans l'heure et demie suivant l'administration de Spravato. Une augmentation significative de la pression artérielle peut survenir après chaque administration, même si les administrations antérieures de Spravato n'ont présenté que des effets mineurs sur la pression artérielle (voir Mises en garde et précautions). Le tableau 2 présente la fréquence des augmentations marquées de la pression artérielle dans les études cliniques menées sur le traitement de la DRT.
Tableau 2: Élévations de la pression artérielle dans des études à court terme en double aveugle, randomisées et contrôlées, menées avec Spravato + un AD oral par rapport au placebo en spray nasal + un AD oral dans le traitement de la DRT
|
|
Patients < 65 ans
|
Patients ≥65 ans
| |
|
Spravato
+ AD oral
N = 346
|
Placebo
+ AD oral
N = 222
|
Spravato
+ AD oral
N = 72
|
Placebo
+ AD oral
N = 65
| |
Pression artérielle systolique
| |
≥180 mmHg
|
9 (3%)
|
---
|
2 (3%)
|
1 (2%)
| |
Élévation ≥40 mmHg
|
29 (8%)
|
1 (0,5%)
|
12 (17%)
|
1 (2%)
| |
Pression artérielle diastolique
| |
≥110 mmHg
|
13 (4%)
|
1 (0,5%)
|
---
|
---
| |
Élévation ≥25 mmHg
|
46 (13%)
|
6 (3%)
|
10 (14%)
|
2 (3%)
|
En cas d'élévation persistante de la pression artérielle, des mesures médicales doivent immédiatement être mises en œuvre. Les patients présentant des symptômes de crise hypertensive (p.ex. douleurs thoraciques, essoufflement) ou d'encéphalopathie hypertensive (p.ex. céphalées sévères et soudaines, troubles visuels, crises convulsives, troubles de la conscience ou déficits neurologiques focaux) doivent être immédiatement adressés au service des urgences.
Tolérance nasale et odorat
Lors des différentes études, l'examen du nez n'a révélé aucun résultat pathologique chez la grande majorité des patients traités par l'eskétamine. Chez les patients présentant des résultats pathologiques de l'examen du nez (y compris la sécrétion nasale, la formation de croûtes ou une rougeur du nez), tous les événements étaient de nature légère, à l'exception de quelques résultats de sévérité moyenne. Les symptômes nasaux d'intensité modérée ou élevée les plus fréquemment signalés (signalés par au moins 5% des patients) après l'administration du médicament à l'étude dans le cadre des études de phase III ont été le syndrome d'écoulement post-nasal (syndrome sinobronchique), la dysgueusie et l'obstruction nasale. Parmi les autres symptômes nasaux d'intensité modérée ou élevée figuraient l'écoulement nasal, la toux, la sécheresse nasale et les éternuements. De plus, l'odorat a été évalué au cours de l'étude; pendant la phase d'entretien en double aveugle de l'étude TRD3003, il n'y a eu aucune différence entre les patients traités par Spravato plus un AD oral et ceux traités par un AD oral plus placebo en spray nasal.
Poids corporel
Spravato n'a eu aucun effet cliniquement pertinent sur le poids corporel, ni lors d'une administration à court terme ni lors d'une administration à long terme.
Paramètres biologiques
Dans le cas de Spravato, il n'y a pas eu d'association avec des modifications cliniquement pertinentes des paramètres de chimie clinique du sérum, de l'hématologie ou du bilan urinaire.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageAucun cas de surdosage n'a été rapporté à ce jour dans les études cliniques menées avec Spravato. Le risque de surdosage de Spravato par le patient est minime, grâce à la conception du spray nasal et à son administration sous la supervision d'un médecin (voir Posologie/Mode d'emploi).
Signes et symptômes
L'expérience issue des études cliniques menées avec une dose d'eskétamine en spray nasal supérieure à la dose maximale recommandée de 84 mg est limitée. La dose unique la plus élevée d'eskétamine en spray nasal testée sur des volontaires sains était de 112 mg et n'a entraîné aucun signe de toxicité et/ou aucune conséquence clinique indésirable. Toutefois, par rapport à la posologie recommandée, les effets indésirables, notamment des vertiges oscillatoires, une transpiration accrue, une somnolence, une hypoesthésie, une sensation anormale, des nausées et des vomissements, sont survenus plus fréquemment après l'administration de 112 mg d'eskétamine en spray nasal.
Traitement
Il n'existe pas d'antidote spécifique pour un surdosage d'eskétamine. En cas de surdosage, il faut envisager la possibilité que plusieurs médicaments jouent un rôle causal. Il est conseillé de contacter un centre antipoison pour obtenir les dernières recommandations concernant le traitement d'un surdosage. Le traitement d'un surdosage de Spravato doit comprendre le traitement des symptômes cliniques et la surveillance des fonctions essentielles. La surveillance étroite et le suivi doivent être poursuivis jusqu'à ce que le patient se remette des symptômes.
Propriétés/EffetsCode ATC
N06AX27
Mécanisme d'action
L'eskétamine, l'énantiomère S de la kétamine racémique, est un antidépresseur ayant un nouveau mécanisme d'action. Il s'agit d'un antagoniste non sélectif et non compétitif du récepteur Nméthyl-Daspartate (NMDA), un récepteur ionotrope du glutamate.
On sait que les facteurs étiologiques soupçonnés de contribuer à la dépression, notamment le stress et d'autres conditions, entraînent une perturbation structurelle et fonctionnelle des synapses dans les régions du cerveau impliquées dans la régulation de l'humeur et du comportement émotionnel. Selon les informations présentes dans la littérature, l'eskétamine provoque une augmentation temporaire de la libération de glutamate en exerçant un effet antagoniste sur le récepteur NMDA, ce qui entraîne une stimulation accrue du récepteur de l'acide α-amino-3-hydroxy-5-méthyl-4-isoxazole-propionique (AMPAR) et par la suite une production accrue de signaux neurotrophiques, qui restaurent à leur tour la fonction synaptique dans ces zones du cerveau. Contrairement à d'autres traitements antidépresseurs, les récepteurs des monoamines, GABA ou opioïdes ne sont pas directement impliqués dans l'effet antidépresseur principal de l'eskétamine.
Pharmacodynamique
Voir sous Mécanisme d'action.
Efficacité clinique
L'efficacité et la sécurité de Spravato en spray nasal ont été initialement évaluées au cours de cinq études cliniques de phase 3 (TRD3001, TRD3002, TRD3003, TRD3004 et TRD3005) menées chez des patients adultes (de 18 à 86 ans) atteints de DRT qui répondaient aux critères du TDM selon le DSM-5 et qui n'ont pas répondu à au moins deux antidépresseurs oraux à une posologie et sur une durée adéquates pendant l'épisode dépressif actuel (non-répondeurs). 1833 patients adultes ont été inclus dans les études, parmi lesquels 1601 ont reçu Spravato. Par ailleurs, 202 patients ont été randomisés dans l'étude de phase 2 TRD2005 au Japon (parmi lesquels 122 patients ont reçu Spravato), 252 patients ont été randomisés dans l'étude de phase 3 TRD3006 principalement en Chine (parmi lesquels 126 patients ont reçu Spravato), et 676 patients ont été randomisés dans l'étude de phase 3 TRD3013 (parmi lesquels 334 patients ont reçu Spravato).
Dépression résistante au traitement (DRT) – études à court terme
Spravato a été évalué dans trois études de phase III de courte durée (4 semaines), randomisées, en double aveugle, multicentriques et contrôlées contre comparateur actif, menées chez des patients atteints de DRT. Les études TRANSFORM-1 (TRD3001) et TRANSFORM-2 (TRD3002) ont été réalisées chez des adultes (de 18 à < 65 ans) et l'étude TRANSFORM-3 (TRD3005) chez des adultes de ≥65 ans. Les patients des études TRD3001 et TRD3002 ont commencé, au jour 1, le traitement par Spravato à 56 mg en association avec un AD oral nouvellement initié pris quotidiennement ou un placebo en spray nasal en association avec un AD oral nouvellement initié pris quotidiennement. Les doses de Spravato ont été maintenues à 56 mg ou ajustées à 84 mg ou en correspondance au placebo en spray nasal, administrés deux fois par semaine durant une phase d'induction en double aveugle de 4 semaines. Les doses de Spravato de 56 mg et 84 mg ont été administrées selon une posologie fixe dans l'étude TRD3001 et une posologie flexible dans l'étude TRD3002. Dans l'étude TRD3005, les patients âgés de ≥65 ans ont commencé au jour 1, le traitement par Spravato à 28 mg en association avec un AD oral nouvellement initié, pris quotidiennement, un placebo en spray nasal en association avec un AD oral nouvellement initié, pris quotidiennement. Au cours de la phase d'induction de 4 semaines en double aveugle, la dose de Spravato ou du placebo en spray nasal a été ajustée à une dose plus élevée de 56 mg ou 84 mg, deux fois par semaine. Dans les études à posologie flexible (TRD3002 et TRD3005), la dose de Spravato a été ajustée à une dose plus élevée sur la base du jugement clinique, mais pouvait également être ajustée à une dose inférieure en fonction de la tolérance. Dans toutes les études, un traitement ouvert par un AD oral (IRSN: duloxétine, venlafaxine retard; ISRS: escitalopram, sertraline) a été nouvellement initié au jour 1. Le choix du traitement AD oral nouvellement initié a été fait par le médecin investigateur en fonction des antécédents de traitement individuels du patient. Dans toutes les études à court terme, le critère d'efficacité principal était la variation du score MADRS total, entre le début de l'étude (valeur de référence) et le jour 28.
Les caractéristiques démographiques et les caractéristiques liées à la maladie des patients à l'inclusion dans les études TRD3002, TRD3001 et TRD3005 sont présentées dans le tableau 3.
Tableau 3: Caractéristiques démographiques à l'inclusion des études TRD3002, TRD3001 et TRD3005 (ensembles d'analyses complets)
|
|
Étude TRD3002
(N = 223)
|
Étude TRD3001
(N = 342)
|
Étude TRD3005
(N = 137)
| |
Âge, années
| |
Médiane (fourchette)
|
47,0 (19; 64)
|
47,0 (18; 64)
|
69,0 (65; 86)
| |
Sexe, N (%)
| |
Masculin
|
85 (38,1%)
|
101 (29,5%)
|
52 (38,0%)
| |
Féminin
|
138 (61,9%)
|
241 (70,5%)
|
85 (62,0%)
| |
Appartenance ethnique, N (%)
| |
Blanc
|
208 (93,3%)
|
262 (76,6%)
|
130 (94,9%)
| |
Noir ou Afro-Américain
|
11 (4,9%)
|
19 (5,6%)
|
--
| |
Traitement AD oral antérieur sans réponse thérapeutique (c.àd. échec du traitement)
| |
Nombre de traitements AD antérieurs, N (%)
| |
2
|
136 (61,0%)
|
167 (48,8%)
|
68 (49,6%)
| |
3 ou plus
|
82 (36,8%)
|
167 (48,8%)
|
58 (42,3%)
| |
AD oral nouvellement initié le jour de la randomisation, N (%)
| |
IRSN
|
152 (68,2%)
|
196 (57,3%)
|
61 (44,5%)
| |
ISRS
|
71 (31,8%)
|
146 (42,7%)
|
76 (55,5%)
| |
Abandon de l'étude (quelle que soit la raison), n/N (%)
|
30/227 (13,2%)
|
31/346 (9,0%)
|
16/138 (11,6%)
|
Dans l'étude TRD3002 à posologie flexible, 67% des patients randomisés dans le groupe Spravato ont reçu une dose de 84 mg au jour 28. Dans l'étude TRD3002, Spravato associé à un AD oral nouvellement initié a présenté une supériorité statistique par rapport au placebo en spray nasal associé à un AD oral nouvellement initié [IRSN: duloxétine, venlafaxine retard; ISRS: escitalopram, sertraline] (tableau 4). De plus, une réduction des symptômes a déjà été observée 24 heures après l'utilisation.
Dans l'étude TRD3001, l'effet thérapeutique (défini comme la variation du score MADRS total par rapport à la valeur initiale à la fin de la période d'induction de 4 semaines) de Spravato 84 mg associé à un AD oral nouvellement initié n'a pas atteint le seuil de signification statistique par rapport au placebo en spray nasal associé à un AD oral (IRSN: duloxétine, venlafaxine retard; ISRS: escitalopram, sertraline) (tableau 4).
Dans l'étude TRD3005, 64% des patients randomisés traités par Spravato ont reçu une dose de 84 mg au jour 28, 25% une dose de 56 mg et 10% une dose de 28 mg. Dans l'étude TRD3005, l'effet thérapeutique (défini comme la variation du score MADRS total par rapport à la valeur initiale à la fin de la période d'induction de 4 semaines) de Spravato associé à un AD oral nouvellement initié n'a pas atteint le seuil de signification statistique par rapport au placebo en spray nasal associé à un AD oral [IRSN: duloxétine, venlafaxine retard; ISRS: escitalopram, sertraline] (tableau 4). Les analyses de sous-groupes indiquent une efficacité réduite dans le groupe des patients de plus de 75 ans.
Tableau 4: Résultats du critère d'efficacité principal pour la variation du score MADRS total après la semaine 4, dans les études cliniques (ANCOVA LOCF)
|
N° de l'étude
|
Groupe de traitement§
|
Nombre de patients
|
Valeur initiale moyenne (SD)
|
Variation de la LSM à la fin de la semaine 4, par rapport à la valeur initiale (SE)
|
Différence entre les LSM (IC à 95%)†
|
Valeur de p bilatérale
| |
TRD3001
|
Spravato 56 mg + AD oral
|
115
|
37,4 (4,8)
|
-18,7 (1,3)
|
-4,1
(-7,5; -0,6)#
|
N/Aδ
| |
Spravato 84 mg + AD oral
|
114
|
37,8 (5,6)
|
-17,3 (1,3)
|
-2,0
(-5,5; 1,4)#
|
0,250
| |
Placebo en spray nasal + AD oral
|
113
|
37,5 (6,2)
|
-14,8 (1,3)
|
|
| |
TRD3002
|
Spravato (56 mg ou 84 mg) + AD oral
|
114
|
37,0 (5,7)
|
-18,0 (1,3)
|
-3,5
(-6,7; -0,3)‡
|
0,034‡
| |
Placebo en spray nasal + AD oral
|
109
|
37,3 (5,7)
|
-14,5 (1,3)
|
|
| |
TRD3005 (≥65 ans)
|
Spravato (28 mg, 56 mg ou 84 mg) + AD oral
|
72
|
35,5 (5,9)
|
-10,9 (1,7)
|
-3,6
(-7,2; -0,03)#
|
0,052
| |
Placebo en spray nasal + AD oral
|
65
|
34,8 (6,4)
|
-6,9 (1,7)
|
|
| |
SD = écart type (Standard Deviation), SE = erreur type (Standard Error), LSM = moyenne des moindres carrés (Least Square Means), IC = intervalle de confiance, AD = antidépresseur
§ Eskétamine ou placebo par voie nasale; AD oral = standard (un AD nouvellement initié)
† Différence (Spravato + AD oral moins placebo en spray nasal + AD oral) entre les variations de la LSM par rapport à la valeur initiale
‡ Groupe de traitement qui était supérieur de manière statistiquement significative au traitement par placebo en spray nasal + AD oral
# Estimateur non biaisé de la médiane (c.àd. combinaison pondérée des LSM de la différence par rapport au placebo en spray nasal + AD oral) et intervalle de confiance à 95% flexible.
δ Comme 84 mg n'était pas statistiquement significatif, la valeur de p pour la comparaison Spravato 56 mg + AD oral versus placebo *AD oral n'est pas indiquée en raison de la hiérarchie des tests.
|
Évolution de la réponse au traitement au cours du temps
Dans l'étude TRD3002, un effet antidépresseur de Spravato avec une réduction des symptômes de dépression était déjà observé dans les 24 heures suivant l'administration de la première dose. Au cours des semaines qui ont suivi, une amélioration progressive a été observée et l'effet antidépresseur complet de Spravato a été atteint au jour 28. La variation moyenne du score MADRS total pour Spravato à dose flexible (56 mg ou 84 mg) plus AD oral était constamment supérieure à tous les temps de mesure (semaines 1, 2, 3 et 4) à celle de l'AD oral plus placebo administré par voie nasale. Au jour 28, 67% des patients randomisés traités par Spravato ont reçu 84 mg. Un effet de traitement uniforme a été observé dans le cadre des études TRD3001 et TRD3005.
Réponse thérapeutique et taux de rémission
La réponse thérapeutique a été définie comme une réduction du score MADRS total ≥50% par rapport à la valeur initiale (valeur de référence) pendant la phase d'induction. En se basant sur la réduction du score MADRS total par rapport à la valeur initiale, la proportion de patients des études TRD3001, TRD3002 et TRD3005 qui ont présenté une réponse au traitement par Spravato plus un AD oral était plus élevée qu'avec un AD oral plus placebo en spray nasal, pendant l'ensemble de la phase d'induction de 4 semaines en double aveugle (tableau 5).
Une rémission a été définie comme un score MADRS total ≤12. À la fin de la phase d'induction de 4 semaines en double aveugle, la proportion de patients en rémission traités par Spravato plus un AD oral était plus élevée que celle des patients traités par un AD oral plus placebo en spray nasal dans chacune des trois études (tableau 5).
Tableau 5: Taux de réponse et de rémission dans les études cliniques de 4 semaines sur la base des données LOCF
|
N° de l'étude
|
Groupe de traitement§
|
Nombre de patients (%)
| |
Taux de réponse†
|
Taux de rémission‡
| |
24 heures
|
Semaine 1
|
Semaine 2
|
Semaine 3
|
Semaine 4
|
Semaine 4
| |
TRD3001
|
Spravato 56 mg + AD oral
|
20
(19,0%)
|
21
(18,3%)
|
30
(26,1%)
|
52
(45,2%)
|
61
(53,0%)
|
40
(34,8%)
| |
Spravato 84 mg + AD oral
|
17
(16,3%)#
|
16
(14,3%)
|
26
(23,2%)
|
35
(31,0%)
|
54
(47,8%)
|
40
(35,4%)
| |
AD oral + placebo en spray nasal
|
8
(7,9%)
|
5
(4,4%)
|
15
(13,3%)
|
27
(23,9%)
|
42
(37,2%)
|
33
(29,2%)
| |
TRD3002
|
Spravato 56 mg ou 84 mg + AD oral
|
18
(16,5%)
|
15
(13,4%)
|
29
(25,9%)
|
54
(48,2%)
|
71
(63,4%)
|
54
(48,2%)
| |
AD oral + placebo en spray nasal
|
11
(10,8%)
|
13
(11,9%)
|
23
(21,1%)
|
36
(33,0%)
|
54
(49,5%)
|
33
(30,3%)
| |
TRD3005
(≥65 ans)
|
Spravato 28 mg, 56 mg ou 84 mg + AD oral
|
NA
|
4
(6,1%)
|
4
(5,6%)
|
9
(12,7%)
|
17
(23,9%)
|
11
(15,5%)
| |
AD oral + placebo en spray nasal
|
NA
|
3
(4,8%)
|
8
(12,5%)
|
10
(15,6%)
|
8
(12,5%)
|
4
(6,3%)
| |
AD = antidépresseur; NA = aucune donnée (not available)
§ Spravato ou placebo administré par voie nasale; AD oral = traitement standard (AD nouvellement initié)
† Une réponse a été définie comme une réduction du score MADRS total ≥50% par rapport à la valeur initiale
‡ Une rémission a été définie comme un score MADRS total ≤12
# La première dose était Spravato 56 mg + AD oral
|
Données à long terme
Dépression résistante au traitement (DRT) – études à long terme
Étude TRD3003 (SUSTAIN-1) - Étude sur la prévention des récidives
SUSTAIN-1 (TRD3003) était une étude à long terme randomisée, en double aveugle, multicentrique, en groupes parallèles avec contrôle actif portant sur la prévention des récidives. Au total, 705 patients ont été inclus dans l'étude, dont 437 ont été recrutés directement, 150 patients ont été inclus à partir de l'étude TRD3001 et 118 patients à partir de l'étude TRD3002. Les patients directement inclus dans l'étude ont été traités par Spravato (56 mg ou 84 mg deux fois par semaine) plus un AD oral pendant une phase d'induction ouverte (sans insu) de 4 semaines. Les patients qui ont répondu au traitement [diminution du score MADRS total de ≥50% par rapport au score initial (valeur de référence)] ont poursuivi le traitement par Spravato plus un AD oral pendant une phase d'optimisation de 12 semaines. À la fin de la phase d'induction ouverte, 52% des patients étaient en rémission (score MADRS total ≤12) et 66% des patients étaient répondeurs (amélioration de ≥50% du score MADRS total). Au total, 455 patients traités par l'eskétamine ont entamé la phase ultérieure d'optimisation; les patients en rémission stable ou présentant une réponse stable ont été randomisés pour soit poursuivre le traitement par Spravato, soit arrêter le traitement par Spravato et passer au placebo en spray nasal. Après les 16 premières semaines de traitement par Spravato plus un AD oral, 176 patients (39%) étaient en rémission stable et 121 patients (27%) présentaient une réponse stable (mais n'étaient pas en rémission stable). Une rémission stable a été définie comme un score MADRS total ≤12 pendant au moins 3 des 4 dernières semaines de la phase d'optimisation et une réponse stable a été définie comme la diminution du score MADRS total de ≥50% par rapport à la valeur initiale au cours des 2 dernières semaines de la phase d'optimisation, mais sans rémission stable.
Les valeurs initiales (valeurs de référence) des données démographiques et des caractéristiques de la maladie des patients randomisés dans la phase d'entretien en double aveugle étaient comparables dans les deux groupes; l'âge médian des patients était de 48 ans (19-64 ans), 66% étaient des femmes et 90% étaient d'origine caucasienne.
Rémission stable
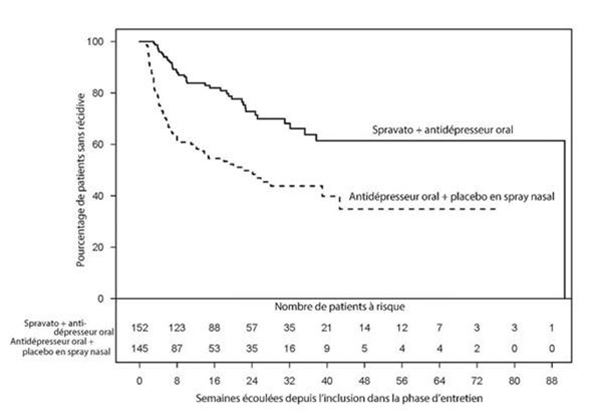
Chez les patients en rémission stable qui ont poursuivi le traitement par Spravato plus un AD oral, le délai jusqu'à une récidive des symptômes de dépression a été, selon les statistiques, significativement plus long que chez les patients du groupe témoin (AD oral plus placebo en spray nasal). La récidive a été définie comme un score MADRS total ≥22 pendant deux semaines consécutives, une hospitalisation due à une aggravation de la dépression ou un autre événement cliniquement pertinent suggérant une récidive. Le délai médian avant une récidive a été de 273 jours dans le groupe témoin (AD oral plus placebo en spray nasal), alors que le délai médian pour Spravato plus AD oral n'a pas pu être estimé, car ce groupe n'a à aucun moment atteint un taux de récidive de 50% pendant l'étude.
Chez les patients en rémission stable, le hazard ratio (rapport des risques instantanés) estimé (intervalle de confiance à 95%) de Spravato en association avec un AD oral, par rapport au groupe témoin (AD oral plus placebo en spray nasal), était, sur la base des estimations pondérées, de 0,49 (intervalle de confiance à 95%: 0,29-0,84), p = 0,003. Cela signifie que les patients en rémission stable qui ont poursuivi le traitement dans le groupe sous Spravato plus AD oral ont en moyenne eu une probabilité de récidive 51% plus basse que les patients qui sont passés dans le groupe témoin (AD oral plus placebo en spray nasal).
Réponse stable
Les résultats relatifs à l'efficacité étaient également concordants chez les patients présentant une réponse stable qui ont poursuivi le traitement par Spravato plus un AD oral; le délai jusqu'à une récidive des symptômes de dépression a été, selon les statistiques, significativement plus long chez eux que chez les patients du groupe témoin (AD oral plus oral plus placebo en spray nasal). Le délai médian avant une récidive a été de 88 jours dans le groupe témoin et de 635 jours dans le groupe traité par Spravato.
Chez les patients présentant une réponse stable, le hazard ratio (rapport des risques instantanés) estimé (intervalle de confiance à 95%) de Spravato en association avec un AD oral, par rapport au groupe témoin (AD oral plus placebo en spray nasal), était, sur la base du modèle à risques proportionnels de Cox, de 0,3 (intervalle de confiance à 95%: 0,16-0,55). Cela signifie que les patients qui étaient répondeurs stables et qui ont poursuivi le traitement dans le groupe sous Spravato en association avec un AD oral ont en moyenne eu une probabilité de récidive 70% plus basse que les patients qui sont passés dans le groupe témoin (AD oral plus placebo en spray nasal).
La figure 1 montre la proportion cumulative de patients présentant une rémission stable et une réponse stable (combinés à partir de l'étude TRD3003) qui sont restés exempts de récidive.
Figure 1: Délai jusqu'à la survenue d'une récidive chez les patients présentant une réponse stable et une rémission stable dans l'étude TRD3003
Fréquence du dosage
Parmi les patients en rémission stable ou présentant une réponse stable, respectivement 23% et 55% ont reçu une dose hebdomadaire pendant la phase d'entretien et respectivement 69% et 34% ont reçu une dose toutes les deux semaines. Certains patients ont également reçu les doses aux deux fréquences, une dose hebdomadaire ou une dose toutes les deux semaines (respectivement 8% et 11%). Parmi les patients qui ont reçu Spravato après randomisation, 60% ont reçu la dose de 84 mg et 40% la dose de 56 mg.
Étude TRD3013 (ESCAPE-TRD)
L'efficacité de Spravato a été évaluée dans une étude à long terme, randomisée, en ouvert, à l'aveugle de l'évaluateur, contrôlée contre traitement actif (TRD3013), dans laquelle Spravato a été comparé à la quétiapine avec une libération prolongée du principe actif (XR) chez 676 patients adultes présentant une DRT (âgés de 18 à 74 ans) et continuant à prendre leur AD oral actuel (un IRSN ou ISRS). Les patients ont reçu un traitement par Spravato à doses flexibles (28, 56 et 84 mg) ou par Quétiapine XR, selon les recommandations posologiques figurant dans l'information professionnelle en vigueur au moment du début du traitement.
Le critère d'évaluation principal de l'efficacité était la rémission (score MADRS total ≤10) à la semaine 8 et le critère d'évaluation secondaire majeur était le maintien de l'absence de récidive jusqu'à la semaine 32, après la rémission à la semaine 8. La récidive était définie par un score MADRS total ≥22 pendant 2 semaines consécutives, un séjour à l'hôpital en raison d'une aggravation de la dépression ou un autre événement cliniquement significatif indiquant une récidive.
Les valeurs initiales démographiques et liées à la maladie des patients du groupe Spravato plus AD oral étaient similaires à celles du groupe Quétiapine XR plus AD oral. Le score MADRS total moyen (SD) au début de l'étude était de 31,4 (6,06) pour le groupe traité par Spravato plus AD oral et de 31,0 (5,83) pour le groupe traité par Quétiapine XR plus AD oral.
Spravato plus AD oral a montré une supériorité cliniquement significative et statistique comparé à Quétiapine XR plus AD oral, aussi bien en ce qui concerne la mesure d'efficacité principale (tableau 6) que la mesure d'efficacité secondaire déterminante (tableau 7).
Tableau 6: Principaux résultats d'efficacité pour l'étude TRD3013 a
|
Groupe de traitement
|
Spravato + AD oral
|
Quétiapine XR + AD oral
| |
Nombre de patients en rémission
à la semaine 8
|
91/336 (27,1%)
|
60/340 (17,6%)
| |
Écart en pourcentage (IC à 95%)
|
9,44 (3,19; 15,68)
|
–
| |
Odds ratio ajusté (IC à 95%)
|
1,74 (1,20; 2,52)
P = 0,003b
|
–
| |
IC = intervalle de confiance; AD = antidépresseur; XR = libération prolongée du principe actif.
a Un patient qui a arrêté l'intervention de l'étude avant la semaine 8 a été considéré comme un résultat négatif (c.-à-d. pas de rémission). Pour les patients pour lesquels aucun résultat MADRS n'était disponible à la semaine 8, mais qui n'ont pas arrêté l'intervention de l'étude et ne sont pas sortis de l'étude avant la semaine 8, la LOCF du score MADRS a été appliquée.
b Valeur de p pour le test de CMH (Cochran-Mantel-Haenszel), ajusté par les groupes d'âge (18–64; ≥65) et le nombre total d'arrêts du traitement.
|
Tableau 7: Résultats d'efficacité secondaires majeurs pour l'étude TRD3013a
|
Groupe de traitement
|
Spravato + AD oral
|
Quétiapine XR + AD oral
| |
Nombre de patients en rémission à la semaine 8 et sans récidive à la semaine 32
|
73/336 (21,7%)
|
48/340 (14,1%)
| |
Écart en pourcentage (IC à 95%)
|
7,61 (1,85; 13,37)
|
–
| |
Odds ratio ajusté (IC à 95%)
|
1,72 (1,15; 2,57)
P = 0,008b
|
–
| |
IC = intervalle de confiance; AD = antidépresseur; XR = libération prolongée du principe actif.
a Un patient qui a arrêté l'intervention de l'étude a été considéré comme un résultat négatif (c.-à-d. pas de rémission). Pour les patients pour lesquels aucun résultat MADRS n'était disponible à la semaine 8, mais qui n'ont pas arrêté l'intervention de l'étude et ne sont pas sortis de l'étude avant la semaine 8, la LOCF du score MADRS a été appliquée.
b Valeur de p pour le test de CMH (Cochran-Mantel-Haenszel), ajusté par les groupes d'âge (18–64; ≥65) et le nombre total d'arrêts du traitement.
|
Taux de rémission et de réponse
Le taux de rémission à la semaine 32 était de 55,0% chez les patients du groupe Spravato plus AD oral et de 37,0% dans le groupe Quétiapine XR plus AD oral, avec un odds ratio (IC à 95%) de 2,09 (1,53; 2,85). Le taux de réponse (défini comme la diminution du score MADRS total de ≥50% par rapport à la valeur initiale ou un score MADRS total ≤10) était, à la semaine 32, de 75,5% des patients dans le groupe Spravato plus AD oral et de 55,5% dans le groupe Quétiapine XR plus AD oral, avec un odds ratio (IC à 95%) de 2,48 (1,78; 3,46).
Sur la période de traitement de 32 semaines, les taux d'arrêt du traitement en raison d'événements indésirables, d'un manque d'efficacité ou en général étaient respectivement de 4,2%, 8,3% et 23,2% pour les patients du groupe Spravato plus AD oral, et respectivement de 11,5%, 15,0% et 40,3% pour les patients du groupe Quétiapine XR plus AD oral.
Étude sur la relation entre la dose et la réponse thérapeutique lors de DRT
Une étude de phase II à double randomisation, en double aveugle et contrôlée contre placebo, visant à déterminer le dosage a recruté 108 patients adultes atteints de DRT. En plus de la poursuite d'un traitement antidépresseur oral, les patients ont reçu 14 mg, 28 mg, 56 mg ou 84 mg d'eskétamine ou un placebo par voie nasale, deux fois par semaine pendant 2 semaines. Le traitement avec des doses de 28 mg, 56 mg et 84 mg de Spravato a significativement amélioré les symptômes dépressifs chez les patients atteints de DRT, ce qui s'est traduit par une modification du score MADRS total après 1 semaine. Bien que les doses de 28 mg, 56 mg et 84 mg de Spravato aient été efficaces dans le traitement de la DRT, la durée d'action de la dose de 28 mg était plus courte.
Dépression résistante au traitement – étude à court terme menée chez des patients japonais
L'efficacité de Spravato a également été évaluée dans une étude à court terme (TRD2005) randomisée, en double aveugle, contrôlée contre traitement actif (sur 4 semaines), menée chez 202 patients japonais adultes présentant une DRT. Tout en continuant leur traitement en cours par l'AD oral, les patients ont reçu un traitement d'induction de 4 semaines par Spravato en spray nasal à des doses fixes de 28 mg, 56 mg ou 84 mg, ou par placebo. Le critère d'efficacité principal était la variation du score MADRS total entre le début de l'étude (valeur de référence) et le jour 28. Au début de l'étude, les caractéristiques démographiques et liées à la maladie des patients étaient comparables entre le groupe Spravato plus AD et le groupe placebo en spray nasal plus AD.
Dans l'étude TRD2005, à la fin de la phase d'induction de 4 semaines, aucune différence statistiquement significative n'a été observée pour l'une des 3 doses de Spravato (plus AD oral) comparées au placebo (plus AD oral), quant à la variation du score MADRS total par rapport au début de l'étude.
Dépression résistante au traitement – étude à court terme menée chez des patients chinois
L'efficacité de Spravato a également été évaluée dans une étude à court terme (TRD3006) randomisée, en double aveugle, contrôlée contre traitement actif, menée (sur 4 semaines) chez 252 patients adultes (224 patients chinois, 28 patients non chinois) présentant une DRT. Les patients ont reçu un traitement d'induction de 4 semaines par Spravato à des dosages flexibles (56 mg ou 84 mg) ou par placebo, en plus d'un AD oral nouvellement initié. Le critère d'efficacité principal était la variation du score MADRS total entre le début de l'étude (valeur de référence) et le jour 28. Les caractéristiques démographiques et liées à la maladie des patients étaient comparables entre le groupe Spravato plus AD et le groupe placebo en spray nasal plus AD.
Dans l'étude TRD3006, à la fin de la phase d'induction de 4 semaines, aucune différence statistiquement significative n'a été observée entre Spravato (plus AD oral) et le placebo (plus AD oral), quant à la variation du score MADRS total par rapport au début de l'étude.
Traitement aigu de courte durée d'une urgence psychiatrique dans le cadre d'une dépression majeure
Spravato a été étudié dans deux études identiques de phase 3, randomisées, en double aveugle, multicentriques, contrôlées contre placebo et de courte durée (4 semaines), ASPIRE I (SUI3001; NCT03039192) et ASPIRE II (SUI3002; NCT03097133), menées auprès de patients adultes atteints de TDM modéré à sévère (score MADRS total > 28) et présentant des pensées suicidaires actives avec intention suicidaire. Dans ces études, les patients ont reçu, deux fois par semaine pendant 4 semaines, un traitement par 84 mg de Spravato ou par un placebo en spray nasal. Tous les patients ont reçu un traitement standard (SOC) complet qui comprenait un séjour hospitalier initial et un traitement nouvellement initié ou optimisé par un AD oral (AD en monothérapie, ou AD plus potentialisation), selon la décision du médecin investigateur. Après la première dose, une réduction unique de la dose de Spravato à 56 mg était autorisée chez les patients qui ne toléraient pas la dose de 84 mg.
Au début des études SUI3001 et SUI3002, les caractéristiques démographiques et liées à la maladie des patients étaient comparables entre le groupe traité par Spravato + SOC et le groupe sous placebo en spray nasal + SOC. L'âge médian des patients était de 40 ans (entre 18 et 64 ans), 61% étaient des femmes, 73% des Caucasiens et 6% des Noirs, et 63% des patients avaient déjà fait au moins une tentative de suicide. Avant leur recrutement dans l'étude, 92% des patients avaient été traités par un AD. Au cours de l'étude, 40% des patients ont reçu un AD en monothérapie dans le cadre du traitement standard, 54% ont reçu un AD plus potentialisation, et 6% des patients ont reçu à la fois un AD en monothérapie et un AD plus potentialisation.
Le critère d'efficacité principal était la réduction des symptômes du TDM, mesurée par la variation du score MADRS total, 24 heures après la première dose (au jour 2), par rapport à sa valeur initiale.
Dans les études SUI3001 et SUI3002, le traitement par Spravato + SOC a présenté une supériorité statistique sur le critère d'efficacité principal par comparaison au placebo en spray nasal + SOC (voir tableau 8).
Tableau 8: Principaux résultats d'efficacité concernant la variation du score MADRS total, 24 heures après la première dose par rapport à la valeur initiale (dans les études SUI3001 et SUI3002; ANCOVA*)
|
No de l'étude
|
Groupe de traitement§
|
Nombre de patients
|
Score moyen
au début de l'étude
(SD)
|
Variation de la LSM entre le début de l'étude et 24 heures après la première dose
(SE)
|
Variation de la LSM
(IC à 95%)†
Valeur de p
| |
SUI3001
|
84 mg Spravato + SOC
|
111
|
41,3 (5,87)
|
-15,9 (1,04)
|
-3,8
(-6,56; -1,09)‡
p = 0,006
| |
Placebo en spray nasal + SOC
|
112
|
41,0 (6,29)
|
-12,0 (1,02)
|
-
| |
SUI3002
|
84 mg Spravato + SOC
|
113
|
39,4 (5,21)
|
-16,0 (1,02)
|
-3,9
(-6,60; -1,11)‡
p = 0,006
| |
Placebo en spray nasal + SOC
|
113
|
39,9 (5,76)
|
-12,2 (1,05)
|
-
| |
Études combinées (SUI3001 et SUI3002)
|
84 mg Spravato + SOC
|
224
|
40,3 (5,61)
|
-16,0 (0,72)
|
-3,8
(-5,75; -1,89)‡
| |
Placebo en spray nasal + SOC
|
225
|
40,4 (6,04)
|
-12,1 (0,72)
|
-
| |
SD = écart type, SE = erreur type, LSM = moyenne des moindres carrés, IC = intervalle de confiance, SOC = traitement standard (Standard of Care).
* ANCOVA LOCF: dans l'étude SUI3001, pour 1 participant (dans le groupe de traitement placebo + SOC), on n'a disposé d'aucun score MADRS total au jour 2 (24 heures après la première dose), et son score MADRS total a été remplacé par la valeur obtenue 4 heures après la première dose («carried forward»). Dans l'étude SUI3002, pour 5 des 6 participants chez lesquels on ne disposait pas de score MADRS total au jour 2 (24 heures après la première dose), leur score MADRS total a été remplacé par la valeur obtenue 4 heures après la première dose.
§ Eskétamine ou placebo administrés par voie nasale.
† Différence (Spravato + SOC moins placebo en spray nasal + SOC) de variation de la moyenne des moindres carrés (LSM), par rapport au début de l'étude.
‡ Groupes de traitement qui ont présenté une supériorité statistiquement significative par rapport au placebo en spray nasal + SOC.
|
Les différences (IC à 95%) de variation du score MADRS total au jour 2 (24 heures après la première dose) par rapport à la valeur initiale entre le traitement par Spravato + SOC et celui par placebo + SOC ont été de -4,81 (-7,26; -2,36) dans le sous-groupe avec antécédents de tentative de suicide (N = 282) et de -2,32 (-5,54; 0,91) dans le sous-groupe sans antécédents de tentative de suicide (N = 166).
Dans une analyse posthoc des données regroupées de SUI3001 et SUI3002, Spravato plus traitement standard n'a présenté aucune supériorité par rapport au placebo plus traitement standard, au jour 2 (24 heures après la première dose), chez les 18% de patients présentant un épisode dépressif modéré (score MADRS total < 35 au début de l'étude).
Évolution au cours du temps de la réponse au traitement
Dans les deux études SUI3001 et SUI3002, une différence a été observée entre le traitement par Spravato et celui par placebo, à partir de 4 heures. Des améliorations supplémentaires ont été observées dans l'intervalle entre 4 heures et le jour 25, tant dans le groupe Spravato que dans le groupe placebo. La différence entre les groupes a généralement persisté, mais n'a pas semblé s'accentuer au cours du temps jusqu'au jour 25. La figure 3 montre l'évolution au cours du temps du score MADRS total, le critère d'efficacité principal, sur la base des données combinées des études SUI3001 et SUI3002.
Figure 3: Variation au cours du temps de la moyenne des moindres carrés (LSM) du score MADRS total, par rapport au début de l'étude, dans les études SUI3001 et SUI3002* (groupe total analysé combiné) – MMRM)
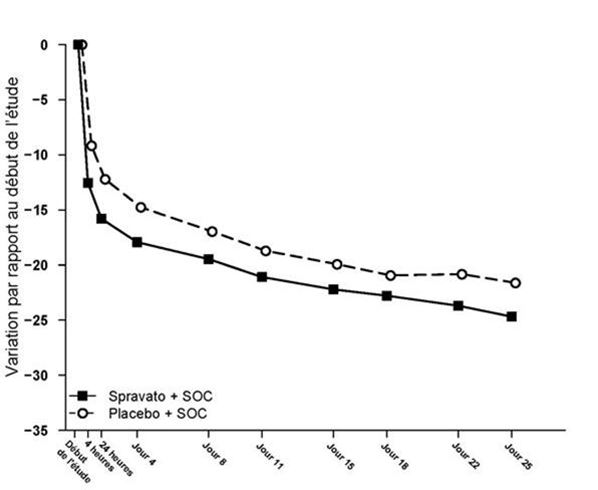
* Remarque: dans ces études, chez les patients qui ne toléraient pas la dose de 84 mg, une réduction unique de la dose de Spravato à 56 mg était autorisée après la première dose. Chez environ 16% des patients, la posologie de Spravato a été réduite de 84 mg à 56 mg, deux fois par semaine.
Taux de rémission
Dans les études de phase 3, le pourcentage de patients ayant obtenu une rémission (score MADRS total ≤12 à tout moment de l'étude) a été plus élevé dans le groupe Spravato + SOC que dans le groupe placebo + SOC, à tout moment de la phase de traitement en double aveugle (tableau 9).
Tableau 9: Patients ayant obtenu une rémission du TDM; phase de traitement en double aveugle; groupe total analysé concernant l'efficacité
|
|
SUI3001
|
SUI3002
|
Études combinées
(SUI3001 et SUI3002)
| |
|
Placebo + SOC
|
Spravato + SOC
|
Placebo + SOC
|
Spravato + SOC
|
Placebo + SOC
|
Spravato + SOC
| |
|
112
|
112
|
113
|
114
|
225
|
226
| |
Jour 1, 4 heures après la première dose
| |
Patients présentant une rémission du TDM
|
9 (8,0%)
|
12 (10,7%)
|
4 (3,5%)
|
12 (10,5%)
|
13 (5,8%)
|
24 (10,6%)
| |
Jour 2, 24 heures après la première dose
| |
Patients présentant une rémission du TDM
|
10 (8,9%)
|
21 (18,8%)
|
12 (10,6%)
|
25 (21,9%)
|
22 (9,8%)
|
46 (20,4%)
| |
Jour 25
| |
Patients présentant une rémission du TDM
|
38 (33,9%)
|
46 (41,1%)
|
31 (27,4%)
|
49 (43,0%)
|
69 (30,7%)
|
95 (42,0%)
| |
SOC = traitement standard
Remarque: la rémission est définie comme un score MADRS total ≤12. N'ont pas été considérés comme ayant obtenu une rémission les participants qui n'ont pas rempli ce critère ou dont le traitement a été arrêté pour une raison quelconque avant ce terme.
|
Effets sur la suicidalité
Le critère d'évaluation secondaire de l'efficacité était la variation sur l'échelle «Clinical Global Impression of Suicidal Severity – revised» (CGI-SSr), 24 heures après l'administration de la première dose (au jour 2).
Le CGI-SSr est une évaluation clinique à une dimension, utilisée pour classifier la sévérité actuelle des pensées et des comportements suicidaires d'un patient. Le score CGI-SSr varie de 0 à 6, les valeurs plus élevées correspondant à des pensées et des comportements suicidaires plus sévères. Dans les études SUI3001 et SUI3002, Spravato plus traitement standard n'a pas présenté de supériorité pour améliorer le CGI-SSr, par comparaison au placebo en spray nasal plus traitement standard.
L'efficacité à long terme de Spravato pour la prévention du suicide n'a pas été étudiée.
Informations complémentaires
Effet sur l'aptitude à la conduite
Les effets de Spravato sur la capacité de conduire un véhicule automobile ont été évalués dans le cadre de deux études, l'une menée chez des adultes atteints de TDM et l'autre menée chez des sujets sains. La capacité de conduite sur route a été évaluée à l'aide de l'écart type moyen de la position latérale du véhicule (SDLP, standard deviation of the lateral position), une mesure de la perturbation de la conduite.
Les effets d'une dose unique de 84 mg d'eskétamine en spray nasal, sur la conduite le jour suivant ainsi que l'effet d'une dose intranasale répétée de 84 mg de Spravato sur la conduite le jour même ont été évalués dans le cadre d'une étude en simple aveugle contrôlée contre placebo, menée auprès de 25 patients adultes atteints de TDM. Une boisson alcoolisée a servi de témoin positif pour la phase de traitement par dose unique. Le SDLP, 18 heures après l'administration d'une dose unique de 84 mg d'eskétamine en spray nasal, a été semblable à celui observé après l'administration du placebo. Pendant la phase de traitement par doses multiples, le SDLP après l'utilisation intranasale répétée de 84 mg de Spravato 6 heures après la dernière dose aux jours 11, 18 et 25 a été similaire à celui après le placebo. La limite supérieure de l'intervalle de confiance bilatéral à 95% de la différence moyenne entre une dose unique d'eskétamine et de placebo a été de 0,58 cm, soit moins que la limite de non-infériorité prédéfinie de 2,4 cm. La limite inférieure de l'intervalle de confiance à 95% de la différence moyenne entre l'éthanol et le placebo a été de 1,03 cm (p < 0,001), ce qui confirme la sensibilité de l'étude.
Les effets d'une dose unique de 84 mg d'eskétamine en spray nasal sur la conduite ont été évalués dans le cadre d'une étude randomisée, en double aveugle, croisée et contrôlée contre placebo, menée auprès de 23 sujets sains. La mirtazapine a servi de témoin positif. La capacité de conduire a été évaluée 8 heures après l'administration de l'eskétamine ou de la mirtazapine. Le SDLP après l'administration d'eskétamine en spray nasal a été semblable à celui observé après l'administration du placebo. La limite supérieure de l'intervalle de confiance bilatéral à 95% de la différence moyenne entre l'eskétamine et le placebo a été de 0,86 cm, soit moins que la limite de non-infériorité prédéfinie de 2,4 cm. La limite inférieure de l'intervalle de confiance à 95% de la différence moyenne entre la mirtazapine et le placebo a été de 1,12 cm (p = 0,001), ce qui confirme la sensibilité de l'étude. Sur les 23 sujets évalués, 21 ont passé le test avec succès. Deux sujets ont annulé le test de conduite après l'administration d'eskétamine, car ils avaient l'impression de ne pas être aptes à la conduite.
Effet sur l'intervalle QT/QTc et l'électrophysiologie cardiaque
Le traitement par Spravato n'a pas prolongé l'intervalle QTc. L'effet de Spravato (84 mg en spray nasal et 0,8 mg/kg d'eskétamine en perfusion intraveineuse pendant 40 minutes) sur l'intervalle QTc a été évalué dans le cadre d'une étude croisée randomisée, en double aveugle, contrôlée contre placebo et avec témoin positif (moxifloxacine 400 mg), en 4 phases, menée auprès de 60 sujets sains. Les concentrations maximales d'eskétamine dans le plasma après perfusion intraveineuse étaient environ 3 fois plus élevées que celles après administration de la dose de 84 mg par voie nasale. La limite supérieure de l'intervalle de confiance à 90% pour le plus grand intervalle QTc ajusté en fonction du placebo après correction en fonction des valeurs initiales (valeurs de référence), calculé grâce à la formule de correction de Fridericia (QTcF) pour les deux groupes de traitement, est restée inférieure à 10 ms, à tous les moments évalués.
PharmacocinétiqueAbsorption
La biodisponibilité absolue moyenne de 84 mg d'eskétamine après administration en spray nasal est d'environ 48%.
L'eskétamine est rapidement absorbée par la muqueuse nasale après administration nasale et peut être mesurée dans le plasma en l'espace de 7 minutes après une dose de 28 mg. Le temps nécessaire pour atteindre la concentration plasmatique maximale (tmax) est généralement de 20 à 40 minutes après la dernière pulvérisation nasale d'une séance de traitement (voir Posologie/Mode d'emploi).
La Cmax et l'AUCinf de l'eskétamine ont présenté une augmentation moins que proportionnelle à la dose, après une administration nasale d'une dose comprise entre 28 mg et 56 mg. Entre 56 mg et 84 mg, les deux paramètres ont présenté une augmentation proportionnelle à la dose administrée.
Le profil pharmacocinétique de l'eskétamine est semblable, sans accumulation dans le plasma, après administration d'une dose unique et après administration répétée, lorsque l'eskétamine est administrée deux fois par semaine.
Distribution
Le volume moyen de distribution de l'eskétamine à l'état d'équilibre (steady state) après administration intraveineuse est de 709 l.
Chez l'être humain, la proportion d'eskétamine liée aux protéines dans la concentration plasmatique totale est en moyenne de 43 à 45%. La mesure dans laquelle l'eskétamine se lie aux protéines plasmatiques ne dépend pas de la fonction hépatique ou rénale.
Métabolisme
L'eskétamine est largement métabolisée dans le foie. La voie métabolique principale de l'eskétamine dans les microsomes hépatiques humains est la Ndéméthylation, ce qui entraîne la formation de noreskétamine. Les principales enzymes du CYP responsables de la Ndéméthylation de l'eskétamine sont le CYP2B6 et le CYP3A4. D'autres enzymes du CYP, parmi lesquelles le CYP2C19 et le CYP2C9, y contribuent dans une bien moindre mesure. La noreskétamine est ensuite convertie en d'autres métabolites, dont certains sont glucuronidés, via les voies métaboliques dépendantes du CYP. La Cmax et l'AUC∞ de la noreskétamine dans le plasma sont en moyenne respectivement environ deux et trois fois plus élevées que les valeurs correspondantes pour l'eskétamine. L'activité pharmacologique de l'eskétamine administrée par voie intranasale est toutefois en grande partie attribuable à la substance mère, car l'eskétamine est plus puissante que la noreskétamine en tant qu'antagoniste des récepteurs NMDA et présente des concentrations non liées plus élevées dans le cerveau des animaux.
Élimination
La clairance moyenne de l'eskétamine administrée par voie intraveineuse était d'environ 89 l/h. Après administration nasale et obtention de la Cmax, la concentration plasmatique d'eskétamine a rapidement diminué dans les premières heures qui ont suivi, puis progressivement par la suite. La demi-vie terminale moyenne après administration en spray nasal était généralement de l'ordre de 7 à 12 heures.
Après administration intraveineuse d'eskétamine radiomarquée, environ 78% de la radioactivité administrée ont été retrouvés dans l'urine et 2% dans les selles. Après administration orale d'eskétamine radiomarquée, environ 86% de la radioactivité administrée ont été retrouvés dans l'urine et 2% dans les selles. La radioactivité mesurée dans l'urine et les selles était principalement due aux métabolites de l'eskétamine. Après administration intraveineuse et orale, moins de 1% de la dose a été excrété sous forme inchangée dans l'urine.
Cinétique pour certains groupes de patients
Troubles de la fonction hépatique
La Cmax et l'AUC∞ de l'eskétamine après une dose de 28 mg étaient similaires chez les sujets présentant une altération légère de la fonction hépatique (stade A de Child-Pugh) et les sujets sains. Chez les sujets présentant une altération modérée de la fonction hépatique (stade B de Child-Pugh), la Cmax de l'eskétamine était 8% plus élevée, et l'AUC∞ 103% plus élevée que celles des sujets sains.
On ne dispose d'aucune expérience clinique concernant l'utilisation d'un spray nasal d'eskétamine chez les patients atteints d'une altération sévère de la fonction hépatique (stade C de Child-Pugh).
Troubles de la fonction rénale
Après administration d'une dose de 28 mg d'eskétamine en spray nasal, la Cmax de l'eskétamine était en moyenne de 20 à 26% plus élevée chez les sujets présentant une altération de la fonction rénale légère, modérée ou sévère (clairance de la créatinine [CLCR] de respectivement 58-77 ml/min, 30-47 ml/min, ou 5-28 ml/min et non dialysés) que chez les sujets présentant une fonction rénale normale (88-140 ml/min). L'AUC∞ était de 36% plus élevée chez les sujets présentant une altération de la fonction rénale légère à sévère.
On ne dispose d'aucune expérience clinique concernant l'administration d'eskétamine en spray nasal chez les patients dialysés.
Patients âgés
La pharmacocinétique de l'eskétamine après administration en spray nasal a été comparée entre des sujets âgés, mais par ailleurs sains, et des sujets sains, plus jeunes. Après administration d'une dose de 28 mg, les valeurs moyennes de la Cmax et de l'AUC∞ de l'eskétamine étaient respectivement 21% et 18% plus élevées chez les sujets âgés (de 65 à 81 ans) que chez les sujets plus jeunes (de 22 à 50 ans). Après administration d'une dose de 84 mg, les valeurs moyennes de la Cmax et de l'AUC∞ de l'eskétamine étaient respectivement 67% et 38% plus élevées chez les sujets âgés (de 75 à 85 ans) que chez les sujets adultes plus jeunes (de 24 à 54 ans). La demi-vie terminale de l'eskétamine était similaire chez les sujets adultes âgés et plus jeunes.
Polymorphismes génétiques
Pour les personnes ayant une activité enzymatique du CYP2B6 normale, réduite ou nulle («extensive metabolizer» avec les variants de l'allèle *1/*1, *5/*5 ou *1/*5, «intermediate metabolizer» avec les variants de l'allèle *1/*6 ou *5/*6, ou «poor metabolizer» avec le variant de l'allèle *6/*6), le polymorphisme du CYP2B6 n'a aucune influence sur la pharmacocinétique de l'eskétamine administrée par voie intranasale, car les plages de valeurs de la Cmax et l'AUClast de l'eskétamine plasmatique coïncident dans une large mesure.
Origine ethnique
La pharmacocinétique de l'eskétamine en spray nasal a été comparée entre des sujets sains asiatiques et caucasiens. Après l'administration d'une dose unique de 56 mg d'eskétamine, les valeurs plasmatiques moyennes de la Cmax et de l'AUC∞ étaient respectivement environ 14% et 33% plus élevées chez les sujets chinois que chez les sujets caucasiens. Ces deux paramètres étaient environ 40% plus élevés chez les sujets japonais que chez les sujets caucasiens. Chez les sujets coréens, la Cmax de l'eskétamine était en moyenne 10% plus basse, et l'AUC∞ en moyenne 17% plus élevée que chez les sujets caucasiens. La demi-vie terminale moyenne de l'eskétamine dans le plasma était de 7,1 à 8,9 heures chez les sujets asiatiques et de 6,8 heures chez les sujets caucasiens.
Sexe
Des sujets sains (138 hommes et 118 femmes) et des patients atteints de TDM (295 hommes et 496 femmes) ont participé à une analyse pharmacocinétique de population. Les résultats ont montré que la pharmacocinétique de l'eskétamine après administration en spray nasal n'était pas influencée par le sexe.
Poids corporel
Une analyse pharmacocinétique de population a été effectuée sur 256 sujets sains et 791 patients atteints de TDM. Le poids corporel des participants à l'étude se situait entre 39 kg et 207 kg. Les résultats ont montré que la pharmacocinétique de l'eskétamine après administration en spray nasal n'était pas influencée par le poids corporel.
Rhinite allergique
La pharmacocinétique d'une dose unique de 56 mg d'eskétamine administrée en spray nasal était semblable chez les sujets atteints de rhinite allergique avec une exposition aux pollens de graminées et chez les sujets sains.
Données précliniquesPharmacologie de sécurité
Chez le chien, une augmentation temporaire de la fréquence cardiaque et de la pression artérielle a été observée à des expositions à l'eskétamine comparables à l'exposition humaine avec la dose maximale recommandée chez l'être humain (maximum recommended human dose, MRHD) de 84 mg.
Toxicité en cas d'administration répétée
Dans les études de toxicité avec administrations répétées, aucun effet indésirable n'a été observé chez le rat sur une période allant jusqu'à 6 mois, ni chez le chien sur une période allant jusqu'à 9 mois, à des expositions à l'eskétamine inférieures ou comparables à l'exposition humaine avec la MRHD de 84 mg.
Génotoxicité
Lors du test d'Ames, l'eskétamine n'était pas mutagène, que cela soit avec ou sans activation métabolique. Des effets génotoxiques de l'eskétamine ont été observés lors d'un test du micronoyau réalisé in vitro en présence d'une activation métabolique, utilisé pour un dépistage. L'eskétamine administrée par voie intraveineuse n'a toutefois présenté aucune propriété génotoxique lors d'un test du micronoyau réalisé in vivo dans la moelle osseuse de rats, ni lors d'un test des comètes réalisé in vivo dans les cellules hépatiques de rats. Dans du suc gastrique artificiel, aucune indication suggérant la formation de Nnitroso-eskétamine à partir de la fraction absorbée par voie orale d'une dose d'eskétamine administrée par voie nasale n'a été mise en évidence.
Carcinogénicité
Au cours d'une étude de carcinogénicité de 2 ans effectuée chez le rat, l'administration nasale d'eskétamine, une fois par jour, à des doses allant jusqu'à 9 mg par jour n'a pas entraîné d'augmentation de l'incidence des tumeurs. À cette dose, l'exposition à l'eskétamine était inférieure à l'exposition humaine avec la MRHD de 84 mg. De plus, dans une étude de 6 mois réalisée chez des souris transgéniques (Tg.rasH2), l'eskétamine n'était pas carcinogène après une administration sous-cutanée, une fois par jour, à des doses allant jusqu'à 70/40 mg/kg/jour. En se basant sur l'AUC, l'exposition à l'eskétamine à cette dose était environ 4 fois plus élevée qu'après la MRHD de 84 mg.
Toxicité sur la reproduction
Dans une étude toxicologique chez le rat sur le développement embryofœtal avec administration nasale de kétamine, le mélange racémique d'arkétamine et d'eskétamine, les ratons n'ont pas présenté de lésions malgré une toxicité maternelle avec des doses allant jusqu'à 150 mg/kg/jour. La marge de sécurité basée sur l'AUC, estimée pour l'eskétamine à la dose de kétamine de 150 mg/kg/jour, était environ 12 fois plus élevée qu'avec la MRHD de 84 mg d'eskétamine. Dans une étude toxicologique chez le lapin sur le développement embryofœtal avec administration nasale de kétamine, des malformations du squelette ont été observées à des doses de 30 et de 100/50 mg/kg/jour en présence de toxicité maternelle. Un lien avec l'administration de kétamine ne peut pas être exclu. L'exposition estimée à l'eskétamine avec la NOAEL de 10 mg/kg/jour était inférieure à l'exposition maximale à l'eskétamine avec la dose de 84 mg chez l'être humain.
Les expérimentations animales avec la kétamine ont révélé des signes de neurotoxicité au cours de la phase de développement. Un potentiel d'effets neurotoxiques de l'eskétamine sur le fœtus en développement ne peut pas être exclu. La kétamine a causé des anomalies des cellules neuronales dans le cerveau des ratons entraînant des changements comportementaux et des troubles de la mémoire jusqu'à un âge adulte précoce lorsqu'elle a été administrée à leurs mères par voie intraveineuse à des doses anesthésiques élevées au cours du deuxième trimestre de la gestation. L'administration de kétamine par voie intraveineuse à fortes doses anesthésiques au cours du troisième trimestre de la gestation à des singes femelles a entraîné une mort cellulaire neuronale dans le cerveau de leur fœtus. Le traitement intrapéritonéal ou sous-cutané postnatal précoce de ratons et souriceaux pendant une phase de croissance rapide du cerveau a également entraîné une mort cellulaire neuronale induite par la kétamine. Cette phase de développement du cerveau correspond au troisième trimestre de la grossesse chez l'être humain.
Une étude toxicologique sur le développement prénatal et postnatal, menée avec de l'eskétamine administrée par voie nasale à une dose allant jusqu'à 9 mg par jour, chez le rat n'a montré aucun effet indésirable chez les mères ou les ratons.
Fertilité
Dans une étude de toxicité sur la fertilité et le développement embryonnaire précoce chez le rat, l'eskétamine administrée par voie nasale, à des doses de 0,9, 3 ou 9 mg/jour, a entraîné une toxicité maternelle et paternelle à 3 et 9 mg/jour. Aucun effet négatif sur la fertilité et la capacité de reproduction n'a été observé à ces doses.
Remarques particulièresStabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l'emballage.
Remarques particulières concernant le stockage
Ne pas conserver au-dessus de 30 °C.
Conserver hors de portée des enfants.
Remarques concernant la manipulation
Chaque emballage de Spravato est fourni avec un mode d'emploi séparé qui contient une description détaillée de l'administration du spray nasal.
Le médicament non utilisé ou les déchets doivent être éliminés conformément aux dispositions locales.
Numéro d’autorisation67103 (Swissmedic)
PrésentationLa préparation est emballée dans un récipient primaire, un flacon de type I muni d'un bouchon en caoutchouc. Le flacon rempli muni d'un bouchon se trouve dans un spray nasal à usage unique à activer manuellement. Le dispositif libère deux pulvérisations avec un volume total de la préparation de 0,2 ml.
Spravato est disponible en conditionnements de 1, 2 ou 3 sprays nasaux à usage unique. Dans chaque emballage, chaque dispositif est emballé individuellement dans un blister scellé. [A]
Titulaire de l’autorisationJanssen-Cilag AG, Zoug
Mise à jour de l’informationSeptembre 2024
Mode d'emploi
Spravato®
(chlorhydrate d'eskétamine)

Remarque importante
Ce dispositif est destiné à être utilisé par le patient lui-même sous la supervision directe d'un médecin (veuillez consulter l'information professionnelle). Veuillez lire ce mode d'emploi dans son intégralité avant d'instruire et de superviser le patient.
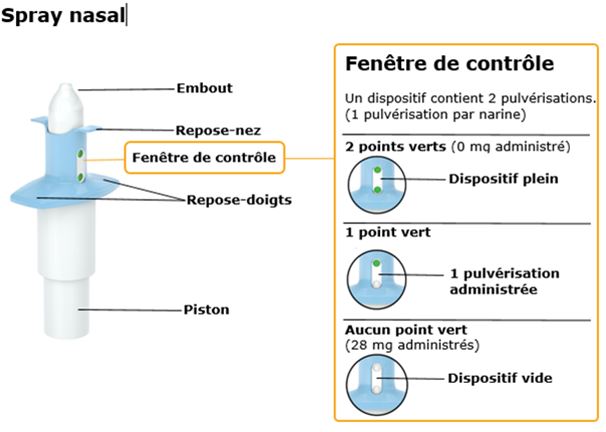

Uniquement avant la première utilisation:
|
|

|
Demandez au patient de se moucher uniquement avant la première pulvérisation.
| |
|

|
Vérifiez le nombre de sprays nasaux nécessaires.
|


Vérifier la date d'expiration «EXP».
S'il est périmé, prendre un nouveau dispositif.
Retirer le film de protection et sortir le dispositif.
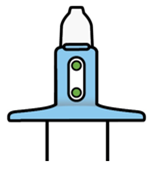
Ne pas appuyer sur le piston du dispositif.
Il en résulterait une perte du principe actif.
La fenêtre de l'indicateur doit afficher 2 points verts. Si ce n'est pas le cas, éliminer le dispositif et en prendre un nouveau.
Donner le dispositif au patient.

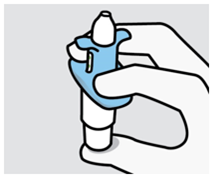
Le patient doit:
tenir le dispositif comme indiqué, en soutenant délicatement le piston avec le pouce.
Ne pas appuyer sur le piston.
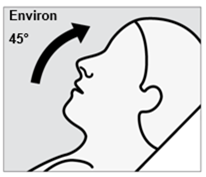
Le patient doit:
incliner la tête vers l'arrière à environ 45 degrés pendant la pulvérisation, de telle sorte que le médicament reste à l'intérieur du nez.

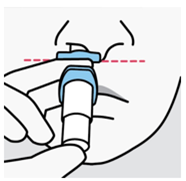
Le patient doit:
introduire l'embout dans la première narine en gardant le dispositif bien droit.
Le repose-nez doit toucher la peau entre les narines.
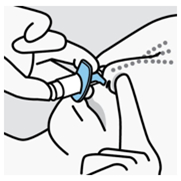
Le patient doit:
boucher la narine opposée;
inspirer par le nez tout en poussant le piston jusqu'à la butée.
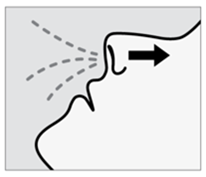
Le patient doit:
renifler doucement après la pulvérisation, de telle sorte que le médicament reste à l'intérieur du nez.
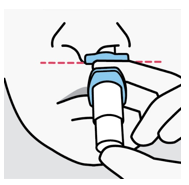
Le patient doit:
changer de main pour insérer l'embout dans l'autre narine.
Répéter l'étape 4 pour administrer la deuxième pulvérisation.

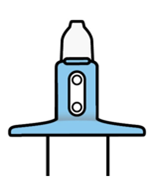
Reprendre le dispositif du patient.
Vérifier que l'indicateur n'affiche aucun point vert.
Si un point vert est visible, le patient doit répéter l'administration de la pulvérisation dans la deuxième narine.
Vérifier de nouveau l'indicateur pour s'assurer que le dispositif est vide.
Le patient doit:
se reposer dans une position confortable (de préférence semi-inclinée) pendant 5 minutes après l'utilisation de chaque dispositif.

Ne pas se moucher.
Si du liquide s'écoule, sécher le nez en tamponnant avec un mouchoir en papier.

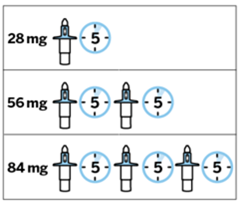
Répéter les étapes 2 à 5 si plus d'un dispositif est nécessaire.


|



























