Propriétés/EffetsCode ATC
R03DX09
Mécanisme d'action
Le mépolizumab est un anticorps monoclonal humanisé (IgG1, kappa) qui est dirigé avec une haute affinité spécifiquement contre l'interleukine 5 (IL-5) humaine. L'IL-5 est la cytokine la plus importante pour la croissance, la différenciation, le recrutement, l'activation et la survie des éosinophiles. Le mépolizumab en concentrations d'ordre nanomolaire inhibe les effets biologiques de l'IL-5 en empêchant celle-ci de se lier à la chaîne alpha du complexe récepteur d'IL-5 exprimé à la surface cellulaire des éosinophiles. Ainsi, le mépolizumab bloque la voie de signalisation de l'IL-5 et réduit de cette manière la production et la survie des éosinophiles.
Pharmacodynamique
Dans les études cliniques, une diminution du taux des éosinophiles dans le sang a été observée après un traitement par le mépolizumab. L'ampleur et la durée de cette diminution étaient dose-dépendantes après l'administration sous-cutanée de doses de 12,5 à 125 mg.
Chez des patients souffrant d'asthme sévère l'administration sous-cutanée de 100 mg toutes les 4 semaines pendant une période de 32 semaines a permis de diminuer le taux sanguin d'éosinophiles à une valeur (moyenne géométrique) de 40 cellules/µl. Cela correspond à une réduction de 84% (moyenne géométrique) par rapport au placebo. Cette réduction dans cet ordre de grandeur a déjà été observée au cours des 4 premières semaines de traitement. Le degré de cette réduction du taux sanguin d'éosinophiles s'est maintenu chez les patients atteints d'asthme sévère (n=998) qui avaient été traités dans les études de prolongation en ouvert pendant une durée médiane de 2,8 ans (intervalle de 4 semaines à 4,5 ans).
Après une administration sous-cutanée de 100 mg toutes les 4 semaines pendant une période de 52 semaines chez des patients atteints de RSCaPN, le taux sanguin d'éosinophiles a baissé à 60 cellules/µl (moyenne géométrique). Cela correspond à une réduction de 83% (moyenne géométrique) versus placebo. Cette réduction a été observée au cours des 4 premières semaines de traitement et s'est maintenue pendant la durée du traitement.
Après une administration sous-cutanée de 300 mg toutes les 4 semaines pendant une période de 52 semaines chez des patients avec GEPA, le taux sanguin d'éosinophiles avait baissé à 38 cellules/µl (moyenne géométrique). Cela correspond à une réduction de 83% (moyenne géométrique) versus placebo.
Après une administration sous-cutanée de 300 mg toutes les 4 semaines pendant une période de 32 semaines chez des patients atteints de SHE, le taux sanguin d'éosinophiles avait baissé à 70 cellules/µl (moyenne géométrique). Cela correspond à une réduction de 92% (moyenne géométrique) par rapport au placebo. Une réduction de cet ordre de grandeur s'est maintenue pendant encore 20 semaines chez les patients qui ont poursuivi le traitement par mépolizumab durant la phase ouverte de prolongation de l'étude.
Immunogénicité
En raison du potentiel immunogène des médicaments à base de protéines ou de peptides, les patients peuvent développer des anticorps contre le mépolizumab après le traitement.
Sur 260 patients atteints d'asthme sévère ayant reçu au moins une dose sous-cutanée de 100 mg, 15 patients (6%) ont développé des anticorps contre le mépolizumab.
Le profil d'immunogénicité de Nucala chez les patients souffrant d'asthme sévère (n=998) qui avaient été traités dans les études de prolongation en ouvert pendant une durée médiane de 2,8 ans (intervalle de 4 semaines à 4,5 ans) était similaire à celui observé dans les études contrôlées contre placebo.
Sur 196 patients atteints de RSCaPN ayant reçu au moins une dose sous-cutanée de mépolizumab de 100 mg, 6 patients (3%) ont développé des anticorps contre le mépolizumab.
Au total, 1 patient sur 68 (1%) souffrant de GEPA ayant reçu au moins une dose sous-cutanée de 300 mg de mépolizumab a développé des anticorps contre le mépolizumab.
Au total, 1 patient sur les 53 (2%) atteints de SHE et traités avec au moins une dose sous-cutanée de 300 mg de mépolizumab a développé des anticorps dirigés contre le mépolizumab.
Toutes indications confondues, des anticorps neutralisants ont été trouvés chez un adulte (souffrant d'asthme sévère).
Chez la majorité des patients, la présence d'anticorps anti-mépolizumab n'a pas eu d'influence notable sur la PC ou la PD du mépolizumab; aucun indice suggérant un rapport des titres d'anticorps avec des modifications du taux d'éosinophiles n'a été trouvé.
Efficacité clinique
Asthme sévère à éosinophiles
L'efficacité du mépolizumab dans le traitement de l'asthme sévère à éosinophiles a été évaluée dans le cadre de 3 études cliniques randomisées, en double aveugle, par groupes parallèles, de 24 à 52 semaines, auprès de patients à partir de 12 ans. Ces études étaient conçues pour évaluer l'efficacité du mépolizumab administré sous forme d'injection sous-cutanée ou intraveineuse à intervalles de quatre semaines chez des patients dont l'asthme n'était pas contrôlé malgré un traitement standard en cours (par exemple corticostéroïdes à inhaler [CSI], association de CSI et d'agonistes bêta2-adrénergiques à longue durée d'action [LABA], antagonistes des leucotriènes et agonistes bêta2-adrénergiques à courte durée d'action [SABA]). Les exacerbations de l'asthme cliniquement importantes sont définies comme suit dans MEA112997 et MEA115588: aggravation des symptômes d'asthme, exigeant une corticothérapie orale/systémique et/ou une hospitalisation ou une admission dans un service d'urgence.
Études contrôlées versus placebo
Étude de recherche de dose MEA112997 (étude DREAM)
Les résultats de l'étude MEA112997 – une étude multicentrique de 52 semaines, randomisée, en double aveugle, avec contrôle versus placebo, par groupes parallèles, auprès de 616 patients – montrent que le mépolizumab (75 mg, 250 mg ou 750 mg) administré par voie intraveineuse a provoqué une réduction significative des exacerbations de l'asthme versus placebo. Aucune différence significative d'efficacité n'a été constatée entre les 3 posologies étudiées (voir le Tableau 1).
Tableau 1: Fréquence des exacerbations cliniquement importantes à 52 semaines dans la population en intention de traitement
|
|
Mépolizumab IV
|
Placebo
| |
75 mg
n = 153
|
250 mg
n = 152
|
750 mg
n = 156
|
n = 155
| |
Exacerbations par an
|
1,24
|
1,46
|
1,15
|
2,40
| |
Pourcentage de réduction
|
48%
|
39%
|
52%
|
| |
Rapport (IC à 95%)
|
0,52 (0,39; 0,69)
|
0,61 (0,46; 0,81)
|
0,48 (0,36; 0,64)
|
| |
Valeur de p
|
<0,001
|
<0,001
|
<0,001
|
-
|
Les résultats de cette étude suggèrent qu'un taux sanguin d'éosinophiles ≥150 cellules/µl lors des examens préalables et ≥300 cellules/µl dans les 12 mois précédents peut être utilisé comme marqueur biologique pour prédire quels patients peuvent profiter d'un traitement par le mépolizumab. Dans le groupe sous placebo, un tiers des patients présentant ces caractéristiques est cependant aussi resté exempt d'exacerbations pendant la période de traitement d'un an.
Les patients sélectionnés selon une valeur seuil plus élevée du taux sanguin d'éosinophiles ont présenté une plus forte réduction de la fréquence d'exacerbations. Il n'a cependant pas été vérifié dans quelle mesure des patients ayant profité du traitement complémentaire par le mépolizumab ont été exclus par la définition d'une valeur seuil élevée.
Tableau 2: Réduction estimée du taux d'exacerbations cliniquement significatives en fonction des valeurs seuils du taux sanguin d'éosinophiles à l'inclusion
|
Étude
|
Taux sanguin d'éosinophiles à l'inclusion
|
Rapport (IC à 95%)
| |
MEA112997
|
150 cellules/µl
|
0,70 (0,53; 0,93)
| |
|
300 cellules/µl
|
0,52 (0,41; 0,65)
| |
|
500 cellules/µl
|
0,42 (0,32; 0,54)
| |
MEA115588
|
150 cellules/µl
|
0,61 (0,45; 0,82)
| |
|
300 cellules/µl
|
0,49 (0,38; 0,63)
| |
|
500 cellules/µl
|
0,42 (0,31; 0,55)
|
Les résultats de cette étude ont servi de base pour définir les doses à évaluer dans les études ultérieures sur l'administration du mépolizumab par voie sous-cutanée. Nucala ne doit pas être administré par voie intraveineuse. Ce médicament doit être administré exclusivement par voie sous-cutanée.
Réduction des exacerbations (étude MEA115588), étude MENSA
L'étude MEA115588 (Mepolizumab as adjunctive therapy in patients with Severe Asthma) était une étude multicentrique randomisée, en double aveugle, avec contrôle versus placebo, par groupes parallèles, pour évaluer l'efficacité et la sécurité du mépolizumab en tant que médicament complémentaire chez 576 patients atteints d'asthme sévère à éosinophiles.
Les patients étaient âgés pour la plupart d'au moins 18 ans, avaient subi au moins deux exacerbations de l'asthme au cours des 12 derniers mois et leur asthme n'était pas contrôlé malgré leur pharmacothérapie anti-asthmatique en cours (corticostéroïdes à inhaler [CSI] à haute dose en association avec au moins un autre médicament approprié pour le contrôle de l'asthme, par exemple un agoniste bêta2-adrénergique à longue durée d'action [LABA] ou un antagoniste des leucotriènes). Pendant l'étude, les patients pouvaient utiliser des corticostéroïdes oraux et ont continué à recevoir leurs médicaments habituels contre l'asthme.
Un asthme sévère à éosinophiles était défini comme un taux d'éosinophiles ≥150 cellules/μl dans le sang périphérique au cours des 6 semaines précédant la randomisation (première dose) ou un taux sanguin ≥300 cellules/μl pendant l'année précédant la randomisation. Pendant 32 semaines, les patients ont reçu toutes les quatre semaines une injection de 100 mg de mépolizumab par voie sous-cutanée (s.c.), une injection de 75 mg de mépolizumab par voie intraveineuse (i.v.) ou un placebo. Les résultats du critère primaire de l'étude – la réduction de la fréquence des exacerbations cliniquement importantes de l'asthme – étaient statistiquement significatifs (p <0,001).
Le Tableau 3 donne un aperçu des résultats du critère primaire et des critères secondaires de l'étude MEA115588.
Tableau 3: Résultats du critère primaire et des critères secondaires à 32 semaines dans la population en intention de traitement (étude MEA115588)
|
|
Mépolizumab
(100 mg s.c.)
n = 194
|
Placebo
n = 191
| |
Critère primaire
| |
Fréquence des exacerbations cliniquement importantes
| |
Exacerbations par an
|
0,83
|
1,74
| |
Pourcentage de réduction
Rapport (IC à 95%)
|
53%
0,47 (0,35; 0,64)
|
-
| |
Valeur de p
|
<0,001
|
| |
Critères secondaires
| |
Fréquence des exacerbations ayant exigé une hospitalisation ou un traitement d'urgence
| |
Exacerbations par an
|
0,08
|
0,20
| |
Pourcentage de réduction
Rapport (IC à 95%)
|
61%
0,39 (0,18; 0,83)
|
-
| |
Valeur de p
|
0,015
|
| |
Fréquence des exacerbations ayant exigé une hospitalisation
| |
Exacerbations par an
|
0,03
|
0,10
| |
Pourcentage de réduction
Rapport (IC à 95%)
|
69%
0,31 (0,11; 0,91)
|
-
| |
Valeur p
|
0,034
|
| |
VEMS (ml) à 32 semaines avant l'administration d'un bronchodilatateur
| |
Variation moyenne versus valeur initiale (erreur type)
|
183 (31,1)
|
86 (31,4)
| |
Différence (mépolizumab vs placebo)
|
98
|
| |
IC à 95%
|
(11, 184)
|
| |
Valeur de p
|
0,028
|
| |
St. George's Respiratory Questionnaire (SGRQ) à 32 semaines
| |
Variation moyenne versus valeur initiale (erreur type)
|
-16,0 (1,13)
|
-9,0 (1,16)
| |
Différence (mépolizumab vs placebo)
|
-7,0
|
| |
IC à 95%
|
(-10,2; -3,8)
|
| |
Valeur de p
|
<0,001
|
|
Étude sur la réduction des corticostéroïdes oraux (étude SIRIUS)
L'étude MEA115575 a évalué l'effet du mépolizumab (100 mg par voie s.c.) pour réduire le besoin de corticostéroïdes oraux (CSO) dans le traitement d'entretien, en maintenant le contrôle de l'asthme chez des patients atteints d'asthme sévère à éosinophiles exigeant une corticothérapie systémique. Les patients, dont les taux d'éosinophiles dans le sang périphérique avaient été ≥300/µl dans les 12 mois précédant le screening/≥150/µl avant le début du traitement, ont reçu du mépolizumab ou un placebo à intervalles de quatre semaines pendant la phase de traitement. Au cours de la phase de réduction des CSO (semaines 4 à 20), la dose de CSO a été réduite toutes les 4 semaines tant que le contrôle de l'asthme restait maintenu. Les patients ont poursuivi leur traitement anti-asthmatique préexistant (corticostéroïdes à inhaler [CSI] à haute dose en association avec au moins un autre médicament pour le contrôle de l'asthme, par exemple agoniste bêta2-adrénergique à longue durée d'action [LABA] ou antagoniste des leucotriènes) pendant l'étude.
La population de l'étude, de 135 patients au total, présentait les caractéristiques suivantes: âge moyen de 50 ans, 55% de sexe féminin; 48% prenaient des corticostéroïdes oraux depuis au moins 5 ans et utilisaient une dose moyenne équivalente à environ 13 mg de prednisolone par jour au début de l'étude.
L'étude avait pour critère primaire la réduction de la dose journalière du CSO (semaines 20 à 24) obtenue sans perte du contrôle de l'asthme sous mépolizumab versus placebo (voir le Tableau 4).
Tableau 4: Résultats du critère primaire et des critères secondaires dans la population en intention de traitement de l'étude MEA115575
|
|
Mépolizumab
(100 mg s.c.)
n = 69
|
Placebo
n = 66
| |
Critère primaire
| |
Réduction (%) de la dose de CSO après 20 à 24 semaines par rapport à la dose initiale
| |
90% à 100%
|
16 (23%)
|
7 (11%)
| |
75% à <90%
|
12 (17%)
|
5 (8%)
| |
50% à <75%
|
9 (13%)
|
10 (15%)
| |
>0% à <50%
|
7 (10%)
|
7 (11%)
| |
Aucune réduction de la dose de CSO/contrôle insuffisant de l'asthme/arrêt prématuré du traitement
|
25 (36%)
|
37 (56%)
| |
Odds Ratio (IC à 95%)
|
2,39 (1,25; 4,56)
|
| |
Valeur de p
|
0,008
|
| |
Critères secondaires
| |
Réduction (%) de la dose journalière de CSO
| |
Réduction d'au moins 50%
|
37 (54%)
|
22 (33%)
| |
Odds Ratio (IC à 95%)
|
2,26 (1,10; 4,65)
|
| |
Valeur de p
|
0,027
|
| |
Réduction (%) de la dose journalière de CSO
| |
À ≤5 mg par jour
|
37 (54%)
|
21 (32%)
| |
Odds Ratio (IC à 95%)
|
2,45 (1,12; 5,37)
|
| |
Valeur de p
|
0,025
|
| |
Réduction (%) de la dose journalière de CSO
| |
À zéro
|
10 (14%)
|
5 (8%)
| |
Odds Ratio (IC à 95%)
|
1,67 (0,49; 5,75)
|
| |
Valeur de p
|
0,414
|
| |
Réduction médiane (%) de la dose journalière de CSO
| |
Réduction médiane (%) versus dose initiale (IC à 95%)
|
50,0 (20,0; 75,0)
|
0,0 (-20,0; 33,3)
| |
Différence médiane (IC à 95 %)
|
-30,0 (-66,7; 0,0)
|
| |
Valeur de p
|
0,007
|
|
À part cela, la qualité de vie liée à la santé a été évaluée à l'aide du SGRQ. À 24 semaines, une amélioration significative du score SGRQ moyen était constatable sous Nucala versus placebo: -5,8 (IC à 95%: -10,6; -1,0; p = 0,019). À 24 semaines, le pourcentage de patients ayant atteint une réduction cliniquement importante du score SGRQ (définie comme une réduction d'au moins 4 unités par rapport au score initial) était plus élevé sous Nucala (58%, 40/69) que sous placebo (41%, 27/66).
Le profil d'efficacité à long terme de Nucala chez les patients souffrant d'asthme sévère (n=998) qui avaient été traités dans les études de prolongation en ouvert MEA115666, MEA115661 et 201312 pendant une durée médiane de 2,8 ans (intervalle de 4 semaines à 4,5 ans) correspondait, en général, à celui des trois études contrôlées contre placebo.
Rhinosinusite chronique avec polypes nasaux (RSCaPN)
L'étude 205687 était une étude de 52 semaines, randomisée, en double aveugle et contrôlée contre placebo, dans laquelle 407 patients atteints de RSCaPN âgés de plus de 18 ans ont été examinés.
Les patients inclus dans cette étude devaient présenter un score VAS (échelle visuelle analogique) des symptômes d'obstruction nasale >5 (au max. 10 points), un score VAS total des symptômes >7 (au max. 10 points) et un score endoscopique bilatéral des polypes nasaux de 5 (au max. 8 points possibles; avec un score minimal de 2 par narine). En outre, les patients devaient avoir subi au moins une chirurgie des polypes nasaux au cours des 10 années précédentes.
Les patients ont reçu une dose de 100 mg de mépolizumab ou un placebo, administrés par voie sous-cutanée toutes les 4 semaines en complément de leur traitement de fond par corticostéroïdes intranasaux.
Les données démographiques et les propriétés à l'inclusion des patients ayant participé à l'étude 205687 sont présentés ci-dessous dans le Tableau 5:
Tableau 5: Données démographiques et propriétés à l'inclusion de la RSCaPN
|
|
N = 407
| |
Âge (années) des patients, moyenne (ET)
|
49 (13)
| |
Sexe féminin, n (%)
|
143 (35)
| |
Origine européenne, n (%)
|
379 (93)
| |
Durée (ans) de la RSCaPN, moyenne (ET)
|
11,4 (8,39)
| |
Patients ayant subi ≥1 chirurgie antérieure, n (%)
|
407 (100)
| |
Patients ayant subi ≥3 chirurgies antérieures, n (%)
|
124 (30)
| |
Utilisation de CSO à cause des PN (≥1 cure) dans les 12 derniers mois, n (%)
|
197 (48)
| |
Score endoscopique total des PNa b c, moyenne (ET), score max. = 8
|
5,5 (1,29)
| |
Score VASa d d'obstruction nasale, moyenne (ET), score max.= 10
|
9,0 (0,83)
| |
Score VAS total des symptômesa d, moyenne (ET), score max. = 10
|
9,1 (0,74)
| |
Score SNOT-22 totale, moyenne (ET), intervalle 0-110
|
64,1 (18,32)
| |
Score VAS composite des symptômesa, moyenne (ET), score max. = 10
|
9,0 (0,82)
| |
Score VASa,d de perte d'odorat, moyenne (ET), score max. = 10
|
9,7 (0,72)
| |
Asthme, n (%)
|
289 (71)
| |
AERD, n (%)
|
108 (27)
| |
Moyenne géométrique du taux d'éosinophiles à l'inclusion, cellules/µl (IC à 95%)
|
390 (360, 420)
|
RSCaPN = rhinosinusite chronique avec polypes nasaux, ET = écart-type, CSO = corticostéroïde oral, PN = polypes nasaux, VAS = échelle visuelle analogique, SNOT-22 = Sino-Nasal-Outcome-Test, AERD = maladie respiratoire exacerbée par l'aspirine
a Des scores plus élevés indiquent une sévérité plus importante de la maladie.
b Tels qu'évalués de manière aveugle par des investigateurs indépendants.
c Le score de PN est la somme des scores des deux narines (sur une échelle allant de 0 à 8), ceux-ci ayant été évalués pour chaque narine (0=absence de polypes; 1=petits polypes dans le méat nasal moyen, ne dépassant pas le dessous du bord inférieur du cornet moyen; 2=polypes atteignant le dessous du bord inférieur du cornet moyen; 3=grands polypes dépassant le bord inférieur du cornet inférieur ou polypes situés au centre du cornet moyen; 4=grands polypes provoquant une congestion/obstruction presque complète du méat nasal inférieur).
d Évalués tous les jours par les patients à l'aide d'une échelle allant de 0 à 10 (0=absence; 10=extrêmement grave).
e Le SNOT-22 est un test évaluant la qualité de vie liée à la santé et comprend 22 items dans 6 domaines de symptômes et de conséquences liés à la RSCaPN (nasaux, non nasaux, oreille/visage, sommeil, fatigue, conséquences émotionnelles). Des scores plus élevés indiquent une plus mauvaise qualité de vie liée à la santé.
Les critères d'évaluation co-primaires étaient la variation du score endoscopique total des PN à la semaine 52 par rapport à l'inclusion et la variation du score VAS moyen d'obstruction nasale aux semaines 49-52 par rapport à l'inclusion.
Les patients ayant reçu le mépolizumab présentaient par rapport au placebo des améliorations (réductions) significativement plus importantes du score endoscopique total des PN à la semaine 52 et du score VAS d'obstruction nasale aux semaines 49-52 (voir Tableau 6).
Tableau 6: Analyses des critères d'évaluation co-primaires (population en intention de traitement)
|
|
Placebo
(N=201)
|
Mépolizumab
100 mg s.c.
(N=206)
| |
Score endoscopique total à la semaine 52 a
| |
Score médian à l'inclusion (min, max)
|
6,0 (0, 8)
|
5,0 (2, 8)
| |
Variation médiane par rapport à l'inclusion
|
0,0
|
-1,0
| |
Valeur de p b
|
|
<0,001
| |
Différence ajustée des médianes entre les traitements (IC à 95%) c
|
|
-0,73 (-1,11, -0,34)
| |
Amélioration ≥1 point, n (%)
|
57 (28)
|
104 (50)
| |
Amélioration ≥2 points, n (%)
|
26 (13)
|
74 (36)
| |
Score VAS d'obstruction nasale (semaines 49 à 52) a
| |
Score médian à l'inclusion (min, max)
|
9,14 (5,31, 10,00)
|
9,01 (6,54, 10,00)
| |
Variation médiane par rapport à l'inclusion
|
-0,82
|
-4,41
| |
Valeur de p b
|
|
<0,001
| |
Différence ajustée des médianes entre les traitements (IC à 95%) c
|
|
-3,14 (-4,09, -2,18)
| |
Amélioration >1 point, n (%)
|
100 (50)
|
146 (71)
| |
Amélioration ≥3 points, n (%)
|
73 (36)
|
124 (60)
|
a Les participants à l'étude ayant subi une chirurgie nasale/sinusoplastie avant le rendez-vous de l'étude se sont vus attribuer le score le plus mauvais observé avant la chirurgie nasale/sinusoplastie. Les participants sortis de l'étude sans chirurgie nasale/sinusoplastie se sont vus attribuer le score le plus mauvais observé avant l'abandon de l'étude.
b Sur la base du test de la somme des rangs de Wilcoxon.
c Régression quantile avec comme covariables le groupe de traitement, la région géographique, le score à l'inclusion et le taux sanguin d'éosinophiles (log(s)) à l'inclusion.
Figure 1: Score endoscopique total des polypes nasaux (lecture centralisée) des répondeurs par contrôle
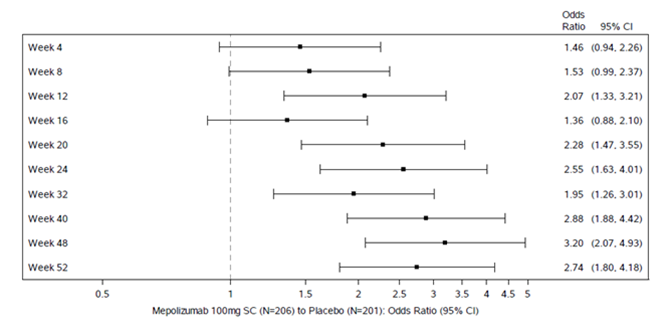
Tous les critères d'évaluation secondaires étaient statistiquement significatifs et confortaient les critères d'évaluation co-primaires. Le principal critère d'évaluation secondaire était le délai jusqu'à la première chirurgie des PN jusqu'à la semaine 52 (voir Figure 1). Les données sur les autres critères d'évaluation secondaires sont présentées dans le Tableau 7.
Délai jusqu'à la première chirurgie des PN
Pendant toute la période de traitement de 52 semaines, les patients du groupe mépolizumab ont eu une probabilité moindre de devoir subir une chirurgie des PN que les patients du groupe placebo (la chirurgie a été définie comme toute intervention impliquant des instruments entraînant une incision ou l'ablation de tissus [polypectomie] dans la cavité nasale).
Jusqu'à la semaine 52, 18 patients (9%) du groupe mépolizumab avaient subi une chirurgie des PN, contre 46 patients (23%) du groupe placebo.
Le délai jusqu'à la première chirurgie des PN était plus long chez les patients ayant reçu le mépolizumab que chez ceux sous placebo. Chez les patients traités par le mépolizumab, le risque de subir une intervention chirurgicale pendant la période de traitement était de 57% inférieur à celui observé chez les patients ayant reçu le placebo et était ainsi significativement plus faible (Hazard Ratio: 0,43; IC à 95% 0,25, 0,76; p ajusté/non ajusté =0,003); une analyse post-hoc a montré une réduction de 61% de la probabilité d'une intervention chirurgicale (Odds Ratio: 0,39, IC à 95%: 0,21, 0,72; p= 0,003).
Figure 2: Courbe de Kaplan-Meier pour le délai jusqu'à la première chirurgie des polypes nasaux
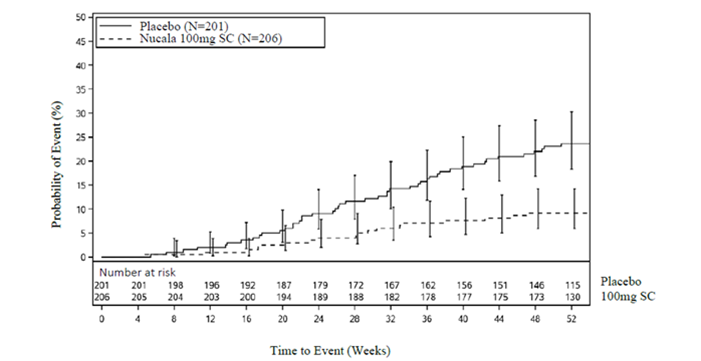
Tableau 7: Résultats des autres critères d'évaluation secondaires dans la population en intention de traitement
|
|
Placebo
(N=201)
|
Mépolizumab
(N=206)
| |
Score VAS total (semaines 49-52) a
| |
Score médian à l'inclusion (min, max)
|
9,20 (7,21, 10,00)
|
9,12 (7,17, 10,00)
| |
Variation médiane par rapport à l'inclusion
|
-0,90
|
-4,48
| |
Valeur de p ajustée/non ajustée b,c
|
|
<0,001/0,003
| |
Différence ajustée des médianes entre les traitements (IC à 95%) d
|
40
|
-3,18 (-4,10, -2,26)
| |
Amélioration ≥2,5 points (%)
|
|
64
| |
Score SNOT-22 total à la semaine 52 a, g
| |
N
|
198
|
205
| |
Score médian à l'inclusion (min, max)
|
64,0 (19, 110)
|
64,0 (17, 105)
| |
Variation médiane par rapport à l'inclusion
|
-14,0
|
-30,0
| |
Valeur de p ajustée/non ajustée b,c
|
|
<0,001/0,003
| |
Différence ajustée des médianes entre les traitements (IC à 95%) d
|
32
|
-16,49 (-23,57, -9,42)
| |
Amélioration ≥28 points (%)g
|
|
54
| |
Patients nécessitant des stéroïdes systémiques jusqu'à la semaine 52 à cause de polypes nasaux
| |
Nombre de patients avec ≥1 cure
|
74 (37)
|
52 (25)
| |
Odds Ratio par rapport au placebo (IC à 95%)
|
|
0,58 (0,36, 0,92)
| |
Valeur de p ajustée/non ajustée c, e
|
|
0,020/0,020
| |
Score VAS composite – symptômes nasaux (semaines 49-52) a,f
| |
Score médian à l'inclusion (min, max)
|
9,18 (6,03, 10,00)
|
9,11 (4,91, 10,00)
| |
Variation médiane par rapport à l'inclusion
|
-0,89
|
-3,96
| |
Valeur de p ajustée/non ajustée b,c
|
|
<0,001/0,020
| |
Différence ajustée des médianes entre les traitements (IC à 95%) d
|
40
|
-2,68 (-3,44, -1,91)
| |
Amélioration ≥2 points (%)h
|
|
66
| |
Score VAS de perte d'odorat (semaines 49-52) a
| |
Score médian à l'inclusion (min, max)
|
9,97 (6,69, 10,00)
|
9,97 (0,94, 10,00)
| |
Variation médiane par rapport à l'inclusion
|
0,00
|
-0,53
| |
Valeur de p ajustée/non ajustée b,c
|
|
<0,001/0,020
| |
Différence ajustée des médianes entre les traitements (IC à 95%) d
|
19
|
-0,37 (-0,65, -0,08)
| |
Amélioration ≥3 points (%)h
|
|
36
|
a Les patients ayant subi une chirurgie nasale/sinusoplastie avant le rendez-vous de l'étude se sont vus attribuer le score le plus mauvais observé avant la chirurgie nasale/sinusoplastie. Les participants sortis de l'étude sans chirurgie nasale/sinusoplastie se sont vus attribuer le score le plus mauvais observé avant l'abandon de l'étude.
b Sur la base du test de la somme des rangs de Wilcoxon.
c Multiplicité contrôlée à l'aide de tests des critères d'évaluation secondaires selon une hiérarchie prédéfinie.
d Régression quantile avec comme covariables le groupe de traitement, la région géographique, le score à l'inclusion et le taux sanguin d'éosinophiles (log(s)) à l'inclusion.
e Analyse ayant utilisé un modèle de régression logistique avec comme covariables le groupe de traitement, la région géographique, le nombre de cures de CSO pour les PN au cours des 12 derniers mois (0,1, >1 comme nombre ordinal), le score endoscopique total des PN à l'inclusion (lecture centralisée), le score VAS d'obstruction nasale et le taux sanguin d'éosinophiles (log(s)) à l'inclusion.
f Score VAS composite pour l'obstruction nasale, l'écoulement nasal, le mucus pharyngé et la perte d'odorat.
g Une amélioration a été observée dans les 6 domaines des symptômes et conséquences liés à la RSCaPN.
h La valeur limite de l'amélioration de chaque critère d'évaluation a été déterminée comme variation intra-individuelle judicieuse.
Critères d'évaluation du sous-groupe de patients atteints d'un asthme comorbide
Chez 289 (71%) patients atteints d'un asthme comorbide, des analyses prédéfinies chez les patients ayant reçu 100 mg de mépolizumab ont montré des améliorations des critères d'évaluation co-primaires par rapport au placebo, qui concordaient avec celles de la population totale.
Granulomatose éosinophilique avec polyangéite (GEPA)
MEA115921 était une étude d'une durée de 52 semaines, randomisée, en double aveugle, contrôlée contre placebo portant sur 136 patients à partir de 18 ans souffrant d'une GEPA récidivante ou réfractaire au traitement, sous dose stable de corticostéroïdes oraux (CSO; ≥7,5 à ≤50 mg/jour de prednisolone/prednisone). 53% (n = 72) des participants ont reçu simultanément des immunosuppresseurs à une dose stable.
Les patients ont reçu une dose de 300 mg de mépolizumab ou de placebo par voie sous-cutanée toutes les quatre semaines en complément de leur traitement de base par la prednisolone/prednisone avec ou sans immunosuppresseurs. La dose de corticostéroïde oral a été progressivement réduite à la discrétion du médecin investigateur.
Les critères d'évaluation primaire étaient la durée globale cumulative de rémission, la rémission étant définie par un Birmingham Vasculitis Activity Score (BVAS) de 0 (pas de vascularite active) plus une dose de prednisolone/prednisone ≤4 mg/jour, ainsi que le pourcentage de participants en rémission au bout de 36 et 48 semaines de traitement.
Rémission
Par rapport au groupe sous placebo, les participants sous 300 mg de mépolizumab ont obtenu une durée de rémission globale significativement plus longue. Par ailleurs, le pourcentage de participants en rémission sous 300 mg de mépolizumab à la semaine 36 et à la semaine 48 était significativement plus élevé que sous placebo (Tableau 8).
Tableau 8: Analyses des deux critères d'évaluation primaires (population ITT)
|
|
Nombre (%) de participants
| |
Placebo n = 68
|
Mépolizumab 300 mg n = 68
| |
Durée de rémission globale pendant 52 semaines
| |
0 semaine
|
55 (81)
|
32 (47)
| |
>0 à <12 semaines
|
8 (12)
|
8 (12)
| |
12 à <24 semaines
|
3 (4)
|
9 (13)
| |
24 à <36 semaines
|
0
|
10 (15)
| |
≥36 semaines
|
2 (3)
|
9 (13)
| |
Odds Ratio (mépolizumab/placebo)
|
|
5,91
| |
IC à 95 %
|
----
|
2,68; 13,03
| |
Valeur de p
|
----
|
<0,001
| |
Participants en rémission aux semaines 36 et 48
|
2 (3)
|
22 (32)
| |
Odds Ratio (mépolizumab / placebo)
|
|
16,74
| |
IC à 95%
|
----
|
3,61; 77,56
| |
Valeur de p
|
----
|
<0,001
|
Un Odds Ratio >1 parle en faveur du mépolizumab
Les participants sous 300 mg de mépolizumab ont obtenu une durée de rémission globale significativement plus longue (p <0,001), et le pourcentage de participants en rémission sous 300 mg de mépolizumab selon la définition de la rémission appliquée pour le critère d'évaluation secondaire (BVAS = 0 plus prednisolone/prednisone ≤7,5 mg/jour) était supérieur à celui sous placebo (p <0,001) tant à la semaine 36 qu'à la semaine 48.
Récidive
Par rapport au placebo, la durée jusqu'à la première récidive (définie comme une aggravation liée à une vascularite, de l'asthme ou des symptômes sinonasaux nécessitant une augmentation de la dose de corticostéroïdes ou d'immunosuppresseurs ou une hospitalisation) était significativement plus longue chez les participants sous 300 mg de mépolizumab (p <0,001). En outre, le taux annualisé de récidives était inférieur de 50% chez les patients sous mépolizumab par rapport à ceux sous placebo: 1,14 vs 2,27.
Réduction de la dose de corticostéroïdes oraux
Par rapport aux participants sous placebo, les participants sous 300 mg de mépolizumab ont reçu une dose quotidienne moyenne de corticostéroïdes oraux inférieure (p <0,001) durant les semaines 48 à 52. Dans le groupe sous 300 mg de mépolizumab, 12 participants (18%) ont pu complètement arrêter, de manière progressive, le traitement par les corticostéroïdes oraux contre 2 participants (3%) dans le groupe sous placebo.
Syndrome hyperéosinophilique (SHE)
L'étude 200622 était une étude de 32 semaines randomisée, contrôlée contre placebo, en double aveugle, dans laquelle 108 patients atteints de SHE âgés de ≥12 ans ont été examinés. Les patients atteints de SHE secondaire non hématologique (par ex. hypersensibilité aux médicaments, infection parasitaire, infection par le VIH, tumeur maligne non hématologique) ou de SEH F/P positif ont été exclus de l'étude. Les patients ont reçu par voie sous-cutanée 300 mg de mépolizumab ou un placebo toutes les 4 semaines, en plus de leur traitement stable pour le SHE. Un des 4 adolescents inclus a reçu 300 mg de mépolizumab, les autres 3 ont reçu le placebo, pendant 32 semaines pour chacun d'entre eux. Le traitement standard du SHE pouvait englober des CSO, des immunosuppresseurs ou des cytotoxiques. Les participants à l'étude avaient souffert d'au moins deux poussées de SHE au cours des 12 derniers mois et présentaient lors de la sélection un taux d'éosinophiles sanguins ≥1000 cellules/µl.
Le critère d'évaluation primaire de l'étude 200622 était le pourcentage de participants à l'étude qui ont souffert d'une poussée de SHE pendant la période de traitement de 32 semaines. Une poussée de SHE était définie comme une aggravation des signes et symptômes cliniques de SHE ou comme une élévation des éosinophiles (à deux moments au minimum) ayant nécessité une augmentation des CSO ou une augmentation de la dose ou l'administration d'un traitement adjuvant cytotoxique ou immunosuppresseur du SHE.
L'analyse primaire a comparé les patients des groupes du mépolizumab et du placebo qui avaient subi une poussée de SHE ou qui avaient quitté l'étude. Par rapport au groupe sous placebo, le nombre de patients du groupe ayant reçu 300 mg de mépolizumab qui ont subi une poussée de SHE ou qui ont quitté l'étude a été réduit de 50% pendant la période de traitement de 32 semaines; 28% versus 56% (OR 0,28, IC à 95% 0,12–0,64) (voir Tableau 9).
Les critères d'évaluation secondaires étaient le temps écoulé jusqu'à la première poussée de SHE, le pourcentage de participants à l'étude qui ont souffert d'une poussée de SHE entre la semaine 20 et la semaine 32, le taux de poussées de SHE et la variation du degré de gravité de la fatigue par rapport à la valeur initiale. Tous les critères d'évaluation secondaires ont été statistiquement significatifs et ont corroboré le critère d'évaluation primaire (voir Figure 3 et Tableau 10).
Tableau 9: Résultats obtenus pour le critère d'évaluation primaire / résultats de l'analyse primaire dans la population en intention de traitement (étude 200622)
|
|
Mépolizumab
N = 54
|
Placebo
N = 54
| |
Pourcentage de patients qui ont subi une poussée de SHE
| |
Participants à l'étude avec ≥1 poussée de SHE ou ayant arrêté l'étude (%)
|
15 (28)
|
30 (56)
| |
Participants à l'étude avec ≥1 poussée de SHE (%)
|
14 (26)
|
28 (52)
| |
Participants à l'étude sans poussée de SHE qui ont arrêté l'étude (%)
|
1 (2)
|
2 (4)
| |
Odds Ratio (IC à 95%)
|
0,28 (0,12–0,64)
|
| |
Valeur p au CMH
|
0,002
|
|
CMH = Cochran-Mantel-Haenszel
Temps écoulé jusqu'à la première poussée
Chez les participants à l'étude sous 300 mg de mépolizumab, le temps écoulé jusqu'à la première poussée de SHE a été significativement plus long que chez les patients sous placebo. Le risque d'une première poussée de SHE pendant la période de traitement a été inférieur de 66% chez les patients sous mépolizumab que chez les patients sous placebo (Hazard Ratio: 0,34, IC à 95% 0,18–0,67, p = 0,002).
Figure 3: Courbe de Kaplan-Meier pour le temps écoulé jusqu'à la première poussée de SHE
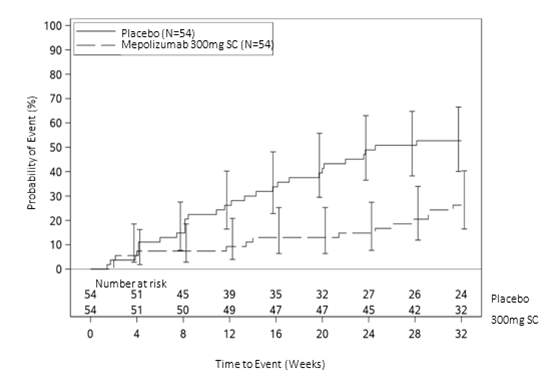
Tableau 10 Résultats pour d'autres critères d'évaluation secondaires dans la population en intention de traitement (étude 200622)
|
|
Mépolizumab
N = 54
|
Placebo
N = 54
| |
Poussées de SHE entre la semaine 20 et la semaine 32 incluse
| |
Participants à l'étude avec ≥1 poussée de SHE ou ayant quitté l'étude (%)
|
9 (17)
|
19 (35)
| |
Odds Ratio (IC à 95%)
|
0,33 (0,13–0,85)
| |
Valeur p CMH (non corrigée/corrigée)a
|
0,02/0,02
| |
Taux des poussées de SHE
| |
Taux annuel moyen estimé
|
0,50
|
1,46
| |
Rapport des taux (IC à 95%)
|
0,34 (0,19–0,63)
| |
Valeur p de Wilcoxon (ajustée/ajustée)a
|
0,002/0,02
| |
Variation du degré de gravité de la fatigue par rapport à la valeur initiale, sur la base de l'item 3 du Brief Fatigue Inventory (BFI) (manifestation la plus grave de la fatigue au cours des dernières 24 heures) à la semaine 32b
| |
Variation médiane de l'item 3 du BFI
|
-0,66
|
0,32
| |
Comparaison des valeurs p (mépolizumab vs placebo) (ajustée/ajustée) a
|
0,036/0,036
|
|
a Valeurs p ajustées, sur la base d'une hiérarchie de critères préalablement établie.
b Les patients dont les données manquaient ont été inclus en utilisant la valeur observée la plus mauvaise.
CMH = Cochran-Mantel-Haenszel
Phase ouverte de prolongation pour le SHE
Après la fin de l'étude 200622, des patients appropriés, dont 4 adolescents, ont poursuivi avec l'étude ouverte de prolongation de 20 semaines 205203, dans laquelle le profil de sécurité à long terme a été examiné et des données additionnelles ont été obtenues sur le bénéfice clinique du mépolizumab au-delà de 32 semaines chez les patients atteints de SHE.
L'effet du traitement par le mépolizumab sur la réduction des poussées de SHE observé dans l'étude 200622 s'est maintenu chez les patients qui ont poursuivi le traitement par le mépolizumab dans l'étude 205203: dans cette étude, 94% (47/50) des patients n'ont pas présenté de poussées.
Durant les semaines 16 à 20, 28% de tous les patients qui avaient reçu une dose moyenne de CSO > 0 mg/jour (prednisone ou équivalent) pendant les semaines 0 à 4, ont réussi à atteindre une réduction de ≥50% de leur dose journalière moyenne de CSO. Les données d'efficacité de cette étude suggèrent que le bénéfice clinique du mépolizumab se maintient sur 52 semaines et permet une réduction du traitement par CSO chez les patients atteints de SHE.
|



