Propriétés/EffetsATC-Code
L04AB04
Imraldi est un biosimilaire.
Mécanisme d'action
L'adalimumab est un anticorps monoclonal humain fabriqué dans des cellules CHO par une technologie à base d'ADN recombinant. Il a été mis au point avec des chaînes lourdes et légères humaines par la méthode «phage display». On obtient ainsi un anticorps doté de régions variables des chaînes lourdes et légères sans séquence peptidique animale, ce qui permet une spécificité pour le facteur de nécrose tumorale (TNF) humain, mais aussi doté de régions constantes humaines IgG1 (chaîne lourde) et kappa (chaîne légère). L'adalimumab se lie avec une affinité et une spécificité élevées au facteur de nécrose tumorale soluble (TNF-α), mais pas à la lymphotoxine (TNF-β). Il comporte 1330 acides aminés et son poids moléculaire est de 148 kilodalton environ.
L'adalimumab se lie spécifiquement au TNF et neutralise la fonction biologique du TNF par inhibition de son interaction avec les récepteurs du TNF p55 et p75 à la surface des cellules. Le TNF est une cytokine naturelle importante pour les réponses inflammatoires et immunitaires normales. Chez les patients atteints de polyarthrite rhumatoïde, d'arthrite psoriasique ou de spondylarthrite ankylosante (maladie de Bechterew), on observe des concentrations élevées de TNF dans le liquide synovial, qui jouent un rôle important aussi bien dans le cadre de l'inflammation pathologique que de la destruction de l'articulation, signes caractéristiques de la polyarthrite rhumatoïde.
L'adalimumab module aussi des réactions biologiques provoquées ou gouvernées par le TNF, entre autres les modifications des concentrations en molécules d'adhésion, responsables de la migration des leucocytes (ELAM-1, VCAM-1 et ICAM-1, avec une CI50 de 1-2× 10-10 M).
Pharmacodynamique
Après traitement par adalimumab, en comparaison avec les valeurs initiales, on observe chez les patients atteints de polyarthrite rhumatoïde une régression plus rapide des valeurs des paramètres de la phase aiguë de l'inflammation (protéine C réactive [CRP]), de la vitesse de sédimentation des érythrocytes (VSE) et des cytokines sériques (IL-6). La concentration sérique des métalloprotéinases matricielles (MMP-1 et MMP-3), qui entraînent la dégradation tissulaire responsable de la destruction du cartilage, diminue également après administration d'adalimumab. On constate souvent, chez les patients atteints de polyarthrite rhumatoïde, d'arthrite psoriasique ou de spondylarthrite ankylosante (maladie de Bechterew), une anémie légère à modérée, une diminution du nombre de lymphocytes et une augmentation des nombres de neutrophiles et de thrombocytes. Chez les patients traités par adalimumab, on observe généralement une amélioration de ces signes hématologiques d'inflammation chronique.
Une régression rapide des taux de CRP après le traitement par adalimumab a été observée aussi chez les patients atteints de la maladie de Crohn, de colite ulcéreuse, de la forme polyarticulaire de l'arthrite juvénile idiopathique et de l'hidradénite suppurée.
Chez les patients atteints de la maladie de Crohn, une diminution (statistiquement non significative) des cellules exprimant des marqueurs d'inflammation dans le côlon, y compris une diminution significative de l'expression de TNF-α, a été également observée.
Efficacité clinique
Polyarthrite rhumatoïde
L'adalimumab a été étudié chez plus de 3000 patients dans le cadre de toutes les études cliniques sur la polyarthrite rhumatoïde. Certains patients ont été traités sur une période de plus de 60 mois. L'efficacité et la tolérance de l'adalimumab en tant que traitement de la polyarthrite rhumatoïde ont été étudiées dans cinq études randomisées, en double aveugle et bien contrôlées.
L'étude 1 a permis d'évaluer 271 patients souffrant d'une polyarthrite rhumatoïde active modérée à sévère, âgés de ≥18 ans, ne répondant pas au traitement avec au moins un, mais pas plus de quatre antirhumatismaux de fond, chez lesquels on avait observé une efficacité insuffisante du méthotrexate à une dose de 12,5 à 25 mg (10 mg en cas d'intolérance au méthotrexate) par semaine, et pour lesquels la dose de méthotrexate était restée constante pendant l'étude, entre 10 et 25 mg par semaine. Les patients avaient ≥6 articulations enflées et ≥9 articulations sensibles à la pression. La polyarthrite rhumatoïde avait été diagnostiquée en appliquant les critères de l'American College of Rheumatology (ACR). Pendant 24 semaines, les patients ont reçu, toutes les deux semaines, des doses de 20, 40 ou 80 mg d'adalimumab ou un placebo.
L'étude 2 a permis d'évaluer 544 patients présentant une polyarthrite rhumatoïde active modérée à sévère, âgés de ≥18 ans et n'ayant pas répondu à un traitement comportant au moins un antirhumatismal de fond. Les patients présentaient ≥10 articulations enflées et ≥12 articulations sensibles à la pression, et ils avaient également été diagnostiqués selon les critères de l'ACR. Pendant 26 semaines, les patients ont reçu 20 ou 40 mg d'adalimumab toutes les deux semaines par injection sous-cutanée en alternance avec un placebo la semaine suivante, ou chaque semaine. Le placebo a été administré chaque semaine pour la même durée. Les patients ne suivaient aucun traitement d'appoint par agents antirhumatismaux de fond.
L'étude 3 a permis d'évaluer 619 patients souffrant d'une polyarthrite rhumatoïde active modérée à sévère, âgés de ≥18 ans, chez lesquels le méthotrexate à une dose de 12,5 à 25 mg (10 mg en cas d'intolérance au méthotrexate) par semaine avait eu une efficacité insuffisante et pour lesquels la dose de méthotrexate était restée constante pendant l'étude, entre 12,5 et 25 mg par semaine. À la différence de l'étude 1, l'inclusion des patients de l'étude 3 ne supposait pas obligatoirement l'échec préalable d'un traitement par antirhumatismaux de fond (méthotrexate exclu). Les patients avaient ≥6 articulations enflées et ≥9 articulations sensibles à la pression. La polyarthrite rhumatoïde avait été diagnostiquée en appliquant les critères de l'ACR. Cette étude comprenait trois groupes. Le groupe 1 a reçu une injection de placebo chaque semaine pendant 52 semaines. Le deuxième groupe a reçu 20 mg d'adalimumab chaque semaine pendant 52 semaines. Le troisième groupe a reçu 40 mg d'adalimumab toutes les deux semaines, en alternance avec une injection de placebo. À la fin des 52 premières semaines, 457 patients ont été inclus dans une phase d'extension en ouvert de 5 ans maximum pendant laquelle ils ont reçu 40 mg d'adalimumab toutes les deux semaines.
L'étude 4 a permis d'évaluer 636 patients souffrant de polyarthrite rhumatoïde active modérée à sévère, âgés ≥18 ans. Ces patients remplissaient les critères diagnostiques de polyarthrite rhumatoïde de l'ACR depuis au moins trois mois et présentaient ≥6 articulations enflées et ≥9 articulations sensibles à la pression. Ces patients soit n'avaient jamais été traités par antirhumatismaux de fond, soit pouvaient poursuivre leur traitement rhumatologique en cours, à la condition que celui-ci soit resté stable depuis au moins 28 jours. Les patients ont été randomisés dans le groupe de traitement par 40 mg d'adalimumab ou de placebo toutes les deux semaines, pendant 24 semaines.
Dans l'étude 5 concernant la polyarthrite rhumatoïde précoce, 525 patients adultes (≥18 ans) atteints d'une polyarthrite rhumatoïde active modérée à sévère précoce (durée de la maladie inférieure à 3 ans), et n'ayant pas été traités par méthotrexate, ont été évalués. Dans cette étude, l'efficacité de l'adalimumab associé au méthotrexate a été comparée au méthotrexate en monothérapie en ce qui concerne la réduction de signes, de symptômes et de la progression de lésions articulaires dans la polyarthrite rhumatoïde. Les patients ont été randomisés dans le groupe de traitement adalimumab 40 mg toutes les deux semaines associé au méthotrexate ou dans le groupe traité par méthotrexate toutes les deux semaines en monothérapie. Le traitement a duré 104 semaines.
Les résultats de ces cinq études ont été exprimés sous forme du pourcentage de patients présentant une amélioration de leur polyarthrite rhumatoïde selon les critères de réponse de l'ACR. Le critère d'évaluation primaire des études 1, 2 et 3 et le critère secondaire de l'étude 4 était le pourcentage de patients ayant atteint un taux de réponse ACR 20 à la semaine 24 ou 26. Le critère d'évaluation primaire de l'étude 5 portant sur la polyarthrite rhumatoïde précoce a été de déterminer le pourcentage de patients atteignant une réponse ACR 50 à la semaine 52. Les études 3 et 5 ont défini comme critère d'évaluation primaire supplémentaire un retard de progression de la maladie (constaté par radiographie) à la semaine 52. Dans l'étude 3, les changements de la qualité de vie ont été également étudiés dans le cadre du critère d'évaluation primaire.
Taux de réponse selon l'ACR
Le pourcentage de patients traités par adalimumab ayant atteint des taux de réponse ACR 20, ACR 50 et ACR 70 a été cohérent dans les études 1, 2, 3 et 4. Les résultats obtenus à la dose de 40 mg d'adalimumab administrée toutes les deux semaines sont résumés dans le tableau 1.
Tableau 1: Taux de réponse ACR au cours des études contrôlées contre placebo (en pourcentage de patients)
|
Taux de réponse
|
Étude 1a*
|
Étude 2a*
|
Étude 3a*
|
Étude 4
| |
|
Placebo/ MTXc n=60
|
Adalimumabb/ MTXc n=63
|
Placebo n=110
|
Adalimumabb n=113
|
Placebo/ MTXc n=200
|
Adalimumabb/ MTXc n=207
|
Traitement standard/ Placebo n=318
|
Traitement standard/ Adalimumab n=318
| |
ACR 20
| |
6 mois
|
13,3%
|
65,1%
|
19,1%
|
46,0%
|
29,5%
|
63,3%
|
34,9%
|
53,0%
| |
12 mois
|
NA
|
NA
|
NA
|
NA
|
24,0%
|
58,9%
|
NA
|
NA
| |
ACR 50
| |
6 mois
|
6,7%
|
52,4%
|
8,2%
|
22,1%
|
9,5%
|
39,1%
|
11,1%
|
29,2%
| |
12 mois
|
NA
|
NA
|
NA
|
NA
|
9,5%
|
41,5%
|
NA
|
NA
| |
ACR 70
| |
6 mois
|
3,3%
|
23,8%
|
1,8%
|
12,4%
|
2,5%
|
20,8%
|
3,2%
|
14,9%
| |
12 mois
|
NA
|
NA
|
NA
|
NA
|
4,5%
|
23,2%
|
NA
|
NA
|
a Étude 1 à 24 semaines, étude 2 à 26 semaines et étude 3 à 24 et 52 semaines.
b 40 mg d'adalimumab administrés toutes les deux semaines
c MTX = méthotrexate
* p<0,01, Adalimumab vs. Placebo
NA = sans objet
Les patients ayant reçu, au cours de l'étude 2, 40 mg d'adalimumab par semaine, ont atteint des taux de réponse ACR20, ACR50 et ACR70 statistiquement significatifs à hauteur de 53,4%, 35,0% et 18,4% après 6 mois.
Au cours des études 1-4, une amélioration de toutes les composantes individuelles des critères de réponse de l'ACR a été observée par comparaison avec le placebo à 24 et 26 semaines (nombre d'articulations sensibles à la pression et enflées, évaluation de l'activité de la maladie et des douleurs par le médecin et le patient, évaluation en fonction de l'index de handicap [HAQ] et des concentrations de CRP [mg/dl]). Au cours de l'étude 3, ces améliorations se sont aussi maintenues pendant 52 semaines. De plus, les taux de réponse selon les critères de l'ACR ont été maintenus jusqu'à la semaine 104 pour la majorité des patients participant à la phase d'extension en ouvert. Les résultats à deux ans de l'étude montrent que chez 24% des patients traités par adalimumab, il a été possible d'obtenir un effet clinique, défini comme un taux de réponse ACR70 maintenu pendant 6 mois. Un effet clinique durable jusqu'à 5 ans a pu être démontré pendant les phases non contrôlées de l'étude III. Le taux de réponse ACR observé à la semaine 52 a pu être maintenu lorsque l'adalimumab a été administré sans interruption pendant 5 ans, avec un taux de réponse ACR20 de 75,5% dans le sous-groupe de 220 patients évalués après 5 ans. Le taux de réponse ACR70 à 5 ans était de 34,7%. Chez 25,7% des patients, la dose de méthotrexate administrée concomitamment a pu être réduite sans diminution de l'effet clinique; le même phénomène a été observé pour les corticostéroïdes chez 29,9% de ces patients.
La figure 1 illustre la persistance du taux de réponse ACR20 obtenu sous adalimumab au cours de l'étude 3. Dans le cadre de cette étude, 84,7% des patients ayant atteint un taux de réponse ACR20 à la semaine 24 l'ont maintenu jusqu'à la semaine 52.
Figure 1: Taux de réponse ACR20 sur 52 semaines pendant l'étude 3
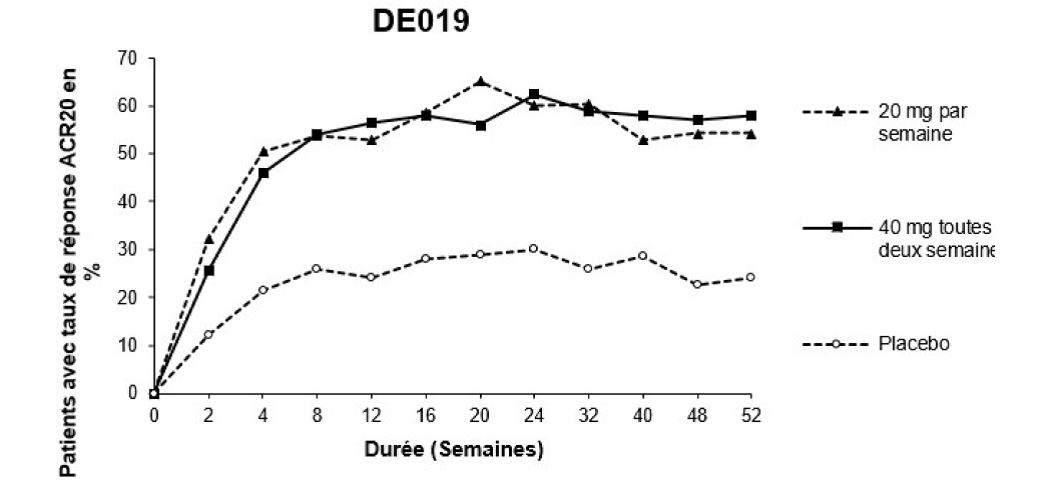
Au cours de l'étude 4, les taux de réponse ACR20 des patients traités par adalimumab en plus du traitement standard ont été meilleurs, de manière statistiquement significative, que ceux des patients prenant un placebo en plus du traitement standard (p <0,001).
Dans les quatre études, les patients traités par adalimumab ont atteint les taux de réponse ACR20, ACR50 et ACR70 plus élevés et plus rapidement que les patients recevant le placebo. Au cours de l'étude 1, une différence statistiquement significative a été observée pour les taux de réponse ACR20 à la semaine 1 (premier examen dans le cadre de l'étude) entre les patients traités par adalimumab (26,0%) et ceux recevant un placebo (5,0%). Des différences statistiquement significatives des taux de réponse ACR20 ont aussi été observées au cours des études 2, 3 et 4 à la semaine 2 (premier examen dans le cadre de l'étude) entre les patients traités par adalimumab (36,4%, 29,1% et 33,7%) et les patients recevant le placebo (7,3%, 13,0% et 8,6%). Un modèle similaire s'est dégagé des quatre études pour la période précédant l'obtention d'une première réponse ACR50 et ACR70.
Pour quelques patients qui ne prennent pas concomitamment du méthotrexate, une augmentation de la fréquence d'administration d'adalimumab à 40 mg par semaine pourrait apporter un bénéfice supplémentaire. Cette observation a été faite lors d'une étude au long cours en ouvert, pendant laquelle la fréquence d'administration a été augmentée pour les patients ne répondant que partiellement au traitement, passant de 40 mg toutes les deux semaines à 40 mg par semaine.
Dans l'étude 5, le traitement associant l'adalimumab et le méthotrexate chez des patients atteints de polyarthrite rhumatoïde précoce et n'ayant jamais été traités par méthotrexate, a entraîné un taux de réponse rapide et significativement plus élevé à la semaine 52 qu'avec le méthotrexate en monothérapie, avec un taux de réponse maintenu jusqu'à la semaine 104 (voir tableau 2).
Tableau 2: Taux de réponse dans l'étude 5 (en pourcentage du nombre de patients)
|
Taux de réponse*
|
MTX n=257
|
Adalimumab/MTX n=268
| |
ACR 20
| |
Semaine 52
|
62,6%
|
72,8%
| |
Semaine 104
|
56,0%
|
69,4%
| |
ACR 50
| |
Semaine 52
|
45,9%
|
61,6%
| |
Semaine 104
|
42,8%
|
59,0%
| |
ACR 70
| |
Semaine 52
|
27,2%
|
45,5%
| |
Semaine 104
|
28,4%
|
46,6%
|
* p <0,05, adalimumab/méthotrexate comparé au méthotrexate pour ACR20
* p <0,001, adalimumab/méthotrexate comparé au méthotrexate pour ACR50 et 70
Tous les critères de réponse ACR ont montré une amélioration à la semaine 52 sous traitement par adalimumab/méthotrexate, maintenue jusqu'à la semaine 104. Au cours de l'étude sur deux ans, 48,5% des patients ayant été traités par l'association adalimumab/méthotrexate ont atteint une réponse clinique majeure (ACR70 pendant six mois). En comparaison, 27,2% des patients traités par méthotrexate en monothérapie (p <0,001) ont atteint ces résultats.
Tableau 3: Taux de réponse DAS28 dans l'étude 5 en cas de polyarthrite rhumatoïde précoce
|
DAS28
Réponse
|
MTX n=257
|
Adalimumab/MTX n=268
| |
Différence moyenne par rapport au début de l'étude
| |
Début de l'étude (valeur moyenne)
|
6,3
|
6,3
| |
Semaine 52 (valeur moyenne ± écart type)
|
-2,8 ± 1,4
|
-3,6 ± 1,3*
| |
Semaine 104 (valeur moyenne ± écart type)
|
-3,1 ± 1,4
|
-3,8 ± 1,3*
| |
Rémission (DAS28<2,6)
| |
Semaine 52 (pourcentage de patients)
|
20,6%
|
42,9%*
|
* p <0,001, adalimumab/méthotrexate comparé au méthotrexate
Réponse radiographique
Au cours de l'étude 3, dans laquelle les patients traités par adalimumab étaient atteints de polyarthrite rhumatoïde depuis environ 11 ans en moyenne, les lésions articulaires structurelles ont été évaluées par radiographie et exprimées en termes de modification du score global de Sharp (SST) modifié et de ses composantes, à savoir le score d'érosion et le joint space narrowing score (JSN, score évaluant l'amincissement de l'espace articulaire). Une différence statistiquement significative a été observée à 6 mois pour le changement du score global de Sharp modifié, ainsi que pour le score d'érosion, et cette différence s'est maintenue jusqu'à 12 mois. À 52 semaines, les patients traités par adalimumab/méthotrexate présentaient moins de modifications radiologiques que les patients traités par le méthotrexate seul. Cet effet de ralentissement de la progression des lésions structurelles a pu être maintenu pendant 5 ans.
Parmi les patients initialement traités par 40 mg d'adalimumab toutes les deux semaines, 55% ont subi un examen radiologique après 5 ans. Le ralentissement de la progression des lésions structurelles a pu être maintenu et, chez 50% de ces patients, la progression des lésions structurelles a pu être complètement stoppée, ce qui se manifeste par une modification du score SST de zéro ou moins. Les patients ayant été traités par méthotrexate pendant la phase en double aveugle de l'étude ont présenté une progression minimale des lésions structurelles lorsqu'ils ont été traités par adalimumab lors de la phase ouverte de l'étude.
Tableau 4: Modification radiographique à 12 mois pour l'étude 3 avec traitement d'arrière-plan par méthotrexate
|
|
Placebo n=200
|
Adalimumaba n=113
|
Différence entre l'adalimumab et le placebo
|
Valeur de p
| |
Changement du score global de Sharp modifié (moyenne)
|
2,7
|
0,1
|
-2,6
|
=0,001b
| |
Modification des érosions (moyenne)
|
1,6
|
0,0
|
-1,6
|
=0,001
| |
Pas de nouvelles érosions (pourcentage des patients)
|
46,2
|
62,9
|
16,7
|
=0,001
| |
Modification du score JSN (moyenne)
|
1,0
|
0,1
|
-0,9
|
=0,002
|
a 40 mg, administrés toutes les deux semaines
b sur la base des valeurs moyennes, mesurées par le SST
Dans l'étude 5 portant sur des patients atteints de polyarthrite rhumatoïde précoce, les patients traités par adalimumab avaient une durée de maladie moyenne inférieure à 9 mois et n'avaient auparavant pas été traités par méthotrexate. Les lésions articulaires structurelles ont été évaluées par radiographie et exprimées en termes de score global de Sharp modifié. Les résultats obtenus à la semaine 52 sont décrits dans le tableau 5. Un changement statistiquement significatif concernant le score global de Sharp modifié et le score d'érosion a été constaté à la semaine 52 et a été maintenu jusqu'à la semaine 104.
Tableau 5: Différences radiographiques moyennes à la semaine 52 dans l'étude 5
|
|
MTX n=257 (IC à 95%)
|
Adalimumab/MTX n=268
IC à 95%
|
Valeur de p*
| |
Score global de Sharp
|
5,7 (4,2-7,3)
|
1,3 (0,5-2,1)
|
<0,001
| |
Score d'érosion
|
3,7 (2,7-4,7)
|
0,8 (0,4-1,2)
|
<0,001
| |
Score JSN
|
2,0 (1,2-2,8)
|
0,5 (0-0,1)
|
<0,001
|
*Comparaison entre adalimumab/méthotrexate et méthotrexate au moyen du test U de Mann-Whitney
Le pourcentage de patients sans progression de la maladie (augmentation par rapport aux valeurs initiales du score global de Sharp modifié ≤0,5) était significativement plus élevé sous l'association adalimumab/méthotrexate comparée au méthotrexate en monothérapie à la semaine 52 (63,8% vs. 37,4%, p <0,001) et à la semaine 104 (61,2% vs. 33,5%, p <0,001).
Dans le cadre de la phase de prolongation en ouvert de l'étude 3,77% des patients traités à l'origine par adalimumab ont été évalués par radiographie au bout de deux ans. L'inhibition de la progression des lésions structurelles a été maintenue. 54% des patients étudiés ne présentaient pas de progression des lésions structurelles, se traduisant par une modification du SST de 0 ou inférieure.
Qualité de vie et capacités fonctionnelles
La qualité de vie en rapport avec l'état de santé, qui constituait un critère d'évaluation défini à la semaine 52 dans l'étude 3, a été évaluée au moyen de l’index de handicap du Questionnaire d’Évaluation de l’état de Santé (Health Assessment Questionnaire, HAQ) dans les quatre essais adéquats et correctement contrôlés. Au cours des quatre études, des améliorations statistiquement significatives et plus fortes de l'index de handicap du HAQ ont été observées pour l'ensemble des doses/plans thérapeutiques d'adalimumab, par comparaison avec le placebo, entre les valeurs initiales et les valeurs à 6 mois. Au cours de l'étude 3, l'amélioration moyenne (IC) du HAQ entre avant le traitement et à la semaine 52 a été de -0,60 (-0,65, -0,55) pour les patients traités par adalimumab/méthotrexate et de -0,25 (-0,33, -0,17) chez les patients traités par placebo/méthotrexate (p <0,001). Chez 82% des patients traités par adalimumab/méthotrexate, et pour lesquels une amélioration de 0,5 ou plus au questionnaire HAQ a été obtenue à la semaine 52, cette amélioration a été maintenue jusqu'au mois 60 de la phase de prolongation en ouvert.
Dans l'étude 5, c'est-à-dire l'étude contrôlée dans le cas de polyarthrite rhumatoïde précoce par comparaison avec le méthotrexate, l'amélioration de l'index de handicap du HAQ et des composants physiques du SF36 à la semaine 52 était plus importante (p <0,001) sous l'association adalimumab/méthotrexate que sous méthotrexate en monothérapie et elle s'est maintenue jusqu'à la semaine 104.
Par ailleurs, la qualité de vie globale en rapport avec l'état de santé a été évaluée pour les quatre études adéquates et bien contrôlées à l'aide du Short Form Health Survey (SF36 = analyse rapide de l'état de santé). Au cours des quatre études, des améliorations statistiquement significatives et plus fortes du score sommaire pour les composantes physiques du questionnaire SF36 ont été observées pour l'ensemble des doses/fréquences d'injection d'adalimumab, par comparaison avec le placebo, entre les valeurs initiales et le mois 6, et ont été maintenues jusqu'à la semaine 52 au cours de l'étude 3. Les scores sommaires des composantes mentales du questionnaire SF36 au cours des études 2 et 4 ont ont été statistiquement significativement élevée au mois 6 pour l'adalimumab par comparaison avec le placebo. On a observé une amélioration statistiquement significative et plus forte des scores de douleur et de vitalité du questionnaire SF36 au cours des quatre études à la dose de 40 mg d'adalimumab toutes les deux semaines, par comparaison avec le placebo, entre les valeurs initiales et le mois 6. Ces résultats ont été renforcés par les scores atteints dans le cadre du Functional Assessment of Chronic Illness Therapy (FACIT = évaluation fonctionnelle du traitement des maladies chroniques), selon lesquels, pour les trois études analysées, on a obtenu une diminution significative de la fatigue au mois 6, qui s'est maintenue jusqu'à la semaine 52 au cours de l'étude 3. Le score SF36 a été calculé jusqu'à la semaine 156 (3 ans) et l'amélioration a été maintenue pendant cette période pour les patients restés dans l'étude.
Arthrite juvénile idiopathique polyarticulaire (AJIp)
La sécurité et l'efficacité de l'adalimumab ont été évaluées dans une étude multicentrique randomisée, en double aveugle, par groupes parallèles, auprès de 171 enfants (de 4 à 17 ans) atteints d'AJI polyarticulaire. L'analyse a été effectuée pour deux strates de patients: ceux qui recevaient du méthotrexate (MTX) et ceux qui n'en recevaient pas. Les patients ont reçu des doses stables d'AINS et/ou de prednisone (≤0,2 mg/kg/jour ou au maximum 10 mg/jour). Dans la phase initiale en ouvert («open-label lead-in», OL LI), d'une durée de 16 semaines, tous les patients ont reçu une dose d'adalimumab de 24 mg/m2 toutes les deux semaines (sans dépasser une dose maximale de 40 mg).
La répartition des patients est présentée dans le Tableau 6.
Tableau 6: Répartition des patients par âge et par dose d'adalimumab administrée dans la phase OL-LI
|
Groupe d'âge
|
Nombre de patients au début de l'étude, n (%)
|
Dose minimale, intermédiaire et maximale
| |
4 à 7 ans
|
31 (18,1)
|
10, 20 et 25 mg
| |
8 à 12 ans
|
71 (41,5)
|
20, 25 et 40 mg
| |
13 à 17 ans
|
69 (40,4)
|
25, 40 et 40 mg
|
Les patients ayant atteint une réponse ACR-30 pédiatrique à 16 semaines ont été randomisés pour la phase d'étude en double aveugle (double blind, DB), dans laquelle ils ont reçu toutes les 2 semaines une dose d'adalimumab (24 mg/m2 jusqu'à une dose unique maximale de 40 mg) ou une dose de placebo pendant 32 semaines maximum ou jusqu'à une nouvelle poussée de la maladie. Les critères définissant une nouvelle poussée de la maladie ont englobé une aggravation de ≥30% par rapport au début de l'étude pour ≥3 sur 6 critères ACR pédiatriques, une activité de la maladie dans ≥2 articulations et pas plus d'un critère sur 6 présentant une amélioration de >30%. Au bout de 32 semaines ou en présence d'une nouvelle poussée de la maladie, les patients étaient éligibles à une participation à la phase d'extension en ouvert («open-label extension», OLE).
Au bout de 16 semaines (à l'issue de la phase OL LI), 94,1% (80 patients sur 85) du groupe sous adalimumab et MTX et 74,4% (64 patients sur 86) du groupe sous adalimumab en monothérapie avaient atteint une réponse ACR 30. Les résultats de la période en double aveugle sont présentés dans le Tableau 7.
Tableau 7: Réponse ACR-30 pédiatrique dans l'étude sur l'AJI Résultats d'efficacité
|
En double aveugle, 32 semaines
|
Adalimumab/MTX (n=38)
|
Placebo/MTX (n=37)
|
Adalimumab (n=30)
|
Placebo (n=28)
| |
Nouvelle poussée de la maladie après 32 semainesa (n/N)
|
36,8% (14/38)
|
64,9% (24/37)b
|
43,3% (13/30)
|
71,4% (20/28)c
| |
Délai médian jusqu'à une nouvelle poussée de la maladie
|
>32 semaines
|
20 semaines
|
>32 semaines
|
14 semaines
|
a La réponse ACR-30/50/70 pédiatrique à 48 semaines était significativement supérieure à celle des patients ayant reçu le placebo
b p = 0,015
c p = 0,031
Parmi les patients ayant atteint une réponse à 16 semaines (n = 144), la réponse ACR-30/50/70/90 pédiatrique s'est maintenue jusqu'à six ans dans la phase OLE (phase de prolongation en ouvert) chez ceux qui ont reçu de l'adalimumab pendant toute la durée de l'étude. Au total, 19 patients (11 qui avaient de 4 à 12 ans au début de l'étude et 8 qui avaient de 13 à 17 ans au début de l'étude) ont été traités 6 ans ou plus.
Il est apparu que la réponse globale au traitement associant l'adalimumab et le MTX était supérieure et moins de patients ayant reçu ce traitement ont développé des anticorps en comparaison avec le groupe sous adalimumab seul. Compte tenu de ces résultats, il est recommandé d'utiliser l'adalimumab en association avec le MTX. L'utilisation de l'adalimumab en monothérapie n'est recommandée que chez les patients pour lesquels le MTX est inapproprié (cf. «Posologie/Mode d'emploi»).
Arthrite psoriasique
L'efficacité de l'adalimumab a été étudiée chez 413 patients. Dans l'étude principale, 313 patients adultes atteints d'arthrite psoriasique modérée à sévère, n'ayant pas répondu suffisamment à la thérapie non stéroïdienne anti-inflammatoire, ont été traités. 158 (50,5%) des patients étaient traités par méthotrexate au moment de la randomisation. L'adalimumab a été administré à la dose de 40 mg toutes les 2 semaines pendant 24 semaines. Une fois les études terminées, 383 patients ont été intégrés à une phase de prolongation en ouvert pendant laquelle l'adalimumab a été administré toutes les deux semaines. 382 des patients inclus ont été traités par adalimumab au moins au début de cette phase de prolongation. Concernant les patients évaluables à 48 et 144 semaines, voir plus bas.
Taux de réponse ACR et PASI
Le Tableau 8 montre que l'adalimumab est significativement plus efficace que le placebo concernant tous les paramètres de développement de la maladie (p <0,001). Chez les patients atteints d'arthrite psoriasique traités par adalimumab, on note une efficacité clinique dès le premier contrôle (2 semaines); cette efficacité est significative après 12 semaines et a été maintenue pendant les 24 semaines de traitement.
Les patients présentant au moins 3% de la surface corporelle atteinte de psoriasis ont été évalués d'après le Psoriatic Area and Severity Index (PASI, zone psoriasique et indice de gravité). Les lésions cutanées dues au psoriasis se sont améliorées chez ces patients par rapport au placebo, selon le PASI.
Le taux de réponse était comparable lors du traitement avec ou sans méthotrexate.
Les taux de réponse ACR se sont maintenus jusqu'à 136 semaines pendant la phase de prolongation en ouvert.
Tableau 8: Taux de réponse ACR et PASI dans une étude contrôlée contre placebo chez des patients atteints d'arthrite psoriasique (en pourcentage du nombre de patients)
|
Taux de réponse*
|
Placebo
|
Adalimumab
| |
|
N=162
|
N=151
| |
ACR 20
| |
Semaine 12
|
14%
|
58%
| |
Semaine 24
|
15%
|
57%
| |
ACR 50
| |
Semaine 12
|
4%
|
36%
| |
Semaine 24
|
6%
|
39%
| |
ACR 70
| |
Semaine 12
|
1%
|
20%
| |
Semaine 24
|
1%
|
23%
| |
|
N=69
|
N=69
| |
PASI 50
| |
Semaine 12
|
15%
|
72%
| |
Semaine 24
|
12%
|
75%
| |
PASI 75
| |
Semaine 12
|
4%
|
49%
| |
Semaine 24
|
1%
|
59%
|
*p <0,001 pour toutes les comparaisons d'adalimumab et de placebo
Les modifications radiographiques ont été évaluées au cours des études portant sur l'arthrite psoriasique. Des radiographies des mains, des poignets et des pieds ont été réalisées au début de l'étude et à la semaine 24 de la phase en double aveugle pendant laquelle les patients ont reçu soit l'adalimumab soit un placebo, ainsi qu'à la semaine 48, pendant laquelle tous les patients recevaient de l'adalimumab. Un score global de Sharp modifié (SSTm) incluant les articulations interphalangiennes distales (différent du score total de Sharp pour la polyarthrite rhumatoïde) a été utilisé.
Comparativement au placebo, l'adalimumab a réduit la vitesse de progression des lésions articulaires périphériques. Une modification du score global de Sharp modifié de 0,8 ± 2,5 (moyenne ± écart type) par rapport à la valeur initiale a été observée dans le groupe placebo (à la semaine 24), contre 0,0 ± 1,9 dans le groupe adalimumab (à la semaine 48, n = 133); p <0,001).
84% des patients qui ont été traités par adalimumab et qui n'ont présenté aucune progression radiographique entre la période avant traitement et la semaine 48 (n=102) n'ont pas non plus présenté de progression radiographique jusqu'à la semaine 144.
L'évaluation de l'index de handicap du HAQ et du questionnaire Short Form Health Survey (SF36) a montré, dans le groupe de patients traités par adalimumab, une amélioration statistiquement significative des capacités fonctionnelles physiques à la semaine 24, comparativement aux patients traités par placebo.
L'amélioration des capacités fonctionnelles physiques s'est maintenue au cours de la phase de prolongation en ouvert, jusqu'à la semaine 136.
Maladie de Crohn
La sécurité et l'efficacité d'une dose multiple d'adalimumab ont été étudiées chez plus de 1500 patients atteints d'une forme active modérée à sévère de la maladie de Crohn (indice d'activité de la maladie de Crohn [CDAI = Crohn's Disease Activity Index] ≥220 et ≤450) dans le cadre d'études randomisées contrôlées contre placebo, en double-aveugle. L'administration concomitante d'aminosalicylates, de corticostéroïdes et/ou d'immunomodulateurs en dosage constant était permise, et l'un de ces médicaments au moins a continué à être administré à 80% des patients.
L'apparition d'une rémission clinique (définie comme étant CDAI <150) a été évaluée dans le cadre de deux études (CLASSIC I et GAIN). 299 patients n'ayant pas reçu de traitement par antagonistes du TNF au préalable, répartis par randomisation dans quatre groupes de traitement, ont participé à l'étude CLASSIC I. Un placebo a été administré au groupe placebo aux semaines 0 et 2, le groupe 160/80 a reçu 160 mg d'adalimumab à la semaine 0 et 80 mg à la semaine 2, le groupe 80/40 a été traité par 80 mg à la semaine 0 et 40 mg à la semaine 2, et le groupe 40/20 a été traité par 40 mg à la semaine 0 et 20 mg à la semaine 2. L'étude GAIN regroupait 325 patients qui soit ne réagissaient plus à l'infliximab, soit ne le supportaient pas, et qui ont été randomisés avant de recevoir soit 160 mg d'adalimumab à la semaine 0 et 80 mg à la semaine 2, soit un placebo aux semaines 0 et 2.
Le maintien de la rémission clinique a été évalué dans le cadre de l'étude CHARM. Celle-ci portait sur 854 patients qui ont reçu en ouvert 80 mg d'adalimumab à la semaine 0 et 40 mg à la semaine 2. À la semaine 4, les patients ont été randomisés et on leur a administré soit 40 mg d'adalimumab toutes les deux semaines, soit 40 mg d'adalimumab toutes les semaines, soit un placebo. L'étude a duré 56 semaines au total. Les patients présentant une réaction clinique (diminution de CDAI ≥70) à la semaine 4 ont été stratifiés puis analysés (séparés de ceux qui ne présentaient aucune réaction clinique à la semaine 4). Une réduction des corticostéroïdes a été autorisée après la semaine 8.
Résultats cliniques
En comparaison avec le placebo, un pourcentage plus élevé et significatif au plan statistique de groupes traités par 160/80 mg d'adalimumab a obtenu une rémission clinique à la semaine 4, dans le cadre des études CLASSIC I et GAIN, indépendamment du fait que les patients n'aient jamais suivi au préalable de traitement par antagonistes TNF ou aient déjà subi un traitement par infliximab (voir tableau 9).
Tableau 9: Apparition d'une rémission et d'une réaction cliniques (en pourcentage de patients)
|
|
CLASSIC I: Patients n'ayant pas été traités par infliximab
|
GAIN: Patients ayant été traités par infliximab
| |
Placebo N=74
|
Adalimumab 160/80 mg N=76
|
Placebo
N=166
|
Adalimumab 160/80 mg N=159
| |
Semaine 4
| |
Rémission clinique
|
12%
|
36%*
|
7%
|
21%*
| |
Réaction clinique (CR-100)
|
24%
|
50%**
|
25%
|
38%**
| |
Réaction clinique (CR-70)
|
34%
|
58%**
|
34%
|
52%**
|
Toutes les valeurs p sont des comparaisons par paires de pourcentage entre l'adalimumab et le placebo
* p<0,001
** p<0,01
58% (499/854) des patients participant à l'étude CHARM ont montré une réaction clinique à la semaine 4 et ont été évalués dans le cadre de l'analyse primaire. 48% des patients qui présentaient une réaction clinique à la semaine 4 avaient reçu au préalable un autre traitement anti-TNF. Aux semaines 26 et 56, un pourcentage plus élevé et significatif au plan statistique des groupes recevant un traitement d'entretien par adalimumab et ayant affiché une réaction clinique à la semaine 4 a atteint une rémission clinique, par comparaison avec le groupe bénéficiant d'un traitement d'entretien par placebo. Par ailleurs, toujours par comparaison avec le groupe ayant reçu un traitement d'entretien par placebo, on a observé que dans les groupes ayant été traités par un traitement d'entretien par adalimumab et ayant bénéficié simultanément de corticostéroïdes au début du traitement, le pourcentage de patients avec une rémission clinique aux semaines 26 et 56 était statistiquement plus élevé (voir tableau 10) et étaient en mesure d'interrompre l'administration de corticostéroïdes pendant au moins 90 jours
Une analyse post hoc indique que les hospitalisations liées à la maladie et les opérations intra-abdominales avaient statistiquement diminué en phase double aveugle sous adalimumab, par rapport au placebo.
Tableau 10: Maintien d'une rémission et d'une réaction cliniques (en pourcentage de patients)
|
|
Placebo
|
40 mg d'adalimumab toutes les deux semaines
|
40 mg d'adalimumab toutes les semaines
| |
Semaine 26
|
N=170
|
N=172
|
N=157
| |
Rémission clinique
|
17%
|
40%*
|
47%*
| |
Réaction clinique (CR-100)
|
27%
|
52%*
|
52%*
| |
Réaction clinique (CR-70)
|
28%
|
54%*
|
56%*
| |
Patients présentant une rémission sans stéroïdes
pour ≥90 joursa
|
3% (2/66)
|
19% (11/58)**
|
15% (11/74)**
| |
Semaine 56
|
N=170
|
N=172
|
N=157
| |
Rémission clinique
|
12%
|
36%*
|
41%*
| |
Réaction clinique (CR-100)
|
17%
|
41%*
|
48%*
| |
Réaction clinique (CR-70)
|
18%
|
43%*
|
49%*
| |
Patients présentant une rémission sans stéroïdes pour ≥90 jours a
|
5% (3/66)
|
29% (17/58)*
|
20% (15/74)**
|
⃰ p<0,001 pour l'adalimumab vs. placebo (comparaison par paires des pourcentages)
** p<0,002 pour l'adalimumab vs. placebo (comparaison par paires des pourcentages)
a Parmi ceux ayant reçu initialement des corticostéroïdes
Les résultats de rémission clinique présentés dans le tableau 10 sont restés relativement constants, en dépit d'une exposition préalable aux antagonistes du TNF.
Parmi les patients qui ont affiché une réaction à la semaine 4 et atteint une rémission au cours de l'étude, les patients issus des groupes de traitement d'entretien par adalimumab ont pu maintenir cette rémission significativement plus longtemps que les patients issus du groupe de traitement d'entretien par placebo (voir figure 2).
Figure 2: Jours de rémission clinique chez les patients qui ont atteint une rémission clinique durant l'étude CHARM (Intent-to-Treat-Population)
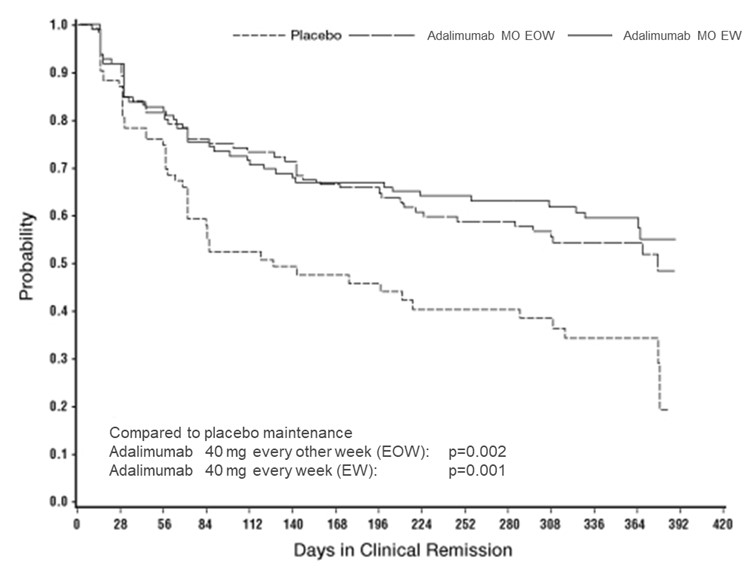
Parmi les patients qui n'affichaient aucune réaction à la semaine 4, on notait une réaction chez 43% des patients issus des groupes de traitement d'entretien par adalimumab jusqu'à la semaine 12, contre un taux de 30% chez les patients issus du groupe de traitement d'entretien par placebo. Ces résultats permettent de conclure que la poursuite d'un traitement d'entretien jusqu'à la semaine 12 peut présenter un avantage pour certains patients qui n'avaient affiché aucune réaction à la semaine 4. La poursuite de la thérapie au-delà des 12 semaines n'a pas donné lieu à beaucoup plus de réponses (voir «Posologie/Mode d'emploi»).
Dans l'étude CLASSIC I, 117/276 patients et dans les études GAIN et CHARM, 272/777 patients ont été traités par adalimumab au moins pendant 3 ans lors d'une phase de prolongation en ouvert. Trois ans plus tard, respectivement 88 et 189 patients étaient toujours en rémission clinique. Le taux de réponse clinique (RC-100) a été conservé chez respectivement 102 et 233 patients.
Dans l'étude M05-769 (EXTEND) endoscopique, randomisée et contrôlée contre placebo, 135 patients ont été examinés en prenant comme critère d'évaluation principal la guérison de la muqueuse (définie comme la disparition des ulcérations de la muqueuse). Après une phase d'induction de l'adalimumab de 4 semaines, les patients ont été randomisés. À la semaine 12, 27,4% des patients traités par adalimumab présentaient une guérison de la muqueuse contre 13,1% de ceux sous placebo (p=0,056). À la semaine 52, 24,2% des patients sous adalimumab présentaient une guérison de la muqueuse contre 0% de ceux sous placebo (p<0,001).
Résultats déclarés par les patients/Patient-Reported Outcomes
Le score total obtenu à la semaine 4 au questionnaire portant sur les maladies inflammatoires de l'intestin (inflammatory bowel disease questionnaire = IBDQ), spécialement conçu pour la maladie, a indiqué une amélioration statistiquement significative, en comparaison avec le placebo, chez les patients qui avaient été randomisés pour bénéficier d'un traitement par adalimumab 160/80 mg dans le cadre des études CLASSIC I et GAIN. En comparaison avec le groupe placebo, les groupes traités par adalimumab dans le cadre de l'étude CHARM ont affiché une amélioration statistiquement significative du score total IBDQ par rapport aux valeurs initiales observées aux semaines 26 et 56.
Qualité de vie et capacités fonctionnelles physiques
La qualité de vie en rapport avec l'état de santé et la capacité fonctionnelle physique ont été évaluées dans l'étude sur l'arthrite psoriasique à l'aide du Questionnaire d’évaluation de la santé (Health Assessment Questionnaire, HAQ). Les patients traités par adalimumab ont montré, par rapport aux patients traités par placebo, des améliorations statistiquement significatives plus fortes de l'index de handicap du HAQ, si l'on compare les valeurs initiales à la semaine 24.
Les résultats du Short Form Health Survey (SF36) étayent ces résultats avec un Score sommaire des composants physiques (Physical Component Summary (PCS) Score) ainsi que des Scores de domaine de la douleur et de la vitalité (Pain and Vitality Domain Scores) statistiquement significatifs.
Colite ulcéreuse
La sécurité et l'efficacité ont été examinées chez des patients adultes atteints de colite ulcéreuse active modérée à sévère (score Mayo de 6 à 12, avec sous-score endoscopique de 2 à 3) dans deux études randomisées, en double aveugle, avec contrôle contre placebo. Les patients pouvaient prendre en même temps une médication permanente sous forme d'aminosalicylates, de glucocorticoïdes et/ou d'immunomodulateurs.
L'induction d'une rémission clinique (définie comme un score Mayo ≤2 sans sous-score >1) a été examinée chez 390 patients naïfs de tout traitement aux anti-TNF. Ces patients ont été traités les semaines 0 et 2 par placebo ou par adalimumab 160 mg et 80 mg ou bien par adalimumab 80 mg et 40 mg, puis les semaines 4 et 6 par placebo ou par adalimumab 40 mg. Les patients sont ensuite tous passés à un traitement d'entretien par adalimumab 40 mg toutes les 2 semaines.
La semaine 8, on a pu constater une rémission clinique chez 18% des patients traités avec une dose d'induction de 160 mg/80 mg d'adalimumab, contre 9% des patients ayant reçu le placebo (p = 0,031). Aucune supériorité statistiquement significative de l'adalimumab n'a été observée avec la dose d'induction de 80 mg/40 mg (10%, p = 0,833).
L'efficacité au cours de la phase d'induction et de la phase d'entretien (52 semaines au total) a été évaluée chez 248 patients traités par 160 mg/80 mg/40 mg toutes les 2 semaines versus 246 patients sous placebo. Une rémission à 8 et 52 semaines a été constatée chez 16,5% (p = 0,019) et 17,3% (p = 0,004) des patients sous adalimumab versus 9,3% et 8,5% des patients sous placebo. Les taux de réponse persistante, de rémission persistante et de guérison durable de la muqueuse sont présentés en aperçu dans le tableau 11:
Tableau 11: Taux de réponse persistante, de rémission et de guérison de la muqueuse dans l'étude UC II Pourcentage de patients (intervalle de confiance à 95%)
|
|
Placebo et
95% intervalle de confiance
|
Adalimumab 40 mg
toutes les deux semaines et intervalle de confiance à 95%
| |
Semaines 8 et 52
| |
Réponse persistante
|
12% (IC: 8,1-16,3)
|
24%** (IC: 18,5 - 29,1)
| |
Rémission persistante
|
4% (IC 1,6 - 6,5)
|
8%* (IC 5,0 - 11,9)
| |
Guérison durable de la muqueuse
|
11% (IC: 6,7 - 14,4)
|
19%* (IC: 13,7 - 23,4)
|
a Intervalle de confiance pour la proportion, sur la base d'une approximation de la distribution binomiale par loi normale
La rémission clinique signifie un score Mayo ≤2 sans sous-score >1;
* p <0,05 pour l'adalimumab vs. placebo
** p <0,001 pour l'adalimumab vs. placebo
La guérison de la muqueuse correspond à un sous-score endoscopique de 0 ou de 1
Une réponse signifie un score Mayo réduit de ≥3 points et inférieur de ≥30% au score initial, ainsi qu'un sous-score d'hémorragies rectales de 0 ou de 1 ou réduit de ≥1 point par rapport à la valeur initiale.
Sur les 125 patients ayant atteint une réponse à 8 semaines, 59 (47%) étaient encore répondeurs à 52 semaines; 36 (29%) étaient en rémission, 51 (41%) présentaient une guérison de la muqueuse et 18 (20% des 90 patients répondeurs à 8 semaines et initialement sous corticostéroïdes) étaient en rémission sans utilisation de corticostéroïdes depuis ≥90 jours.
Une réduction statistiquement significative des taux d'hospitalisations toutes causes confondues et des taux d'hospitalisations imputables à la colite ulcéreuse a été observée dans l'analyse des deux études UC (Colite ulcérose).
Le traitement anti-TNF par infliximab avait échoué auparavant chez presque 40% des patients de l'étude UC II. L'efficacité de l'adalimumab était plus faible chez ces patients que chez les patients naïfs de traitements par anti-TNF. Dans ce sous-groupe, une rémission à 52 semaines a été atteinte dans 10% des cas sous adalimumab versus 3% des cas sous placebo (p = 0,039).
Les patients des études UC-I et UC-II ont pu continuer à être traités dans le cadre de l'étude à long terme en ouvert (UC-III). Trois ans après le traitement par adalimumab, 75% (301/402) des patients étaient encore en rémission clinique d'après le score Mayo partiel.
Une amélioration de la qualité de vie spécifique en rapport avec la maladie, évaluée à l'aide du score IBDQ total (Inflammatory Bowel Disease Questionnaire), était atteinte à 52 semaines versus placebo (p = 0,007).
Spondylarthrite ankylosante (maladie de Bechterew)
L'efficacité de 40 mg d'adalimumab toutes les deux semaines en injection par voie sous-cutanée a été étudiée dans deux études randomisées en double aveugle contrôlées contre placebo pendant 24 semaines chez 393 patients atteints de spondylarthrite ankylosante active (valeurs d'activité de la maladie [Bath Ankylosing Spondylitits Disease Activity Index (BASDAI)]) >4 (valeurs initiales moyennes de 6,3 aussi bien dans le groupe adalimumab que dans le groupe placebo) n'ayant pas répondu suffisamment aux traitements courants. 79 patients (20,1%) ont reçu simultanément un agent antirhumatismal de fond et 37 patients (9,4%) des glucocorticoïdes. La période en aveugle a été suivie d'une phase de prolongation en ouvert allant jusqu'à 28 semaines supplémentaires, pendant laquelle les patients ont reçu 40 mg d'adalimumab par injection sous-cutanée toutes les deux semaines.
Dans l'étude de plus grande ampleur portant sur 315 patients, les résultats ont indiqué des améliorations statistiquement significatives des signes et des symptômes de la spondylarthrite ankylosante chez les patients ayant reçu de l'adalimumab, par rapport aux patients sous placebo. Une réponse significative a été constatée pour la première fois après 2 semaines de traitement et s'est maintenue jusqu'à la semaine 24.
Les taux de réponse selon l'évaluation dans spondylarthrite ankylosante (Assessment in Ankylosing Spondylitis, ASAS) 20/50/70 ont été atteints à la semaine 12 chez 58%, 38% et 23% des patients sous adalimumab, comparé aux 21%, 10% et 5% des patients sous placebo (p <0,001 adalimumab vs. placebo). Une réponse généralement comparable a été constatée à la semaine 24.
Comme constaté avec le BASDAI, le traitement par adalimumab a entraîné une amélioration des signes et symptômes. Chez 45% des patients traités par adalimumab, une réduction d'au moins 50% des valeurs BASDAI initiales a été obtenue à la semaine 12, comparé aux 16% des patients traités par placebo (p <0,01). Des résultats comparables ont été constatés à la semaine 24.
De plus, la diminution moyenne du taux initial de protéine C-réactive (CRP) à la semaine 12 pour le traitement par adalimumab (-1,3 mg/dl) était plus importante que celle obtenue sous placebo (-0,1 mg/dl), (p<0,001).
Des résultats comparables (qui ne sont pas tous statistiquement significatifs) ont été constatés dans une étude plus réduite, randomisée, en double aveugle, contrôlée contre placebo, menée chez 82 patients adultes atteints de spondylarthrite ankylosante active.
Dans les études portant sur la spondylarthrite ankylosante, les résultats rapportés par les patients ont été évalués à l'aide du Formulaire court de questionnaire générique sur l’état de santé (Generic Health Status Questionnaire Short Form-36, SF36) et du Questionnaire sur la qualité de vie de la spondylarthrite ankylosante spécifique à la maladie (Disease Specific Ankylosing Spondylitis Quality of Life Questionnaire, ASQoL). Des améliorations significativement plus importantes de l'ASQoL et des paramètres physiques («physical components») du SF36 ont été observées à la semaine 12 chez les patients traités par adalimumab, par rapport aux patients du groupe placebo, lesquelles se sont maintenues jusqu'à la semaine 24.
Psoriasis
L'efficacité et la sécurité de l'adalimumab ont été examinées au cours d'études randomisées, en double aveugle et contrôlées, menées sur plus de 1600 patients atteints de psoriasis en plaques chronique modéré à sévère, âgés ≥18 ans et candidats à un traitement systémique ou à une photothérapie.
Au cours de l'étude 1, 1212 patients, atteints de psoriasis en plaques chronique sur ≥10% de leur surface corporelle (Body Surface Area, BSA) et présentant un score PASI (Psoriatic Area and Severity Index, Zone psoriasique et indice de gravité) ≥12, ont été évalués pendant trois périodes de traitement. Pendant la période A, les patients ont reçu par voie sous-cutanée le placebo ou une dose initiale de 80 mg d'adalimumab à la semaine 0, suivie de 40 mg d'adalimumab toutes les deux semaines à partir de la semaine 1. Les patients ayant obtenu au minimum une réponse PASI 75 (amélioration d'au moins 75% du score PASI par rapport à la valeur initiale) au bout de 16 semaines ont poursuivi leur traitement en ouvert pendant la phase de prolongation B. Ils ont reçu 40 mg d'adalimumab toutes les deux semaines. Après 17 semaines de traitement en ouvert, les patients ayant conservé au minimum une réponse PASI 75 à la semaine 33 et ayant reçu un traitement actif pendant la période A, sont passés à la période de traitement C. Ils ont reçu 40 mg d'adalimumab ou un placebo toutes les 2 semaines durant 19 semaines supplémentaires. Le score PASI initial moyen était de 18,9 tous groupes de traitement confondus. Le score PGA (Physician's Global Assessment, Évaluation globale du médecin) initial tous groupes confondus allait de «modéré» (52,6%) à «sévère» (41,3%), et même «très sévère» (6,1%).
L'étude 2 a comparé l'efficacité et la sécurité de l'adalimumab à celle du méthotrexate et du placebo sur 271 patients atteints de psoriasis en plaques chronique, avec un BSA de 10% et un score PASI ≥10. Pendant 16 semaines, les patients ont reçu un placebo, du méthotrexate (7,5–20 mg) ou une dose initiale de 80 mg d'adalimumab par voie sous-cutanée à la semaine 0, suivie de 40 mg d'adalimumab toutes les deux semaines à partir de la semaine 1. Le score PASI initial moyen était de 19,7 tous groupes de traitement confondus. Le score PGA initial était, tous groupes confondus, «léger» (0,4%), «modéré» (47,8%), «sévère» (45,6%) et «très sévère» (6,3%).
1469 patients provenant des études de phase II et III ont été inclus dans une étude de prolongation ouverte en 3 phases, comportant une phase de poursuite du traitement (104-252 semaines), une phase d'interruption du traitement (jusqu'à récidive ou au maximum de 52 semaines), puis une phase de reprise du traitement (16 semaines).
Dans l'étude 3, 148 patients atteints de psoriasis en plaques chronique avec un BSA ≥5% ont été évalués pendant au moins 1 an. Les patients ont reçu un placebo ou une dose initiale de 80 mg d'adalimumab à la semaine 0, suivie de 40 mg d'adalimumab toutes les deux semaines à partir de la semaine 1, ou bien une dose initiale de 80 mg d'adalimumab à la semaine 0, suivie de 40 mg d'adalimumab chaque semaine à partir de la semaine 1.
Résultats cliniques
Le critère d'évaluation primaire des études 1, 2 et 3 était le pourcentage de patients ayant atteint une réduction de leur score PASI d'au moins 75% par rapport à la valeur initiale (PASI 75) à la semaine 16 (études 1 et 2) ou à la semaine 12 (étude 3). Les études 1–3 menées sur le psoriasis ont également porté, entre autres, sur le score PGA et d'autres valeurs PASI.
Étude 1: en plus du critère d'évaluation primaire ci-dessus, l'étude 1 avait comme second primaire critère la perte d'une réponse appropriée après la semaine 33, et pendant ou avant la semaine 52. La perte d'une réponse appropriée était définie comme une réponse < PASI 50 par rapport à la valeur initiale, avec un minimum d’augmentation de 6 points du score PASI par rapport à la semaine 33.
Des données contrôlées portant sur un traitement par adalimumab versus placebo sont disponibles pour une durée de traitement de 52 semaines. Dans une étude comparative contrôlée contre placebo, menée auprès des patients sous adalimumab ayant obtenu une disparition prolongée des troubles à l'issue de la semaine 33, 95,1% des patients poursuivant le traitement par adalimumab n'ont pas connu de récidive jusqu'à la semaine 52, contre 71,6% des patients sous placebo (c'est-à-dire après l'arrêt de l'administration d'adalimumab à la semaine 33).
Parmi les patients présentant une diminution de réponse appropriée après la nouvelle randomisation dans le groupe placebo et qui ont été ensuite recrutés dans la phase de prolongation en ouvert, 38% (25/66) et 55% (36/66) ont retrouvé une réponse PASI 75 après respectivement 12 et 24 semaines de traitement actif.
Cette réponse tardive après récidive est probablement liée à une évolution sévère du psoriasis dans ce sous-groupe de patients.
Dans les études 1 et 2 sur le psoriasis, un plus grand nombre de patients traités par adalimumab a par rapport au score initial, à la semaine 16, par rapport aux patients sous placebo. D'autres paramètres cliniques significatifs incluant le score PASI 100 (p.ex. disparition complète des signes cutanés du psoriasis) et le score PGA «aucun ou minime» ont connu également une amélioration par rapport au placebo.
Étude 2: Dans l'étude 2 sur le psoriasis, les patients recevant l'adalimumab ont présenté de meilleurs résultats pour les scores PASI 75, PASI 100 et PGA «clair ou minimal» que les patients sous méthotrexate.
Tableau 12: Étude 1 sur le psoriasis - Efficacité à la semaine 16 (% des patients)
|
|
Placebo N=398
|
Adalimumab 40 mg toutes les 2 semaines N=814
| |
≥PASI 75
|
6,5
|
70,9 a
| |
PASI 100
|
0,8
|
20,0 a
| |
PGA:
Clair/minimal
|
4,3
|
62,2 a
|
a p<0,001, adalimumab vs. Placebo
Tableau 13: Étude 2 sur le psoriasis - Efficacité à la semaine 16 (% des patients)
|
|
Placebo N=53
|
MTX N=110
|
Adalimumab 40 mg
1 sem./2 N=108
| |
≥PASI 75
|
18,9
|
35,5
|
79,6 a, b
| |
PASI 100
|
1,9
|
7,3
|
16,7 a, b
| |
PGA:
Clair/minimal
|
11,3
|
30,0
|
73,1 a, b
|
a p<0,001, adalimumab vs. Placebo
b p<0,001, adalimumab vs. méthotrexate
Étude de prolongation en ouvert: au total, 233 patients qui avaient obtenu une réponse PASI 75 à la semaine 16 et à la semaine 33 et qui avaient reçu, dans l'étude 1 sur le psoriasis, un traitement prolongé par adalimumab pendant 52 semaines, ont poursuivi le traitement par adalimumab dans l'étude de prolongation en ouvert. La réponse PASI 75 ou la réponse PGA définie comme un score PGA «clair» ou «minimal» ont été respectivement de 74,7% et 59,0% chez ces patients après 108 semaines supplémentaires de traitement en ouvert (au total 160 semaines). Dans une analyse NRI (Non Responder Imputation), dans laquelle tous les patients qui avaient interrompu leur participation à l'étude en raison d'effets indésirables ou d'absence d'efficacité, ou chez lesquels la dose avait été augmentée, ont été considérés comme non répondeurs, la réponse PASI 75 et la réponse PGA, définie comme un score PGA «clair» ou «minimal», ont été respectivement de 69,6% et 55,7% chez ces patients après 108 semaines supplémentaires de traitement en ouvert (au total 160 semaines).
Dans l'étude de prolongation, 347 patients ayant présenté une réponse durable ont participé à une analyse de l'interruption du traitement et de la reprise du traitement. Pendant la phase d'interruption du traitement, les symptômes psoriasiques sont réapparus chez 54,2% (188/347) au fil du temps avec un temps moyen de récurrence d'environ 5 mois (diminution du score PGA à «modéré» voire pire). Aucun de ces patients n'a connu de phénomène de rebond pendant la phase d'interruption. Au total, 76,5% (218/285) des patients ayant participé à la phase ultérieure de reprise du traitement ont présenté une réponse PGA, définie comme un score PGA «clair» ou «minimal» 16 semaines après la reprise du traitement, qu'ils aient eu une récidive pendant l'arrêt (69,1% [123/178]) ou non (88,8% [95/107]). Le profil de sécurité observé pendant la phase de reprise du traitement a été similaire à celui observé avant l'interruption du traitement.
Étude 3: Les résultats de l'étude 3 sur le psoriasis confirment l'efficacité démontrée dans les études 1 et 2.
Les patients de l'étude 1 ayant présenté une réponse PASI 75 et ayant été à nouveau randomisés à la semaine 33 dans le groupe adalimumab ont présenté une diminution de réponse appropriée inférieure à celle présentée par les patients à nouveau randomisés dans le groupe placebo (4,9% contre 28,4%, p <0.001) à la semaine 52 ou avant.
Dans une étude d’extension ouverte, une réponse PASI-75 a été observée chez 28,3% (63/223) et 39,5% (88/223) des patients à la semaine 12 et 24, respectivement, chez les patients qui, après une réponse initiale au moins partielle, ont présenté un échec secondaire du traitement, c’est-à-dire qui ne présentaient plus de réponse PASI-50 par rapport à la situation initiale, et chez lesquels la dose a été augmentée de 40 mg une semaine sur deux à 40 mg par semaine.
Qualité de vie
Les résultats déclarés par les patients (Patient reported Outcomes, PRO) ont été évalués à l'aide de divers paramètres. La qualité de vie a été déterminée au cours des études 1 et 2 à l'aide de l'indice spécifique de la maladie DLQI (Dermatology Life Quality Index, Indice de qualité de vie en dermatologie). Dans l'étude 1, les patients sous adalimumab ont présenté des améliorations du score total DLQI, du degré de la maladie, des douleurs et du prurit aux semaines 4 et 16, en comparaison avec les patients sous placebo. Les résultats DLQI ont été maintenus jusqu'à la semaine 52.
Dans l'étude 2, les patients sous adalimumab ont présenté à la semaine 16 des améliorations en ce qui concerne le score total DLQI, le degré de la maladie et le prurit en comparaison avec les patients sous placebo ou sous méthotrexate, ainsi que des améliorations cliniquement significatives des douleurs comparativement aux patients sous placebo.
La qualité de vie générale en rapport avec l'état de santé a été définie à l'aide du questionnaire Short Form Health Survey (SF36) dans l'étude 1. Les patients recevant de l'adalimumab ont présenté une amélioration significativement plus importante des scores de la composante physique (Physical Component Summary - PCS) et de la composante mentale (Mental Component Summary - MCS) du SF36.
Psoriasis en plaques chez l’enfant et l’adolescent
L’efficacité de l’adalimumab a été évaluée dans une étude randomisée, en double aveugle et contrôlée portant sur 114 patients pédiatriques âgés de 4 ans et plus atteints de psoriasis en plaques chronique sévère dont le traitement topique et l’héliothérapie ou la photothérapie étaient insuffisants (le psoriasis en plaques chronique sévère est défini par un score PGA ≥4 ou BSA >20% ou BSA >10% avec des lésions très épaisses ou PASI ≥ 20 ou ≥10 avec une atteinte cliniquement significative du visage, de la région génitale ou des mains/pieds).
Les patients ont reçu de l’adalimumab à une dose de 0,8 mg/kg une semaine sur deux (jusqu’à 40 mg), de 0,4 mg/kg une semaine sur deux (jusqu’à 20 mg) ou du méthotrexate 0,1-0,4 mg/kg per os une fois par semaine (jusqu’à 25 mg). Aucune comparaison n’a été effectuée avec le MTX à plus forte dose administré par voie sous-cutanée.
La répartition par âge des patients est présentée dans le tableau 14.
Tableau 14: Répartition des patients par âge (patients randomisés pour recevoir de l’adalimumab 0,8 mg/kg, une semaine sur deux)
|
Tranche d’âge (ans)
|
Nombre de patients au début de l’étude n (%)
| |
>6-9
|
7 (18,4)
| |
>9-12
|
8 (21,1)
| |
>12-15
|
13 (34,2)
| |
>15
|
10 (26,3)
|
17 (45%) des patients avaient été préalablement traités par voie générale (étanercept et/ou agents non biologiques, y compris acitrétine, ciclosporine, méthotrexate et autres). Les patients qui n’ont pas répondu à des traitements antérieurs par méthotrexate ont été exclus.
Les critères d’évaluation primaires correspondaient à un score PASI 75 et à un PGA «Blanchi» ou «Minime». À la semaine 16, davantage de patients randomisés dans le groupe adalimumab à 0,8 mg/kg présentaient des preuves d’efficacité supérieures à celles des patients randomisés dans le groupe MTX.
Tableau 15: Résultats d’efficacité dans le psoriasis en plaques pédiatrique à la semaine 16
|
|
MTXa
N=37
|
Adalimumab 0,8 mg/kg, une semaine sur deux
N=38
| |
PASI 75b
|
12 (32,4%)
|
22 (57,9%)
| |
PGA: blanchi/minimec
|
15 (40,5%)
|
23 (60,5%)
| |
a
MTX = méthotrexate
b P=0,027, adalimumab 0,8 mg/kg versus MTX
c P=0,083, adalimumab 0,8 mg/kg versus MTX
|
Il n’existe pas de données comparatives avec le méthotrexate au-delà de 16 semaines.
Chez les patients ayant atteint le score PASI-75 et un PGA défini comme «blanchi» ou «minime», le traitement a été arrêté pendant jusqu’à 36 semaines. Ces patients ont été suivis afin de déterminer s’ils avaient rechuté (perte de la réponse au niveau du score PGA). Le traitement des patients a ensuite repris à une dose de 0,8 mg d’adalimumab/kg une semaine sur deux pendant 16 semaines supplémentaires. Les taux de réponse observés au cours du nouveau traitement ont été les suivants: Réponse PASI-75 de 78,9% (15 patients sur 19) et PGA (défini comme «blanchi» ou «minime») de 52,6% (10 patients sur 19).
Dans la phase d’extension ouverte de l’étude, une réponse PASI-75 et un PGA, défini comme «blanchi» ou «minime», ont été maintenus jusqu’à 52 semaines supplémentaires; il n’y a pas eu de nouveaux éléments concernant la sécurité.
Hidradénite suppurée
L'efficacité et la sécurité de l'adalimumab ont été évaluées dans des études randomisées effectuées en double aveugle, avec contrôle contre placebo, et dans une étude d'extension en ouvert menée auprès de 727 patients adultes atteints d'hidradénite suppurée modérée à sévère. Les patients présentaient une contre-indication, une réponse insuffisante ou une intolérance à une antibiothérapie systémique et leur maladie était de stade II ou III selon la classification de Hurley, avec au moins 3 abcès ou nodules enflammés.
Deux études randomisées de phase III (HS-I et HS-II) effectuées en double aveugle, contrôlées contre placebo, totalisant 633 patients adultes, comprenaient chacune une phase initiale de 12 semaines de traitement en double aveugle (période A), suivie d'une période de traitement de 24 semaines en double aveugle (période B). Dans la période A, les patients ont reçu de l'adalimumab (160 mg la semaine 0, puis 80 mg la semaine 2 et 40 mg par semaine au cours des semaines 4 à 11) ou un placebo. Au bout de 12 semaines, les patients ayant reçu de l'adalimumab pendant la période A ont été à nouveau randomisés pour la période B, pour y recevoir 40 mg d'adalimumab par semaine, ou 40 mg d'adalimumab toutes les 2 semaines, ou un placebo, jusqu'à la semaine 35. Les patients ayant reçu un placebo pendant la période A ont été randomisés pour la période B pour y recevoir 40 mg d'adalimumab par semaine (HS-I) ou un placebo (HS-II).
Un traitement concomitant par un antibiotique oral était autorisé dans l'étude HS-II.
Les patients des deux études HS ont pu participer à une étude d'extension en ouvert avec administration hebdomadaire de 40 mg d'adalimumab. Chez toutes les populations recevant de l’adalimumab, l’exposition moyenne a été de 762 jours. Dans les 3 études, les patients effectuaient quotidiennement des nettoyages avec une solution topique antiseptique.
Efficacité clinique
La réduction des lésions inflammatoires et la prévention de l'aggravation des abcès et des fistules drainantes ont été évaluées à l'aide du score HiSCR (Hidradenitis Suppurativa Clinical Response; réduction d'au moins 50% du nombre de tous les abcès et nodules inflammatoires, sans augmentation du nombre d'abcès ou de fistules drainantes par rapport aux valeurs initiales).
À 12 semaines, on a pu constater dans les deux études (HS-I et HS-II) qu'un pourcentage significativement plus élevé de patients traités par adalimumab avaient atteint une réponse HiSCR, par rapport aux patients sous placebo. Dans l'étude HS-II, un pourcentage significativement plus élevé de patients a présenté une réduction significative des douleurs cutanées liées à l'HS (voir le Tableau 16). De plus, le risque de nouvelle poussée de la maladie au cours du traitement initial de 12 semaines était significativement réduit chez les patients traités par adalimumab.
Tableau 16: Études HS-I et HS-II, efficacité à 12 semaines
|
|
Étude HS I
|
Étude HS II
| |
Placebo
|
Adalimumab 40 mg par semaine
|
Placebo
|
Adalimumab 40 mg par semaine
| |
Efficacité clinique du traitement de l'hidradénite suppurée
|
N=154
40 (26,0%)
|
N=153
64 (41,8%)*
|
N=163
45 (27,6%)
|
N=163
96 (58,9%)***
| |
Efficacité
| |
(HiSCR)a
|
⃰ P <0,05, *** P <0,001, Adalimumab vs Placebo
a Sur l'ensemble des patients randomisés.
Chez les patients traités par adalimumab une fois par semaine, le taux de réponse HiSCR total s'est maintenu jusqu'à la semaine 96.
Uvéite
La sécurité et l’efficacité d’adalimumab ont été évaluées dans le cadre de deux études randomisées, en double aveugle, avec contrôle versus placebo (études UV 1 [M10-877] et UV 2 [M10-880]) sur une durée maximale de 80 semaines chez des patients adultes atteints d’uvéite non infectieuse de localisation intermédiaire/postérieure/panuvéite (ou «uvéite non infectieuse de la partie postérieure de l’œil»). Les patients atteints uniquement d’uvéite antérieure étaient exclus. Les patients ont reçu soit un placebo soit adalimumab (dose initiale de 80 mg, puis 40 mg toutes les deux semaines à partir de la semaine suivante).
Une co-médication par un immunosuppresseur conventionnel (ciclosporine A, méthotrexate, mycophénolate mofétil, azathioprine, tacrolimus) à dose stable était autorisée. Dans les deux études, le critère d’efficacité primaire était «le temps jusqu’à un échec thérapeutique». L’échec thérapeutique était défini en tant que critère composite incluant les éléments suivants: 1) lésions vasculaires chorio-rétiniennes inflammatoires et/ou rétiniennes inflammatoires, 2) grade des cellules de la chambre antérieure, 3) degré d’opacification du corps vitré (vitreous haze) et 4) la meilleure acuité visuelle après correction (BCVA).
L’étude UV 1 a inclus 217 patients souffrant d’uvéite active malgré une corticothérapie (prednisone orale à raison de 10 à 60 mg par jour). Tous les patients recevaient lors de leur inclusion à l’étude une dose standardisée de prednisone de 60 mg par jour, avec schéma obligatoire de réduction de la dose jusqu’à l’arrêt complet de la corticothérapie à la semaine 15.
L’étude UV 2 a inclus 226 patients présentant une uvéite inactive qui exigeait une corticothérapie (prednisone orale à raison de 10 à 35 mg par jour) au début de l’étude. Le traitement par le médicament à l’étude a été commencé parallèlement à la poursuite de la corticothérapie en cours, après quoi la dose du corticostéroïde a été réduite progressivement jusqu'à l’arrêt complet de la corticothérapie à la semaine 19.
Réponse clinique
Les résultats des deux études montrent de façon statistiquement significative que le temps écoulé jusqu’au premier échec thérapeutique était plus long chez les patients traités par adalimumab que chez les patients sous placebo (voir le tableau 17). De même, les deux études ont mis en évidence une efficacité rapide et persistante d’ adalimumab versus placebo pour retarder le premier échec thérapeutique (voir la figure 3).
Tableau 17: Temps écoulé jusqu’au premier échec thérapeutique dans les études UV 1 et 2
|
Traitement évalué
|
N
|
Échec
N (%)
|
Délai médian (en mois) jusqu'à l’échec
|
HRa
|
IC à 95%
pour HRa
|
Valeur pb
| |
Temps écoulé jusqu’à un échec thérapeutique pendant ou après la semaine 6 dans l’étude UV 1
| |
Analyse primaire (ITT)
| |
Placebo
|
107
|
84 (78,5)
|
3,0
|
--
|
--
|
--
| |
Adalimumab
|
110
|
60 (54,5)
|
5,6
|
0,50
|
0,36; 0,70
|
<0,001
| |
Temps écoulé jusqu’à un échec thérapeutique pendant ou après la semaine 2 dans l’étude UV 2
| |
Analyse primaire (ITT)
| |
Placebo
|
111
|
61 (55,0)
|
8,3
|
--
|
--
|
--
| |
Adalimumab
|
115
|
45 (39,1)
|
n.e.c
|
0,57
|
0,39; 0,84
|
0,004
|
Remarque: Un échec thérapeutique pendant ou après la semaine 6 dans l’étude UV 1 ou un échec thérapeutique pendant ou après la semaine 2 dans l’étude UV 2 a été compté comme événement. Les arrêts prématurés dus à d’autres raisons qu’un échec thérapeutique ont été censurés lors de leur survenue.
a HR pour l’adalimumab vs placebo à partir de la régression en modèle à risques proportionnels, avec le traitement en tant que facteur.
b Valeur p bilatérale à partir du test du log-rank.
c n.e. = non estimable. Moins de la moitié des patients entrant en ligne de compte ont eu un événement au cours de la durée d’étude de 80 semaines.
Figure 3: Courbes de Kaplan-Meier pour le temps écoulé jusqu’au premier échec thérapeutique pendant ou après la semaine 6 dans l’étude UV 1 ou pendant ou après la semaine 2 dans l’étude UV 2
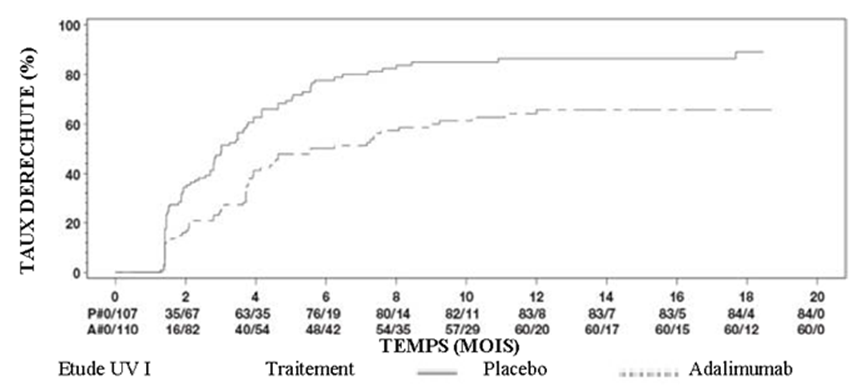
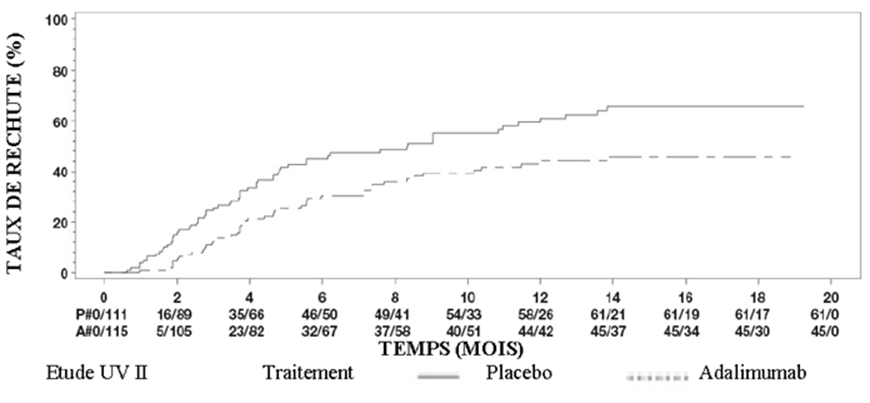
Une analyse de sensibilité du critère primaire, comptabilisant comme échecs thérapeutiques les patients avec arrêt prématuré du traitement et les patients avec une co-administration interdite de corticostéroïdes, a révélé un effet puissant du traitement en faveur d’adalimumab (UV I: HR = 0,66; IC à 95%: 0,48 à 0,88, p = 0,005; UV II: HR = 0,59; IC à 95%: 0,42 à 0,81; p = 0,001).
Dans les deux études, tous les éléments du critère primaire ont contribué de façon cumulative à la différence totale entre le groupe sous adalimumab et le groupe sous placebo.
Dans l’étude UV 1, des différences statistiquement significatives ont été constatées en faveur de l’adalimumab pour la variation du nombre de cellules dans la chambre antérieure, le grade d’opacification du corps vitré et l’acuité visuelle (logMAR BCVA) (variation moyenne par rapport à la meilleure valeur atteinte avant la semaine 6, analyse LOCF; valeurs p: 0,011; <0,001 et 0,003).
Les résultats de l’étude UV II vont en tendance dans le même sens sans être statistiquement significatifs.
Dans l’étude UV I, l’évolution moyenne concernant le grade des cellules de la chambre antérieure, le degré d’opacification du corps vitré et l’acuité visuelle (logMAR BCVA) était caractérisée par des améliorations similaires dans les deux bras de l’étude pendant les 4 à 6 premières semaines de traitement avec réduction progressive de la corticothérapie concomitante. À la suite de cette période, l’augmentation du degré d’inflammation et la perte d’acuité visuelle étaient plus faibles sous adalimumab que sous placebo. Dans l’étude UV II, l’augmentation du degré d’inflammation et la perte d’acuité visuelle étaient également plus faibles que sous placebo.
Sur un total de 417 participants inclus à l'étude d'extension à long terme non contrôlée des études UV I et UV II, 46 participants ont été exclus de l'analyse primaire de l'efficacité, pour laquelle ils avaient été jugés inappropriés (p.ex. développement de complications secondaires à une rétinopathie diabétique, en raison d’une opération d'une cataracte ou vitrectomie). Sur les 371 patients restants, 276 patients analysables ont poursuivi le traitement en ouvert par l'adalimumab jusqu'à la semaine 78. D'après les données enregistrées, 222 (80,4%) des patients recevant en même temps des corticostéroïdes à raison de ≤7,5 mg par jour ont atteint un contrôle de la maladie (aucune lésion inflammatoire active, grade des cellules de la chambre antérieure ≤0,5+, grade d'opacification du corps vitré ≤0,5+), tandis que 184 (66,7%) des patients ont atteint un contrôle de la maladie sans utilisation de corticostéroïdes. À 78 semaines, BCVA était améliorée ou inchangée chez 88,4% des yeux (réduction de <5 lettres). Parmi les patients ayant quitté l'étude avant la semaine 78, cette décision était due à des effets indésirables chez 11% et à une réponse insuffisante à l'adalimumab chez 5%.
Qualité de vie
Dans l’étude UV 1, le traitement par adalimumab a permis de préserver la fonction dépendante de la capacité visuelle et la qualité de vie en fonction de la santé (évaluée à l’aide du NEI VFQ-25).
|




