CompositionPrincipes actifs
Idécabtagène vicleucel: immunothérapie à base de cellules T autologues génétiquement modifiées, consistant en des cellules T transduites avec un vecteur lentiviral (LVV) codant pour un récepteur antigénique chimérique (CAR) qui reconnaît l'antigène de maturation des cellules B.
Excipients
Cryostor CS10 (5 % DMSO, Dextran-40), chlorure de sodium, gluconate de sodium, acétate de sodium trihydraté, chlorure de potassium, chlorure de magnésium et eau pour préparations injectables.
Abecma contient jusqu'à 752 mg de sodium et 274 mg de potassium par dose.
Indications/Possibilités d’emploiAbecma est indiqué pour le traitement des patients adultes atteints d'un myélome multiple en rechute et réfractaire:
·ayant reçu deux lignes de traitement antérieures, incluant un agent immunomodulateur, un inhibiteur du protéasome et un anticorps anti-CD38 et dont la maladie a progressé sous traitement ou dans les 60 jours après le dernier traitement.
·ayant reçu au moins trois lignes de traitement antérieures, incluant un agent immunomodulateur, un inhibiteur du protéasome et un anticorps anti-CD38, et dont la maladie a progressé pendant le dernier traitement.
Posologie/Mode d’emploiAbecma doit être administré dans un centre de traitement qualifié avec un accès immédiat à des soins médicaux intensifs appropriés. Le traitement par Abecma doit être instauré sous la supervision d'un médecin qui a l'expérience du traitement des hémopathies malignes et qui a reçu une formation pour l'administration et la prise en charge des patients traités par Abecma, y compris le traitement du syndrome de libération des cytokines (CRS) et de la neurotoxicité.
Avant la perfusion d'Abecma, il convient de disposer d'au moins deux doses de tocilizumab à utiliser en cas de CRS ainsi que d'un équipement d'urgence. Le centre de traitement doit avoir accès à une dose supplémentaire de tocilizumab dans les 8 heures suivant chaque dose précédente.
Abecma est destiné exclusivement à un usage autologue.
Il est préparé sous forme d'une perfusion unique et contient une dispersion de cellules T chimériques viables positives aux récepteurs de l'antigène dans une ou plusieurs poches de perfusion. La dose cible est de 420 x 106 cellules T viables CAR-positives dans une plage de 260 à 500 × 106 cellules T viables CAR-positives.
De plus amples informations sur la dose se trouvent dans le certificat RFI joint.
Prétraitement
Une chimiothérapie lymphodéplétive, composée de cyclophosphamide 300 mg/m2 par voie intraveineuse (i.v.) et de fludarabine 30 mg/m2 i.v., doit être administrée sur 3 jours.
Pour plus d'informations sur l'ajustement posologique en cas de troubles de la fonction rénale, veuillez consulter les informations professionnelles du cyclophosphamide et de la fludarabine.
Abecma est administré 2 jours à un maximum de 9 jours après la fin de la chimiothérapie lymphodéplétive. La disponibilité d'Abecma doit être confirmée avant le début du régime de chimiothérapie lymphodéplétive. Si plus de 4 semaines s'écoulent entre la fin de la chimiothérapie lymphodéplétive et la perfusion, le patient doit être à nouveau traité par chimiothérapie lymphodéplétive avant le traitement par Abecma.
Évaluation clinique avant la perfusion
La perfusion d'Abecma doit être reportée jusqu'à 7 jours si l'une des situations suivantes s'applique à un patient:
·Effets secondaires graves persistants (notamment effets secondaires pulmonaires ou cardiaques ou hypotension), y compris ceux consécutifs à une chimiothérapie antérieure.
·Infections actives ou maladies inflammatoires.
·Maladie du greffon contre l'hôte (GVHD, graft-versus-host-disease) active.
·Développement d'une aggravation cliniquement significative du myélome multiple qui entraîne un dysfonctionnement organique cliniquement significatif.
Prémédication
Pour minimiser le risque de réactions à la perfusion, le patient doit recevoir du paracétamol (acétaminophène) (500-1000 mg par voie orale) et de la diphénhydramine (12,5 mg par voie intraveineuse ou 25-50 mg par voie orale) ou un autre antihistaminique H1 environ 30 à 60 minutes avant la perfusion d'Abecma.
L'utilisation prophylactique de la dexaméthasone ou d'autres corticostéroïdes systémiques doit être évitée, car ces médicaments peuvent affecter l'activité d'Abecma. Les doses thérapeutiques de corticostéroïdes doivent être évitées 72 heures avant le début de la chimiothérapie de déplétion lymphatique et après la perfusion d'Abecma, sauf pour le traitement du CRS, des toxicités neurologiques et d'autres urgences mettant en jeu le pronostic vital (voir rubrique « Mises en garde et précautions »).
Surveillance
·Les patients doivent être surveillés au moins quotidiennement pour détecter les signes et symptômes du syndrome de libération des cytokines et des toxicités neurologiques pendant les 10 jours suivant la perfusion d'Abecma dans l'établissement clinique qualifié.
·Après l'expiration des 10 premiers jours suivant la perfusion, le patient doit être surveillé à la discrétion du médecin.
·Les patients doivent être invités à rester à proximité d'un centre clinique qualifié pendant au moins 4 semaines après la perfusion (à une distance de 2 heures maximum).
Groupes de patients particuliers
Patients présentant une infection au virus de l'immunodéficience humaine (VIH), au virus de l'hépatite B (VHB) et au virus de l'hépatite C (VHC)
Il n'existe aucune expérience clinique avec des patients présentant une infection active au VIH, au VHB ou au VHC. Avant le prélèvement cellulaire pour la production, il faut effectuer un dépistage de l'infection par le VHB, de l'infection active par le VIH et de l'infection active par le VHC conformément aux lignes directrices cliniques. Le matériel de leucaphérèse des patients présentant une infection active par le VIH ou le VHC n'est pas accepté pour la production d'Abecma (voir rubrique « Mises en garde et précautions »).
Patients présentant des troubles de la fonction hépatique
Aucune étude n'a été réalisée sur les troubles de la fonction hépatique avec Abecma.
Patients présentant des troubles de la fonction rénale
Aucune étude n'a été réalisée sur les troubles de la fonction rénale avec Abecma.
Patients âgés
Aucun ajustement de la dose n'est nécessaire chez les patients âgés de plus de 65 ans (voir la rubrique « Sécurité et efficacité chez les patients âgés »).
Enfants et adolescents
La sécurité et l'efficacité d'Abecma chez les patients pédiatriques ou adolescents (moins de 18 ans) n'ont pas été étudiées.
Mode d'administration
Abecma est destiné uniquement à une utilisation intraveineuse.
Précautions à prendre avant la manipulation ou l'administration du médicament
Ce médicament contient des cellules sanguines humaines génétiquement modifiées. Le personnel médical qui travaille avec Abecma doit prendre les mesures de précaution appropriées (porter des gants et des lunettes de protection) afin d'éviter une transmission potentielle de maladies infectieuses.
Préparation d'Abecma pour la perfusion
·Avant la préparation d'Abecma, il faut confirmer que l'identité du patient correspond aux coordonnées du patient figurant sur les cassettes Abecma et les poches de perfusion.
·La poche pour perfusion Abecma ne doit pas être retirée de la cassette si les informations figurant sur l'étiquette spécifique au patient ne correspondent pas au patient prévu. En cas de divergence entre les étiquettes et les indications sur le patient, il faut contacter le titulaire de l'autorisation de mise sur le marché.
·Le moment de la décongélation d'Abecma doit être coordonné avec le moment de la perfusion. Il faut confirmer au préalable à quel moment la perfusion doit être effectuée. Le temps de décongélation doit alors être adapté de manière à ce que Abecma soit disponible pour la perfusion dès que le patient est prêt.
·La poche de perfusion doit être examinée avant la décongélation pour déceler tout dommage, comme des déchirures ou des fissures. Si la poche est endommagée, le titulaire de l'autorisation de mise sur le marché doit être contacté.
·Placez la poche de perfusion dans une deuxième poche stérile conformément aux directives locales.
·Si le traitement comporte plus d'une poche de perfusion, décongelez chaque poche à perfusion individuellement.
·Décongelez Abecma à environ 37 °C avec un dispositif de décongélation autorisé ou dans un bain-marie jusqu'à ce qu'il ne reste plus de glace visible dans la poche de perfusion. Mélangez délicatement le contenu de la poche pour dissoudre les agglomérats visibles de matière cellulaire. Des petits agglomérats de matière cellulaire peuvent subsister malgré un mélange précautionneux. Abecma ne doit pas être lavé, centrifugé, ni remis en suspension dans de nouveaux milieux avant la perfusion.
Administration
·N'utilisez PAS de filtre de leucodéplétion.
·Assurez-vous que le tocilizumab et un équipement d'urgence sont disponibles avant la perfusion et pendant la phase de récupération.
·Un cathéter veineux central peut être utilisé pour perfuser Abecma, ce qui est recommandé pour les patients ayant un mauvais accès périphérique.
·Confirmez que l'identité du patient concorde avec les indications relatives au patient sur la poche de perfusion d'Abecma.
·Préparez la tubulure du set de perfusion avant la perfusion avec une solution injectable de chlorure de sodium à 9 mg/ml (0,9 %). Un set de perfusion avec filtre en ligne doit être utilisé pour les produits décongelés (ne PAS utiliser de filtre de leucodéplétion).
·Perfusez Abecma dans l'heure qui suit le début de la décongélation.
·Après avoir perfusé la totalité du contenu de la poche de perfusion, rincez la tubulure, y compris le filtre en ligne, au même débit de perfusion, avec une solution injectable de chlorure de sodium à 9 mg/ml (0,9 %) pour s'assurer que le patient reçoive le plus grand nombre de cellules possible.
·Suivez la même procédure pour toutes les poches de perfusion suivantes pour le patient déterminé.
Pour les précautions particulières d'élimination, veuillez vous référer à la rubrique « Remarques particulières ».
Contre-indicationsHypersensibilité au principe actif ou à l'un des excipients mentionnés dans la rubrique «Composition».
Les contre-indications de la chimiothérapie lymphodéplétive doivent être respectées.
Mises en garde et précautionsSyndrome de libération de cytokines (Cytokine Release Syndrome, CRS)
Des cas de CRS, y compris des réactions mortelles ou potentiellement mortelles, sont survenus après le traitement par Abecma. Dans les études cliniques, le délai médian jusqu'à la survenue d'un CRS était de 1 jour (plage: entre 1 et 17 jours) (voir rubrique « Effets indésirables »).
Surveillance et traitement du CRS
Le CRS doit être identifié sur la base du tableau clinique. Les patients doivent être examinés pour déceler d'autres causes de fièvre, d'hypoxie et d'hypotension et traités en conséquence. Il a été rapporté que le CRS est associé à des signes de lymphohistiocytose hémophagocytaire/syndrome d'activation des macrophages (HLH/MAS) et que la physiologie de ces syndromes peut se chevaucher. Le MAS est une maladie potentiellement mortelle et les patients doivent être étroitement surveillés pour déceler tout signe de MAS. Le traitement du MAS doit être mené conformément aux normes institutionnelles.
Il convient de s'assurer qu'au moins deux traitements par tocilizumab sont disponibles avant la perfusion d'Abecma. Le centre de traitement doit avoir accès à une dose supplémentaire de tocilizumab dans les 8 heures suivant chaque dose précédente.
Les patients doivent être surveillés au moins quotidiennement pendant 10 jours après la perfusion d'Abecma dans l'établissement clinique qualifié afin de déceler tout signe ou symptôme de CRS. Les signes ou symptômes de CRS doivent être surveillés pendant au moins 4 semaines après la perfusion.
Lors des premiers signes de CRS, un traitement par mesures de soutien, tocilizumab ou corticostéroïdes doit être instauré si indiqué. En cas de suspicion de CRS, suivre les recommandations du tableau 1. Les fonctions cardiaque et organique des patients présentant un CRS doivent être surveillées étroitement jusqu'à la disparition des symptômes. En cas de CRS sévère ou potentiellement mortel, une surveillance en soins intensifs et un traitement de soutien doivent être envisagés.
Il convient d'informer les patients et de leur recommander de consulter immédiatement un médecin si des signes ou symptômes de CRS apparaissent à un moment quelconque.
Une escalade précoce (c'est-à-dire une dose plus élevée de corticostéroïdes, des agents anticytokines alternatifs, des thérapies anti-cellules T) est recommandée pour les patients présentant un CRS persistant dans les 72 heures suivant la perfusion d'Abecma, caractérisé par une fièvre persistante, une toxicité des organes terminaux (par exemple, hypoxie, hypotension), et/ou une HLH/un MAS qui ne s'améliore pas dans les 12 heures suivant les interventions de première intention.
Tableau 1: Classification du CRS et directives thérapeutiques
|
Degré de CRSa
|
Tocilizumab
|
Corticostéroïdes
| |
Grade 1
Les symptômes nécessitent uniquement un traitement symptomatique (p.ex. fièvre, nausées, fatigue, maux de tête, myalgie, malaise).
|
Si les symptômes apparaissent 72 heures ou plus après la perfusion, traiter de manière symptomatique.
Si les symptômes surviennent moins de 72 heures après la perfusion, une perfusion de 1 heure de tocilizumab 8 mg/kg i.v. doit être envisagée (pas plus de 800 mg).
|
─
| |
Grade 2
Les symptômes nécessitent une intervention modérée et y réagissent.
Besoin en oxygène inférieur à 40 % FiO2 ou hypotension répondant aux fluides ou à de faibles doses d'un vasopresseur, ou toxicité organique de grade 2.
|
Administration de tocilizumab 8 mg/kg i.v. en 1 heure (pas plus de 800 mg).
|
Envisager la dexaméthasone 10 mg i. v. toutes les 12 à 24 heures.
| |
En l'absence d'amélioration ou en cas de progression rapide en l'espace de 24 heures, répéter l'administration du tocilizumab et augmenter la dose et la fréquence de la dexaméthasone (20 mg i.v. toutes les 6 à 12 heures).
Si aucune amélioration n'est constatée en l'espace de 24 heures ou si la progression rapide persiste, passer à la méthylprednisolone 2 mg/kg, suivie de 2 mg/kg administrés en quatre fois par jour.
Si des stéroïdes sont instaurés, poursuivre les stéroïdes au moins trois fois et diminuer progressivement pendant 7 jours maximum.
Après deux traitements par le tocilizumab, d'autres anticytokines doivent être envisagées.
Ne pas dépasser trois traitements par le tocilizumab en l'espace de 24 heures ou quatre traitements par le tocilizumab en tout.
| |
Grade 3
Les symptômes nécessitent une intervention agressive et y réagissent.
Fièvre, besoin en oxygène supérieur ou égal à 40 % FiO2 ou hypotension nécessitant des vasopresseurs hautement dosés ou plusieurs vasopresseurs, ou toxicité organique de grade 3 ou élévation des transaminases de grade 4.
|
Administration de tocilizumab 8 mg/kg i.v. en 1 heure (pas plus de 800 mg).
|
Administration de la dexaméthasone (p.ex. 10 mg i. v. toutes les 12 heures).
| |
En l'absence d'amélioration ou en cas de progression rapide en l'espace de 24 heures, répéter l'administration du tocilizumab et augmenter la dose et la fréquence de la dexaméthasone (20 mg i. v. toutes les 6 à 12 heures).
Si aucune amélioration n'est constatée en l'espace de 24 heures ou si la progression rapide persiste, passer à la méthylprednisolone 2 mg/kg, suivie de 2 mg/kg administrés en quatre fois par jour.
Si des stéroïdes sont instaurés, poursuivre les stéroïdes au moins trois fois et diminuer progressivement pendant 7 jours maximum.
Après deux traitements par le tocilizumab, d'autres anticytokines doivent être envisagées.
Ne pas dépasser trois traitements par le tocilizumab en l'espace de 24 heures ou quatre traitements par le tocilizumab en tout.
| |
Grade 4
Symptômes mettant en jeu le pronostic vital.
Ventilation assistée requise, hémodialyse veino-veineuse continue (CVVHD) ou toxicité organique de grade 4 (sauf augmentation des transaminases).
|
Administration de tocilizumab 8 mg/kg i.v. en 1 heure (pas plus de 800 mg).
|
Administration de la dexaméthasone 20 mg i. v. toutes les 6 heures.
| |
Après deux traitements par le tocilizumab, d'autres anticytokines doivent être envisagées. Ne pas dépasser trois traitements par le tocilizumab en l'espace de 24 heures ou quatre traitements par le tocilizumab en tout.
En l'absence d'amélioration dans les 24 heures, envisager un traitement par méthylprednisolone (1 à 2 g, à répéter toutes les 24 heures si nécessaire ; diminuer progressivement selon l'indication clinique) ou des thérapies anti-cellules T telles que le cyclophosphamide 1,5 g/m2 ou autres.
|
a Critères Lee d'évaluation du CRS (Lee et al., 2014).
Toxicités neurologiques
Des toxicités neurologiques, y compris le syndrome de neurotoxicité lié aux cellules effectrices de l'immunité (ICANS), pouvant être graves ou potentiellement mortelles sont survenues après le traitement par Abecma, également en même temps qu’un CRS, après disparition du CRS et sans CRS.
Le délai médian jusqu'à l'apparition du premier événement de neurotoxicité constaté par le médecin investigateur était de 3 jours (plage: entre 1 et 317 jours), un patient a développé une encéphalopathie le 317e jour, suite à l'aggravation d'une pneumonie et d'une colite à Clostridium difficile (voir rubrique « Effets indésirables »).
Parkinsonisme
Un parkinsonisme de grade 3 est survenu après le traitement par Abecma au cours d'une étude sur le myélome multiple. Les symptômes signalés comprenaient tremblement, dysphasie, bradykinésie et réflexes parkinsoniens.
Surveiller les patients pour détecter tout signe ou symptôme de toxicité neurologique, y compris les symptômes de parkinsonisme. Les informations sur la prise en charge du parkinsonisme chez les patients ayant reçu un traitement par Abecma sont insuffisantes. Le traitement des toxicités neurologiques, y compris du parkinsonisme, doit se baser sur la pratique institutionnelle ou clinique standard et doit être déterminé par le médecin traitant.
Surveillance et traitement des toxicités neurologiques
Les patients doivent être surveillés à la recherche de signes et symptômes de toxicités neurologiques au moins quotidiennement pendant les 10 jours suivant la perfusion d'Abecma dans l'établissement clinique qualifié (tableau 2). D'autres causes de symptômes neurologiques doivent être exclues. Les patients doivent être surveillés pendant au moins 4 semaines après la perfusion pour déceler tout signe ou symptôme de toxicité neurologique, et immédiatement traités. En cas de suspicion de toxicité neurologique, il convient de suivre les recommandations du tableau 2, si nécessaire avec des mesures de soutien et des corticostéroïdes. En cas de toxicités neurologiques sévères ou potentiellement mortelles, un traitement médical de soutien intensif doit être instauré.
Si un SRC concomitant est suspecté lors d'une toxicité neurologique, il doit être traité selon les recommandations du tableau 1, et l'intervention la plus agressive de celles énumérées dans les tableaux 1 et 2 doit être utilisée.
Les patients doivent être invités à consulter immédiatement un médecin si des signes ou symptômes de toxicité neurologique apparaissent à un moment quelconque.
Tableau 2: Classification des toxicités neurologiques et directives thérapeutiques
|
Degré de toxicité
neurologiquea
|
Corticostéroïdes et anticonvulsifs
| |
Grade 1
|
Instauration d'anticonvulsifs non sédatifs (p.ex. lévétiracétam) pour prévenir les convulsions.
Si 72 heures ou plus après la perfusion, observer le patient.
Si moins de 72 heures après la perfusion, envisager un traitement par la dexaméthasone 10 mg i. v. toutes les 12 à 24 heures pendant 2 à 3 jours.
| |
Grade 2
|
Instauration d'anticonvulsifs non sédatifs (p.ex. lévétiracétam) pour prévenir les convulsions.
Instauration de la dexaméthasone 10 mg i. v. toutes les 12 heures pendant 2 à 3 jours, et plus longtemps en cas de symptômes persistants. En cas d'exposition aux stéroïdes d'une durée totale de 3 jours, envisager une diminution progressive. Les stéroïdes ne sont pas recommandés en cas de céphalées isolées de grade 2.
En l'absence d'amélioration ou en cas d'aggravation de la toxicité neurologique après 24 heures, augmenter la dose ou la fréquence de la dexaméthasone jusqu'à un maximum de 20 mg i.v. toutes les 6 heures.
| |
Grade 3
|
Instauration d'anticonvulsifs non sédatifs (p.ex. lévétiracétam) pour prévenir les convulsions.
Instauration de la dexaméthasone 10 à 20 mg i. v. toutes les 8 à 12 heures. Les stéroïdes ne sont pas recommandés en cas de céphalées isolées de grade 3.
En l'absence d'amélioration ou d'aggravation de la toxicité neurologique après 24 heures, passage à la méthylprednisolone (dose de charge de 2 mg/kg, suivie de 2 mg/kg répartis en quatre fois par jour ; diminution progressive en l'espace de 7 jours).
En cas de suspicion d'œdème cérébral, envisager une hyperventilation et un traitement hyperosmolaire. Administration de méthylprednisolone à haute dose (1 à 2 g, répéter toutes les 24 heures si nécessaire ; diminuer progressivement selon l'indication clinique) et de cyclophosphamide 1,5 g/m2.
| |
Grade 4
|
Instauration d'anticonvulsifs non sédatifs (p.ex. lévétiracétam) pour prévenir les convulsions.
Administration de dexaméthasone 20 mg i. v. toutes les 6 heures.
En l'absence d'amélioration ou en cas d'aggravation de la toxicité neurologique après 24 heures, passer à une dose élevée de méthylprednisolone (1 à 2 g, à répéter toutes les 24 heures si nécessaire ; diminuer progressivement selon l'indication clinique). Envisager un traitement par cyclophosphamide 1,5 g/m2.
En cas de suspicion d'œdème cérébral, envisager une hyperventilation et un traitement hyperosmolaire. Administration de méthylprednisolone à haute dose (1 à 2 g, répéter toutes les 24 heures si nécessaire ; diminuer progressivement selon l'indication clinique) et de cyclophosphamide 1,5 g/m2.
|
a Critères de terminologie généraux pour les événements indésirables du National Cancer Institute (USA) pour la classification des toxicités neurologiques.
Réactions d'hypersensibilité
Des réactions allergiques peuvent survenir lors de la perfusion d'Abecma. Des réactions d'hypersensibilité sévères, y compris une anaphylaxie, peuvent être dues au diméthylsulfoxyde (DMSO) contenu dans Abecma.
Infections et neutropénie fébrile
Abecma ne doit pas être administré aux patients présentant des infections actives ou des maladies inflammatoires. Des infections graves, potentiellement mortelles ou mortelles sont survenues chez des patients après la perfusion d'Abecma (voir rubrique « Effets indésirables »). Les patients doivent être surveillés avant et après la perfusion d'Abecma pour déceler tout signe et symptôme d'infection et traités en conséquence. Des antimicrobiens prophylactiques, préventifs ou thérapeutiques, doivent être administrés conformément aux directives institutionnelles locales.
Une neutropénie fébrile a été observée chez des patients après la perfusion d'Abecma (voir rubrique « Effets indésirables ») et peut survenir en même temps que le CRS. En cas de survenue d'une neutropénie fébrile, le patient doit être examiné pour détecter une éventuelle infection et, en fonction de l'indication médicale, traité avec des antibiotiques à large spectre, des liquides et d'autres mesures de soutien.
Réactivation virale
Des infections au cytomégalovirus (CMV) ayant entraîné une pneumonie et la mort sont survenues après l'administration d'Abecma. Une réactivation du CMV doit être surveillée et traitée conformément aux directives cliniques.
Une réactivation du virus de l'hépatite B (VHB), qui entraîne dans certains cas une hépatite fulminante, une défaillance hépatique et la mort, peut survenir chez les patients traités par des médicaments dirigés contre les plasmocytes.
Le dépistage du CMV, du VHB, du VIH actif et du VHC actif doit être effectué conformément aux directives cliniques avant la collecte des cellules pour la préparation.
Envisagez un traitement antiviral conformément aux directives cliniques locales/à la pratique clinique afin d'éviter une réactivation du virus.
Cytopénies prolongées
Les patients peuvent développer des cytopénies prolongées après une chimiothérapie lymphodéplétive et la perfusion d'Abecma (voir rubrique « Effets indésirables »).
Les paramètres hématologiques doivent être surveillés avant et après la perfusion d'Abecma. Une cytopénie doit être surveillée. La surveillance doit être effectuée conformément aux directives cliniques locales, avec l'aide de facteurs de croissance myéloïdes et de transfusions de produits sanguins.
Hypogammaglobulinémie
Une aplasie des plasmocytes et une hypogammaglobulinémie peuvent survenir chez les patients traités par Abecma (voir rubrique « Effets indésirables »).
Les taux d'immunoglobulines doivent être surveillés après le traitement par Abecma et gérés conformément aux lignes directrices cliniques locales, y compris les précautions contre les infections, la prophylaxie antibiotique ou antivirale et un traitement substitutif par immunoglobulines.
Utilisation de vaccins vivants
La sécurité de l'immunisation par des vaccins viraux vivants pendant et après le traitement par Abecma n'a pas été étudiée. La vaccination avec des vaccins viraux vivants n'est pas recommandée pendant au moins 6 semaines avant le début de la chimiothérapie lymphodéplétive, pendant le traitement par Abecma et jusqu'à la récupération immunitaire après le traitement par Abecma.
Tumeurs malignes secondaires
Les patients traités par Abecma peuvent développer des tumeurs malignes secondaires. Les patients doivent être surveillés à vie pour déceler d'éventuelles tumeurs malignes secondaires. En cas de survenue d'une tumeur maligne hématologique secondaire, le titulaire de l'autorisation de mise sur le marché doit être contacté pour obtenir des instructions relatives à la déclaration et les tests possibles.
Don de sang, dons d'organes, de tissus et de cellules
Les patients traités par Abecma ne doivent pas faire de don de sang, d'organes, de tissus et de cellules pour les transplantations.
Antécédents de greffe de cellules souches
Il n'est pas recommandé aux patients de recevoir Abecma dans les 4 mois suivant une greffe de cellules souches (GCS) allogéniques, car il existe un risque potentiel d'aggravation de la maladie du greffon contre l'hôte (GVHD). La leucaphérèse permettant de produire Abecma doit être réalisée au plus tôt 12 semaines après une GCS allogénique.
Excipients
Abecma contient jusqu'à 33 mmol (752 mg) de sodium par dose, ce qui équivaut à 37,6 % de l'apport alimentaire quotidien maximal recommandé par l'OMS de 2 g de sodium pour un adulte.
Abecma contient jusqu'à 7 mmol (274 mg) de potassium par dose. Ceci doit être pris en compte chez les patients présentant une insuffisance rénale et chez les patients ayant une alimentation contrôlée pauvre en potassium.
InteractionsAucune étude d'interaction n'a été réalisée.
Interactions entre les médicaments et les analyses de laboratoire
Le VIH et le lentivirus utilisé pour la fabrication d'Abecma présentent du matériel génétique identique (ARN) sur un domaine limité et court. C'est pourquoi certains tests commerciaux de dépistage du VIH utilisant les acides nucléiques peuvent avoir des résultats faux positifs chez les patients ayant reçu Abecma.
Grossesse, allaitementFemmes en âge de procréer/méthodes de contraception chez l'homme et la femme
Le statut de grossesse des femmes en âge de procréer doit être contrôlé avant le début du traitement par Abecma au moyen d'un test de grossesse.
Les données d'exposition disponibles sont insuffisantes pour émettre une recommandation concernant la durée de la contraception après le traitement par Abecma.
Pour de plus amples informations sur la nécessité d'une méthode contraceptive efficace chez les patientes ayant reçu une chimiothérapie lymphodéplétive, veuillez consulter les informations professionnelles de la fludarabine et du cyclophosphamide.
Grossesse
Il n'existe pas de données sur l'utilisation d'Abecma chez les femmes enceintes. Aucune étude de toxicité sur la reproduction et le développement n'a été réalisée chez l'animal avec Abecma pour évaluer si Abecma peut entraîner une lésion du fœtus en cas d'administration à une femme enceinte.
On ne sait pas si Abecma peut être transmis au fœtus. Sur la base du mécanisme d'action, les cellules transduites, si elles passent la barrière placentaire, peuvent provoquer une toxicité fœtale, notamment une aplasie des plasmocytes ou une hypogammaglobulinémie. Par conséquent, Abecma n'est pas recommandé pour les femmes enceintes et toute grossesse survenant après la perfusion d'Abecma doit faire l'objet d'une discussion avec le médecin traitant. Les taux d'immunoglobuline chez les nouveau-nés de mères traitées par Abecma doivent être mesurés.
Allaitement
Il n'existe aucune donnée sur la présence d'Abecma dans le lait maternel, l'effet sur le nourrisson allaité et les effets sur la production de lait. Les bénéfices de l'allaitement pour le développement et la santé doivent être pris en compte, ainsi que la nécessité clinique d'Abecma pour la mère et les effets indésirables potentiels sur le nourrisson allaité d'Abecma ou de l'affection sous-jacente de la mère.
Fertilité
Aucune donnée n'est disponible sur les effets d'Abecma sur la fertilité.
Effet sur l’aptitude à la conduite et l’utilisation de machinesÉtant donné que des événements neurologiques, y compris des modifications de la conscience et des crises convulsives, peuvent survenir, il existe un risque de modification ou de diminution de l'état de conscience ou de la coordination chez les patients ayant reçu Abecma au cours des 8 semaines suivant la perfusion d'Abecma. Indiquez aux patients de ne pas conduire de véhicule pendant au moins 8 semaines après la perfusion d'Abecma et de ne pas effectuer d'activités ou de travaux dangereux tels que l'utilisation de machines lourdes ou potentiellement dangereuses.
Effets indésirablesLes données de sécurité décrites dans cette section reflètent l'exposition à Abecma dans les études KarMMa, CRB-401 et KarMMa-3, dans lesquelles 409 patients atteints de myélome multiple récidivant et réfractaire ont reçu Abecma (voir la rubrique «Efficacité clinique»). Dans KarMMa (n = 128) et CRB-401 (n = 56), la durée médiane du suivi (de la perfusion d'Abecma à la date de référence de la collecte des données) était de 20,8 mois. Dans KarMMa-3 (N = 225), la durée médiane du suivi était de 29,3 mois.
Les effets indésirables les plus fréquents (incidence ≥20 %) ont été les suivants: CRS (84,6 %), neutropénie (80,0 %), anémie (63,6 %), thrombocytopénie (55,0 %), infections – agent pathogène non spécifié (43,8 %), hypophosphatémie (33,3 %), diarrhée (33,0 %), leucopénie (32,8 %), hypokaliémie (32,0 %), fatigue (29,8 %), nausées (28,1 %), lymphopénie (26,9 %), pyrexie (24,7 %), infections virales (23,2 %), céphalées (22,5 %), hypocalcémie (22,0 %), hypomagnésémie (21,3 %), arthralgie (20,0 %); les autres effets indésirables fréquents qui sont survenus à une fréquence moindre et qui ont été considérés comme cliniquement pertinents incluent hypotension (18,6 %), infection des voies respiratoires supérieures (15,6 %), hypogammaglobulinémie (13,7 %), neutropénie fébrile (11,2 %), pneumonie (11,0 %), tremblements (5,6 %), somnolence (5,6 %), encéphalopathie (3,4 %), syncope (3,2 %) et aphasie (2,9 %).
Des effets secondaires graves sont survenus chez 57,2 % des patients. Les effets indésirables graves les plus fréquents (5 % des patients ou plus) ont été: CRS (10,3 %) et pneumonie (7,1 %); les autres effets indésirables graves survenus à une fréquence moindre et considérés comme cliniquement pertinents incluent: neutropénie fébrile (4,2 %), pyrexie (3,7 %), neutropénie (2,7 %), sepsis (2,7 %), état confusionnel (2,4 %), lymphohistiocytose hémophagocytaire (1,7 %), thrombocytopénie (1,5 %), encéphalopathie (1,5 %), dyspnée (1,5 %), convulsions (1,0 %), altérations de l'état mental (1,0 %), hypoxie (0,7 %) et coagulation intravasculaire disséminée (0,5 %).
Les effets indésirables de grade 3 ou 4 les plus fréquents (5 % des patients ou plus) ont été neutropénie (77,3 %), anémie (50,9 %), thrombocytopénie (42,5 %), leucopénie (31,5 %), lymphopénie (25,9 %), hypophosphatémie (19,8 %), infections (agents pathogènes non spécifiés; 15,2 %), neutropénie fébrile (10,5 %), infections virales (7,6 %), pneumonie (6,8 %), hypertension (6,6 %), hypocalcémie (5,6 %) et infections bactériennes (5,4 %).
Les effets indésirables du médicament observés, survenus chez 409 patients traités par Abecma dans les fourchettes de doses autorisées de 150 à 540 x 106 cellules CAR-T positives (voir le tableau 3 de la rubrique «Efficacité clinique» pour la fourchette de doses correspondante de cellules T viables CAR-positives dans KarMMa) dans les études cliniques sont présentés ci-dessous par classe d'organe du système MedDRA et par fréquence. Les fréquences sont définies comme: très fréquent (≥1/10); fréquent (≥1/100 à < 1/10), occasionnel (≥1/1000 à < 1/100), rare (≥1/10 000 à < 1/1000), très rare (< 1/10 000) et fréquence inconnue (la fréquence ne peut pas être estimée sur la base des données disponibles). Au sein de chaque groupe de fréquence, les effets indésirables sont présentés par fréquence décroissante.
Infections et infestationsa
Très fréquents: infections (agents pathogènes non spécifiés) (43,8 %), infections virales (23,2 %), infections bactériennes (15,4 %).
Fréquents: infections fongiques.
Affections hématologiques et du système lymphatique
Très fréquents: neutropénie (80,0 %), anémie (63,6 %), thrombocytopénie (55,0 %), leucopénie (32,8 %), lymphopénie (26,9 %), neutropénie fébrile (11,2 %).
Fréquents: coagulation intravasculaire disséminée.
Affections du système immunitaire
Très fréquents: syndrome de libération de cytokines (84,6 %), hypogammaglobulinémie (13,7 %).
Fréquents: lymphohistiocytose hémophagocytaire.
Troubles du métabolisme et de la nutrition
Très fréquents: hypophosphatémie (33,3 %), hypokaliémie (32,0 %), hypocalcémie (22,0 %), hypomagnésémie (21,3 %), perte d'appétit (17,8 %), hyponatrémie (13,9 %), hypoalbuminémie (11,5 %).
Affections psychiatriques
Très fréquents: insomnie (10,3 %).
Fréquents: délireb.
Affections du système nerveux
Très fréquents: encéphalopathied (23,5 %), céphaléesc (22,5 %), vertigese (16,1 %).
Fréquents: dysfonction motricef, tremblements, aphasieg, ataxieh, convulsions.
Rares: hémiparésie.
Affections cardiaques
Très fréquents: tachycardiei (18,3 %).
Fréquents: fibrillation auriculaire.
Affections vasculaires
Très fréquents: hypotensionj (18,6 %), hypertension (13,9%).
Affections respiratoires, thoraciques et médiastinales
Très fréquents: touxk (18,8 %), dyspnéel (14,4 %).
Fréquents: hypoxie, œdème pulmonaire.
Affections gastro-intestinales
Très fréquents: diarrhée (33,0 %), nausées (28,1 %), constipation (18,3 %), vomissements (15,2 %).
Fréquents: hémorragies gastro-intestinalesm.
Affections musculo-squelettiques et du tissu conjonctif
Très fréquents: arthralgie (20,0 %).
Fréquents: myalgie.
Troubles généraux et anomalies au site d'administration
Très fréquents: fatiguen (29,8 %), pyrexie (24,7 %), œdèmeso (19,6 %), frissons (10,5 %).
Fréquents: asthénie.
Examens
Très fréquents: élévation de l'aspartate aminotransférase (12,2 %) et de l'alanine aminotransférase (11,2 %).
Fréquents: augmentation de la phosphatase alcaline dans le sang, augmentation de la protéine C réactive.
a Les effets indésirables du médicament liés à la classe de systèmes d'organes des infections et des maladies parasitaires sont groupés en fonction du type de pathogène et de syndromes cliniques sélectionnés.
b Le délire englobe délire, désorientation, agitation, hallucination et fébrilité.
c Les céphalées englobent maux de tête et migraines.
d L'encéphalopathie comprend amnésie, bradyphrénie, trouble cognitif, état confusionnel, humeur dépressive, troubles de l'attention, dyscalculie, dysgraphie, encéphalopathie, incohérence, léthargie, troubles de la mémoire, troubles psychiques, modifications de l'état mental, encéphalopathie métabolique, neurotoxicité, somnolence, stupeur.
e Les vertiges englobent vertiges, présyncope, syncope et étourdissements.
f La dysfonction motrice englobe dysfonction motrice, crampes musculaires et faiblesse musculaire.
g L'aphasie englobe aphasie et dysarthrie, élocution lente et troubles de l'élocution.
h L'ataxie englobe ataxie, dysmétrie et troubles de la marche.
i La tachycardie englobe tachycardie sinusale et tachycardie.
j L'hypotension englobe hypotension et hypotension orthostatique.
k La toux englobe toux et syndrome de toux des voies respiratoires supérieures.
l La dyspnée englobe dyspnée et essoufflement à l'effort.
m Les hémorragies gastro-intestinales englobent saignements gastro-intestinaux, saignements gingivaux, hématochézie, saignements hémorroïdaux, méléna et saignements buccaux.
n La fatigue englobe fatigue et malaise.
o Les œdèmes englobent œdèmes, œdèmes périphériques, œdèmes faciaux, œdèmes généralisés, et gonflements périphériques.
Effets indésirables après la mise sur le marché
Sans objet.
Description de certains effets indésirables du médicament
Immunogénicité
Abecma peut induire la production d'anticorps dirigés contre le médicament. Dans des études cliniques, l'immunogénicité humorale d'Abecma a été mesurée avant et après l'administration par détermination des anticorps anti-CAR dans le sérum.
Dans les études groupées (KarMMa, CRB-401 et KarMMa-3), 3,2 % des patients ont été testés positifs aux anticorps anti-CAR avant la perfusion et 54,0 % des patients ont présenté des anticorps anti-CAR après la perfusion. Il n'existe aucune preuve que la présence d'anticorps anti-CAR avant ou après la perfusion ait un quelconque effet sur l'expansion cellulaire, la sécurité ou l'efficacité d'Abecma.
Syndrome de libération de cytokines
Dans les études groupées, 84,6 % des patients ayant reçu Abecma ont présenté un CRS. Un CRS de grade 3 ou supérieur (système de classement selon Lee, 2014) a été observé chez 5,1 % des patients et, chez 0,7 % des patients, il s'est avéré mortel (grade 5). Le délai médian jusqu'à l'apparition (indépendamment du degré d'intensité) était de 1 jour (entre 1 et 17 jours) et la durée médiane du CRS était de 4 jours (entre 1 et 63 jours).
Les manifestations les plus courantes du CRS (≥10 %) étaient une pyrexie (82,6 %), une hypotension (29,1 %), une tachycardie (24,7 %), des frissons (18,8 %), une hypoxie (15,9 %), des céphalées (11,2 %) et une élévation de la protéine C réactive (10,5 %). Parmi les événements de grade 3 ou supérieur observés en lien avec le CRS, on trouve une fibrillation auriculaire, un syndrome de fuite capillaire, une hypotension, une hypoxie et une lymphohistiocytose hémophagocytaire/syndrome d'activation des macrophages (LHH/MAS).
Sur les 409 patients, 59,7 % ont reçu le tocilizumab; 37,2 % ont reçu une administration unique et 22,5 % ont reçu plus d'une dose de tocilizumab pour le traitement du CRS. D'une manière générale, 22,7 % des patients ont reçu au moins 1 dose de corticoïdes pour le traitement du CRS. Parmi les 92 patients dans KarMMa et CRB-401 recevant une dose cible de 450 x 106 cellules CAR-T positives, 54,3 % ont reçu du tocilizumab et 22,8 % ont reçu au moins une dose de corticostéroïdes pour le traitement du CRS. Parmi les 225 patients de l'étude KarMMa-3 ayant reçu une perfusion d'Abecma, 71,6 % ont reçu du tocilizumab et 28,4 % ont reçu au moins une dose de corticostéroïdes pour le traitement du CRS.
Toxicités neurologiques
Dans les études groupées, les effets indésirables neurologiques ou psychiatriques les plus fréquents chez les 409 patients (que l'investigateur ait déterminé ou non une neurotoxicité) englobaient des céphalées (22,5 %), des vertiges (12,5 %), un état confusionnel (11,0 %), des insomnies (10,3 %), une anxiété (5,9 %), des tremblements (5,6 %) et une somnolence (5,6 %). Parmi les autres effets indésirables neurologiques moins fréquents et considérés comme cliniquement pertinents, on compte une encéphalopathie (3,4 %) et une aphasie (2,9 %).
La neurotoxicité détectée par l'investigateur, principale méthode d'évaluation de la neurotoxicité associée aux cellules CAR-T, est survenue chez 57 (16,1 %) des 353 patients recevant Abecma dans les études KarMMa et KarMMa-3, dont un grade 3 ou 4 chez 3,1 % des patients (à l'exclusion des événements de grade 5). Le délai médian jusqu'à l'apparition du premier événement de la neurotoxicité était de 3 jours (entre 1 et 317 jours, un patient a développé une encéphalopathie le 317e jour, suite à l'aggravation d'une pneumonie et d'une colite à Clostridium difficile). La durée médiane de la neurotoxicité constatée par le médecin investigateur était de 3 jours (entre 1 et 252 jours, un patient a développé une neurotoxicité de grade 3 la plus élevée 43 jours après la perfusion d'ide-cel qui a disparu après 252 jours). Dans l'ensemble 7,1 % des patients ont reçu au moins un traitement par corticostéroïdes pour traiter la neurotoxicité associée aux cellules CAR-T. Dans KarMMa, pour tous les niveaux de dose cible, 7,8 % des patients ont reçu au moins une dose de corticostéroïdes pour traiter la neurotoxicité associée aux cellules CAR-T et à la dose cible de 450 x 106 cellules CAR-T positives, 14,8 % des patients ont reçu au moins un traitement par corticostéroïdes. Dans KarMMa-3, 6,7 % des patients recevant une perfusion d'Abecma ont reçu au moins une dose de corticostéroïdes pour traiter la neurotoxicité associée aux cellules CAR-T.
Les manifestations les plus courantes de neurotoxicité (≥2 %) constatées par les médecins investigateurs dans les études KarMMa et KarMMa-3 (total de 353 patients) comprenaient un état confusionnel (8,5 %), une encéphalopathie (3,4 %), une aphasie (2,5 %), des tremblements (2,3 %), des troubles de l'attention (2,0 %) et une dysgraphie (2,0 %).
Le syndrome de neurotoxicité lié aux cellules effectrices de l'immunité (ICANS) a été identifié comme un effet indésirable lors de l'utilisation d'Abecma après sa mise sur le marché. Comme il s'agit de déclarations provenant d'une population de taille inconnue, il n'est pas possible d'en estimer la fréquence.
Infections et neutropénie fébrile
Dans les études groupées, des infections sont survenues chez 62,8 % des patients. Des infections de grade 3 ou 4 sont survenues chez 23,2 % des patients. Des infections de grade 3 ou 4 avec un agent pathogène non spécifié sont survenues chez 15,2 % des patients, des infections virales chez 7,6 %, des infections bactériennes chez 4,6 % des patients et des infections fongiques chez 1,2 % des patients. Des infections fatales dues à un agent pathogène non spécifié ont été observées chez 2,0 % des patients et 0,7 % des patients ont eu une infection fongique ou virale fatale et 0,2 % des patients ont eu une infection bactérienne fatale.
Une neutropénie fébrile (degré 3 ou 4) a été observée chez 10,8 % des patients après la perfusion d'Abecma et peut survenir en même temps qu'un CRS.
Cytopénies prolongées
Après une chimiothérapie lymphodéplétive et une perfusion d'Abecma, des cytopénies prolongées peuvent survenir chez les patients. Dans les études groupées, 151 des 395 patients (38,2 %) ont présenté une neutropénie de grade 3 ou 4 et 164 des 230 patients (71,3 %) ont présenté une thrombocytopénie de grade 3 ou 4 au cours du premier mois après la perfusion d'Abecma, non résolue lors du dernier examen du premier mois. Parmi les 151 patients dont la neutropénie ne s'est pas résorbée au cours du premier mois, 88,7 % ont récupéré d'une neutropénie de grade 3 ou 4 dans un délai médian de récupération de 1,9 mois après la perfusion d'Abecma. Parmi les 164 patients dont la thrombocytopénie ne s'est pas résorbée au cours du premier mois, 79,9 % ont récupéré d'une thrombocytopénie de grade 3 ou 4 dans un délai médian de récupération de 2,0 mois. Les données relatives à la surveillance et au traitement sont présentées dans la rubrique «Mises en garde et précautions».
Hypogammaglobulinémie
Une hypogammaglobulinémie a été rapportée chez 13,7 % des patients traités par Abecma dans le cadre d'études groupées, avec un délai moyen de survenue de 90 jours (plage de 1 à 326 jours).
Déclaration de suspicion d'effets secondaires
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageAbecma est administré uniquement par un personnel médical formé. Les risques de surdosage ne sont pas connus.
Propriétés/EffetsCode ATC
L01XL07
Mécanisme d'action
Abecma est une thérapie par cellules T positives pour le récepteur d'antigène chimérique (thérapie par cellules CAR-T positives) qui cible l'antigène de maturation des cellules B exprimé à la surface des plasmocytes normaux et malins. La construction CAR contient un fragment scFv anti-BCMA pour la spécificité antigénique, un domaine transmembranaire, un domaine d'activation des lymphocytes T CD3 zeta et un domaine de costimulation 4-1BB. L'activation spécifique de l'antigène d'Abecma entraîne la prolifération de lymphocytes CAR-T positifs, la sécrétion de cytokines et la destruction cytolytique ultérieure des cellules exprimant BCMA.
Pharmacodynamique
Sans objet.
Efficacité clinique
KarMMa-3
KarMMa-3 est une étude clinique multicentrique, randomisée, contrôlée, ouverte, visant à évaluer l'efficacité et la sécurité d'Abecma par rapport aux schémas thérapeutiques standards chez des patients adultes atteints d'un myélome multiple récidivant et réfractaire, ayant reçu deux à quatre lignes de traitement antérieures contre le myélome, dont un immunomodulateur, un inhibiteur du protéasome et le daratumumab. Les patients étaient réfractaires à leur dernier traitement contre le myélome. Avant la randomisation, chaque patient a été assigné à un traitement standard en fonction de son dernier traitement contre le myélome. Les thérapies standards étaient composées de: daratumumab, pomalidomide, dexaméthasone (DPd); daratumumab, bortézomib, dexaméthasone (DVd); ixazomib, lénalidomide, dexaméthasone (IRd); carfilzomib, dexaméthasone (Kd) ou élotuzumab, pomalidomide, dexaméthasone (EPd). Lorsque cliniquement indiqué, les patients randomisés sur le bras Abecma ont utilisé la thérapie standard assignée comme thérapie de transition.
L'étude incluait des patients ayant répondu à au moins 1 traitement antérieur (faible réponse ou mieux) et présentant un statut de performance ECOG (Eastern Cooperative Oncology Group) de 0 ou 1. Les patients présentant une clairance de la créatinine sérique < 45 ml/min, un taux d'aspartate aminotransférase (AST) ou d'alanine aminotransférase (ALT) sériques correspondant à > 2,5 fois la valeur normale supérieure et une fraction d'éjection du ventricule gauche (FEVG) < 45 % ont été exclus de l'étude. Les patients avec un nombre absolu de neutrophiles < 1000/µl et une numération plaquettaire < 75000/μl, chez lesquels < 50 % des cellules nucléées de la moelle osseuse étaient des plasmocytes, ainsi que les patients avec une numération plaquettaire < 50000/μl, chez lesquels ≥50 % des cellules nucléées de la moelle osseuse étaient des plasmocytes, étaient également exclus.
L'âge moyen de la population de l'étude était de 63 ans (plage entre 30 et 83 ans); 40,9 % avaient 65 ans ou plus et 60,9 % étaient des hommes. Le statut de performance ECOG au début de l'étude était de 0 chez 48,2 %, de 1 chez 50,5 % et de 2 chez 0,8 % des patients.
Nonante pour cent des patients étaient réfractaires à un médicament immunomodulateur (IMiD), 74 % étaient réfractaires à un inhibiteur du protéasome (IP) et 95 % étaient réfractaires à un anticorps monoclonal anti-CD38. Soixante-six pour cent étaient triplement réfractaires aux classes (réfractaires à un IP, un IMiD et un anticorps monoclonal anti-CD38).
Les patients ont été randomisés avec un rapport de 2:1 sur un traitement par Abecma (n = 254) ou le traitement standard (n = 132) pour le myélome multiple récidivant et réfractaire. La randomisation était stratifiée selon l'âge, le nombre de traitements antérieurs du myélome et les anomalies cytogénétiques de haut risque. Les patients recevant le traitement standard pouvaient être traités par Abecma en cas de progression confirmée de la maladie.
Les patients randomisés sur Abecma devaient recevoir une chimiothérapie lymphodéplétive composée de cyclophosphamide (300 mg/m2 comme perfusion i. v. une fois par jour pendant 3 jours) et de fludarabine (30 mg/m2 comme perfusion i. v. une fois par jour pendant 3 jours), qui devait être instaurée 5 jours avant la date cible de la perfusion d'Abecma. Entre l'aphérèse et jusqu'à 14 jours avant le début de la chimiothérapie lymphodéplétive, un cycle de traitement anticancéreux par DPd, DVd, IRd, Kd ou EPd (thérapie de transition) était autorisé pour contrôler la maladie.
Parmi les 254 patients randomisés sur Abecma, 249 (98 %) ont reçu une leucaphérèse et 225 (88,6 %) patients ont reçu Abecma. Parmi les 225 patients, 192 (85,3 %) ont reçu une thérapie de transition. Abecma n'a pas été administré chez 29 patients en raison du décès (n = 4), d'événements indésirables (n = 5), de retrait (n = 2), de décision du médecin (n = 7), de la non-conformité aux critères de la chimiothérapie lymphodéplétive (n = 8) ou d'un défaut de fabrication (n = 3).
L'intervalle de doses autorisé était de 150 à 540 x 106 cellules CAR-T positives. La dose médiane effectivement administrée était de 445,3 x 106 cellules CAR-T positives (fourchette: 174,9 à 529,0 x 106 cellules CAR-T positives). Le délai médian entre la leucaphérèse et la disponibilité de la préparation était de 35 jours (fourchette: 24 à 102 jours) et le délai médian entre la leucaphérèse et la perfusion était de 49 jours (fourchette: 34 à 117 jours).
Parmi les 132 patients randomisés sur le traitement standard, 126 (95,5 %) ont reçu un traitement. Six patients ont arrêté l'étude à cause de la progression de la maladie (n = 1), d'un retrait (n = 3) ou d'une décision du médecin (n = 2) sans avoir reçu de traitement. Sur demande du médecin investigateur, les patients recevant un traitement standard ont pu recevoir Abecma lorsque le comité de contrôle indépendant (IRC) avait confirmé une progression de la maladie sur la base des critères de l'International Myeloma Working Group (IMWG) et l'aptitude à la participation à l'étude. Parmi les patients admissibles, 69 (54,8 %) ont reçu une leucaphérèse et 60 (47,6 %) ont reçu Abecma.
Le critère principal pour l'évaluation de l'efficacité était la survie sans progression (PFS), définie selon les critères IMWG Uniform Response Criteria for Multiple Myeloma et évaluée par l'IRC. Les autres critères d'efficacité étaient le taux de réponse global (ORR), la survie globale (OS) et le patient reported outcome (PRO). Dans la population cible (Intent-to-Treat, ITT), la durée de suivi médiane de la randomisation au jour de référence de la collecte des données était de 18,6 mois. Le tableau 3 présente un résumé de l'analyse intermédiaire des résultats d'efficacité.
Dans le bras Abecma, la durée médiane de réponse (DOR) chez les patients avec réponse partielle (partial response, PR) ou mieux était de 13,9 mois (IC à 95 %: 11,2; 17,8). Chez les patients ayant atteint une réponse complète (complete response, CR) ou mieux, la durée médiane de réponse (duration of response, DOR) était de 20 mois (IC à 95 %: 15,8; 24,3).
Tableau 3: Résumé des résultats d'efficacité sur la base de KarMMa-3 (Intent-to-Treat-Population)
|
|
Bras Abecma
(n = 254)
|
Bras de traitement standard (n = 132)
| |
Survie sans progression (PFS)
| |
Nombre d'événements, n (%)
|
149 (58,7)
|
93 (70,5)
| |
Médiane, mois [IC à 95 %] a
|
13,3 [11,8; 16,1]
|
4,4 [3,4; 5,9]
| |
Hazard ratio [IC à 95 %]b
|
0,49 [0,38; 0,65]
| |
Valeur de p unilatéralec
|
< 0,0001
| |
Taux de réponse global (ORR)
| |
n (%)
|
181 (71,3)
|
55 (41,7)
| |
IC à 95 (%)d
|
(65,7; 76,8)
|
(33,3; 50,1)
| |
Valeur de p unilatéralee
|
< 0,0001
| |
CR ou mieux (sCR+CR)
|
98 (38,5)
|
7 (5,3)
| |
sCR
|
90 (35,4)
|
6 (4,5)
| |
CR
|
8 (3,1)
|
1 (0,8)
| |
VGPR
|
55 (21,7)
|
13 (9,8)
| |
PR
|
28 (11,0)
|
35 (26,5)
| |
MRD négative par NGS et ≥ CR
| |
Taux de négativité de la MRD, n (%)f
|
51 (20,1)
|
1 (0,8)
| |
IC à 95 (%)d
|
(15,2; 25,0)
|
(0,0; 2,2)
|
IC = intervalle de confiance; CR = réponse complète; MRD = minimal residual disease; PR = réponse partielle; sCR = réponse complète stricte; VGPR = très bonne réponse partielle.
a Estimation de Kaplan-Meier.
b Basé sur le Cox proportional hazards model stratifié univarié.
c Valeur de p unilatérale basée sur le test du log-rank stratifié.
d Intervalle de confiance bilatéral de Forest.
e Valeur de p unilatérale basée sur le test de Cochran-Mantel-Haenszel (CMH) stratifié.
f La négativité de la MRD était définie comme le pourcentage de patients de la population en ITT atteignant une CR ou CR stricte et étant MRD négatifs à un moment quelconque dans les trois mois avant l'atteinte de la CR ou de la CR stricte jusqu'à la progression ou le décès. Basé sur une valeur seuil de 10-5 en utilisant ClonoSEQ, un test de séquençage nouvelle génération (NGS).
Au moment de l'analyse PFS finale (date de référence de la collecte des données: 28.04.2023) avec une durée médiane de suivi de 30,9 mois, la PFS médiane pour Abecma était de 13,8 mois (IC à 95 %: 11,8; 16,1) comparé à 4,4 mois pour le traitement standard (IC à 95 %: 3,4; 5,8); HR = 0,49 (IC à 95 %: 0,38; 0,63), ce qui concorde avec les résultats de l'analyse intermédiaire.
74 % des événements OS planifiés étaient atteints lors de l'analyse finale de la PFS. Les patients ayant reçu le traitement standard pouvaient recevoir Abecma en cas de progression confirmée de la maladie. Les données OS sont donc influencées par les 74 (56,1 %) patients du bras de traitement standard ayant reçu Abecma comme traitement de suivi. L'OS médiane pour Abecma était de 41,4 mois (IC à 95 %: 30,9; NA) contre 37,9 mois pour le traitement standard (IC à 95 %: 23,4; NA); HR = 1,01 (IC à 95 %: 0,73; 1,40).
Patient reported outcome (PRO)
Analyses descriptives
Trois mesures des PRO (EORTC QLQ-C30, EORTC QLQ-MY20, EQ-5D-5L) ont été réalisées au début de l'étude (sélection), tous les mois jusqu'au mois 24 et tous les trois mois ensuite. Parmi les patients ayant répondu au questionnaire (Abecma n = 211; traitement standard n = 108), des tendances à l'amélioration et des différences au niveau des variations de la valeur moyenne par rapport à la valeur de référence, incluant la fatigue, la douleur, la capacité fonctionnelle physique et le statut GHS/QoL, ont été observées chez les patients traités par Abecma comparé aux patients recevant le traitement standard (voir figure 1).
Figure 1: EORTC QLQ-C30 - variations de la valeur moyenne aux mois 3, 6, 9, 12 et 15 par rapport à la valeur de référence pour les domaines fatigue, douleur, capacité fonctionnelle physique et GHS/QoL dans l'étude KarMMa-3
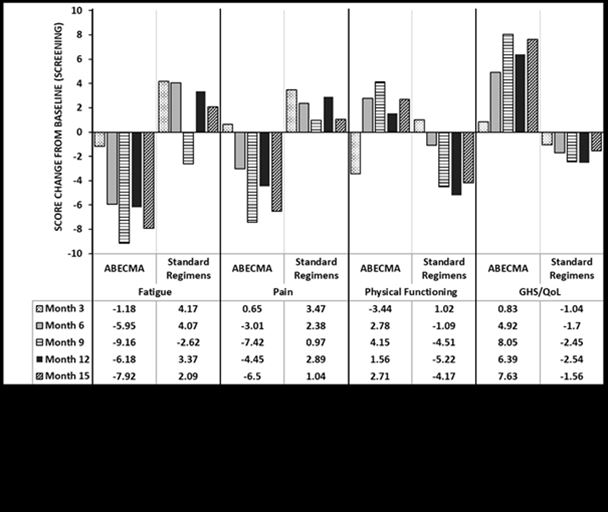
Analyse longitudinale de données avec contraintes (Constrained longitudinal data analysis (cLDA))
En comparant les variations moyennes des moindres carrés (Least Square - LS) entre la valeur de référence et le 25e mois à l'aide de la cLDA, les valeurs moyennes de variation des LS étaient en faveur des patients traités par Abecma pour la plupart des domaines des trois mesures PRO avec des tailles d'effet significatives (Hedge's g > 0,2) (voir figure 2).
Figure 2: Forest plot des différences entre les groupes pour l'ensemble de la cLDA concernant la variation moyenne des LS par rapport à la valeur de référence selon les groupes de traitement a, b, c dans l'étude KarMMa-3 (Abecma n = 211; traitement standard n = 108)
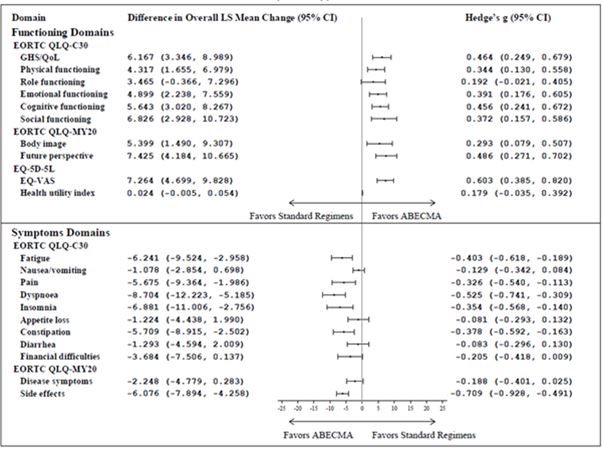
IC = intervalle de confiance; EORTC QLQ-C30 = European Organization for Research and Treatment of Cancer Quality of Life-of-Core 30 Questionnaire; EORTC QLQ-MY20 = European Organization for Research and Treatment of Cancer Quality of Life-of-Questionnaire Multiple Myeloma Module; EQ-VAS = Visual Analogue Scale; GHS = Global health status; LS = Least square; QoL = Quality of Life.
a Selon les directives de Cohen (1998, 1992) pour l'interprétation des valeurs g de Hedges, 0,20 indique de petits effets, 0,50 des effets moyens et 0,80 de grands effets.
b Domaines d'intérêt principaux: EORTC QLQ-C30 domaines de l'état de santé global/qualité de vie (QoL), fonction physique, fonction cognitive, fatigue et douleur; EORTC QLQ-MY20 domaines des symptômes de la maladie et effets indésirables du traitement; EQ-5D-5L indice de l'état de santé et EQ-VAS. Les autres domaines sont considérés comme secondaires.
c L'analyse ne comprenait pas d'ajustement en fonction des multiplicateurs.
Analyses PRO du temps écoulé avant l'événement (PRO-Time-to-Event)
Dans l'étude KarMMa-3, le temps écoulé avant l'événement (Time-to-Event) a été évalué à l'aide de l'estimation de Kaplan-Meier. L'analyse a montré le temps écoulé jusqu'à la confirmation d'une amélioration cliniquement significative ou une dégradation des domaines d'intérêt PRO chez les patients traités par Abecma versus ceux recevant le traitement standard. La survenue d'une dégradation ou d'une amélioration était définie comme une variation par rapport à la valeur de référence sur la base des valeurs seuils validées et confirmée par une évaluation consécutive ≥84 jours après l'apparition. Elle était indiquée sous forme de Hazard Ratio (HR); un HR<1,0 pour la dégradation et un HR>1,0 pour l'amélioration étaient en faveur d'Abecma. Chez les patients traités par Abecma, le temps écoulé jusqu'à une dégradation confirmée était significativement prolongé pour la plupart des domaines des trois PRO (HR>1,0). Chez les patients traités par Abecma, le temps écoulé jusqu'à une amélioration confirmée était également plus court pour la plupart des domaines des mesures PRO (HR>1,0).
KarMMa
KarMMa est une étude multicentrique ouverte, à un bras, visant à évaluer l'efficacité et la sécurité d'Abecma chez des patients adultes atteints d'un myélome multiple récidivant et réfractaire, qui ont reçu au moins trois traitements antérieurs contre le myélome, dont un immunomodulateur, un inhibiteur de protéasome et un anticorps anti-CD38.
L'étude comprenait un prétraitement (dépistage, leucaphérèse et thérapie de transition [si nécessaire]), un traitement (chimiothérapie lymphodéplétive [CLD] et perfusion d'Abecma) et un suivi (continu) pendant au moins 24 mois après la perfusion d'Abecma ou jusqu'à la progression documentée de la maladie, selon la période la plus longue. La période de CLD consistait en un cycle de 3 jours de cyclophosphamide (300 mg/m2 en perfusion i.v. quotidienne pendant 3 jours) et de fludarabine (30 mg/m2 en perfusion i.v. quotidienne pendant 3 jours) commençant 5 jours avant la date de perfusion prévue d'Abecma.
Les patients devaient rester à l'hôpital pendant 14 jours après la perfusion d'Abecma; la survenue potentielle d'un CRS et d'une neurotoxicité a été surveillée et les patients ont été traités en conséquence le cas échéant.
La population traitée par Abecma a été fortement réfractaire aux traitements précédents contre le myélome: 84,4 % des participants à l'étude étaient triplement réfractaires (c'est-à-dire réfractaires à un agent immunomodulateur, à un inhibiteur de protéase et à un anticorps anti-CD38).
Les doses cibles dans l'étude clinique étaient de 150, 300 ou 450 x 106 cellules CAR-T positives par perfusion. La plage posologique autorisée était de 150 à 540 x 106 cellules CAR-T positives. Le tableau 4 ci-dessous présente les doses cibles utilisées dans l'essai clinique, basées sur le nombre total de cellules CAR-T positives, et la plage correspondante de doses réellement administrées, définies comme cellules T viables CAR-positives.
Tableau 4: Dose totale de cellules CAR-T positives avec la plage posologique correspondante de cellules T viables CAR positives (x106) – étude KarMMa
|
Dose cible basée sur le nombre total de cellules CAR-T positives, incluant les cellules viables et non viables (x106)
|
Cellules T viables CAR-positives (x106)
(min, max)
| |
150
|
133 à 181
| |
300
|
254 à 299
| |
450
|
307 à 485
|
Sur 140 patients ayant subi une leucaphérèse, 128 ont reçu de l'Abecma. Un des 140 patients n'a pas reçu le produit en raison de défauts de fabrication. 11 autres patients n'ont pas été traités par Abecma sur décision du médecin (n = 3), en raison de l'abandon du patient (n = 4), d'événements indésirables (n = 1), de la progression de la maladie (n = 1) ou du décès (n = 2) avant de recevoir Abecma.
L'âge médian de la population étudiée était de 60,5 ans (plage: 33 à 78 ans); 35 % avaient au moins 65 ans et 59 % étaient des hommes. Le statut de performance de l'Eastern Cooperative Oncology Group (ECOG) au départ était de 0 chez 45 % des patients, de 1 chez 53 % des patients et de 2 chez 2 % des patients.
La plupart des patients (87,5 %) traités par Abecma ont reçu un traitement de transition pour contrôler leur myélome multiple pendant le processus de fabrication. Le délai médian entre la leucaphérèse et la disponibilité du produit a été de 32 jours (plage: entre 24 et 55 jours) et le temps médian entre la leucaphérèse et la perfusion de 40 jours (plage: entre 33 et 79 jours). La dose médiane réelle reçue dans tous les niveaux de dose cible a été de 315,3 x 106 cellules CAR-positives (plage: 150,5 à 518,4).
L'efficacité a été déterminée sur la base du taux de réponse global (overall response rate, ORR), du taux de réponse complète (complete response, CR) et de la durée de la réponse (duration of response, DOR) par un comité de contrôle indépendant (Independent Review Committee, IRC).
Un autre critère d'évaluation était la maladie résiduelle minimale (minimal residual disease, MRD), évaluée au moyen d'un séquençage de nouvelle génération (next generation sequencing, NGS)
Les résultats d'efficacité pour les niveaux de dose cibles de 150 à 450 x 106 cellules CAR-T positives sont présentés dans le tableau 4.
Dans l'analyse principale, portant sur la population traitée, l'ORR a été de 73,4 % (IC à 95 %: 65,8; 81,1) et le taux de réponse complète (CR) de 32,87 % (IC à 95 %: 24,7; 40,9). Pour les patients présentant une réponse partielle (partial response, PR) ou mieux, la durée médiane de la DOR a été de 10,6 mois (IC à 95 %: 8,0, 11,4). Chez les patients présentant une CR ou mieux, la durée médiane de la DOR a été de 23,3 mois (IC à 95 %: 11,4; 23,3). La durée de suivi médiane a été de 15,4 mois pour tous les patients traités (plage: entre 0,2 et 24,2).
Sur 140 patients de la population incluse, l'ORR a été de 67,1 % et la CR de 30 %. D'autres résultats d'efficacité pour la population incluse étaient conformes à ceux de la population traitée.
Tableau 5: Résumé des résultats d'efficacité sur la base de l'étude KarMMa
|
|
Population incluse
(n = 140)
|
Population traitée
Dose cible d'Abecma (cellules CAR-T positives)
| |
[150 x 106]
(n = 4)
|
[300 x 106]
(n = 70)
|
[450 x 106]
(n = 54)
|
[150 bis 450 x 106]
(n = 128)
| |
Taux de réponse global (SCR + CR + VGPR + PR), n (%)
|
94 (67,1)
|
2 (50,0)
|
48 (68,6)
|
44 (81,5)
|
94 (73,4)
| |
IC à 95 %a
|
59,4; 74,9
|
6,8; 93,2
|
56,4; 79,1
|
68,6; 90,7
|
65,8; 81,1
| |
CR ou mieux, n (%)
|
42 (30,0)
|
1 (25,0)
|
20 (28,6)
|
21 (38,9)
|
42 (32,8)
| |
IC à 95 %a
|
22,4; 37,6
|
0,6; 80,6
|
18,4; 40,6
|
25,9; 53,1
|
24,7; 40,9
| |
VGPR ou mieux, n (%)
|
68 (48,6)
|
2 (50,0)
|
31 (44,3)
|
35 (64,8)
|
68 (53,1)
| |
IC à 95 %a
|
40,3; 56,9
|
6,8; 93,2
|
32,4; 56,7
|
50,6; 77,3
|
44,5; 61,8
| |
Patients avec statut MRD négatifb et ≥ CR, n
|
|
1
|
17
|
15
|
33
| |
Sur la base de la population traitée, %
|
─
|
25,0
|
24,3
|
27,8
|
25,8
| |
IC à 95 %a
|
|
0,6; 80,6
|
14,8; 36,0
|
16,5; 41,6
|
18,5; 34,3
| |
Sur la base des participants à l'étude avec ≥ CR, %
|
|
100
|
85,0
|
71,4
|
78,6
| |
IC à 95 %a
|
|
2,5; 100,0
|
62,1; 96,8
|
47,8; 88,7
|
63,2; 89,7
| |
Temps jusqu'à la réponsec, n
|
94
|
2
|
48
|
44
|
94
| |
Médiane (mois)
|
1
|
1
|
1
|
1
|
1
| |
min., max.
|
0,5; 8,8
|
1,0; 1,0
|
0,5; 8,8
|
0,9; 2,0
|
0,5; 8,8
| |
Durée de la réponsec (PR ou mieux), n
|
94
|
2
|
48
|
44
|
94
| |
Médianed (mois)
|
10,6
|
13,0
|
8,5
|
11,3
|
10,6
| |
IC à 95 %a
|
8,0; 11,4
|
2,8; 23,3
|
5,4; 10,9
|
10,3; NE
|
8,0; 11,4
| |
Durée de la réponse (CR ou mieux), n
|
42
|
1
|
20
|
21
|
42
| |
Médianed (mois)
|
23,3
|
23,3
|
16,2
|
NE
|
23,3
| |
IC à 95 %a
|
11,4; 23,3
|
NE; NE
|
8,0; NE
|
11,4; NE
|
11,4; 23,3
| |
Survie globalee (OS), mois, n
|
140
|
4
|
70
|
54
|
128
| |
Médiane (mois)
|
21,4
|
18,2
|
NE
|
NE
|
NE
| |
IC à 95 %a
|
19,3; NE
|
9,4; NE
|
18,0; NE
|
NE; NE
|
18,9; NE
| |
Taux sans événement à 6 mois, %
|
87,4
|
100
|
89,6
|
86,9
|
88,8
| |
Taux sans événement à 12 mois, %
|
75,8
|
75,0
|
78,5
|
77,3
|
77,9
|
CAR = récepteur antigénique chimérique; IC = intervalle de confiance; CR = complete response (réponse complète); Max = maximum; Min = minimum; MRD = Minimal Residual Disease (maladie résiduelle minimale); NE = non évaluable; PR = partial response (réponse partielle); sCR = stringent complete response (réponse complète stricte); VGPR = very good partial response (très bonne réponse partielle).
a Pour le total («population traitée» et «population enregistrée»): IC de Forest; pour des niveaux de dose cibles individuels: IC exact selon Clopper-Pearson.
b Sur la base d'une valeur seuil de 10-5 en utilisant un test de séquençage de nouvelle génération.
c La réponse est définie comme l'atteinte d'une sCR, d'une CR, d'une VGPR ou d'une PR selon les critères IMWG.
d La médiane est basée sur l'estimation Kaplan-Meier.
e L'OS était définie comme la période allant de la date de la leucaphérèse (population enregistrée) ou de la perfusion d'Abecma (population traitée) jusqu'au décès, toutes causes confondues.
Remarque: La dose cible est de 450 × 106 cellules CAR-T positives dans une plage de 150 à 540 × 106 cellules CAR-T positives. La dose de 150 × 106 cellules CAR-T positives ne fait pas partie de la fourchette de doses approuvées.
Qualité de vie liée à la santé (health-related Quality of life, HRQoL)
La HRQoL a été évaluée à l'aide du questionnaire C30 sur la qualité de vie (EORTC-QLQ-C30) et du module sur le myélome multiple (EORTC-QLQ-MY20) de l'Association européenne pour la recherche et le traitement des cancers (European Organisation for Research and Treatment of Cancer EORTC) en se concentrant principalement sur la fatigue, les douleurs, la fonction physique, la fonction cognitive et l'état de santé général/la qualité de vie, les effets secondaires et les symptômes de la maladie comme sous-échelles. Selon les résultats des données obtenues 10 mois après la perfusion d'Abecma, les patients traités par Abecma ont connu des améliorations cliniquement significatives des scores de fatigue, des douleurs, du fonctionnement physique et de l'état de santé général peu après la perfusion, qui sont devenues statistiquement significatives (p < 0,05) à plusieurs moments du mois 3 au mois 9 après le traitement, sans détérioration du fonctionnement cognitif ni aggravation des symptômes de la maladie ou des effets secondaires. Pour la plupart des critères d'évaluation et des points d'observation, un pourcentage plus important de patients a rapporté une amélioration cliniquement significative qu'une détérioration.
Étude de preuves en conditions réelles (real world, RW)
L'étude de preuves RW (étude NDS-MM-003) était une étude d'observation rétrospective, qui a recueilli en conditions réelles des données sur des patients atteints de myélome multiple récidivant et réfractaire (RRMM) qui avaient reçu au moins trois traitements antérieurs, dont un agent immunomodulateur, un IP et un anticorps anti-CD38. Dans ce groupe, on a sélectionné les patients qui répondaient aux critères de sélection les plus proches possibles de ceux de l'étude KarMMa (c'est-à-dire l'absence de comorbidités et l'initiation d'un nouveau traitement après être devenu réfractaire au dernier traitement anti-myélome). L'ORR et la survie globale (OS) ont été évalués pour les deux groupes en utilisant la méthode du Propensity Score pour évaluer l'efficacité comparative des patients traités avec les thérapies disponibles par rapport à Abecma dans l'essai KarMMa. Le risque relatif d'ORR a été de 2,4 (IC à 95 %: 1,7; 3,3) p < 0,0001. Le hazard ratio de l'OS a été de 0,41 (IC 95 % 0,26, 0,65), favorisant significativement la cohorte traitée par Abecma par rapport à la cohorte RRMM correspondante traitée par les thérapies disponibles (p = 0,0002).
Sécurité et efficacité chez les patients âgés
Dans les études cliniques sur Abecma, 163 patients (39,9 %) étaient âgés d'au moins 65 ans et 17 d'au moins 75 ans (4,2 %). Aucune différence cliniquement significative n'a été observée concernant la sécurité ou l'efficacité d'Abecma entre ces patients et les patients âgés de moins de 65 ans.
PharmacocinétiqueAbsorption
Les informations ne sont pas pertinentes pour Abecma (un produit à base de cellules CAR-T).
Distribution
Les informations ne sont pas pertinentes pour Abecma (un produit à base de cellules CAR-T).
Métabolisme
Les informations ne sont pas pertinentes pour Abecma (un produit à base de cellules CAR-T).
Élimination
Les informations ne sont pas pertinentes pour Abecma (un produit à base de cellules CAR-T).
Pharmacocinétique
Après la perfusion d'Abecma, les cellules CAR-T positives se multiplient et présentent une expansion multilogarithmique rapide, suivie d'une diminution biexponentielle. Le temps médian d'expansion maximale dans le sang périphérique (tmax) est atteint 11 jours après la perfusion. Abecma peut persister dans le sang périphérique jusqu'à 1 an après la perfusion. Un résumé des tmax, ASC0-28 jours et Cmax dans les études KarMMa et KarMMa-3 est présenté dans le tableau 6.
Tableau 6: Paramètres pharmacocinétiques d'Abecma chez les patients atteints de myélome multiple récidivant/réfractaire
|
Paramètres pharmacocinétiques
|
Statistiques résumées
|
Étude KarMMa
Total [150 à 450 x 106]
Cellules CAR-T positives
(quantifiées par qPCR)a
|
Étude KarMMa-3
Total [150 à 450 x 106]
Cellules CAR-T positives
(quantifiées par ddPCR)b
| |
Tmax (jours)
|
Médiane (plage)
|
11 (7-30)
n=127
|
11 (2-31)
n=220
| |
Cmax (copies/µg)
|
Moyenne géométrique (CV géométrique %)
|
231 278 (178)
n=127
|
115 701 (223)
n=220
| |
ASC0-28jours
(jours*copies/µg)
|
Moyenne géométrique (CV géométrique %)
|
2 860 340 (197)
n=125
|
1 084 349 (231)
n=218
|
ASC0-28jours = aire sous la courbe de la concentration du transgène depuis l'administration de la dose jusqu'à 28 jours après la perfusion; Cmax = concentration maximale du transgène; ddPCR = droplet digital polymerase chain reaction; qPCR = quantitative polymerase chain reaction; PK = pharmacocinétique;
Tmax = temps de la concentration transgène maximale observée.
a Les paramètres PK de l'étude KarMMa ont été établis à partir du décours temporel des copies transgène par microgramme d'ADN extrait des cellules CD3+ triées et quantifié par quantitative polymerase chain reaction (qPCR).
b Les paramètres PK de l'étude KarMMa-3 ont été établis à partir du décours temporel des copies transgène par microgramme d'ADN extrait du sang complet et quantifié par droplet digital PCR (ddPCR).
Note: les paramètres PK ne doivent pas être directement comparés entre KarMMa et KarMMa-3, puisque différents tests PK ont été utilisés.
Les concentrations de transgènes Abecma ont été positivement associées à une réponse tumorale objective (réponse partielle ou mieux). Dans KarMMa, les valeurs de Cmax médianes chez les répondeurs (n = 93) ont été environ 4,5 fois supérieures aux valeurs correspondantes chez les non-répondeurs (n = 34). L'ASC0-28jours médiane chez les répondeurs (n = 93) était environ 5,5 fois supérieure à celle des non-répondeurs (n = 32). Dans KarMMa-3, les valeurs de Cmax médianes chez les répondeurs (n = 180) ont été environ 5,4 fois supérieures aux valeurs correspondantes chez les non-répondeurs (n = 40). L'ASC0-28jours médiane chez les répondeurs (n = 180) était environ 5,5 fois supérieure à celle des non-répondeurs (n = 38).
Utilisation du tocilizumab ou du siltuximab et de corticostéroïdes
Certains patients ont eu besoin de tocilizumab ou de siltuximab et/ou de corticostéroïdes pour le traitement d'un SLC. Abecma peut continuer son expansion et persister après l'administration de tocilizumab, de siltuximab ou de corticostéroïdes (voir rubrique «Mises en garde et précautions»).
Dans l'étude KarMMa, les patients atteints de SLC traités par le tocilizumab présentaient des niveaux d'expansion cellulaire d'Abecma plus élevés, comme le montrent les valeurs médianes de Cmax (n = 66) et d'ASC0-28jours (n = 65) respectivement 1,4 et 1,6 fois plus élevées, par rapport aux patients qui n'ont pas reçu de tocilizumab (n = 61 pour la Cmax et n = 60 pour l'ASC0-28jours).
Les patients atteints de SLC traités par corticostéroïdes présentaient des niveaux d'expansion cellulaire d'Abecma plus élevés, comme le montrent les valeurs médianes de Cmax (n = 18) et d'ASC0-28jours (n = 18) respectivement 1,7 et 2,2 fois plus élevées, par rapport aux patients ne recevant pas de corticostéroïdes (n = 109 pour la Cmax et n = 107 pour l'ASC0-28jours).
Dans l'étude KarMMa-3, les patients atteints de SLC traités par le tocilizumab ou le siltuximab présentaient des niveaux d'expansion cellulaire d'Abecma plus élevés, comme le montrent les valeurs médianes de Cmax (n = 156) et d'ASC0-28jours (n = 155) respectivement 3,1 et 2,9 fois plus élevées, par rapport aux patients qui n'ont pas reçu de tocilizumab ni de siltuximab (n = 64 pour la Cmax et n 63 pour l'ASC0-28jours).
Les patients atteints de SLC traités par corticostéroïdes présentaient des niveaux d'expansion cellulaire d'Abecma plus élevés, comme le montrent les valeurs médianes de Cmax (n = 60) et d'ASC0-28jours (n = 60) respectivement 2,3 et 2,4 fois plus élevées, par rapport aux patients ne recevant pas de corticostéroïdes (n = 160 pour la Cmax et n = 158 pour l'ASC0-28jours).
Cinétique pour certains groupes de patients
Troubles de la fonction hépatique
Aucune étude n'a été réalisée sur les troubles de la fonction hépatique avec Abecma.
Troubles de la fonction rénale
Aucune étude n'a été réalisée sur les troubles de la fonction rénale avec Abecma.
Patients âgés
L'âge (entre 30 et 81 ans) n'a pas eu d'influence significative sur les paramètres d'expansion.
Enfants et adolescents
La pharmacocinétique d'Abecma chez les patients de moins de 18 ans n'a pas été étudiée.
Autres facteurs intrinsèques
Le sexe, l'ethnie et l'origine ethnique n'ont pas d'influence significative sur les paramètres d'expansion d'Abecma. Les patients ayant un poids corporel faible ont présenté une expansion plus élevée. En raison de la grande variabilité de l'expansion cellulaire pharmacocinétique, l'effet global du poids sur la pharmacocinétique d'Abecma n'est pas considéré comme cliniquement pertinent.
Données précliniquesEn raison de la nature de ce produit, aucune étude classique de toxicité, de fertilité et de pharmacocinétique n'a été réalisée avec Abecma.
Les tests de génotoxicité et les études de carcinogénicité chez les rongeurs ne sont pas adaptés pour évaluer le risque de mutagenèse d'insertion pour les produits de traitement cellulaire génétiquement modifiés. Il n'y a pas d'autres modèles d'animaux adaptés.
Les études in vitro d'expansion avec des cellules CAR-T positives (Abecma) de donneurs sains et de patients n'ont révélé aucune transformation ni aucune immortalisation de lymphocytes T. L'analyse du site d'insertion génomique du vecteur lentiviral a été réalisée à partir des échantillons d'Abecma, y compris ceux des patients. Il n'y a pas de preuves d'une intégration privilégiée à proximité de gènes dangereux ou d'une croissance préférentielle de cellules dans lesquelles l'intégration a eu lieu à un endroit dangereux.
Remarques particulièresIncompatibilités
Aucune étude de compatibilité n'ayant été réalisée, ce médicament ne doit pas être mélangé à d'autres médicaments.
Stabilité
Ce médicament ne doit pas être utilisé au-delà de la date de péremption indiquée sur l'étiquette du produit («EXP»).
Le volume prévu pour la perfusion dans chaque poche doit être entièrement perfusé dans l'heure qui suit le début de la décongélation.
Remarques particulières concernant le stockage
Stocker congelé dans des sacs de cryoconservation en éthylène-acétate de vinyle dans un conteneur pour le stockage cryogénique dans la phase vapeur de l'azote liquide (≤ -130 °C).
Tenir hors de la portée des enfants.
Remarques concernant la manipulation
Voir rubrique («Posologie/Mode d'emploi»).
Précautions particulières pour la manipulation et l'élimination
Abecma contient des cellules sanguines humaines génétiquement modifiées. Il est préparé à partir de sang autologue du patient, qui est obtenu par leucaphérèse. Le matériel de leucaphérèse du patient et Abecma peuvent présenter un risque de transmission de virus infectieux aux professionnels de santé, qui manipulent le produit. Par conséquent, les professionnels de santé doivent prendre les précautions appropriées (port de gants et de lunettes) lorsqu'ils manipulent le matériel de leucaphérèse ou Abecma afin d'éviter une éventuelle transmission de l'infection.
Les surfaces de travail, qui ont été ou pourraient avoir été en contact avec Abecma, doivent être décontaminées avec un désinfectant approprié. Les médicaments non utilisés ou les matériaux qui sont entrés en contact avec Abecma (déchets solides et liquides) doivent être manipulés et éliminés comme des déchets potentiellement infectieux, conformément aux directives locales en matière de biosécurité.
Numéro d’autorisation67575 (Swissmedic)
PrésentationLe produit fini se compose d'une ou plusieurs poches de perfusion, contenant une dispersion cellulaire totale de 260 à 500 × 106 cellules T viables CAR-positives. Chaque poche de perfusion contient 10-30 ml (poche de 50 ml), 30-70 ml (poche de 250 ml) ou 55-100 ml (poche de 500 ml) de dispersion cellulaire. [A]
Chaque poche de perfusion d'Abecma est emballée séparément dans une cassette métallique. Abecma est stocké dans la phase vapeur d'azote liquide et livré dans un récipient d'expédition contenant de la vapeur d'azote liquide.
Un certificat RFI est joint au conteneur d'expédition.
Titulaire de l’autorisationBristol-Myers Squibb SA, Steinhausen
Mise à jour de l’informationMars 2025.
|


