Propriétés/EffetsCode ATC
L04AB01
Nepexto est un biosimilaire.
Mécanisme d'action
L'étanercept est une protéine humaine de fusion du récepteur p75 Fc du facteur nécrosant des tumeurs (TNF); il est produit par la méthode des recombinants d'ADN et exprimé dans des cellules ovariennes de hamster chinois (CHO). L'étanercept est un dimère d'une protéine chimère qui a été obtenue génétiquement en fusionnant le domaine de liaison extracellulaire du récepteur 2 humain du facteur nécrosant des tumeurs (TNFR2/p75) au domaine Fc de l'IgG1 humaine. Ce fragment Fc contient les régions charnière, CH2 et CH3, mais pas la région CH1 de l'IgG1. L'étanercept est constitué de 934 acides aminés et son poids moléculaire est d'environ 150 kilodaltons. L'activité de l'étanercept est déterminée en mesurant sa capacité à neutraliser l'inhibition de la croissance des cellules A375 médiée par le TNF-α. L'activité spécifique de l'étanercept est de 1.7×106 unités/mg.
Pharmacodynamique
Le facteur nécrosant des tumeurs (TNF) est une cytokine dominante dans le processus inflammatoire de la polyarthrite rhumatoïde (PR). Des taux élevés de TNF sont également retrouvés dans les membranes synoviales et les plaques de psoriasis des patients atteints d'arthrite psoriasique, et dans le sérum et le tissu synovial des patients atteints de spondylarthrite ankylosante.
Dans le psoriasis en plaques, la migration des cellules de l'inflammation, entre autres les lymphocytes T, induit une concentration accrue du taux de TNF dans les lésions psoriasiques en comparaison avec les régions de la peau non touchées.
L'étanercept est un inhibiteur compétitif de la liaison du TNF à ses récepteurs de surface, inhibant ainsi l'activité biologique du TNF.
Le TNF et la lymphotoxine sont des cytokines pro-inflammatoires qui lient deux récepteurs distincts à la surface des cellules: les récepteurs du facteur nécrosant des tumeurs (TNFR) de 55 kilodaltons (p55) et de 75 kilodaltons (p75). Ces deux TNFR existent naturellement sous des formes membranaires et solubles. On pense que les TNFR solubles régulent l'activité biologique du TNF.
Le TNF et la lymphotoxine existent principalement sous forme d'homotrimères, leur activité biologique étant dépendante de la réticulation des TNFR à la surface des cellules. Les récepteurs dimères solubles tels que l'étanercept présentent une affinité plus marquée pour le TNF que les récepteurs monomères et sont ainsi des inhibiteurs compétitifs plus puissants de la liaison du TNF à ses récepteurs cellulaires. De plus, l'utilisation d'une région Fc d'immunoglobuline en tant qu'élément de liaison dans la construction d'un récepteur dimère confère à la molécule une demi-vie sérique plus longue.
L'étanercept peut également moduler les réponses biologiques contrôlées par d'autres molécules de la cascade inflammatoire (par ex. cytokines, adhésines ou protéinases) dont l'activité est induite ou régulée par le TNF.
Efficacité clinique
Cette rubrique présente les données issues de quatre études contrôlées randomisées et de deux études supplémentaires en ouvert (V et VI) chez l'adulte atteint de polyarthrite rhumatoïde, de trois études dans l'arthrite juvénile idiopathique, d'une étude chez l'adulte atteint d'arthrite psoriasique, de quatre études chez l'adulte atteint de spondylarthrite ankylosante, d'une étude chez des patients pédiatriques atteints de psoriasis en plaques et de quatre études en ouvert chez l'adulte atteint de psoriasis en plaques.
Polyarthrite rhumatoïde de l'adulte
La sécurité et l'efficacité de l'étanercept ont été évaluées chez 2'680 patients atteints de polyarthrite rhumatoïde active (PR).
La sécurité et l'efficacité de l'étanercept ont été évaluées dans quatre études randomisées, en double aveugle, contrôlées contre placebo et deux études supplémentaires (V et VI).
L'étude I a évalué 234 patients, âgés de ≥18 ans, ayant une polyarthrite rhumatoïde active, qui ne répondaient pas au moins à un, et au plus à quatre traitements de fond (DMARD, p.ex.: hydroxychloroquine, sels d'or injectables ou per os, méthotrexate, azathioprine, D-pénicillamine, sulfasalazine). Ces patients avaient une polyarthrite rhumatoïde active définie par ≥12 articulations douloureuses, ≥10 articulations gonflées et l'un des critères suivants: VS ≥28 mm/h, CRP >2.0 mg/dl ou raideur matinale ≥45 min. Des doses de 10 mg ou 25 mg d'étanercept ou un placebo ont été administrés par voie sous-cutanée 2x par semaine pendant 6 mois consécutifs.
Les résultats des études contrôlées ont été exprimés en pourcentage d'amélioration de la PR, en utilisant les critères de réponse de l'American College of Rheumatology (ACR). Le critère principal d'évaluation était l'obtention d'une réponse ACR 20 à 3 mois. Par définition, une réponse ACR 20 est obtenue si le patient a une amélioration de 20% du nombre d'articulations gonflées et du nombre d'articulations douloureuses, associée à ≥20% d'amélioration d'au moins trois des 5 critères suivants: (1) évaluation de la douleur par le patient, (2) évaluation globale de la maladie par le patient, (3) évaluation globale de la maladie par le médecin, (4) évaluation de la limitation fonctionnelle par le patient, et (5) réaction de phase aiguë (VS ou CRP). Les réponses ACR 50 et 70 sont définies selon les mêmes critères, avec respectivement une amélioration de 50% et de 70%.
Les réponses ACR 20 et ACR 50 étaient supérieures chez les patients traités par étanercept par rapport au placebo à 3 et 6 mois (ACR 20: étanercept 62% et 59%, placebo 23% et 11% respectivement à 3 et 6 mois; ACR 50: étanercept 41% et 40%, placebo 8% et 5% respectivement à 3 et 6 mois; p<0.01 étanercept vs placebo à tous les moments de mesure pour les réponses ACR 20 et ACR 50).
Environ 15% des patients recevant l'étanercept ont obtenu une réponse ACR 70 à 3 mois et à 6 mois, comparativement à moins de 5% des patients sous placebo.
Parmi les patients recevant de l'étanercept, les améliorations cliniques ont généralement débuté 1 à 2 semaines après l'initiation du traitement, et ont été quasiment toujours obtenues dans les 3 mois. Une réponse dose-dépendante a été observée; les résultats avec 10 mg étaient intermédiaires entre le placebo et 25 mg. L'étanercept était significativement supérieur au placebo sur tous les items des critères ACR, ainsi que sur les autres mesures d'activité de la polyarthrite rhumatoïde non compris dans ces critères de réponse ACR, comme la durée de la raideur matinale. L'échelle HAQ (Health Assessment Questionnaire), incluant le handicap, l'activité, l'état mental, l'état général et l'état des fonctions articulaires, a été évaluée tous les 3 mois pendant l'étude. Tous les domaines de l'échelle HAQ ont été améliorés chez les patients traités par éternacept comparés aux patients sous placebo à 3 et 6 mois.
Après l'arrêt de l'étanercept, les symptômes d'arthrite sont généralement réapparus au cours du mois suivant. Selon les résultats des études en ouvert, la reprise du traitement par étanercept après des arrêts allant jusqu'à 24 mois a entrainé la même amplitude de réponse que chez les patients recevant l'étanercept sans interruption de traitement. Des réponses durables ont été observées chez les patients recevant l'étanercept sans interruption jusqu'à 10 ans dans les études d'extension en ouvert.
L'efficacité de l'étanercept a été comparée avec le méthotrexate administré par voie orale dans une étude randomisée, contrôlée contre traitement actif avec des examens radiographiques réalisés en aveugle comme critère principal d'évaluation, chez 632 patients adultes ayant une polyarthrite rhumatoïde active (de durée <3 ans) qui n'avaient jamais reçu de traitement par méthotrexate auparavant. Les patients devaient avoir >12 articulations sensibles à la pression, >10 articulations gonflées et soit une vitesse de sédimentation (VS) >28 mm/h, soit une concentration sérique de protéine C réactive >2.0 mg/dl, soit une raideur matinale >45 min. Des doses de 10 mg ou de 25 mg d'étanercept ont été administrées par voie sous-cutanée 2x par semaine jusqu'à 24 mois. Les doses de méthotrexate ont été augmentées de 7.5 mg/semaine à 20 mg/semaine maximum au cours des 8 premières semaines de l'essai, puis maintenues jusqu'à 24 mois. Avec étanercept 25 mg, l'amélioration clinique et la réponse au traitement sous deux semaines ont été similaires à celles observées lors des essais précédents, et se sont maintenues jusqu'à 24 mois. Le temps de latence a été plus court avec la dose de 25 mg d'étanercept qu'avec le méthotrexate. A l'inclusion, les patients avaient un degré d'invalidité modéré, avec des scores moyens de HAQ de 1.4 à 1.5. Le traitement par étanercept à 25 mg a entraîné une amélioration importante à 12 mois, avec environ 44% de patients obtenant un score de HAQ normal (moins de 0.5). Ce bénéfice a été maintenu la deuxième année de cette étude.
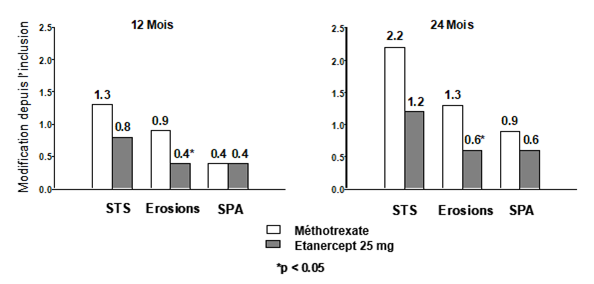
Dans cette étude, les dommages structuraux articulaires ont été évalués radiographiquement et exprimés en modification du Score Total de Sharp (STS) et de ses composants: le «score d'érosion» et le «Score de Pincement Articulaire (SPA)». Les radiographies des mains/poignets et pieds ont été lues à l'inclusion, puis à 6, 12 et 24 mois. La dose de 10 mg d'étanercept a eu constamment moins d'effet sur les dommages articulaires que la dose de 25 mg. L'étanercept à 25 mg a été significativement supérieur au méthotrexate pour le STS et le score d'érosion dans l'étude de 24 mois. Les résultats sont présentés dans la figure ci-dessous.
Evolution radiographique: comparaison d'étanercept vs méthotrexate chez des patients ayant une polyarthrite rhumatoïde d'ancienneté inférieure à 3 ans
Dans une autre étude contrôlée versus traitement actif, randomisée, en double aveugle, l'efficacité clinique, l'innocuité, et la progression radiographique chez des patients atteints de PR traités par étanercept seul (25 mg 2x par semaine), le méthotrexate seul (7.5 à 20 mg par semaine, dose médiane 20 mg) ou l'étanercept associé au méthotrexate débutés simultanément, ont été comparées chez 682 patients adultes ayant une polyarthrite rhumatoïde active d'ancienneté de 6 mois à 20 ans (médiane 5 ans) et qui avaient eu une réponse insuffisante à au moins un DMARD autre que le méthotrexate.
Les patients traités par étanercept associé au méthotrexate avaient des réponses ACR 20, ACR 50 et ACR 70 ainsi qu'une amélioration des scores DAS (Disease Activity Score) et HAQ significativement plus élevées à la fois à 24 et 52 semaines, comparativement aux patients de chacun des groupes en monothérapie (résultats présentés dans le tableau ci-dessous). Des avantages significatifs avec l'étanercept associé au méthotrexate comparé à l'étanercept en monothérapie et au méthotrexate en monothérapie ont aussi été observés après 24 mois.
Résultats d'efficacité clinique à 12 mois: comparaison étanercept vs méthotrexate vs étanercept associé au méthotrexate chez des patients ayant une PR d'ancienneté de 6 mois à 20 ans
|
Critère
|
Méthotrexate
(n=228)
|
Etanercept
(n=223)
|
Etanercept + Méthotrexate
(n=231)
| |
Réponses ACRa
| |
ACR 20
|
58.8%
|
65.5%
|
74.5%†,φ
| |
ACR 50
|
36.4%
|
43.0%
|
63.2%†,φ
| |
ACR 70
|
16.7%
|
22.0%
|
39.8%†,φ
| |
DAS
| |
Score à l'inclusionb
|
5.5
|
5.7
|
5.5
| |
Semaine 52b
|
3.0
|
3.0
|
2.3†,φ
| |
Rémissionc
|
14%
|
18%
|
37%†,φ
| |
HAQ
| |
Score à l'inclusion
|
1.7
|
1.7
|
1.8
| |
Semaine 52
|
1.1
|
1.0
|
0.8†,φ
| |
a
: les patients qui n'avaient pas terminé les 12 mois de l'étude ont été considérés comme non-répondeurs.
b: les valeurs du Disease Activity Score (DAS) sont des moyennes.
c: la rémission est définie par un DAS <1.6.
Valeur du p lors des comparaisons deux à deux:
†: p<0.05 pour les comparaisons des groupes étanercept + méthotrexate vs méthotrexate.
φ: p<0.05 pour les comparaisons des groupes étanercept + méthotrexate vs étanercept.
|
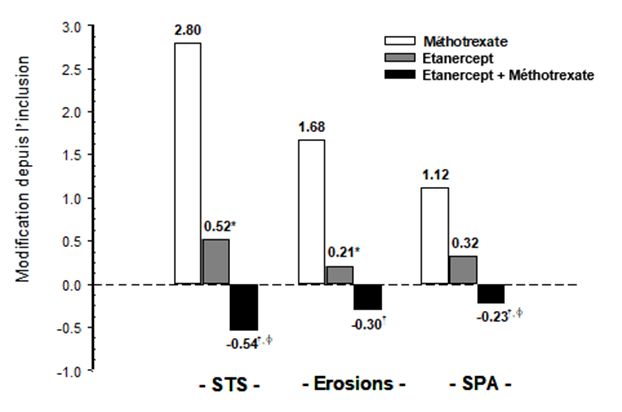
La progression radiographique à 12 mois était significativement moins importante dans le groupe étanercept que dans le groupe méthotrexate, alors que l'association était significativement meilleure que chacune des monothérapies pour ralentir la progression radiographique (voir figure ci-dessous).
Progression radiographique: comparaison étanercept vs méthotrexate vs étanercept associé au méthotrexate chez des patients ayant une PR d'ancienneté de 6 mois à 20 ans (résultats à 12 mois)
Valeur du p lors des comparaisons deux à deux:
*: p<0.05 pour les comparaisons d'étanercept vs méthotrexate.
†: p<0.05 pour les comparaisons d'étanercept + méthotrexate vs méthotrexate.
φ: p<0.05 pour les comparaisons d'étanercept + méthotrexate vs étanercept.
Des avantages significatifs avec l'étanercept associé au méthotrexate comparativement à l'étanercept en monothérapie et au méthotrexate en monothérapie ont aussi été observés après 24 mois. De même, des avantages significatifs avec l'étanercept en monothérapie comparativement au méthotrexate en monothérapie ont aussi été observés après 24 mois.
Dans une analyse où tous les patients sortis prématurément de l'étude, quelle qu'en soit la raison, étaient considérés comme ayant subi une progression, le pourcentage de patients sans progression (variation du STS ≤0.5) à 24 mois était plus élevé dans le groupe étanercept associé au méthotrexate, comparativement à l'étanercept seul et au méthotrexate seul (respectivement 62%, 50% et 36%; p<0.05). La différence entre l'étanercept seul et le méthotrexate seul a aussi été significative (p<0.05). Parmi les patients ayant terminé la totalité des 24 mois de traitement dans l'étude, les taux de patients sans progression étaient respectivement de 78%, 70% et 61%.
L'innocuité et l'efficacité de l'étanercept à la dose de 50 mg (deux injections de 25 mg en sous-cutanée) ont été évaluées dans une étude en double aveugle, contrôlée versus placebo chez 420 patients atteints de PR active. Dans cette étude, 53 patients ont reçu du placebo, 214 patients ont reçu 50 mg d'étanercept 1x par semaine et 153 patients ont reçu 25 mg d'étanercept 2x par semaine. Les profils de sécurité et d'efficacité des deux schémas posologiques de l'étanercept ont été similaires à la 8e semaine sur les signes et symptômes de la PR.
A la 16e semaine cependant, les deux schémas posologiques n'étaient plus équivalents, avec une tendance non significative en faveur de l'administration plus fréquente de l'étanercept.
La biodisponibilité d'une injection unique de 50 mg d'étanercept s'est avérée semblable à celle de 2 injections simultanées de 25 mg.
L'étude V a évalué 89 patients présentant des critères d'inclusion similaires à ceux de l'étude I, en dehors du fait que les patients de l'étude V avaient reçu, en plus, du méthotrexate pendant au moins 6 mois à une dose stable (12.5 à 25 mg/semaine) pendant au moins 4 semaines, et avaient au moins 6 articulations douloureuses. Les patients ont reçu, en plus de leur dose stable de méthotrexate, une dose de 25 mg d'étanercept ou un placebo, par voie sous-cutanée, 2x par semaine pendant 6 mois.
L'étude VI enfin, a évalué 559 patients remplissant des critères d'inclusion similaires à ceux de l'étude I. Les patients ont été traités par étanercept pendant une période allant jusqu'à 6 mois, selon un des quatre schémas thérapeutiques suivants: 10 mg 1x par semaine, 10 mg 2x par semaine, 25 mg 1x par semaine ou 25 mg 2x par semaine.
Les résultats des études contrôlées V et VI ont été exprimés en pourcentage d'amélioration de la PR, en utilisant les critères de réponse de l'American College of Rheumatology (ACR). Le critère principal d'évaluation de l'étude V était l'obtention d'une réponse ACR 20 à 6 mois. Par définition, une réponse ACR 20 est obtenue si le patient a une amélioration de 20% du nombre d'articulations douloureuses et du nombre d'articulations gonflées, associée à ≥20% d'amélioration d'au moins trois des cinq critères suivants: (1) évaluation de la douleur par le patient, (2) évaluation globale de la maladie par le patient, (3) évaluation globale de la maladie par le médecin, (4) évaluation de la limitation fonctionnelle par le patient, et (5) réaction de phase aiguë (VS ou CRP). Les réponses ACR 50 et 70 sont définies selon les mêmes critères, avec respectivement une amélioration de 50% et de 70%. Dans l'étude VI, le critère principal était le pourcentage d'amélioration des articulations douloureuses et gonflées à 3 mois.
Dans les études V et VI, les réponses ont été supérieures chez les patients traités par étanercept, à 3 et à 6 mois.
Dans l'étude V, environ 15% des patients recevant de l'étanercept ont obtenu une réponse ACR 70 à 3 mois et à 6 mois, comparativement à moins de 5% des patients sous placebo. Parmi les patients recevant de l'étanercept, les réponses cliniques ont généralement débuté sous 1 à 2 semaines après l'initiation du traitement, et ont été quasiment toujours obtenues dans les 3 mois.
Enfants et adolescents atteints d'arthrite juvénile idiopathique
La sécurité et l'efficacité de l'étanercept ont été évaluées dans une étude en 2 phases, chez 69 enfants atteints d'arthrite juvénile idiopathique polyarticulaire ayant présenté différentes formes de début de la maladie (polyarthrite, oligoarthrite, origine systémique). Les patients inclus dans l'étude étaient âgés de 4 à 17 ans, présentaient une arthrite juvénile idiopathique polyarticulaire active modérée à sévère et étaient réfractaires ou intolérants au méthotrexate. Une dose stable d'un seul anti-inflammatoire non stéroïdien et/ou de prednisolone (<0.2 mg/kg/jour ou 10 mg maximum) a été maintenue chez les patients. Dans la première phase de l'étude, tous les patients ont reçu 0.4 mg/kg (maximum 25 mg par injection) d'étanercept administré en sous-cutané 2x par semaine. Dans la deuxième phase, les patients présentant une réponse clinique au 90e jour ont été randomisés soit pour rester sous étanercept, soit pour recevoir le placebo pendant 4 mois et ont été surveillés pour détecter toute flambée de la maladie. La réponse a été mesurée en utilisant le score ACR Pedi 30 (score pédiatrique de l'American College of Rheumatology), à savoir une amélioration ≥30% d'au moins 3 des 6 critères-clés de l'ACJ et une aggravation ≥30% d'au plus 1 des 6 critères. Ces critères incluent le nombre d'articulations atteintes, la limitation des mouvements, l'évaluation globale de la maladie par le médecin et le patient/parent, le handicap fonctionnel et la vitesse de sédimentation (VS). Une flambée de la maladie était définie comme une aggravation ≥30% de 3 des 6 critères-clés de l'ACJ et une amélioration ≥30% d'au plus 1 des 6 critères, ainsi qu'un minimum de 2 articulations atteintes.
Dans la première phase de l'étude, 51 des 69 patients (74%) ont bénéficié d'une réponse clinique et ont été inclus dans la deuxième phase de l'étude. Dans la deuxième phase de l'étude, 6 patients sur 25 (24%) maintenus sous étanercept ont eu une flambée de la maladie, en comparaison à 20 patients sur 26 (77%) sous placebo (p=0.007). A partir du début de la deuxième phase de l'étude, le délai moyen d'apparition de la flambée a été supérieur ou égal à 116 jours pour les patients ayant reçu de l'étanercept et de 26 jours pour les patients sous placebo. Chaque item des critères de l'ACJ s'est aggravé dans le groupe placebo et est resté stable ou s'est même amélioré dans le groupe étanercept. Les données suggèrent la possibilité d'un taux plus élevé de flambée chez les patients présentant une VS plus accélérée à l'inclusion. Parmi les patients qui ont bénéficié d'une réponse clinique à 90 jours et qui ont été inclus dans la deuxième phase de l'étude, certains des patients maintenus sous étanercept ont continué à obtenir des améliorations entre le troisième mois et le septième mois alors que ceux sous placebo n'ont montré aucune amélioration.
Chez 58 patients pédiatriques de l'étude mentionnée ci-dessus (âgés d'au moins 4 ans au moment de l'inclusion), le traitement par étanercept a été poursuivi sur une période allant jusqu'à 10 ans dans une étude à long terme ouverte destinée à examiner la sécurité. La fréquence des effets indésirables graves et des infections graves n'a pas augmenté avec l'utilisation à long terme.
La sécurité à long terme de l'étanercept en monothérapie (n=103), de l'étanercept en association avec le méthotrexate (n=294) ou du méthotrexate en monothérapie (n=197) a été évaluée dans une étude de registre réalisée pendant 3 ans chez 594 enfants âgés de 2 à 18 ans atteints d'arthrite juvénile idiopathique. 39 de ces enfants étaient âgés de 2 à 3 ans. Globalement, des infections ont été rapportées plus fréquemment chez les patients traités par l'étanercept que chez les patients traités par le méthotrexate seul (3.8% vs 2%) et les infections associées à l'utilisation d'étanercept ont été plus graves.
Dans une autre étude ouverte à un bras (n=127), 60 patients atteints d'une oligoarthrite étendue (extended oligoarthritis, EO) (15 patients âgés de 2 à 4 ans, 23 patients âgés de 5 à 11 ans et 22 patients âgés de 12 à 17 ans), 38 patients atteints d'arthrite associée à une enthésite (âgés de 12 à 17 ans) et 29 patients atteints d'arthrite psoriasique (âgés de 12 à 17 ans) ont reçu une dose hebdomadaire de 0.8 mg/kg de PC d'étanercept (et au maximum 50 mg par injection) pendant 12 semaines. Dans chaque soustype d'AJI, la majorité des patients a rempli les critères ACR Pedi 30 et a montré des améliorations cliniques dans les critères secondaires d'évaluation tels que le nombre d'articulations douloureuses et l'évaluation globale de la maladie par le médecin. Le profil de sécurité a été cohérent avec celui observé dans les autres études menées sur l'AJI.
Parmi les 127 patients de l'étude principale, 109 ont participé à l'étude d'extension ouverte et ont été suivis pendant 8 ans supplémentaires, soit jusqu'à 10 ans au total. À la fin de l'étude d'extension, 84/109 (77%) des patients avaient complété l'étude; 27 (25%) prenaient encore activement l'étanercept, 7 (6%) avaient interrompu le traitement en raison d'une maladie faible/inactive; 5 (5%) avaient recommencé l'étanercept après un arrêt antérieur du traitement; et 45 (41%) avaient arrêté l'étanercept (mais étaient restés sous surveillance); 25/109 (23%) patients avaient définitivement arrêté l'étude (dont 1 patient en raison d'une réponse insuffisante et 1 patient en raison d'effets indésirables (maladie de Hodgkin)). Les améliorations de l'état clinique obtenues dans l'étude principale se sont généralement maintenues pour tous les critères d'efficacité tout au long de la période de suivi. Les patients qui prenaient étanercept ont pu participer à une phase d'arrêt optionnelle une fois pendant l'étude de prolongation, selon l'évaluation de la réponse clinique par l'investigateur. 30 patients ont participé à la phase d'arrêt. 17 (57%) patients ont présenté une poussée de la maladie (définie comme une aggravation de ≥30% dans au moins 3 des 6 composants ACR Pedi avec une amélioration de ≥30% dans l'un au maximum des 6 composants restants et au moins 2 articulations atteintes); le délai médian de survenue d'une poussée de la maladie après l'arrêt d'étanercept était de 190 jours (EO 190 jours, arthrite associée à l'enthésite 533 jours, arthrite psoriasique 110 jours).
Une affection maligne, la maladie de Hodgkin, a été rapportée chez un patient EO-JIA âgé de 18 ans au cours de la première année de l'étude d'extension. Le nombre (taux d'événements rapporté à l'exposition pour 100 années-patients) d'événements indésirables graves, d'affections malignes et d'infections graves était respectivement de 40 (5.85 EP100PY), 1 et 14 (2.05 EP100PY).
Aucune étude n'a été menée chez les patients atteints d'arthrite juvénile idiopathique dans le but d'évaluer l'influence de la poursuite d'un traitement par étanercept chez les patients qui n'avaient pas répondu 3 mois après le début du traitement par étanercept. En outre, aucune étude n'a été menée chez les patients atteints d'AJI afin d'examiner les effets de la diminution de la dose recommandée d'étanercept après une utilisation à long terme.
Patients adultes atteints d'arthrite psoriasique
L'efficacité de l'étanercept a été évaluée au cours d'un essai clinique randomisé, en double aveugle, contrôlé contre placebo, chez 205 patients atteints d'arthrite psoriasique. Les patients étaient âgés de 18 à 70 ans et souffraient d'une arthrite psoriasique active (≥3 articulations gonflées et ≥3 articulations douloureuses) dans au moins l'une de ces formes: (1) atteinte interphalangienne distale (AID); (2) arthrite polyarticulaire (absence de nodules rhumatoïdes et présence de psoriasis); (3) arthrite mutilante; (4) arthrite psoriasique asymétrique; ou (5) ankylose vertébrale de type inflammatoire. Les patients avaient également un psoriasis en plaques avec une lésion caractéristique présentant un diamètre de ≥2 cm. Les patients étaient préalablement traités avec des anti-inflammatoires non stéroïdiens (86%), des traitements de fond (80%) et des corticostéroïdes (24%). Les patients également traités par méthotrexate (dose stable depuis ≥2 mois) pouvaient continuer le méthotrexate à une dose constante ≤25 mg/semaine. Des doses de 25 mg d'étanercept (basées sur les études de recherche de dose chez les patients atteints de polyarthrite rhumatoïde) ou un placebo étaient administrées par voie s.c. 2x par semaine pendant 6 mois. A la fin de l'étude en double aveugle, les patients pouvaient entrer dans une étude d'extension en ouvert au long cours pour une durée totale allant jusqu'à 2 ans.
La réponse clinique a été exprimée en pourcentages de patients atteignant une réponse ACR 20, 50 et 70, et en pourcentages de patients avec une amélioration des critères de réponse de l'arthrite psoriasique (Psoriatic Arthritis Response Criteria ou PsARC). Les résultats sont résumés dans le tableau ci-après.
Réponses des patients atteints d'arthrite psoriasique dans l'essai contrôlé contre placebo
|
|
Pourcentage de patients
| |
Placebo
|
Etanercepta
| |
Réponse de l'arthrite psoriasique
|
n=104
|
n=101
| |
ACR 20
| |
Mois 3
|
15
|
59b
| |
Mois 6
|
13
|
50b
| |
ACR 50
| |
Mois 3
|
4
|
38b
| |
Mois 6
|
4
|
37b
| |
ACR 70
| |
Mois 3
|
0
|
11b
| |
Mois 6
|
1
|
9c
| |
PsARC
| |
Mois 3
|
31
|
72b
| |
Mois 6
|
23
|
70b
| |
a
: 25 mg d'étanercept s.c. 2x par semaine.
b: p<0.001, comparé au placebo.
c: p<0.01, comparé au placebo.
|
Parmi les patients atteints d'arthrite psoriasique qui ont reçu de l'étanercept, les réponses cliniques étaient visibles dès la première visite (à 4 semaines) et se sont maintenues pendant les 6 mois de traitement. L'étanercept a été significativement supérieur au placebo sur tous les paramètres de l'activité de la maladie (p<0.001), et les réponses étaient similaires avec et sans traitement concomitant par le méthotrexate. La qualité de vie des patients atteints d'arthrite psoriasique a été mesurée à plusieurs moments à l'aide de l'indice de handicap du questionnaire HAQ. L'indice de handicap était significativement amélioré à tous les moments d'évaluation chez les patients traités par étanercept par rapport au groupe placebo (p<0.001).
Les modifications radiographiques ont été évaluées dans l'étude sur l'arthrite psoriasique. Des radiographies des mains et des poignets ont été réalisées à l'inclusion et à 6, 12 et 24 mois. Le score total de Sharp (STS) modifié à 12 mois est présenté dans le tableau ci-dessous:
Différence moyenne annualisée du score total de Sharp comparé à l'inclusion
|
|
Placebo
(n=104)
|
Etanercept
(n=101)
| |
Mois 12
|
1.00 (0.29)
|
-0.03 (0.09)a
| |
a
: p=0.0001, comparé au placebo.
|
Les capacités fonctionnelles ont été améliorées avec le traitement par étanercept pendant la période en double aveugle, et ce bénéfice a été maintenu au cours de l'exposition à long terme jusqu'à 2 ans.
Dans la forme de l'arthrite psoriasique proche de la spondylarthrite ankylosante, les preuves d'efficacité de l'étanercept sont insuffisantes en raison du nombre trop faible de patients étudiés.
Aucune étude n'a été effectuée chez des patients atteints d'arthrite psoriasique avec le schéma posologique de 50 mg d'étanercept 1x par semaine. Les preuves de l'efficacité de ce schéma posologique dans cette population de patients reposent sur des données provenant d'une étude chez des patients atteints de spondylarthrite ankylosante.
Patients adultes atteints de spondylarthrite ankylosante
L'efficacité de l'étanercept dans la spondylarthrite ankylosante a été évaluée dans quatre études randomisées, en double aveugle, comparant l'administration à 2x par semaine de 25 mg d'étanercept au placebo chez 401 patients atteints de spondylarthrite ankylosante. Parmi les 401 patients inclus au total, 203 étaient traités par étanercept. La plus vaste de ces études (n=277) a inclus des patients âgés de 18 à 70 ans et qui avaient une spondylarthrite ankylosante active. Celle-ci était définie par des scores d'échelle visuelle analogique (VAS) ≥30 pour la durée et l'intensité moyennes de la raideur matinale, associés à des scores VAS ≥30 pour au moins 2 des 3 paramètres suivants: évaluation globale par le patient; moyenne des valeurs VAS pour la douleur dorsale nocturne et la douleur dorsale totale; moyenne des 10 questions de l'indice fonctionnel de la spondylarthrite ankylosante de Bath (Bath Ankylosing Spondylitis Functional Index ou BASFI). Les patients recevant des traitements de fond, des anti-inflammatoires non stéroïdiens ou des corticostéroïdes pouvaient continuer ces traitements à des doses constantes. Les patients présentant une ankylose complète de la colonne vertébrale n'ont pas été inclus dans l'étude. Des doses de 25 mg d'étanercept (déterminées lors des études de recherche de dose chez les patients atteints de polyarthrite rhumatoïde) ou un placebo ont été administrés par voie sous-cutanée 2x par semaine pendant 6 mois.
Le critère principal d'efficacité était une amélioration du critère de réponse ASAS (Assessment in Ankylosing Spondylitis, ou évaluation de la spondylarthrite ankylosante) de 20% (ASAS 20). Comparativement au placebo, le traitement par étanercept a montré des améliorations significatives des réponses ASAS 20, ASAS 50 et ASAS 70 dès la deuxième semaine après l'initiation du traitement (voir tableau ci-après).
Réponses des patients atteints de spondylarthrite ankylosante dans un essai contrôlé contre placebo
|
|
Pourcentage de patients
| |
Réponse de la spondylarthrite ankylosante
|
Placebo
n=139
|
Etanercept
n=138
| |
ASAS 20
| |
2 semaines
|
22
|
46a
| |
3 mois
|
27
|
60a
| |
6 mois
|
23
|
58a
| |
ASAS 50
| |
2 semaines
|
7
|
24a
| |
3 mois
|
13
|
45a
| |
6 mois
|
10
|
42a
| |
ASAS 70
| |
2 semaines
|
2
|
12b
| |
3 mois
|
7
|
29b
| |
6 mois
|
5
|
28b
| |
a
: p<0.001, comparé au placebo.
b: p=0.002, comparé au placebo.
|
De plus, des améliorations significatives ont été observées pour les autres mesures d'activité de la maladie chez les patients atteints de spondylarthrite ankylosante. Comparativement au placebo, l'étanercept a montré des améliorations significatives de tous les paramètres du critère ASAS (évaluation globale par le patient, douleurs nocturnes et dorsales globales, BASFI et inflammation), de la concentration de protéine C réactive et la vitesse de sédimentation, de l'évaluation globale par le médecin et de la mobilité du rachis (test de Schober, ampliation thoracique et mesure de la distance occiput-mur).
Parmi les patients atteints de spondylarthrite ankylosante ayant reçu de l'étanercept, les réponses cliniques sont apparues dès la première visite (2 semaines) et se sont maintenues pendant les 6 mois de traitement. Les réponses étaient similaires chez les patients qui initialement recevaient ou non des traitements concomitants.
Des résultats similaires ont été obtenus au cours des deux essais d'effectifs moins importants réalisés dans la spondylarthrite ankylosante.
Dans une quatrième étude, effectuée en double aveugle, contrôlée versus placebo chez 356 patients atteints de spondylarthrite ankylosante, on a évalué la sécurité et l'efficacité de 50 mg d'étanercept (deux injections sous-cutanées de 25 mg) administré 1x par semaine versus 25 mg d'étanercept administré 2x par semaine. Les profils de sécurité et d'efficacité des 2 schémas posologiques (50 mg 1x par semaine et 25 mg 2x par semaine) ont été similaires.
Patients adultes atteints de psoriasis en plaques
La sécurité et l'efficacité de l'étanercept ont été évaluées dans quatre études randomisées, contrôlées en double aveugle par placebo.
Les patients «en échec» dans la population cible sont définis comme présentant une réponse insuffisante (PASI <50 ou PGA [Patient Global Assessment] insatisfaisant), ou une aggravation de la maladie au cours du traitement avec au moins chacun des trois traitements systémiques majeurs disponibles utilisés à une posologie adéquate pendant une durée suffisamment longue pour évaluer la réponse au traitement.
L'efficacité de l'étanercept versus les autres traitements systémiques chez les patients avec un psoriasis modéré à sévère (répondeurs aux autres traitements systémiques) n'a pas été évaluée dans des études comparant directement l'étanercept aux autres traitements systémiques. A la place, l'innocuité et l'efficacité de l'étanercept ont été évaluées dans quatre études randomisées, contrôlées en double aveugle contre placebo. Le critère primaire d'efficacité dans les quatre études était la proportion de patients dans chaque groupe de traitement qui atteignait le PASI 75 (c'est-à-dire une amélioration par rapport à l'inclusion d'au moins 75% du score Psoriasis Area and Severity Index) à 12 semaines.
L'étude 1 était une étude de phase II chez des patients âgés d'au moins 18 ans et présentant un psoriasis en plaques actif mais cliniquement stable atteignant au moins 10% de la surface corporelle. 112 patients ont été randomisés pour recevoir une dose de 25 mg d'étanercept (n=57) ou un placebo (n=55) 2x par semaine pendant 24 semaines.
L'étude 2 a évalué 652 patients atteints de psoriasis chronique en plaques avec les mêmes critères d'inclusion que dans l'étude 1 et un PASI ≥10 au moment du screening. L'étanercept a été administré à des doses de 25 mg 1x par semaine, 25 mg 2x par semaine ou 50 mg 2x par semaine pendant 6 mois consécutifs. Au cours des 12 premières semaines de la période de traitement en double aveugle, les patients ont reçu un placebo ou l'une des trois posologies d'étanercept décrites ci-dessus. Après 12 semaines de traitement, les patients du groupe placebo ont commencé le traitement en aveugle par étanercept (25 mg 2x par semaine); les patients dans les groupes de traitement actif ont continué jusqu'à la semaine 24, à la dose à laquelle ils avaient été initialement randomisés.
L'étude 3 a évalué 583 patients et les critères d'inclusion étaient les mêmes que dans l'étude 2. Dans cette étude, les patients ont reçu une dose de 25 mg ou 50 mg d'étanercept, ou un placebo, 2x par semaine pendant 12 semaines par voie sous-cutanée; puis tous les patients ont reçu 25 mg d'étanercept 2x par semaine en ouvert pendant 24 semaines supplémentaires.
L'étude 4 a évalué 142 patients et les critères d'inclusion étaient similaires à ceux des études 1 et 2. Dans cette étude, les patients ont reçu une dose de 50 mg d'étanercept ou un placebo 1x par semaine pendant 12 semaines; puis tous les patients ont reçu 50 mg d'étanercept 1x par semaine en ouvert pendant 12 semaines supplémentaires.
Dans l'étude 1, le groupe traité par étanercept avait une proportion significativement plus élevée de patients présentant une réponse PASI 75 à la semaine 12 (30%) comparativement au groupe traité par placebo (2%) (p<0.0001). A 24 semaines, 56% des patients dans le groupe traité par étanercept avaient atteint le PASI 75 comparativement à 5% des patients traités par placebo. Les résultats principaux des études 2, 3 et 4 sont présentés ci-dessous.
Réponses des patients atteints de psoriasis dans les études 2, 3 et 4
|
|
Etude 2
|
Etude 3
|
Etude 4
| |
|
Placebo
|
Etanercept
|
Placebo
|
Etanercept
|
Placebo
|
Etanercept
| |
|
|
25 mg
2x/sem
|
50 mg
2x/sem
|
|
25 mg
2x/sem
|
50 mg
2x/sem
|
|
50 mg
1x/sem
|
50 mg
1xsem
| |
|
n=166
|
n=162
|
n=162
|
n=164
|
n=164
|
n=193
|
n=196
|
n=196
|
n=46
|
n=96
|
n=90
| |
Réponse
|
Sem 12
|
Sem 12
|
Sem 24a
|
Sem 12
|
Sem 24a
|
Sem 12
|
Sem 12
|
Sem 12
|
Sem 12
|
Sem 12
|
Sem 24a
| |
PASI 50 [%]
|
14
|
58*
|
70
|
74*
|
77
|
9
|
64*
|
77*
|
9
|
69*
|
83
| |
PASI 75 [%]
|
4
|
34*
|
44
|
49*
|
59
|
3
|
34*
|
49*
|
2
|
38*
|
71
| |
DSGAb, pas de lésions apparentes ou presque pas de lésions apparentes [%]
|
5
|
34*
|
39
|
49*
|
55
|
4
|
39*
|
57*
|
4
|
39*
|
64
| |
*: p≤0.0001, comparé au placebo.
a: Aucune comparaison statistique versus placebo n'a été faite à la semaine 24 dans les études 2 et 4 étant donné que le groupe initialement sous placebo a commencé à recevoir étanercept 25 mg 2x/sem ou 50 mg 1x/sem à partir de la semaine 13 jusqu'à la semaine 24.
b: Dermatologist Static Global Assessment. Pas de lésions apparentes ou presque pas de lésions apparentes définies par 0 ou 1 sur une échelle de 0 à 5.
|
Parmi les patients atteints de psoriasis en plaques qui recevaient de l'étanercept, des réponses significatives comparativement au placebo sont apparues à la première visite (2 semaines). Ces améliorations ont été maintenues durant les 24 semaines de traitement.
L'étude 2 comprenait également une période d'arrêt du traitement au cours de laquelle les patients qui avaient atteint une amélioration du PASI d'au moins 50% à la semaine 24 arrêtaient le traitement. L'apparition d'un rebond (PASI ≥150% de la valeur à l'inclusion) et le délai de rechute (définie par la perte d'au moins la moitié de la valeur obtenue entre l'inclusion et la semaine 24) ont été évalués chez les patients qui n'étaient plus sous traitement. Au cours de la période sans traitement, les symptômes du psoriasis sont progressivement réapparus avec un délai médian de rechute de 3 mois. Aucun effet rebond de la maladie et aucun événement indésirable grave lié au psoriasis n'ont été observés. Il existe des données montrant le bénéfice de la reprise du traitement par étanercept chez les patients qui répondaient initialement au traitement.
Dans l'étude 3, la majorité des patients (77%) qui étaient initialement randomisés à la dose de 50 mg 2x par semaine et avaient leur dose d'étanercept abaissée à 25 mg 2x par semaine à la semaine 12, ont eu une réponse PASI 75 maintenue jusqu'à la semaine 36. Pour les patients qui recevaient 25 mg 2x par semaine tout au long de l'étude, la réponse PASI 75 continuait de s'améliorer entre les semaines 12 et 36.
Dans l'étude 4, le groupe traité par étanercept avait une proportion plus élevée de patients avec une réponse PASI 75 à la semaine 12 (38%) comparativement au groupe traité par placebo (2%) (p<0.0001). Pour les patients qui recevaient 50 mg 1x par semaine tout au long de l'étude, les réponses d'efficacité ont continué à s'améliorer avec un PASI 75 à la semaine 24 atteignant 71%.
Dans les études en ouvert à long terme (jusqu'à 34 mois) au cours desquelles l'étanercept a été administré sans interruption, les réponses cliniques étaient maintenues et la sécurité était comparable aux études à court terme.
Une analyse des données cliniques n'a révélé aucune caractéristique de la maladie à l'inclusion qui pourrait conduire les cliniciens à sélectionner le type de posologie le plus approprié (intermittent ou continu). En conséquence, le choix d'un traitement intermittent ou continu doit être basé sur l'expérience thérapeutique individuelle du patient.
Enfants et adolescents atteints de psoriasis en plaques
L'efficacité de l'étanercept a été évaluée dans une étude randomisée, en double aveugle, contrôlée contre placebo, chez 211 enfants et adolescents âgés de 4 à 17 ans, atteints de psoriasis en plaques modéré à sévère (défini par un score sPGA ≥3, une surface cutanée atteinte ≥10% (BSA) et un PASI ≥12). Les patients inclus avaient déjà reçu une photothérapie ou un traitement systémique ou avaient présenté une réponse insuffisante à un traitement topique.
Pendant 12 semaines, les patients ont reçu soit 0.8 mg d'étanercept/kg de PC 1x par semaine (jusqu'à 50 mg) soit un placebo. À la semaine 12, davantage de patients étaient répondeurs en ce qui concerne l'efficacité (p.ex. PASI 75) dans le groupe étanercept que dans le groupe placebo.
Résultats à 12 semaines chez des enfants et adolescents atteints de psoriasis en plaques
|
|
Etanercept
0.8 mg/kg 1x par semaine
|
Placebo
| |
(n=106)
|
(n=105)
| |
PASI 75, n (%)
|
60 (57%)a
|
12 (11%)
| |
PASI 50, n (%)
|
79 (75%)a
|
24 (23%)
| |
sPGA pas de lésions apparentes ou minimal, n (%)
|
56 (53%)a
|
14 (13%)
| |
Abréviation: sPGA-static Physician Global Assessment.
a: p<0.0001, par rapport au placebo.
|
Après la phase de traitement en double aveugle de 12 semaines, tous les patients ont reçu 0.8 mg d'étanercept/kg de PC (jusqu'à 50 mg) 1x par semaine pendant 24 semaines supplémentaires. Les taux de réponse observés pendant la phase ouverte de l'étude ont été comparables à ceux observés pendant la phase en double aveugle.
Par rapport aux patients à nouveau randomisés dans le groupe étanercept, un nombre significativement plus élevé de patients à nouveau randomisés dans le groupe placebo ont présenté une rechute de la maladie (perte de la réponse au PASI 75) pendant la phase randomisée d'arrêt. En cas de traitement continu, les taux de réponse se sont maintenus pendant une période allant jusqu'à 48 semaines.
La sécurité et l'efficacité continues de l'étanercept 0.8 mg/kg de PC (jusqu'à une dose maximale de 50 mg) 1x par semaine, observées au cours de l'étude de 48 semaines mentionnée ci-dessus, ont été évaluées au cours d'une étude d'extension ouverte allant jusqu'à 2 ans, qui incluait 181 patients pédiatriques atteints de psoriasis en plaques. L'utilisation de l'étanercept sur une longue durée n'a révélé aucun nouvel aspect concernant la sécurité. Le rapport global bénéfice-risque est resté positif et comparable aux résultats de l'étude initiale de 48 semaines.
|


