Propriétés/EffetsCode ATC
C10AX06
Mécanisme d’action
L’icosapent éthyl est un ester éthylique stable de l’acide gras oméga-3 acide eicosapentaénoïque (EPA). Les mécanismes d’action de l’icosapent éthyl contribuant à une réduction des événements cardiovasculaires ne sont pas entièrement élucidés. Les mécanismes sont probablement multifactoriels et incluent un profil des lipoprotéines amélioré avec une réduction des lipoprotéines riches en triglycérides, des effets anti-inflammatoires et antioxydants, la réduction de l’accumulation des macrophages, une fonction endothéliale améliorée, une chape fibreuse d’épaisseur/de stabilité augmentée et des effets antiplaquettaires. Chacun de ces mécanismes peut influencer de façon bénéfique le développement, la progression et la stabilisation des plaques d’athérome, ainsi que les conséquences de la rupture des plaques. Des études précliniques et cliniques confirment ces bénéfices avec l’EPA. Les effets anti-inflammatoires systémiques et localisés de l’EPA résultent potentiellement du déplacement de l’acide arachidonique (AA) pro-inflammatoire, orientant le catabolisme des eicosanoïdes (prostaglandines de la série indice2, thromboxanes et leucotriènes de la série indice4) vers des médiateurs non inflammatoires ou anti-inflammatoires. Cependant, la signification clinique directe des résultats individuels n’est pas claire.
Pharmacodynamique
L’icosapent éthyl améliore le profil des lipoprotéines en supprimant les enzymes synthétisant le cholestérol, les acides gras et les triglycérides (TG), en augmentant la β-oxydation des acides gras et en réduisant la protéine de transfert des triglycérides microsomique (MTTP), entraînant une diminution des triglycérides hépatiques et la synthèse et libération de lipoprotéines de très basse densité (VLDL). L’icosapent éthyl augmente aussi l’expression de la lipoprotéine lipase entraînant l’élimination accrue des TG des particules de VLDL et de chylomicrons en circulation. Chez les patients ayant un taux de TG élevé, l’icosapent éthyl baisse les TG, les VLDL, le cholestérol des lipoprotéines restantes et les taux de marqueurs inflammatoires tels que la protéine C réactive. La réduction des TG apparaît cependant n’apporter qu’une contribution mineure à la réduction du risque d’événements cardiovasculaires avec l’icosapent éthyl.
Efficacité clinique
REDUCE-IT était une étude multinationale, en double-aveugle, randomisée, contrôlée versus placebo, événementielle conduite chez 8179 (4089 icosapent éthyl, 4090 placebo) patients adultes traités par statines inclus avec un taux de lipoprotéines de basse densité-cholestérol (LDL-C) > 1,03 mmol/l (40 mg/dl) et ≤ 2,59 mmol/l (100 mg/dl) et un taux de triglycérides (TG) modérément élevé (≥ 1,53 mmol/l et < 5,64 mmol/l [≥ 135 mg/dl et < 500 mg/dl] mesuré lors de la sélection des patients, c’est-à-dire lors des visites de qualification pré-inclusion) et souffrant soit d’une maladie cardiovasculaire avérée (70,7%) soit d’un diabète et présentant d’autres facteurs de risque de maladies cardiovasculaires (29,3%). Les patients atteints d’une maladie cardiovasculaire établie avaient au moins 45 ans et des antécédents de pathologie artérielle coronaire, de maladie cérébrovasculaire ou carotidienne, ou de pathologie artérielle périphérique. Les patients dans l’autre groupe de risques avaient au moins 50 ans, un diabète nécessitant une prise en charge médicale et au moins un facteur de risque supplémentaire, à savoir l’hypertension ou la prise d’un médicament antihypertenseur; un âge d’au moins 55 ans (hommes) ou d’au moins 65 ans (femmes); un faible taux de lipoprotéines de haute densité-cholestérol; le tabagisme; un taux augmenté de protéine C réactive ultrasensible; l’insuffisance rénale; la microalbuminurie ou la macroalbuminurie; la rétinopathie; ou un index de pression systolique réduit. Les patients ont été répartis de façon aléatoire selon un rapport 1 : 1 pour recevoir soit l’icosapent éthyl soit un placebo (sous forme de 4 capsules par jour). La durée de suivi médiane était de 4,9 ans. Globalement, 99,8% des patients ont été suivis afin d’évaluer leur statut vital jusqu’à la fin de l’étude ou jusqu’à leur décès.
Les paramètres à l’inclusion étaient équilibrés entre les groupes, l’âge médian à l’inclusion était de 64 ans (fourchette: 44 ans à 92 ans), 46% ayant au moins 65 ans; 28,8% étaient des femmes. La population de l’étude incluait 90,2% de blancs, 5,5% d’Asiatiques, 4,2% étant identifiés comme d’origine ethnique hispanique et 1,9% de noirs. En ce qui concerne les diagnostics antérieurs de maladies cardiovasculaires, 46,7% avaient eu un infarctus du myocarde, 9,2% avaient une maladie artérielle périphérique symptomatique et 6,1% avaient eu un accident vasculaire cérébral ou un accident ischémique transitoire (AIT) non connu. Les facteurs de risque supplémentaires à l’inclusion incluaient entre autres l’hypertension (86,6%), le diabète sucré (0,7% type 1; 57,8% type 2), DFGe < 60 ml/min pour 1,73 m2 (22,2%), une insuffisance cardiaque congestive (17,7%) et une consommation actuelle quotidienne de cigarettes (15,2%). La plupart des patients suivaient à l’inclusion un traitement par statines d’intensité modérée (63%) ou forte (31%). À l’inclusion, la plupart des patients prenaient au moins un autre médicament cardiovasculaire, incluant des agents antiplaquettaires et/ou antithrombotiques (85,5%), des bêta-bloquants (70,7%), des antihypertenseurs (95,2%), des inhibiteurs de l’enzyme de conversion de l’angiotensine (inhibiteurs de l’ECA; 51,9%) ou des antagonistes du récepteur de l’angiotensine (ARA; 26,9%); 77,5% prenaient un inhibiteur de l’ECA ou un ARA. Le protocole excluait les patients sous inhibiteur de la PCSK9. Sous un traitement hypolipémiant de fond stable, le LDL-C médian [Q1; Q3] à l’inclusion était de 1,9 [1,6; 2,3] mmol/l (75,0 [62,0; 89,0] mg/dl); la moyenne (SD) était de 2,0 (0,5) mmol/l (76,2 [20,3] mg/dl). Su un traitement hypolipémiant de fond stable, les TG à jeun médians [Q1; Q3] étaient de 2,4 [2,0; 3,1] mmol/l (216,0 [176,0; 272,5] mg/dl); la moyenne (SD) était de 2,6 (0,9) mmol/l (233,2 [80,1] mg/dl).
L’icosapent éthyl a significativement réduit le risque de survenue du critère d’évaluation principal composite (délai de survenue du décès cardiovasculaire, d’un infarctus du myocarde, d’un accident vasculaire cérébral, d’une revascularisation coronaire ou de l’hospitalisation pour un angor instable; p< 0,0001) et du critère d’évaluation secondaire composite principal (délai de survenue du décès cardiovasculaire, d’un infarctus du myocarde ou d’un accident vasculaire cérébral; p< 0,0001). Les résultats du critère d’évaluation de l’efficacité primaire sont présentés dans le tableau 1.
Tableau 1: Effet de l’icosapent éthyl sur le délai jusqu’à la survenue d’un premier événement cardiovasculaire chez les patients ayant un taux de triglycérides élevé et une maladie cardiovasculaire ou du diabète ou d’autres facteurs de risque dans l’étude REDUCE-IT
|
|
Icosapent éthyl
|
Placebo
|
Icosapent éthyl vs placebo
| |
N = 4089
n (%)
|
N = 4090
n (%)
|
Rapport de risque (IC à 95%)
| |
Critère d’évaluation primaire composite
| |
Décès cardiovasculaire, infarctus du myocarde, accident vasculaire cérébral, revascularisation coronaire, hospitalisation pour un angor instable (5 événements cardiovasculaires indésirables graves − 5 points MACE)
|
705
(17,2)
|
901
(22,0)
|
0,75
(0,68; 0,83)
|
Concernant le critère d’évaluation secondaire «3 points MACE» (décès d’origine cardiovasculaire, infarctus du myocarde ou accident vasculaire cérébral), les patients traités par icosapent éthyl présentaient une réduction du risque relatif de 26% (IC à 95%: 0,65; 0,83; p< 0,0001). Une réduction du risque de 13% (IC à 95%: 0,74; 1,02) a été rapportée pour les «décès quelle qu’en soit la cause» (aucune composante du critère d’évaluation primaire ou secondaire). Pour tous les autres critères d’évaluation secondaires, une réduction du risque de 20 à 35% a été obtenue.
Figure 1: Estimation de Kaplan-Meier de l’incidence cumulée du critère d’évaluation primaire composite dans l’étude REDUCE-IT
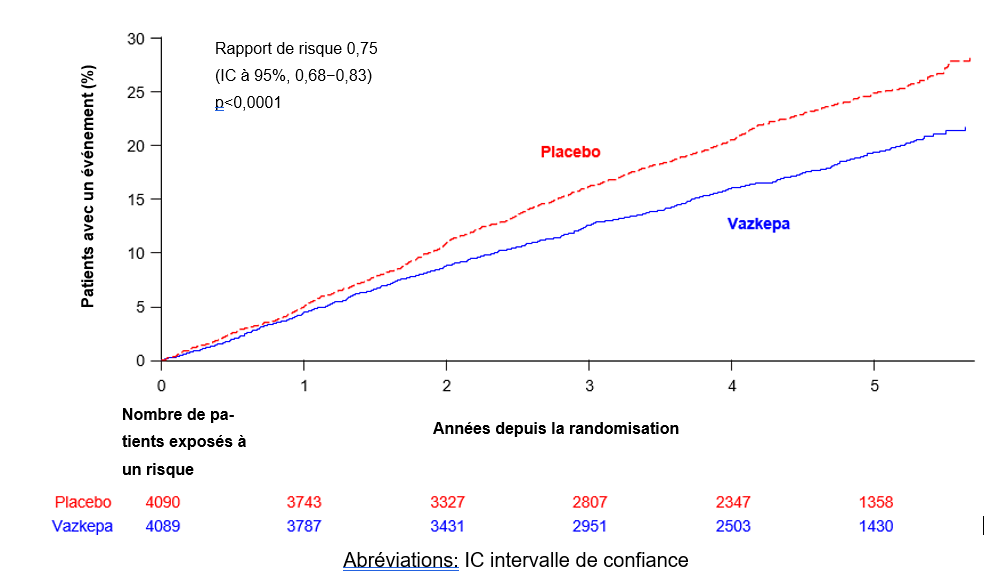
Les taux de TG et LDL-C médians à l’inclusion étaient comparables entre le groupe icosapent éthyl et le groupe placebo. L’évolution médiane des TG de l’inclusion à l’an 1 était de -0,4 mmol/l (-39 mg/dl, -18%) dans le groupe icosapent éthyl et 0,1 mmol/l (5 mg/dl, 2%) dans le groupe placebo. L’évolution médiane du LDL-C de l’inclusion à l’an 1 était de 0,1 mmol/l (2 mg/dl, 3%) dans le groupe icosapent éthyl et 0,2 mmol/l (7 mg/dl, 10%) dans le groupe placebo. Des analyses prédéfinies de l’effet de l’icosapent éthyl sur les résultats cardiovasculaires dans l’étude REDUCE-IT ont montré peu ou pas de corrélation entre la réponse soit des TG soit du LDL-C et les effets cardiovasculaires, sur la base des taux de TG ou de LDL-C obtenus à l’inclusion ou durant l’étude. Pour plus d’informations, voir «Mécanisme d’action».
Pédiatrie
Swissmedic a accordé une dérogation à l’obligation de soumettre les résultats d’études réalisées avec l’icosapent éthyl dans tous les sous-groupes de la population pédiatrique pour le traitement de l’hypertriglycéridémie et pour réduire le risque d’événement cardiovasculaire (voir «Posologie/Mode d’emploi» pour les informations concernant l’usage chez les enfants et les adolescents).
|

