CompositionPrincipes actifs
Isoflurane
Excipients
Aucun
Indications/Possibilités d’emploiSedaconda® est indiqué pour la sédation des patients adultes sous ventilation artificielle pendant les soins intensifs.
Posologie/Mode d’emploiL'expérience de l'utilisation continue de l'isoflurane pendant une durée supérieure à 48 heures est limitée. Si l'isoflurane est utilisé au-delà de cette période, il convient de réévaluer régulièrement la nécessité de l'utiliser.
Durant la sédation, une évaluation clinique de la profondeur de sédation au moyen d'une échelle de sédation clinique validée, telle que la Richmond Agitation-Sedation Scale (RASS), doit être utilisée pour ajuster la dose. Un équipement adéquat doit être disponible pour mesurer la concentration d’isoflurane administrée et la concentration de fin d’expiration.
L'amorçage et l'administration de bolus ne doivent jamais être réalisés manuellement (voir le mode d’emploi fourni avec le dispositif d’administration Sedaconda® ACD (Anaesthetic Conserving Device)).
Posologie
Amorçage
Lors de l’instauration du traitement, la tubulure d’alimentation en agent anesthésique du dispositif d’administration Sedaconda® ACD doit être amorcée avec un volume de 1,2 ml d’isoflurane.
Dose initiale et adaptation de la dose
Le débit de pousse-seringue initial recommandé est de 3 ml/heure. Les adaptations de débit du pousse-seringue doivent être effectuées par paliers de 0,5–1,0 ml/heure. Pour augmenter la sédation rapidement, un bolus programmé de 0,3–0,5 ml peut être administré via le pousse-seringue. L'administration d'autres sédatifs peut normalement être arrêtée une fois que le traitement a démarré.
Dose d’entretien
Le débit du pousse-seringue pour un objectif de sédation déterminé doit être ajusté afin de correspondre à la ventilation minute (VM) du patient. L'augmentation de la VM nécessite généralement une augmentation du débit du pousse-seringue pour maintenir les concentrations de fin d'expiration d’isoflurane et le niveau de sédation requis.
En l’absence d'autres sédatifs, mais avec l'administration continue d'opioïdes intraveineux, le débit d'entretien typique du pousse-seringue pour obtenir un score RASS compris entre -1 et -4 est d'environ 0,4 ml/heure par litre de VM, ce qui se traduit par un débit de pousse-seringue d’environ 3 ml/heure pour un patient ayant une VM de 7 l. Le débit du pousse-seringue doit être ajusté à l’objectif de sédation spécifique en prenant en compte l’âge du patient et sa condition médicale, ainsi que les médicaments à action centrale concomitants. Des débits de pousse-seringue allant jusqu’à 14 ml/heure peuvent être requis. Les besoins posologiques n'augmentent en principe pas avec le temps, sauf si les médicaments à action centrale concomitants sont interrompus pendant le traitement.
La concentration de fin d’expiration maximale recommandée à long terme durant la sédation est de 1,0 %, bien qu’une concentration allant jusqu’à 1,5 % puisse être utilisée sur de courtes périodes, par exemple pendant des interventions brèves nécessitant une sédation légèrement plus profonde. Pour effectuer des interventions brèves ou pour augmenter la sédation rapidement, un bolus programmé de 0,3–0,5 ml peut être administré via le pousse-seringue.
Durant des procédures impliquant la voie d'administration (par ex. la trachée), telles qu’une bronchoscopie, d'autres médicaments à courte durée d’action peuvent être nécessaires pour maintenir une sédation adéquate.
Évaluation clinique du niveau de sédation
Au cours des deux premières heures, ou jusqu’à ce que la profondeur de sédation cible ait été atteinte et soit stable, il est conseillé de procéder à des évaluations fréquentes du niveau de sédation au moyen d’une échelle de sédation validée afin de guider l’ajustement de la dose. Par la suite, la profondeur de sédation doit être évaluée au minimum toutes les 4 heures.
Durant un bloc neuromusculaire continu, il peut être difficile de procéder à une évaluation clinique de la profondeur de sédation. Chez ces patients, la concentration d’isoflurane de fin d’expiration fournit des informations plus pertinentes.
Patients âgés
Chez les adultes, l’âge avancé est associé à une sensibilité plus élevée à l’isoflurane; dès lors, les besoins posologiques sont normalement plus faibles chez les patients âgés.
Patients avec insuffisance rénale
Aucun ajustement de la dose n'est nécessaire chez les patients atteints d’insuffisance rénale (cf. «Pharmacocinétique»).
Patients avec insuffisance hépatique
Aucun ajustement de la dose n'est nécessaire chez les patients atteints d’insuffisance hépatique. L’isoflurane doit être utilisé avec prudence chez les patients atteints de cirrhose, d’hépatite virale ou d'une autre maladie hépatique préexistante (cf. «Pharmacocinétique»).
Enfants et adolescents
La sécurité et l’efficacité de Sedaconda® chez les enfants et les adolescents de moins de 18 ans n’ont pas été établies. L'utilisation dans ce groupe d'âge n'est donc pas recommandée.
Mode d'administration
Sedaconda® est destiné à être inhalé.
Sedaconda® doit uniquement être administré via le dispositif d’administration Sedaconda® ACD et être délivré au moyen de la seringue Sedaconda®, remplie à l'aide de l’adaptateur de remplissage Sedaconda®. Sedaconda® ACD est un échangeur de chaleur et d'humidité passif modifié (ECH) et, en tant que tel, ajoute un espace mort au circuit respiratoire. L’état ventilatoire du patient doit être pris en considération lors du choix de la taille du Sedaconda® ACD. Des instructions d'utilisation sont disponibles dans «Remarques particulières»/«Remarques concernant la manipulation» et à la fin de l'information professionnelle sous «Mode d'emploi pour la mise en place de l'adaptateur de remplissage Sedaconda® sur le flacon Sedaconda®».
Élimination de l'isoflurane expiré
Il est recommandé de purger l'isoflurane restant dans le respirateur afin de réduire la concentration d'isoflurane dans l'environnement. Cela peut se faire par une récupération passive des gaz ou par un système d'aspiration actif.
Contre-indications-Patients présentant une hypersensibilité connue ou suspectée à l'isoflurane ou à d'autres agents anesthésiques inhalés halogénés (par ex. patients ayant des antécédents de troubles de la fonction hépatique, d'ictère, de fièvre, de leucocytose (augmentation du nombre de globules blancs) ou d'éosinophilie d'origine indéterminée après l'utilisation d'une de ces substances).
-Prédisposition génétique connue ou suspectée à l’hyperthermie maligne.
Mises en garde et précautionsSedaconda® ne doit être administré que par du personnel médical adéquatement formé à la prise en charge des patients sous ventilation artificielle dans des locaux de soins intensifs équipés à cet effet.
Hyperthermie maligne
Chez les patients prédisposés, l’isoflurane peut induire un état d’hypermétabolisme des muscles squelettiques, entraînant des besoins élevés en oxygène et induisant un syndrome clinique connu sous le nom d‘hyperthermie maligne. Ce syndrome comprend des symptômes non spécifiques, tels qu’une rigidité musculaire, une tachycardie, une tachypnée, une cyanose, des arythmies et/ou des pressions artérielles instables. Certains de ces signes non spécifiques peuvent également apparaître lors d'une sédation légère, d’une hypoxie aiguë, etc.
Des cas d’hyperthermie maligne ont été signalés dans le cadre de la surveillance post-commercialisation, dont certains ont été fatals.
Le traitement de l’hyperthermie maligne consiste en l’arrêt du facteur déclenchant (par ex. isoflurane), en l’administration intraveineuse de dantrolène sodique (cf. information sur le médicament du dantrolène sodique i.v. pour des informations supplémentaires sur le traitement des patients) et en des mesures de soutien. Cela comprend des mesures visant à normaliser la température corporelle, à fournir un soutien respiratoire et circulatoire et à corriger les déséquilibres électrolytes-fluides-acides-bases. Une insuffisance rénale peut apparaître ultérieurement, raison pour laquelle le débit urinaire doit être contrôlé et, si possible, maintenu.
Maladies hépatiques
Des cas rapportés démontrent que l’isoflurane peut induire des lésions hépatiques allant d'augmentations légères réversibles des enzymes hépatiques à une nécrose hépatique fatale dans de très rares cas. Il a été rapporté qu’une exposition antérieure à des anesthésiques à base d’hydrocarbures halogénés, surtout si l’exposition remonte à ≤3 mois, peut augmenter le risque de lésions hépatiques.
La prudence est de mise chez les patients souffrant d'une maladie hépatique préexistante ou chez les patients prenant des médicaments connus pour altérer la fonction hépatique.
Hyperkaliémie
L’utilisation d’agents anesthésiques inhalés a été associée à de rares augmentations des taux de potassium sérique, qui ont entraîné des arythmies cardiaques et le décès chez des patients pédiatriques au cours de la période post-opératoire. Les patients présentant une maladie neuromusculaire latente ou manifeste, en particulier la myopathie de Duchenne, paraissent être les plus vulnérables. Dans la plupart des cas, de la succinylcholine avait été administrée concomitamment. Les patients ont en outre présenté des élévations significatives des valeurs de créatine kinase et, dans certains cas, des modifications des urines compatibles avec une myoglobinurie. Malgré une présentation similaire à celle de l'hyperthermie maligne, aucun de ces patients n’a montré de signes ou de symptômes de rigidité musculaire ou d’état hypermétabolique. Une intervention précoce et agressive visant à traiter l’hyperkaliémie et les arythmies résistantes est nécessaire, tout comme une évaluation ultérieure visant à détecter une maladie neuromusculaire latente.
Neurotoxicité pédiatrique
Des études précliniques montrent que l'utilisation d'anesthésiques ou de sédatifs (fluranes, propofol, kétamine) qui bloquent les récepteurs NMDA et/ou renforcent l'activité GABA entraîne une perte de cellules dans le cerveau en développement pendant la période de croissance cérébrale rapide ou de synaptogenèse, ce qui peut être associé à des déficits cognitifs durables. La signification clinique de ces résultats n'est pas connue (cf. «Grossesse, Allaitement» et «Données précliniques»).
Maladies cardiaques et rénales
Sedaconda® doit être utilisé avec prudence chez les patients souffrant de maladies cardiaques ou rénales. Le maintien d’une hémodynamique normale est indispensable pour éviter une ischémie myocardique chez les patients présentant une coronaropathie.
Des cas d'allongement de l’intervalle QT, associés à des torsades de pointes (fatals dans certains cas exceptionnels), ont été décrits. La prudence est requise lorsque l’isoflurane est administré à des patients ayant un risque d'allongement de l’intervalle QT.
L’isoflurane doit être administré avec prudence chez les patients souffrant de maladies mitochondriales. Une hypotension et une dépression respiratoire peuvent se produire à mesure que la dose d’isoflurane est augmentée et que la sédation est plus profonde.
L'isoflurane doit être utilisé avec prudence chez les patients présentant une pression intracrânienne élevée (cf. également «Propriétés/Effets»). Dans ces cas, un monitorage neurochirurgical étendu est nécessaire.
L'isoflurane doit être utilisé avec prudence chez les patients susceptibles de développer une bronchoconstriction, car des bronchospasmes peuvent survenir.
L'isoflurane peut déclencher une dépression respiratoire, qui peut être renforcée par d'autres médicaments susceptibles de provoquer une dépression respiratoire. L'isoflurane, comme d'autres anesthésiques inhalés, entraîne une relaxation des muscles utérins chez les femmes enceintes et non enceintes, ce qui augmente le risque d'hémorragie utérine, par exemple après un curetage utérin.
Fin de la sédation
L'isoflurane peut entraîner une légère diminution des capacités intellectuelles pendant 2-4 jours après la fin de la sédation. De même, des changements d'humeur peuvent persister jusqu'à 6 jours après l'administration.
Myasthénie grave
Les patients atteints de myasthénie grave sont particulièrement sensibles aux préparations qui provoquent une dépression respiratoire. L'isoflurane doit donc être utilisé avec prudence chez ces personnes.
Enfants et adolescents
La sécurité et l’efficacité de Sedaconda® chez les enfants et les adolescents de moins de 18 ans n’ont pas été établies. L'utilisation dans ce groupe d'âge n'est donc pas recommandée.
InteractionsAssociations déconseillées:
Inhibiteurs de la monoamine-oxydase (IMAO) non sélectifs:
Risque de crise durant la sédation. L’utilisation d’isoflurane doit être évitée pendant 15 jours après la dernière prise d'un IMAO.
Inducteurs du CYP2E1:
Les médicaments et préparations qui augmentent l'activité de l'isoenzyme CYP2E1 du cytochrome P450, comme l'isoniazide ou l'alcool, peuvent augmenter le métabolisme de l'isoflurane, ce qui entraîne des augmentations significatives des concentrations de fluorure plasmatique.
L'administration concomitante d'isoflurane avec les préparations suivantes nécessite une surveillance stricte des fonctions cliniques et biologiques du patient:
Bêtabloquants:
Risque de blocage du mécanisme de compensation cardiovasculaire, avec pour conséquence une augmentation des effets inotropes négatifs.
Sympathomimétiques, catécholamines:
Les bêta-sympathomimétiques (isoprénaline) et les catécholamines (adrénaline et noradrénaline) doivent être utilisés avec prudence pendant la sédation par isoflurane en raison du risque potentiel d'arythmie ventriculaire.
Sympathomimétiques à action indirecte (amphétamines et leurs dérivés, psychostimulants, anorexigènes, éphédrine et ses dérivés):
Risque d'hypertension artérielle. L'utilisation de l'isoflurane devrait idéalement être évitée pendant plusieurs jours après la dernière prise de sympathomimétiques à action indirecte.
Myorelaxants:
L’action de tous les myorelaxants d'utilisation courante est significativement potentialisée par l’isoflurane, l’effet étant le plus prononcé avec les myorelaxants non-dépolarisants. La néostigmine antagonise l'effet des myorelaxants non-dépolarisants, mais n'a pas d’effet sur l’effet myorelaxant de l’isoflurane lui-même. Il est donc recommandé d'administrer environ un tiers à la moitié de la dose habituelle de ces substances. La disparition de l'effet neuromusculaire est plus longue avec l'isoflurane qu'avec d'autres anesthésiques conventionnels.
L'administration simultanée de succinylcholine et d'anesthésiques inhalés a été associée à des augmentations inhabituelles des concentrations sériques de potassium, ce qui a entraîné des arythmies cardiaques et des décès chez des patients pédiatriques pendant la période postopératoire.
Analgésiques morphiniques, benzodiazépines et autres médicaments sédatifs:
Ces médicaments potentialisent l'effet dépresseur respiratoire de l'isoflurane et ne doivent être utilisés qu'avec prudence simultanément à l'isoflurane.
Antagonistes calciques:
L'isoflurane peut induire une hypotension marquée chez les patients traités par antagonistes calciques, en particulier dérivés des dihydropyridines. La prudence est de rigueur lorsque les antagonistes calciques sont utilisés en association avec des anesthésiques inhalés, y compris l’isoflurane, en raison du risque d’effet inotrope négatif additif.
Adrénaline en injections sous-cutanées ou gingivales:
Il existe un risque d'arythmies ventriculaires graves dues à l’accélération de la fréquence cardiaque. Des données limitées suggèrent que l’infiltration sous-cutanée de maximum 0,25 mg (50 ml d’une solution à 1:200 000) d’adrénaline chez un adulte de 70 kg n’induit pas d’arythmies ventriculaires en l'absence d'hypoxie myocardique coexistante.
Isoniazide:
L’utilisation concomitante d’isoflurane et d’isoniazide peut augmenter le risque de potentialisation des effets hépatotoxiques.
Grossesse, AllaitementGrossesse
Les études chez l'animal conduites avec l'isoflurane à des concentrations anesthésiques n'ont montré aucun effet négatif sur la fertilité, la grossesse ou l'accouchement, ni sur les fœtus.
Étant donné qu'il n'existe pas d'études cliniques contrôlées menées chez des femmes enceintes, Sedaconda® ne doit pas être utilisé pendant la grossesse, sauf si cela s'avère clairement nécessaire.
L'isoflurane, comme d'autres anesthésiques inhalés, entraîne une relaxation des muscles utérins, ce qui augmente le risque d'hémorragie utérine.
Des études chez l'animal publiées, qui ont été conduites avec des anesthésiques/sédatifs, ont fait état d'effets indésirables sur le développement cérébral à un stade précoce (cf. «Mises en garde et précautions» et «Données précliniques»).
Il est admis que Sedaconda® traverse la barrière placentaire et peut entraîner des déficits cognitifs durables chez le nouveau-né.
Allaitement
On ne sait pas si l'isoflurane est excrété dans le lait maternel et il doit donc être utilisé avec prudence chez les mères qui allaitent.
Fertilité
Aucune donnée de fertilité issue de l’utilisation de l’isoflurane chez l’homme n’est disponible. Les études effectuées chez l’animal n’ont pas mis en évidence d’effets sur la fertilité mâle ou femelle (cf. «Données précliniques»).
Effet sur l’aptitude à la conduite et l’utilisation de machinesCe médicament peut affecter l’aptitude à conduire des véhicules et à utiliser des machines. Le patient ne doit pas conduire de véhicules ni utiliser des machines pendant au moins 24 heures après la sédation par isoflurane. Des modifications du comportement et de la fonction intellectuelle peuvent persister jusqu’à 6 jours après la sédation par isoflurane. Il faut en tenir compte lorsque le patient reprend ses activités quotidiennes habituelles, y compris la conduite ou l’utilisation de machines.
Effets indésirablesLes effets indésirables rencontrés lors de l’administration de Sedaconda®, tels que dépression respiratoire, hypotension ou arythmies cardiaques, sont en général des exacerbations dose-dépendantes des effets pharmacologiques.
Les effets indésirables graves potentiels comprennent une hyperthermie maligne, des réactions anaphylactiques/anaphylactoïdes et des réactions indésirables hépatiques (nécrose hépatique avec issue fatale, cf. «Mises en garde et précautions»). Des arrêts cardiaques ont été observés en lien avec des anesthésiques inhalés, y compris l'isoflurane.
Les effets indésirables signalés dans le cadre des études cliniques et de la surveillance post-commercialisation sont énumérés ci-dessous. Les effets indésirables ont été classés par système d'organes.
Les fréquences ont été classées selon la convention suivante: très fréquent (≥ 1/10), fréquent (≥ 1/100 à < 1/10), occasionnel (≥ 1/1 000 à < 1/100), rare (≥ 1/10 000 à < 1/1 000), très rare (< 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Affections du sang et du système lymphatique
Fréquence indéterminée:
Augmentation temporaire de la numération leucocytaire (cf. Description des effets indésirables spécifiques et informations complémentaires)
Affections du système immunitaire
Fréquence indéterminée:
Réactions anaphylactiques, hypersensibilité (cf. Description des effets indésirables spécifiques et informations complémentaires)
Troubles du métabolisme et de la nutrition
Fréquence indéterminée:
Hyperkaliémie1, augmentation de la glycémie
Affections psychiatriques
Fréquent:
Agitation, delirium, altération de l’humeur2
Affections du système nerveux
Fréquence indéterminée:
Anomalies à l'électroencéphalogramme, altérations de la fonction mentale3
Affections cardiaques
Fréquent:
Tachycardie sinusale, tachycardie
Fréquence indéterminée:
Arythmies cardiaques, bradycardie, arrêt cardiaque, allongement de l'intervalle QT (exceptionnellement avec issue fatale), torsade de pointes, diminution des concentrations sanguines de cholestérol
Affections vasculaires
Fréquent:
Hypotension
Affections respiratoires, thoraciques et médiastinales
Fréquence indéterminée:
Bronchospasme, dyspnée, respiration sifflante, dépression respiratoire, laryngospasme
Affections gastro-intestinales
Fréquent:
Vomissements, nausées
Fréquence indéterminée:
Iléus
Affections hépatobiliaires
Fréquence indéterminée:
Nécrose hépatique1, lésions hépatocellulaires1, élévation des enzymes hépatiques1, élévation de la bilirubinémie, diminution de la concentration sanguine de phosphatase alkaline
Affections de la peau et du tissu sous-cutané
Fréquence indéterminée:
Gonflement du visage, dermatite de contact, éruption cutanée
Affections musculo-squelettiques, du tissu conjonctif et osseuses
Fréquence indéterminée:
Myoglobinurie, rhabdomyolyse, concentration accrue de créatine phosphokinase
Affections du rein et des voies urinaires
Fréquent:
Augmentation de la créatininémie
Fréquence indéterminée:
Augmentation de la concentration de fluorure (cf. Description des effets indésirables spécifiques et informations complémentaires), diminution de l’urée sanguine
Troubles généraux et anomalies au site d’administration
Fréquence indéterminée:
Frissons, hyperthermie maligne4, douleurs thoraciques.
1 cf. «Mises en garde et précautions».
2 De faibles altérations de l'humeur et symptômes peuvent persister durant jusqu'à six jours (cf. «Mises en garde et précautions»).
3 Peut provoquer une légère diminution des fonctions intellectuelles pendant 2 à 4 jours après la sédation (cf. «Mises en garde et précautions»).
4 Cf. «Contre-indications».
Description des effets indésirables spécifiques et informations complémentaires
Numération leucocytaire
Des hausses transitoires du nombre de globules blancs ont été observées, même en l’absence de stress chirurgical.
Fluorure inorganique sérique
Une légère élévation des taux sériques de fluorure inorganique peut survenir pendant et après la sédation par isoflurane, en raison du faible degré de biodégradation du médicament.
Réactions d’hypersensibilité
Dans de rares cas, une hypersensibilité (incluant dermatite de contact, rash, dyspnée, respiration sifflante, douleurs thoraciques, gonflement du visage ou réaction anaphylactique/anaphylactoïde allant jusqu’au choc) a été rapportée, particulièrement en association avec une exposition professionnelle à long terme à des anesthésiques inhalés, dont l’isoflurane. Ces réactions ont également été confirmées par des tests cliniques (par ex. test de provocation à la méthacholine). L'étiologie des réactions anaphylactiques observées sous anesthésiques inhalés n'est toutefois pas claire, en raison de l'effet biaisant en cas d'exposition simultanée à plusieurs médicaments, dont beaucoup sont connus pour pouvoir provoquer de telles réactions.
L’annonce d’effets secondaires présumés après l’autorisation est d’une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d’effet secondaire nouveau ou grave via le portail d’annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageSignes et symptômes
Des concentrations plus élevées d’isoflurane peuvent induire une hypotension et une dépression respiratoire.
Traitement
Il est dès lors recommandé de surveiller étroitement la pression artérielle et la respiration. En cas de surdosage sévère, l'administration d'isoflurane doit être interrompue et le dispositif d’administration Sedaconda® ACD retiré. Dans les cas moins sévères, on arrêtera le pousse-seringue jusqu’à ce que la concentration d’isoflurane ait diminué. Des mesures de soutien peuvent s’avérer nécessaires pour corriger l’hypotension et la dépression respiratoire dues à une sédation trop profonde.
Propriétés/EffetsCode ATC
N01AB06
Mécanisme d’action
Bien que le mécanisme exact de l'action anesthésique ne soit pas entièrement élucidé, il est généralement établi que les anesthésiques volatils modifient la fonction neuronale en modulant la transmission synaptique excitatrice et inhibitrice. Il est admis que l’action anesthésique de l’isoflurane repose sur des mécanismes multiples (par ex. effets agonistes exercés sur les canaux ioniques régulés par les neurotransmetteurs, tels que les récepteurs de l'acide gamma aminobutyrique (GABA) et les récepteurs de la glycine, ainsi qu’effets antagonistes exercés sur les récepteurs N-méthyl-D-aspartate (NMDA) dans le système nerveux central) et induit/contribue à l’amnésie et la sédation. Les anesthésiques volatils possèdent aussi généralement des sites d'action au niveau de la moelle épinière, qui contribuent à la relaxation des muscles squelettiques et à l’inhibition de la signalisation nociceptive afférente.
Pharmacodynamique
Chez les patients sous ventilation mécanique, l'isoflurane induit une sédation dose-dépendante à des concentrations de fin d’expiration d'environ 0,2 % à 1,0 %.
L’isoflurane présente une faible solubilité (coefficient de partage sang/gaz: 1,4). Cela permet un démarrage et une récupération rapides et prévisibles de la sédation. Le retour à l'état d'éveil, défini comme le délai jusqu’à l’obtention d’un score RASS ≥ 0 (calme et éveillé) et d’une récupération cognitive, évaluée sur la base de la capacité à réagir à des commandes verbales, se produit généralement entre 10 et 60 minutes suivant la fin de l'administration d’isoflurane.
La pression artérielle est réduite en relation directe avec l'augmentation des concentrations d’isoflurane, essentiellement sous l'effet d’une vasodilatation périphérique (cf. «Mises en garde et précautions»).
L’isoflurane exerce un effet vasodilatateur dans le cerveau.
L’isoflurane à 0,6 % et la présence de concentrations plus élevées en fin d’expiration induisent une bronchodilatation en réduisant le tonus des muscles lisses des voies respiratoires chez les patients réfractaires aux β-agonistes. Ce mécanisme peut faire intervenir de l’oxyde nitrique et des prostaglandines libérés par l’endothélium.
Efficacité clinique
L’efficacité et la sécurité de Sedaconda® pour l’anesthésie au moyen du dispositif d'administration Sedaconda® ACD (Anaesthetic Conserving Device) chez les patients sous ventilation mécanique ont été évaluées dans un essai clinique randomisé, contrôlé, en ouvert et multicentrique, SED001. Cette étude incluait une cohorte mixte composée de patients chirurgicaux et médicaux avec un score moyen (ET) au Simplified Acute Physiology Score II (SAPS II) de 43,1 (± 17,7) et nécessitant une ventilation mécanique et une sédation visant un score RASS cible compris entre –1 et –4. Les patients ont été randomisés pour recevoir de l’isoflurane (n=150) ou du propofol (n=151) en tant que sédatifs uniques pendant jusqu’à 48 ± 6 heures ou jusqu’à l’extubation, selon l’événement survenant en premier. Des opioïdes par voie intraveineuse ont été administrés selon les besoins, sur la base de l'échelle Behavioural Pain Scale (BPS). Les patients toujours intubés au bout de 48 ± 6 heures ont été reconvertis aux soins standards.
Critères d’évaluation de l’efficacité
Efficacité de la sédation dans l’étude SED001
Il a été démontré que Sedaconda® était non inférieur au propofol en termes de délai jusqu’à l’atteinte de la profondeur de sédation cible (RASS –1 à –4) (différence de proportions isoflurane versus propofol -0,452 %, IC 95 % -2,996 à 2,093). Les patients ont passé plus de 90 % du temps dans la profondeur de sédation cible avec l’isoflurane tout comme avec le propofol. Le score RASS moyen pour le Jour 1 et le Jour 2 du traitement respectif était comparable. Chez les patients traités par isoflurane, le débit moyen (ET) du pousse-seringue était de 0,4 (± 0,2) ml/heure par litre de ventilation minute. Cela s’est traduit par une concentration moyenne (ET) d’isoflurane de fin d’expiration de 0,45 (±0,2) %.
Reprise de conscience et temps jusqu’à l’extubation
Dans l'étude SED001, la durée jusqu'à la reprise de conscience (test de réveil) a été mesurée après 24 et 48 heures en tant que durée entre la fin de la sédation continue et le moment où le RASS était ≥0 (éveillé et calme). Après 24 heures, près de 80 % des patients des deux bras ont passé avec succès un test de réveil. Après 48 heures, 77 % des patients sous isoflurane et 65 % des patients sous propofol ont passé avec succès un test de réveil.
Pédiatrie
Il n’existe pas de données d’efficacité issues d'études contrôlées ayant évalué l’isoflurane à des fins de sédation chez les enfants, mais l’isoflurane a été utilisé comme sédatif chez les enfants. Plusieurs études de petite envergure ont noté des doses d’anesthésique similaires à celles rapportées dans les études menées chez l’adulte.
Dans plusieurs études, des troubles neurologiques réversibles ont été observés chez des enfants, principalement lorsqu’ils avaient reçu une sédation par isoflurane pendant plus de 24 heures. Les symptômes neurologiques rapportés étaient l’ataxie, l’agitation, les mouvements involontaires, les hallucinations et la confusion, persistant pendant une période allant jusqu’à 72 heures.
PharmacocinétiqueAbsorption
En raison de sa solubilité sanguine relativement faible (coefficient de partage sang/gaz de 1,43), les délais d’afflux et d’efflux de l’isoflurane sont courts. Les facteurs qui influencent également la vitesse d’afflux et d’efflux sont la ventilation alvéolaire, le débit cardiaque et la concentration inspiratoire.
Distribution
La distribution de l'isoflurane dans les tissus de l'organisme dépend de leur degré de perfusion sanguine et du coefficient de distribution correspondant. Les organes bien perfusés, comme le cerveau, le foie, le cœur et les reins, sont saturés au cours d'une anesthésie prolongée, tandis que les tissus moins bien perfusés, comme le tissu adipeux et les muscles, ne le sont pas. La capacité d'absorption de l'organisme entier est loin d'être saturée par ex. après une durée d'exposition de 60 minutes et une concentration de 1,5 % vol.
Métabolisme
L’isoflurane subit une biotransformation minime chez l’homme. Moins de 0,2 % de l’isoflurane absorbé est retrouvé sous la forme de métabolites urinaires inactifs. Le métabolisme est dépendant du CYP2E1 et débute par une oxydation, entraînant la production d’acide trifluoroacétique (TFA) et de difluorométhanol. Le difluorométhanol est ensuite métabolisé en ion fluorure.
Élimination
L’élimination d’isoflurane s’effectue quasi exclusivement sous forme inchangée via les voies respiratoires. En moyenne, 95 % de l’isoflurane sont éliminés par cette voie.
Cinétique pour certains groupes de patients
Insuffisance rénale
Aucune étude pharmacocinétique n’a été réalisée chez les patients présentant une insuffisance rénale. Toutefois, comme l’excrétion rénale de l’isoflurane est minime, aucun effet sur l’exposition à l’isoflurane n'est anticipé chez les patients ayant une altération de la fonction rénale (cf. «Posologie/Mode d’emploi»).
Insuffisance hépatique
Aucune étude pharmacocinétique n’a été réalisée chez les patients présentant une insuffisance hépatique. Toutefois, compte tenu du métabolisme minime de l’isoflurane, aucun effet sur l’exposition à l’isoflurane n'est anticipé chez les patients ayant une altération de la fonction hépatique (cf. «Posologie/Mode d’emploi» et «Mises en garde et précautions»).
Données précliniquesMutagénicité/carcinogénicité
Des études de génotoxicité ont montré que l'isoflurane n'a pas de potentiel mutagène. Un essai biologique sur des souris a également montré que l'isoflurane n'a pas de potentiel cancérigène.
Toxicité pour la reproduction et le développement
Des études publiées menées chez des animaux (y compris des primates) démontrent que l’utilisation d'agents anesthésiques ou sédatifs (fluranes, propofol, kétamine) qui bloquent les récepteurs NMDA et/ou renforcent l'activité GABA au cours de la période de développement cérébral rapide ou de synaptogenèse entraîne une perte cellulaire dans le cerveau en développement, pouvant s'associer à des déficits cognitifs de longue durée. La signification clinique de ces observations non cliniques n’est pas connue.
Les effets sur la fertilité ont été étudiés chez des rats mâles et femelles exposés à des concentrations anesthésiques d’isoflurane avant l'accouplement. L’isoflurane n’a eu aucun effet sur la fertilité mâle ou femelle. Des études menées sur des souris femelles exposées à l’isoflurane avant et pendant la gestation ainsi que sur des souris mâles exposées à l’isoflurane pendant toute la période de spermatogenèse et durant l'accouplement n'ont mis en évidence aucun effet indésirable sur la reproduction.
Remarques particulièresIncompatibilités
Aucune connue.
Influence sur les méthodes de diagnostic
Une augmentation temporaire de la rétention du BSP, de la glycémie et de la créatinine sérique a été observée, avec une diminution du BUN, du cholestérol et de la phosphatase alcaline.
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date indiquée sur l'emballage par «EXP».
Délai d'utilisation après la mise en place de l'adaptateur de remplissage Sedaconda®: 14 jours.
Remarques particulières concernant le stockage
Conserver hors de portée des enfants.
Conserver à l'abri de la lumière et à une température ne dépassant pas 30°C.
Remarques concernant la manipulation
Sedaconda® ne doit être utilisé qu'avec le dispositif d’administration Sedaconda® ACD prévu à cet effet.
Sedaconda® doit être à température ambiante au moment de son utilisation. La taille du dispositif d’administration Sedaconda® ACD dépend de l'état ventilatoire du patient et de la tolérance de l'espace mort (voir le mode d’emploi fourni avec le dispositif d’administration Sedaconda® ACD).
Fixer l'adaptateur de remplissage Sedaconda® (disponible séparément) sur le flacon Sedaconda® conformément au mode d'emploi figurant à la fin de l'information professionnelle.
Dès que l'adaptateur de remplissage et son capuchon de protection sont fixés au flacon, ils remplacent le couvercle à vis. Le capuchon de protection de l'adaptateur doit être placé sur l'adaptateur entre les utilisations.
Numéro d’autorisation68359 (Swissmedic)
PrésentationCartons de 6 flacons de 100 ml: (B)
Cartons de 6 flacons de 250 ml: (B)
Titulaire de l’autorisationmmpharm GmbH, Cham
Mise à jour de l’informationJuillet 2022
Mode d’emploi.
|
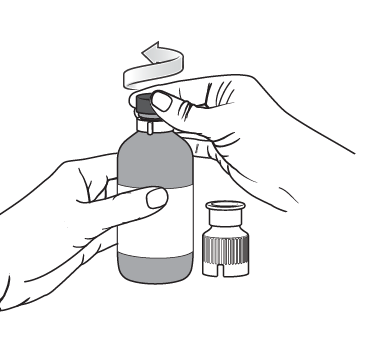
Étape 1
Retirer le film de protection et dévisser le couvercle original du flacon.
|
|
| |
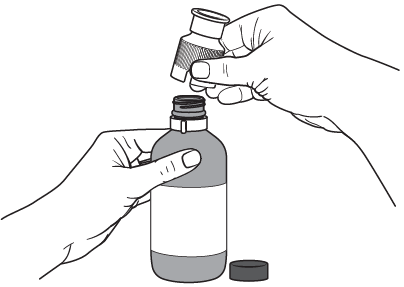
Étape 2
Placer l'adaptateur de remplissage Sedaconda® (disponible séparément) sur le flacon ouvert et l'orienter de manière à ce que les marques apposées coïncident.
|
|
| |
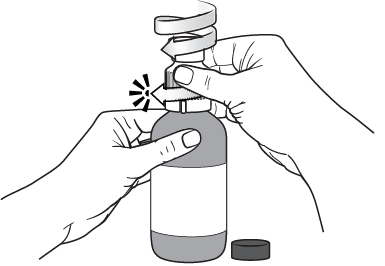
Étape 3
Visser l'adaptateur de remplissage jusqu'à ce qu'un clic se fasse entendre et qu'il ne soit plus possible de tourner davantage.
|
|
| |
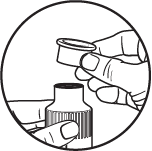
Étape 4
Retirer le capuchon de protection de l'adaptateur de remplissage.
|
|
| |
Étape 5
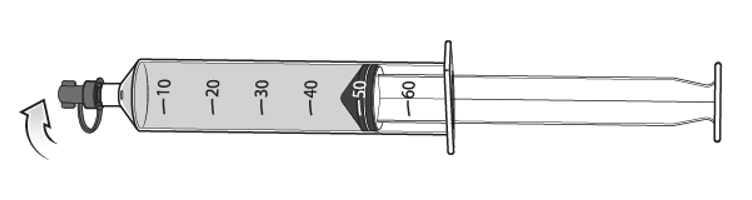
Ouvrir le capuchon de la seringue de 50 ml.
|
|

| |
Étape 6
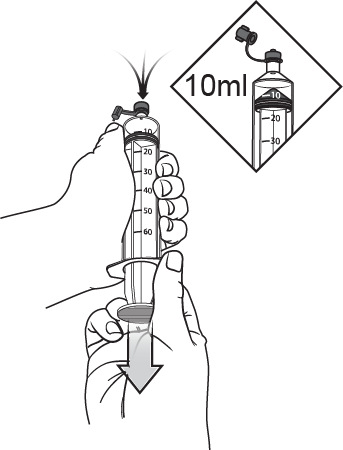
Aspirer 10 ml d'air dans la seringue.
|
|
| |
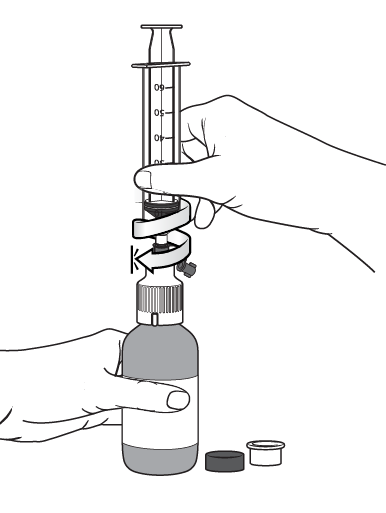
Étape 7
Introduire la seringue de 50 ml verticalement dans l'adaptateur de remplissage jusqu'à l'arrêt.
|
|
| |
Étape 8
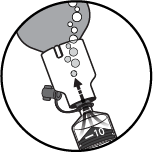
Pousser les 10 ml d'air dans le flacon afin de le mettre sous pression et d'empêcher la vapeur de s'échapper.
|
|

|
| |
Étape 9
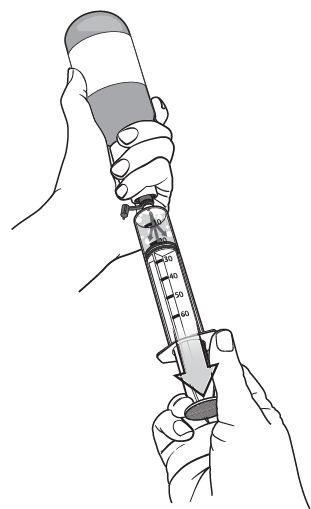
Éjecter un peu de vapeur.
|
|
| |
Étape 10
Tirer sur la seringue jusqu'à ce que des bulles de gaz visibles se forment dans la seringue.
|
|
| |
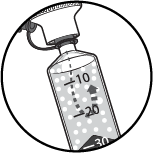
Étape 11
Tenir la seringue et le flacon de manière à ce que les bulles de gaz s'accumulent dans la partie supérieure de la seringue. Renvoyer le gaz contenu dans la seringue dans le flacon.
|
|

| |
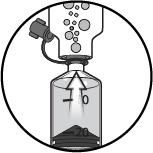
Étape 12
S'assurer que les bulles sont ramenées dans le flacon. Si nécessaire, répéter les étapes 9 à 12.
|
|
| |
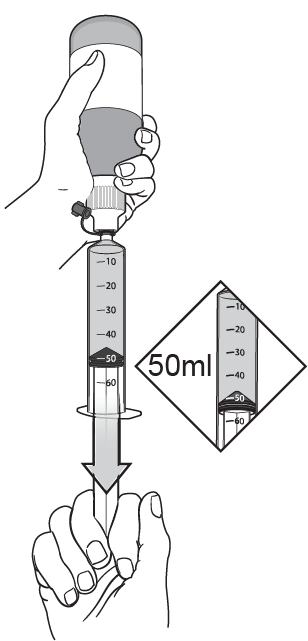
Étape 13
Prélever 50 ml de liquide du flacon.
|
|
| |
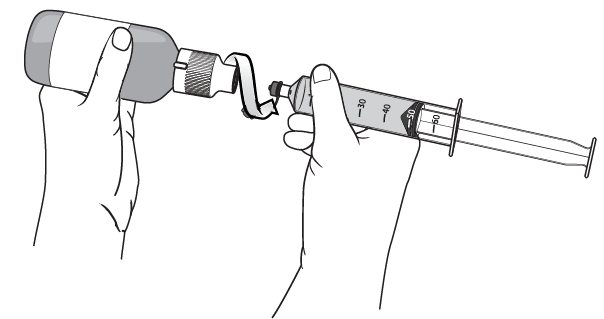
Étape 14
Tenir le flacon et la seringue à l'horizontale et retirer la seringue du flacon.
|
|
| |
Étape 15
En cas d'utilisation non immédiate, placer le capuchon sur la seringue de 50 ml.
La seringue ne doit être utilisée que pour un seul patient.
|
|
| |
Étape 16
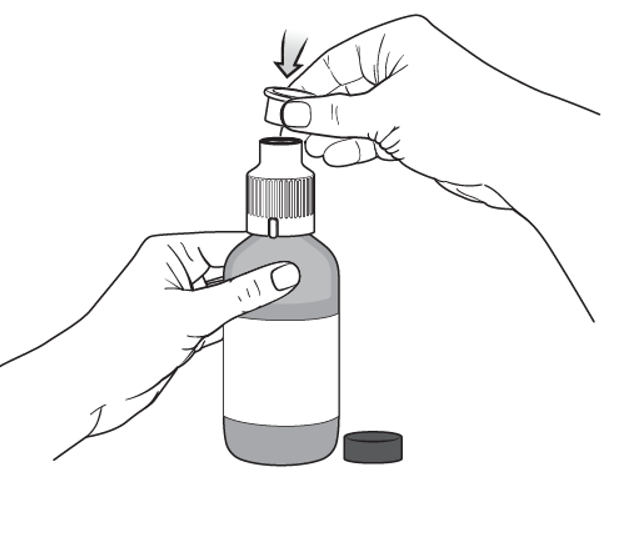
Placer le capuchon de protection sur l'adaptateur de remplissage.
Après avoir été placés sur le flacon, l'adaptateur de remplissage et le capuchon de protection correspondant peuvent remplacer le couvercle pendant 14 jours.
|
|
|
|

















