CompositionPrincipes actifs
Levodopum, Carbidopum ut Carbidopum monohydricum, Entacaponum.
Excipients
Carmellosum natricum, Acidum hydrochloridum, Natrii hydroxidum, Aqua purificata.
47 ml (1 cartouche) contiennent 152,3 mg de sodium.
Indications/Possibilités d’emploiTraitement de la maladie de Parkinson avancée réagissant à la lévodopa, avec de fortes fluctuations motrices et hyperkinésies ou dyskinésies, lorsque les associations médicamenteuses orales disponibles contre la maladie de Parkinson n'ont pas permis d'obtenir des résultats thérapeutiques satisfaisants.
Posologie/Mode d’emploiLecigon est un gel pour usage intestinal continu (administration dans le duodénum ou le jéjunum supérieur).
La réponse clinique au traitement doit être testée au moyen d'une sonde nasoduodénale/nasojéjunale temporaire avant d'effectuer la stomie endoscopique percutanée permanente et de poser la sonde jéjunale (PEG-J).
Lors du traitement de longue durée, le gel doit être administré par une pompe portable au moyen d'une sonde permanente directement dans le duodénum ou le jéjunum supérieur via une gastrostomie percutanée endoscopique. La gastrostomie est effectuée avec une sonde transabdominale externe et une sonde intestinale interne. Alternativement, une gastro-jéjunostomie radiologique peut être envisagée lorsque la gastrostomie percutanée endoscopique n'est pas adaptée, pour une raison quelconque. L'intervention chirurgicale et l'ajustement de la dose doivent être effectués en accord avec un neurologue.
Seule la pompe CRONO LECIG (CE 0476) doit être utilisée pour l'administration de Lecigon. Un mode d'emploi avec des instructions pour utiliser la pompe portable est fourni avec celle-ci.
Une titration de la dose doit avoir lieu afin d'obtenir une réponse clinique optimale chez chaque patient individuel. Cela signifie une maximisation de la phase ON fonctionnelle pendant la journée en minimisant le nombre et la durée des épisodes OFF (bradykinésie) et en minimisant la phase ON avec dyskinésie handicapante.
La dose journalière totale de Lecigon se compose de trois doses définies individuellement: la dose matinale en bolus, la dose d'entretien continue et les doses en bolus supplémentaires. Le traitement est en général limité au temps d'éveil du patient. Si cela est médicalement justifié, Lecigon peut être administré pendant jusqu'à 24 heures par jour. La dose journalière maximale recommandée est de 100 ml (ce qui équivaut à 2000 mg de lévodopa, 500 mg de carbidopa monohydraté et 2000 mg d'entacapone – voir également la rubrique «Mises en garde et précautions»).
Lors de l'administration de la dose d'entretien, le profil de la concentration plasmatique en fonction du temps de la lévodopa présente un aspect légèrement différent (avec une augmentation progressive de la concentration de lévodopa dans le plasma au cours de la journée) de celui noté avec l'association lévodopa/carbidopa seules en gel pour usage intestinal. Un exemple de profil de la concentration plasmatique en fonction du temps lors de l'utilisation de Lecigon se trouve dans la rubrique «Pharmacocinétique». En cas de besoin individuel correspondant, la pompe peut être programmée de manière à administrer jusqu'à trois doses d'entretien par jour/24h. En cas de dyskinésies au cours de la deuxième partie de la journée, une réduction de la dose de 10–20% en milieu de journée peut être pertinente. Toutes les doses d'entretien doivent être titrées jusqu'à l'obtention de l'effet clinique souhaité.
L'administration de doses d'entretien multiples peut aussi être utile par exemple chez les patients avec des dyskinésies persistantes ou une raideur avec un besoin récurrent de doses supplémentaires au cours de la deuxième partie de la journée ou chez les patients sous traitement pendant 24h qui nécessitent une réduction de la dose d'entretien pendant la nuit.
Dose matinale
La dose matinale est administrée par la pompe afin d'atteindre rapidement la dose thérapeutique (en 30 minutes). La dose est réglée avec des paliers de 0,1 ml (2 mg). La dose matinale totale est normalement de 5–10 ml, ce qui correspond à 100–200 mg de lévodopa. La dose matinale totale ne doit pas dépasser 15 ml (300 mg de lévodopa).
Dose d'entretien continue
La dose d'entretien continue est administrée par la pompe pour maintenir la dose à un niveau thérapeutique. La dose d'entretien est réglée avec des paliers de 2 mg/heure (0,1 ml/heure). La dose d'entretien est normalement de 0,7–5,0 ml/heure (15–100 mg de lévodopa/heure). La dose journalière maximale recommandée est de 100 ml (2000 mg de lévodopa).
Doses en bolus supplémentaires
Des doses supplémentaires sont administrées selon les besoins lorsque le patient souffre d'hypokinésie au cours de la journée. La dose supplémentaire est normalement inférieure à 3 ml, mais est déterminée de manière individuelle. S'il s'avère nécessaire d'administrer une dose supplémentaire en bolus plus souvent que 5 fois par jour, la dose d'entretien continue doit être augmentée.
Titration en cas de passage de la lévodopa/carbidopa à Lecigon
Lecigon contient de l’entacapone qui renforce l’effet de la lévodopa. Il peut donc être indispensable de réduire la dose journalière de Lecigon de 20–35% en moyenne par rapport à la dose antérieure de lévodopa et de carbidopa sans inhibiteur de catéchol-O-méthyltransférase (COMT). L’effet de l’entacapone sur la lévodopa étant dose-dépendante, une réduction de la dose plus importante est attendue chez les patients avec une posologie élevée.
La dose initiale est calculée en fonction de l’administration quotidienne antérieure de lévodopa. La dose matinale doit correspondre à la dose matinale antérieure de lévodopa afin d’atteindre le plus rapidement possible une concentration plasmatique thérapeutique, en plus du volume nécessaire pour remplir la sonde. La dose d’entretien continue doit se baser sur la prise journalière antérieure de lévodopa par le patient (sans la dose matinale) en procédant au début à une réduction pour atteindre 65% de la dose journalière initiale de lévodopa. Les doses seront ensuite titrées progressivement en fonction des symptômes cliniques jusqu’à l’obtention de l’effet désiré.
Exemples pour l'ajustement de la dose initiale avant la titration:
Dose journalière totale antérieure de lévodopa: 1360 mg
Dose matinale antérieure de lévodopa: 100 mg
Administration journalière antérieure de lévodopa (sans dose matinale): 1260 mg/jour
Dose matinale: 100 mg
Correspond à un volume de: 100 mg / 20 mg/ml = 5 ml
Dose matinale totale: 5 ml + 3 ml (volumes à remplir dans la sonde) = 8 ml
Dose d'entretien continue: 1260 mg/jour
Dose d'entretien continue réduite à 65%: 1260 mg/jour x 0,65 = 819 mg/jour
Administration par heure (calculée avec une administration pendant 16 heures par jour): 819 mg/16 heures= 51 mg/heure
Correspond à un débit de 51 mg/heure / 20 mg/ml = 2,5–2,6 ml/heure
Titration en cas de passage de la lévodopa/bensérazide à Lecigon
L'entacapone entraîne une légère augmentation (5–10%) de la biodisponibilité de la lévodopa des préparations standards de lévodopa/bensérazide par rapport aux préparations standards de lévodopa/carbidopa. Le passage de la lévodopa/bensérazide à Lecigon n'a pas été étudié.
Titration en cas de passage de la lévodopa/carbidopa/entacapone à Lecigon
La dose initiale est calculée en fonction de l'administration quotidienne antérieure de lévodopa. La dose matinale initiale doit correspondre à la dose matinale de lévodopa antérieure, augmentée du volume nécessaire pour remplir la sonde. La dose d'entretien continue est reprise 1:1 et doit se baser sur l'administration journalière de lévodopa chez le patient (sans la dose matinale). Les doses seront ensuite titrées progressivement en fonction des symptômes cliniques jusqu'à l'obtention de l'effet désiré.
Le passage d'un traitement associé par lévodopa/inhibiteur de DOPA-décarboxylase (inhibiteur de DDC ou DDCI)/tolcapone à Lecigon n'a pas été étudié.
Passage d'un traitement simultané par lévodopa/carbidopa et agonistes de la dopamine à Lecigon
Lors du passage d'un traitement par des agonistes de la dopamine à une monothérapie par Lecigon, le risque d'apparition de symptômes de sevrage susceptibles de survenir avec les agonistes de la dopamine doit être pris en compte. Un arrêt soudain du traitement par des agonistes de la dopamine doit être évité.
Surveillance du traitement
Après la titration initiale, la dose matinale et la dose d'entretien doivent être adaptées précisément en l'espace de quelques semaines.
Lecigon est administré en premier lieu en monothérapie. En cas de besoin, d'autres médicaments pour le traitement de la maladie de Parkinson peuvent être pris simultanément (pour le traitement d'appoint de la maladie de Parkinson, voir également les rubriques «Contre-indications» et «Interactions»). Lorsque le traitement par d'autres médicaments contre la maladie de Parkinson est arrêté ou modifié, la dose de Lecigon doit éventuellement être adaptée.
Une aggravation soudaine de la réponse au traitement avec des fluctuations motrices récurrentes doit conduire à suspecter un déplacement de la sonde duodénale/jéjunale dans l'estomac. La position de la sonde doit être vérifiée par radiographie. Si la sonde n'est pas placée correctement, l'extrémité de la sonde doit être repositionnée dans le duodénum/jéjunum supérieur.
Traitement en cas de démence
En cas de démence suspectée ou diagnostiquée avec abaissement du seuil de confusion (désorientation), la pompe ne doit être manipulée que par le personnel médical, un soignant ou un proche aidant.
Abus du médicament
En cas de suspicion d'abus du médicament, il existe une fonction de verrouillage sur la pompe utilisée avec Lecigon (CRONO LECIG). Cette fonction prévient toute modification du réglage de la pompe par le patient.
Instructions posologiques particulières
Patients présentant des troubles de la fonction hépatique
La posologie de Lecigon est ajustée individuellement par titration pour obtenir une efficacité optimale (ce qui correspond à une exposition plasmatique individuelle optimisée à la lévodopa, la carbidopa et l'entacapone). Par conséquent tous les effets d'une insuffisance hépatique sur l'exposition à la lévodopa, carbidopa et entacapone seront pris en compte lors de la titration. Il n'existe pas d'étude pharmacocinétique sur la carbidopa et la lévodopa chez les patients atteints de troubles de la fonction hépatique. Chez les patients présentant une altération légère à modérée de la fonction hépatique, l'élimination de l'entacapone est réduite. La titration de la dose doit donc être effectuée avec précautions chez les patients avec trouble léger à modéré de la fonction hépatique. La dose doit probablement être réduite (voir la rubrique «Pharmacocinétique»). Lecigon ne doit pas être utilisé chez les patients atteints d'insuffisance hépatique sévère; voir «Contre-indications».
Patients présentant des troubles de la fonction rénale
La posologie de Lecigon est ajustée individuellement par titration pour obtenir une efficacité optimale (ce qui correspond à une exposition plasmatique individuelle optimisée à la lévodopa, la carbidopa et l'entacapone). Par conséquent tous les effets d'une insuffisance rénale sur l'exposition à la lévodopa, carbidopa et entacapone seront pris en compte lors de la titration. Une limitation de la fonction rénale n'influence pas la pharmacocinétique de l'entacapone. Il n'existe pas d'étude pharmacocinétique spécifique sur la carbidopa et la lévodopa chez les patients présentant un trouble de la fonction rénale. La titration de la dose doit cependant être effectuée avec des précautions chez les patients atteints d'une altération grave de la fonction rénale (voir rubrique «Pharmacocinétique»).
Patients âgés
L'expérience acquise lors de l'utilisation de la lévodopa/carbidopa/entacapone chez les patients âgés est très solide. La posologie pour tous les patients, y compris les patients âgés, est adaptée individuellement par titration.
Enfants et adolescents
L'utilisation de Lecigon chez les enfants et les adolescents pour l'indication de maladie de Parkinson avancée avec fortes fluctuations motrices et hyperkinésie/dyskinésie n'est pas pertinente.
Interruption du traitement
Le traitement par Lecigon peut être interrompu à tout moment en retirant la sonde et en laissant cicatriser la plaie.
En cas de nécessité de réduire brusquement la dose ou d'interrompre le traitement, les patients, surtout les patients traités par des antipsychotiques, doivent être mis sous observation rigoureuse; voir rubrique «Mises en garde et précautions».
Si le traitement est interrompu, le patient doit être traité par un traitement alternatif.
Changement de la cartouche
Pour utiliser une nouvelle cartouche, cette dernière doit être montée sur la pompe portable, laquelle doit être connectée à la sonde conformément aux instructions fournies.
La cartouche est destinée à un usage unique et ne doit pas être utilisée pendant plus de 24 heures.
La pompe doseuse contenant une cartouche peut être portée pendant 16 heures au maximum à proximité du corps. Pendant le traitement nocturne, la pompe ne doit pas être portée directement en contact avec le corps. Elle doit être posée à côté, par exemple sur une table de nuit.
Une fois ouverte, une cartouche peut être utilisée jusqu'au jour suivant, c'est-à-dire jusqu'à 24h après ouverture. La cartouche est déconnectée de la pompe après 24h ou utilisation de l'intégralité du médicament, en fonction du cas de figure qui se présente en premier.
Le gel peut prendre une légère coloration jaune/rougeâtre à la fin de la période de conservation. Cela n'exerce aucune influence sur la concentration du médicament ou l'effet du traitement.
Contre-indications·Hypersensibilité à la lévodopa, à la carbidopa, à l'entacapone ou à l'un des excipients
·Glaucome à angle fermé
·Insuffisance cardiaque sévère
·Troubles sévères du rythme cardiaque
·AVC aigu
·Altération sévère de la fonction hépatique
·Les inhibiteurs non sélectifs de la MAO et les inhibiteurs sélectifs de la MAO de type A ne doivent pas être utilisés simultanément avec Lecigon. Ces inhibiteurs doivent être interrompus au moins 2 semaines avant le début du traitement par Lecigon. Lecigon peut être utilisé simultanément avec une dose recommandée par le fabriquant d'un inhibiteur de la MAO avec une sélectivité pour la MAO de type B (par ex. chlorhydrate de sélégiline) (voir rubrique «Interactions»)
·Maladies pour lesquelles les sympathomimétiques (adrénergiques) sont contre-indiqués, par ex. phéochromocytome, hyperthyroïdie et syndrome de Cushing
·Antécédents de syndrome neuroleptique malin (SNM) et/ou rhabdomyolyse non traumatique
·Modification cutanée suspecte non diagnostiquée ou antécédents de mélanome (la lévodopa peut activer un mélanome malin).
Mises en garde et précautionsLecigon n'est pas recommandé pour le traitement des réactions extrapyramidales induites par les médicaments.
Lecigon doit être administré avec une prudence particulière chez les patients atteints d'une pathologie cardiaque ischémique, de troubles cardio-vasculaires ou pulmonaires sévères, d'asthme bronchique, d'une maladie rénale, hépatique ou endocrine et chez les patients avec des antécédents d'ulcère peptique ou de convulsions.
Chez les patients avec des antécédents connus d'infarctus du myocarde et des troubles séquellaires du rythme auriculaire, nodal ou ventriculaire, la fonction cardiaque doit être très étroitement surveillée pendant la période d'ajustement initial de la dose.
Tous les patients traités par Lecigon doivent être étroitement surveillés à la recherche de changements psychiques, dépressions accompagnées de tendances suicidaires et autres anomalies comportementales sévères. Chez les patients souffrant de psychoses ou ceux avec des antécédents de psychoses, le traitement doit s'accompagner de précautions.
L'administration concomitante d'antipsychotiques avec des propriétés de blocage des récepteurs de la dopamine, surtout les antagonistes des récepteurs D2, doit s'accompagner de prudence et les patients doivent être étroitement surveillés à la recherche d'une perte de l'effet antiparkinsonien ou d'une aggravation des symptômes parkinsoniens, voir rubrique «Interactions».
Le traitement par Lecigon des patients souffrant d'un glaucome à angle ouvert chronique est possible avec prudence, pourvu que la pression intraoculaire soit bien contrôlée et que le patient soit étroitement surveillé à la recherche de variations de la pression intraoculaire.
Lecigon peut entraîner une hypotension orthostatique. C'est pourquoi Lecigon doit être utilisé avec précautions chez les patients qui prennent d'autres médicaments pouvant entraîner une hypotension orthostatique, voir rubrique «Interactions».
Les principes actifs dans Lecigon ont été mis en relation avec une somnolence et des épisodes d'endormissement soudain (narcolepsie) chez les patients souffrant de maladie de Parkinson. La prudence est donc recommandée lors de la conduite et de l'utilisation d'outils ou de machines (voir rubriques «Effet sur l'aptitude à la conduite et l'utilisation de machines» et «Effets indésirables»).
Un ensemble de symptômes similaire au syndrome neuroleptique malin (SNM) et comprenant une raideur musculaire, une augmentation de la température corporelle, des changements psychiques (par ex. agitation corporelle, confusion, coma) et une augmentation de la créatine phosphokinase sérique a été rapporté chez les patients ayant arrêté de manière soudaine un médicament contre la maladie de Parkinson. Dans certains rares cas, une rhabdomyolyse secondaire a été rapportée chez les patients parkinsoniens consécutivement à un syndrome neuroleptique malin ou des dyskinésies sévères. Depuis la mise sur le marché de l'entacapone, des cas isolés de SNM ont été rapportés, surtout après réduction soudaine ou arrêt brutal du traitement par l'entacapone et d'autres médicaments dopaminergiques d'appoint. Les patients doivent être étroitement surveillés lors de la réduction de la dose de Lecigon ou de l'arrêt soudain du traitement, surtout chez les patients également sous antipsychotiques/neuroleptiques.
Les patients doivent être surveillés régulièrement à la recherche de l'apparition de troubles du contrôle de l'impulsivité. Les patients et leurs personnes aidantes ou proches doivent être informés que des troubles du contrôle de l'impulsivité comme le jeu compulsif/addiction au jeu, l'augmentation de la libido, l'hypersexualité, les achats compulsifs ou dépenses compulsives d'argent ainsi que crises de boulimie (binge eating) et l'hyperphagie compulsive peuvent survenir chez les patients traités par des agonistes de la dopamine et/ou des médicaments dopaminergiques contenant de la lévodopa, y compris Lecigon. Une révision du traitement est recommandée si de tels symptômes apparaissent.
Les études épidémiologiques ont montré que les patients parkinsoniens courent un risque de développement d'un mélanome plus important que la population générale. On ne sait pas si cette augmentation du risque est due à la maladie de Parkinson ou à d'autres facteurs, comme les médicaments pour traiter la maladie de Parkinson. Il est donc recommandé aux patients et aux soignants d'examiner la peau régulièrement à la recherche d'un mélanome lors de l'utilisation de Lecigon. Dans l'idéal, des examens réguliers par une personne qualifiée (par ex. dermatologue) doivent être effectués.
Si une anesthésie générale est nécessaire, le traitement par Lecigon peut être poursuivi aussi longtemps que le patient est autorisé à prendre des liquides et des médicaments par voie orale. Si le traitement doit être interrompu temporairement, Lecigon peut être administré à nouveau à la même posologie qu'avant l'interruption dès que la prise de liquide par voie orale est à nouveau possible.
Il peut s'avérer nécessaire de réduire la dose de Lecigon pour éviter les dyskinésies induites par la Lévodopa.
Lors d'un traitement de longue durée par Lecigon, des contrôles réguliers de la fonction hépatique et rénale ainsi que des fonctions hématopoïétique et cardiovasculaire sont recommandés.
Lecigon contient de l'hydrazine (voir rubrique «Données précliniques»), un métabolite de la carbidopa, susceptible d'être génotoxique et éventuellement carcinogène. La dose journalière moyenne recommandée de Lecigon est de 46 ml (ce qui correspond à 1,6 mg d'hydrazine/jour) et la dose journalière maximale recommandée de Lecigon est de 100 ml (ce qui correspond à 3,5 mg d'hydrazine/jour au maximum). L'importance clinique de cette absorption d'hydrazine reste inconnue.
Une intervention chirurgicale antérieure au niveau du segment supérieur de l'abdomen peut entraîner des difficultés lors de la réalisation de la gastrostomie ou de la jéjunostomie.
Parmi les complications rapportées pour la lévodopa/carbidopa lors des études cliniques et après la mise sur le marché du médicament, on trouve les troubles suivants: abcès, bézoard, iléus, érosion/ulcère au site de l'implant, saignement intestinal, ischémie intestinale, occlusion intestinale, perforation intestinale, invagination intestinale, pancréatite, péritonite, pneumonie (y compris pneumonie par aspiration), pneumopéritoine, infection postopératoire de la plaie et sepsis. Le bézoard est une accumulation de composants alimentaires non digérés (par ex. fibres indigestes issues des fruits ou des légumes) dans le tractus gastro-intestinal. Un bézoard autour de l'extrémité de la sonde jéjunale peut être à l'origine d'une occlusion intestinale ou d'une invagination intestinale. La plupart des bézoards se trouvent dans l'estomac mais ils peuvent se former dans n'importe quel segment du tractus gastro-intestinal. Les douleurs abdominales peuvent être un symptôme des complications décrites ci-dessus. Certains troubles peuvent évoluer de manière sévère et nécessiter par ex. une intervention chirurgicale et/ou entraîner le décès du patient. Il faut informer le patient de la nécessité pour lui d'alerter son médecin si un symptôme associé à l'une des conditions ci-dessus survient.
Une limitation de la capacité à manipuler le système (pompe, connexion à la sonde) peut conduire à des complications. Dans un tel cas, le soignant (par exemple personnel médical, soignant ou proche) doit aider le patient lors de cette manipulation.
Une aggravation soudaine ou progressive de la bradykinésie peut indiquer une obstruction de la sonde pour une raison quelconque et doit être examinée.
Les principes actifs contenus dans Lecigon ont été associés à une diminution du poids. Les soignants ou les proches doivent donc être informés qu'une diminution du poids est possible. Une surveillance du poids corporel est recommandée pour éviter une perte de poids excessive. Cela s'applique particulièrement aux patients qui développent une diarrhée. Un suivi du poids est recommandé chez les patients souffrant de diarrhée afin d'éviter une éventuelle perte de poids excessive. Une diarrhée persistante ou de longue durée et survenant lors de la prise de l'entacapone peut être un signe de colite. En cas de diarrhée pendant une longue durée ou persistante, le traitement par ce médicament doit être interrompu et un autre traitement médical ainsi qu'un examen doivent être envisagés.
Si cela est considéré comme indispensable, le remplacement de Lecigon soit par la lévodopa et un inhibiteur de la DDC sans entacapone, soit par un autre traitement dopaminergique, doit être réalisé lentement. Une augmentation de la dose de Lévodopa peut être nécessaire.
Chez les patients qui présentent en un temps relativement court une anorexie, une asthénie ou une perte de poids s'aggravant rapidement, un examen médical complet ainsi qu'un contrôle de la fonction hépatique doivent être réalisés.
La lévodopa/carbidopa peut conduire à des résultats faux-positifs lors de la détermination des corps cétoniques dans l'urine sur bandelettes réactives. Cette réaction n'est pas notée après chauffage jusqu'à ébullition de l'échantillon d'urine. Des résultats faux-négatifs au test de la glycosurie sont possibles lorsque des méthodes basées sur la glucose-oxydase sont utilisées.
Le syndrome de dysrégulation dopaminergique (SDD) est une maladie addictive observée chez quelques patients traités par lévodopa/carbidopa. Avant le début du traitement, les patients et les soignants doivent être informés du risque potentiel de l'apparition d'un SDD (voir également rubrique «Effets indésirables»).
En cas de suspicion d'un abus de médicament, la fonction de verrouillage de la pompe utilisée avec Lecigon (CRONO LECIG) peut être activée.
Une polyneuropathie a été rapportée chez des patients traités par lévodopa/carbidopa en gel pour administration intestinale. Avant le début du traitement par Lecigon® , les patients doivent être examinés pour connaître leurs antécédents ou les signes d'une neuropathie existante ainsi que les facteurs de risque connus. Effectuez cet examen à intervalles réguliers, même après le début du traitement.
Excipients
Ce médicament contient 152,3 mg de sodium dans une cartouche de 47 ml, ce qui équivaut à 7,6% de la dose de sodium alimentaire journalière maximale recommandée par l'OMS pour un adulte (2 g).
La dose journalière maximale de ce médicament correspond à 16,2% de la dose de sodium alimentaire journalière maximale recommandée par l'OMS.
Lecigon est considéré comme riche en sodium. Ce point doit être particulièrement pris en compte chez les patients suivant un régime alimentaire pauvre en sodium.
InteractionsAucune étude sur les interactions n'a été réalisée avec Lecigon. Les interactions suivantes sont connues pour l'association générique lévodopa/carbidopa et l'association entacapone/lévodopa/carbidopa.
La prudence est de mise lorsque Lecigon est utilisé en même temps que les médicaments suivants:
Antihypertenseurs
Une hypotension orthostatique symptomatique est survenue lors de l'administration d'une association de lévodopa et d'un inhibiteur de décarboxylase à des patients recevant déjà certains antihypertenseurs. Un ajustement de la dose d'antihypertenseur peut être nécessaire.
Antidépresseurs
Les inhibiteurs non sélectifs de la MAO et les inhibiteurs sélectifs de la MAO de type A ne doivent pas être utilisés simultanément avec Lecigon. Le traitement par ces inhibiteurs doit être arrêté au moins deux semaines avant le début du traitement par Lecigon (voir rubrique «Contre-indications»).
Quelques rares cas de réactions indésirables ont été rapportés (comme l'hypertension ou la dyskinésie) lors de l'utilisation concomitante d'antidépresseurs tricycliques et de préparations de carbidopa/lévodopa.
Un grand nombre de patients parkinsoniens ont été traités simultanément par l'association lévodopa/carbidopa/entacapone et des antidépresseurs tricycliques et aucune interaction pharmacodynamique n'a été notée. Cependant, la prudence reste de mise en cas d'administration concomitante d'antidépresseurs avec Lecigon.
Anticholinergiques
Les anticholinergiques peuvent exercer un effet de synergie avec la lévodopa et diminuer les tremblements. Une utilisation associée peut cependant renforcer les mouvements involontaires anormaux. Les anticholinergiques peuvent diminuer l'effet de la lévodopa en ralentissant l'absorption du principe actif. Une adaptation de la dose de Lecigon peut être nécessaire.
Autres médicaments pour le traitement de la maladie de Parkinson.
Lecigon peut être utilisé simultanément avec la dose recommandée d'inhibiteur de MAO sélectif pour la MAO de type B (par ex. chlorhydrate de sélégiline). L'utilisation simultanée de sélégiline et de lévodopa/carbidopa a été associée à une hypotension orthostatique sévère (syndrome orthostatique). Une administration supplémentaire d'inhibiteur sélectif de la MAO B peut par conséquent nécessiter une réduction de la dose de Lecigon.
L'amantadine et les agonistes de la dopamine comme le piribédil exercent un effet de synergie avec la lévodopa et peuvent renforcer les effets indésirables de celle-ci. Une adaptation de la dose de Lecigon peut éventuellement être nécessaire.
Autres médicaments
Les antagonistes des récepteurs à la dopamine (certains antipsychotiques comme la phénothiazine, la butyrophénone et la rispéridone ainsi que les antiémétiques comme le métoclopramide), les benzodiazépines, l'isoniazide, la phénytoïne et la papavérine peuvent diminuer l'effet thérapeutique de la lévodopa. Les patients recevant ces médicaments en même temps que Lecigon doivent être étroitement surveillés à la recherche d'une perte de la réponse thérapeutique.
Les sympathomimétiques peuvent renforcer les effets indésirables cardiovasculaires associés à la lévodopa.
La lévodopa forme des chélates avec le fer dans le tractus gastro-intestinal, ce qui conduit à une diminution de l'absorption de la lévodopa. C'est pourquoi Lecigon et les préparations martiales doivent être administrés à au moins 2 à 3 heures d'intervalle. La préparation martiale peut par exemple être prise avant d'aller se coucher, lorsque le patient n'utilise pas la pompe pendant la nuit.
En raison de l'affinité in-vitro de l'entacapone envers la P450 2C9 (voir rubrique «Pharmacocinétique»), des interactions restent possibles entre Lecigon et des médicaments dont la métabolisation dépend de cet isoenzyme, comme la S warfarine. Au cours d'une étude d'interactions menée auprès de sujets sains, l'entacapone n'a cependant pas modifié la concentration plasmatique de la S warfarine, alors que l'aire sous la courbe (ASC) de la R warfarine a augmenté de 18% en moyenne (intervalle de confiance à 90%: 11-26%). Les valeurs INR ont augmenté de 13% en moyenne (intervalle de confiance à 90%: 6-19%). C'est pourquoi les valeurs de l'INR chez les patients traités par la warfarine doivent être surveillées au début du traitement par Lecigon.
Les effets de l'utilisation d'antacides et de Lecigon sur la biodisponibilité de la lévodopa n'ont pas été étudiés.
Interactions avec les aliments
L'absorption de la lévodopa peut être limitée chez les patients suivant une alimentation riche en protéines car la lévodopa est en concurrence avec certains acides aminés.
Grossesse, allaitementGrossesse
Jusqu'ici, les données sur l'utilisation de la lévodopa/carbidopa/entacapone chez la femme enceinte sont inexistantes ou seulement limitées. Les expérimentations animales ont montré une toxicité sur la reproduction associée aux principes actifs individuels (voir rubrique «Données précliniques»). Le risque possible pour l'être humain est inconnu. L'utilisation de Lecigon pendant la grossesse et chez les femmes en âge de procréer et n'utilisant pas de moyen de contraception n'est pas recommandée sauf si les bénéfices pour la mère dépassent les risques potentiels pour le fœtus.
Allaitement
La lévodopa et les métabolites possibles de la lévodopa passent dans le lait maternel. Il a été montré que la formation du lait est réprimée sous traitement par la lévodopa.
On ignore si la carbidopa et l'entacapone et/ou leurs métabolites passent dans le lait maternel. Les expérimentations animales ont montré une excrétion de la carbidopa et l'entacapone dans le lait maternel mais on ignore si ces molécules passent dans le lait maternel humain.
Les informations sur les effets de la lévodopa/carbidopa/entacapone et/ou leurs métabolites sur les nouveau-nés/enfants en bas âge sont insuffisantes. L'allaitement doit donc être interrompu lors du traitement par Lecigon.
Fertilité
Au cours des études précliniques, l'administration individuelle d'entacapone, de lévodopa ou de carbidopa n'a pas permis de mettre en évidence des effets néfastes sur la fertilité. Aucune étude de fertilité n'a été menée chez l'animal avec l'association lévodopa/carbidopa/entacapone.
Effet sur l’aptitude à la conduite et l’utilisation de machinesLecigon peut exercer une forte influence sur l'aptitude à la conduite et à l'utilisation d'outils ou de machines. L'association lévodopa/carbidopa/entacapone peut causer des étourdissements et des symptômes orthostatiques (syndrome orthostatique). C'est pourquoi la prudence est de mise lors de la conduite de véhicules et l'utilisation de machines.
Il convient de recommander aux patients traités par Lecigon et sujets à des somnolences et/ou des endormissements soudains de renoncer à conduire des véhicules et à effectuer d'autres activités pouvant représenter, pour eux ou pour autrui, un risque de blessure grave ou fatale en raison d'une baisse de la vigilance (par ex. utilisation de machines) jusqu'à la disparition de tels épisodes récurrents et de la somnolence (voir également rubriques «Mises en garde et précautions» et «Effets indésirables»).
Effets indésirablesLe profil de sécurité attendu pour Lecigon se base sur les données disponibles issues des études cliniques et de l'expérience acquise après la mise sur le marché du gel de lévodopa/carbidopa à usage intestinal et de l'association orale de lévodopa/carbidopa/entacapone.
Parmi les effets médicamenteux indésirables survenant fréquemment sous traitement par le gel de lévodopa/carbidopa à usage intestinal et donc sous Lecigon, on rapporte la nausée et la dyskinésie. Parmi les effets indésirables survenant fréquemment en relation avec la sonde ou l'intervention chirurgicale et le gel de lévodopa/carbidopa à usage intestinal et donc également possibles avec Lecigon, on rapporte les douleurs abdominales, les complications lors de l'introduction de la sonde, un tissu de granulation excessive, un érythème au site d'incision, une infection post-opératoire, des sécrétions après une intervention, des douleurs dues à l'intervention et une réaction au site d'incision. La plupart de ces effets indésirables ont été rapportés peu après le début de l'étude suite à la procédure de gastrostomie percutanée endoscopique et sont survenus pendant les 28 premiers jours.
Les effets indésirables les plus fréquemment rapportés avec la formulation orale de l'association lévodopa/carbidopa/entacapone sont les dyskinésies (qui touchent environ 19% des patients), des symptômes gastro-intestinaux comme la nausée et la diarrhée (qui touchent environ 15% et 12% des patients, respectivement), des troubles musculaires et du tissu conjonctif (qui touchent environ 12% des patients) et une coloration brune inoffensive de l'urine (chromaturie) (qui touche environ 10% des patients). Au cours des études cliniques avec la formulation orale de l'association lévodopa/carbidopa/entacapone ou l'entacapone en association avec la lévodopa et un inhibiteur de DDC, des effets indésirables graves comme des hémorragies gastro-intestinales (rares) et des angiœdèmes (rares) sont survenus.
Une hépatite sévère avec des manifestations principalement cholestatiques, une rhabdomyolyse et un syndrome neuroleptique malin peuvent survenir avec la formulation orale de l'association de lévodopa/carbidopa/entacapone, bien qu'aucun cas issu des études cliniques ne soit connu.
Une étude pharmacocinétique a été menée avec Lecigon auprès de 11 patients souffrant d'une maladie de Parkinson à un stade avancé. Des céphalées, des nausées et des étourdissements ont été notés en tant qu'effets indésirables en relation avec Lecigon. Des effets indésirables graves n'ont pas été rapportés au cours de cette étude de 2 jours. Lors de l'administration de Lecigon, aucun effet indésirable n'a été observé en relation avec la pompe.
Effets indésirables issus des études cliniques et de l'expérience après la mise sur le marché du gel de lévodopa/carbidopa pour usage intestinal et/ou de la formulation orale de l'association lévodopa/carbidopa/entacapone.
Les effets indésirables en relation avec le médicament, l'appareil ou la procédure et issus des études cliniques ou lors de l'utilisation du gel de lévodopa/carbidopa pour usage intestinal ou de la formulation orale de l'association lévodopa/carbidopa/entacapone après la mise sur le marché sont résumés ci-dessous en fonction des classes d'organes et de leur fréquence.
Pour la formulation orale de l'association lévodopa/carbidopa/entacapone, les effets indésirables issus des études cliniques en double aveugle et des données cliniques correspondent à ceux qui ont été notés pendant l'utilisation de l'entacapone après la mise sur le marché du traitement associé par lévodopa/inhibiteur de DDC. Les fréquences sont définies comme suit: très fréquents (≥1/10); fréquents (≥1/100 à <1/10); occasionnels (≥1/1000 à <1/100); rares (≥1/10 000 à <1/1000); très rares (<1/10 000); «fréquence inconnue» (ne peut être estimée sur la base des données disponibles)
Effets indésirables médicamenteux
Affections hématologiques et du système lymphatique
Fréquents: Anémie.
Occasionnels: Leucopénie, thrombocytopénie.
Fréquence inconnue: Agranulocytose.
Affections du système immunitaire
Fréquence inconnue: Réaction anaphylactique.
Troubles du métabolisme et de la nutrition
Très fréquents: Perte de poids.
Fréquents: Augmentation du taux d'acide aminés (augmentation de l'acide méthylmalonique), augmentation de l'homocystéine sanguine, diminution de l'appétit, prise de poids, carence en vitamine B6, carence en vitamine B12.
Affections psychiatriques
Très fréquents: Angoisse, dépression, insomnies.
Fréquents: Cauchemars, agitation corporelle, confusion, hallucination, trouble du contrôle de l'impulsivité, troubles psychotiques, narcolepsie, troubles du sommeil.
Occasionnels: Suicide, désorientation, euphorie, peur, augmentation de la libido (voir «Mises en garde et précautions»), tentative de suicide/comportement suicidaire.
Rares: Pensées anormales.
Fréquence inconnue: Dysrégulation homéostatique hédoniste (syndrome de dysrégulation dopaminergique)a.
Affections du système nerveux
Très fréquents: Dyskinésies, maladie de Parkinson/aggravation des symptômes de la maladie de Parkinson (par ex. bradykinésie).
Fréquents: Étourdissements, dystonie, céphalées, hypesthésie, phénomènes on-off, paresthésie, polyneuropathie, somnolence, syncope, tremblements, hyperkinésie.
Occasionnels: Ataxie, convulsions.
Fréquence inconnue: Syndrome neuroleptique malin, limitation des capacités mémorielles, démence.
Affections oculaires
Fréquents: Vision trouble.
Occasionnels: Glaucome à angle fermé (par fermeture de l'angle), blépharospasme, vision double, neuropathie ischémique du nerf optique.
Affections cardiaques:
Fréquents: Fréquence cardiaque irrégulière, cardiopathie ischémique autre qu'infarctus du myocarde (par ex. angine de poitrine).
Occasionnels: Palpitations, infarctus du myocarde.
Affections vasculaires
Très fréquents: Syndrome orthostatique.
Fréquents: Hypertension, hypotension.
Occasionnels: Phlébite.
Affections respiratoires, thoraciques et médiastinales
Fréquents: Dyspnée, douleurs oropharyngées, pneumonie d'aspiration.
Occasionnels: Dysphonie.
Rares: Respiration anormale.
Affections gastro-intestinales
Très fréquents: Nausées, constipation, diarrhée.
Fréquents: Abdomen gonflé, douleurs abdominales, troubles abdominaux, sécheresse buccale, dysgueusie, dyspepsie, dysphagie, flatulences, vomissements.
Occasionnels: Colite, saignement gastro-intestinal, hypersalivation.
Rares: Bruxisme, glossodynie, hoquet, coloration de la salive.
Affections hépatobiliaires
Occasionnels: Résultats anormaux aux tests de la fonction hépatique.
Fréquence inconnue: Hépatite avec éléments principalement cholestatiques.
Affections de la peau et du tissu sous-cutané
Fréquents: Dermatite de contact, hyperhidrose, prurit, éruption cutanée.
Occasionnels: Alopécie, érythème, urticaire, colorations de la peau, des cheveux, des ongles et de la sueur.
Rares: Mélanome malin (voir rubrique «Contre-indications»), angioedème.
Affections musculo-squelettiques et du tissu conjonctif
Très fréquents: Douleurs musculaires, des tissus et de la musculature squelettique.
Fréquents: Arthralgie, spasmes musculaires, douleurs dans la nuque.
Fréquence inconnue: Rhabdomyolyse.
Affections du rein et des voies urinaires
Très fréquents: Chromaturie, infection urinaire.
Fréquents: Incontinence urinaire, rétention urinaire.
Affections des organes de reproduction et du sein
Rares: Priapisme.
Troubles généraux et anomalies au site d'administration
Fréquents: Asthénie, douleurs thoraciques, fatigue, troubles de la marche, douleurs, œdème périphérique.
Occasionnels: Sensation de malaise.
Lésions, intoxications et complications liées aux procédures
Très fréquents: Chute.
Effets indésirables en relation avec l'appareil ou la procédure
Infections et infestations
Très fréquents: Infection post-opératoire de la plaie.
Fréquents: Cellulite au site d'incision, infection après une intervention.
Occasionnels: Abcès post-opératoire.
Fréquence inconnue: Sepsis.
Affections gastro-intestinales
Très fréquents: Douleurs abdominales.
Fréquents: Troubles abdominaux, douleurs dans la partie supérieure de l'abdomen, péritonite, pneumopéritoine.
Occasionnels: Bézoard, colite ischémique, ischémie gastro-intestinale, occlusion gastro-intestinale, pancréatite, saignement de l'intestin grêle, ulcère de l'intestin grêle, perforation du côlon, invagination intestinale.
Fréquence inconnue Perforation gastrique, perforation gastro-intestinale, ischémie de l'intestin grêle, perforation de l'intestin grêle.
Affections de la peau et du tissu sous-cutané
Très fréquents: Tissu de granulation excessive.
Troubles généraux et anomalies au site d'administration
Très fréquents: Complications lors de l'introduction de la sondeb.
Fréquents: Dislocation d'un dispositif médical, obstruction d'un dispositif médical.
Lésions, intoxications et complications liées aux procédures
Très fréquents: Érythème au site d'incision, excrétions après une intervention, douleurs pendant une intervention, réaction au site d'examen.
Fréquents: Complication d'une stomie gastro-intestinale, douleurs au site d'incision, iléus postopératoire, complication après une intervention, douleurs après une intervention, saignement après une intervention.
a Le syndrome de dysrégulation dopaminergique (SDD) est une maladie addictive observée chez certains patients traités par carbidopa/lévodopa. Les patients touchés montrent un abus compulsif du médicament dopaminergique avec l'utilisation de doses plus importantes que celles nécessaires pour un contrôle adéquat des symptômes moteurs de la maladie de Parkinson. Cela peut entraîner dans certains cas des dyskinésies graves (voir également rubrique «Mises en garde et précautions»).
b Les complications lors de l'insertion de la sonde ont constitué un effet indésirable fréquemment rapporté aussi bien avec la sonde nasojéjunale qu'avec la PEG-J. Cet effet indésirable a été rapporté simultanément avec un ou plusieurs des effets indésirables suivants en relation avec la sonde nasojéjunale: douleur oropharyngée, abdomen gonflé, douleurs abdominales, troubles abdominaux, douleurs, irritation de la gorge, lésion gastro-intestinale, saignement œsophagien, anxiété, dysphagie et vomissements. Pour la PEG-J, cet effet indésirable a été rapporté avec un ou plusieurs des effets indésirables suivants: Douleurs abdominales, troubles abdominaux, abdomen gonflé, flatulences ou pneumopéritoine. Les autres effets indésirables non graves rapportés en relation avec une complication lors de l'introduction de la sonde comprennent les troubles abdominaux, l'ulcère duodénal, les saignements, la duodénite érosive, la gastrite érosive, les saignements gastro-intestinaux, la péritonite, le pneumopéritoine et l'ulcère de l'intestin grêle.
Un déplacement de la sonde intestinale qui retourne dans l'estomac ou une obstruction de la sonde conduit à une réapparition des fluctuations motrices.
Les effets indésirables supplémentaires suivants ont été observés sous lévodopa/carbidopa orale et classés comme rares (≥1/10 000, < 1/1000): anémie hémolytique, trisme, syndrome de Claude Bernard-Horner, mydriase, crise oculogyre et purpura d'Henoch-Schönlein. Les effets indésirables supplémentaires suivants ont été rapportés très rarement (< 1/10 000): agranulocytose.
Paramètres de laboratoire:
Les anomalies suivantes ont été rapportées au niveau des paramètres de laboratoire lors du traitement par lévodopa/carbidopa: augmentation du taux d'azote uréique, des phosphatases alcalines, de la S-AST, de la S-ALT, de la LDH, de la bilirubine, de la glycémie, de la créatinine, de l'acide urique, test de Coomb positif ainsi que diminution des taux d'hémoglobine et d'hématocrite. La présence de leucocytes, de bactéries et de sang dans les urines a aussi été rapportée.
Description d'effets indésirables sélectionnés
L'initiation du traitement par l'entacapone chez les patients ayant déjà été traités par lévodopa/inhibiteur de la DDC peut conduire à une augmentation initiale de l'activité dopaminergique (par ex. dyskinésie, nausées et vomissements). La diminution de la dose de lévodopa permet de réduire le degré de sévérité et la fréquence de ces réactions dopaminergiques.
Troubles du contrôle de l'impulsivité
Le jeu compulsif/addiction au jeu, une augmentation de la libido, une hypersexualité, des achats compulsifs ou des dépenses d'argent compulsives, des crises de boulimie et une boulimie compulsive peuvent survenir chez les patients traités par des agonistes de la dopamine et/ou d'autres médicaments dopaminergiques contenant de la lévodopa, y compris Lecigon (voir rubrique «Mises en garde et précautions»).
Somnolence et narcolepsie
L'entacapone en association avec la lévodopa a été mise en relation avec une somnolence et des épisodes d'endormissement brutal chez des patients parkinsoniens. C'est pourquoi la prudence est de rigueur en cas de conduite de véhicules et d'utilisation de machines (voir rubriques «Mises en garde et précautions» et «Effet sur l'aptitude à la conduite et l'utilisation de machines»).
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageLes principaux symptômes cliniques d'un surdosage par la lévodopa/carbidopa sont la dystonie et la dyskinésie. Un blépharospasme peut être un signe précoce d'un surdosage. La pyridoxine n'est pas efficace pour contrebalancer l'effet de Lecigon. Une surveillance par ECG doit être réalisée et le patient doit être étroitement surveillé à la recherche d'une éventuelle apparition de troubles du rythme cardiaque (arythmies). Au besoin, un traitement adéquat par des antiarythmiques doit être mis en place. La possibilité selon laquelle le patient aurait pu prendre aussi d 'autres médicaments que Lecigon doit être envisagée. Aucune information n'est connue sur l'effet d'une dialyse pour le traitement d'un surdosage.
Des cas isolés de surdosage ont été rapportés. Les doses les plus importantes administrées dans ce contexte ont été d'au moins 10 000 mg de lévodopa et 40 000 mg d'entacapone. Parmi les signes et symptômes aigus notés dans ces cas, on compte: agitation corporelle, confusion, coma, bradycardie, tachycardie ventriculaire, dyspnée de Cheyne-Stokes, colorations de la peau, de la langue et de la conjonctive ainsi que des urines.
Propriétés/EffetsCode ATC
N04BA03
Mécanisme d'action
Lecigon est une association de lévodopa, de carbidopa monohydraté et d'entacapone (proportions 4:1:4) dans un gel pour perfusion intestinale continue chez les patients souffrant de maladie de Parkinson avancée avec fortes fluctuations motrices et hyperkinésie/dyskinésie.
En l'état actuel des connaissances, les symptômes de la maladie de Parkinson sont en relation avec une carence en dopamine dans le corps strié. La dopamine ne traverse pas la barrière hémato-encéphalique.
La lévodopa, le précurseur métabolique de la dopamine, traverse la barrière hémato-encéphalique et atténue les symptômes de la maladie. La lévodopa étant largement métabolisée dans les tissus périphériques, seule une petite partie de la dose administrée atteint le système nerveux central lorsque la lévodopa est utilisée sans inhibiteurs des enzymes métaboliques.
La carbidopa est un inhibiteur périphérique de la DOPA-décarboxylase périphérique (DDCI ou inhibiteur de DDC) qui réduit la transformation métabolique périphérique de la lévodopa en dopamine, afin qu'une quantité plus importante de lévodopa soit disponibles dans le cerveau. Lorsque la décarboxylation de la lévodopa est réduite par l'utilisation simultanée d'un inhibiteur de DDC, une dose plus faible de lévodopa peut être utilisée et l'incidence des effets indésirables comme la nausée peut être diminuée.
En raison de l'inhibition de la décarboxylase par l'inhibiteur de DDC, la catéchol-ométhyltransférase (COMT) devient la voie de métabolisation périphérique principale. L'entacapone est un inhibiteur spécifique, efficace et principalement périphérique de la COMT, avec un effet réversible, développé pour une utilisation en association avec la lévodopa. L'entacapone réduit la clairance de la lévodopa dans le sang, ce qui permet une augmentation de l'aire sous la courbe (ASC) dans le profil pharmacologique de la lévodopa. En conséquence, la réponse clinique à la lévodopa est prolongée.
La perfusion intestinale des doses de Lecigon testées individuellement maintient la concentration plasmatique de la lévodopa dans une fenêtre thérapeutique individuelle à un niveau constant.
Pharmacodynamique
Voir rubrique «Mécanisme d'action».
Efficacité clinique
Voir rubrique «Mécanisme d'action».
PharmacocinétiqueAbsorption
Lecigon est administré directement par une sonde posée dans le duodénum ou le jéjunum. L'absorption de la lévodopa, de la carbidopa et de l'entacapone est sujette à des fluctuations intra- et interindividuelles importantes. La lévodopa et l'entacapone sont toutes deux absorbées et éliminées rapidement. La carbidopa est absorbée et éliminée un peu plus lentement que la lévodopa. Les repas contenant une forte proportion d'acides aminés neutres et de haut poids moléculaire peuvent ralentir et réduire l'absorption de la lévodopa. L'absorption de l'entacapone n'est pas significativement influencée par la prise de nourriture.
Au cours d'une étude clinique ouverte, randomisée (n=11) et avec cross-over utilisant la duodopa comme préparation de comparaison, l'usage intestinal de Lecigon a conduit rapidement à des taux plasmatiques thérapeutiques de lévodopa. Aussi bien pour Lecigon que pour la duodopa, des concentrations de lévodopa comparables ont été maintenues pendant la perfusion, mais une augmentation progressive de la concentration plasmatique de lévodopa pendant la journée a été observée avec Lecigon, comparativement à la duodopa. La biodisponibilité de la lévodopa avec Lecigon a été statistiquement plus élevée que celle avec la duodopa, calculée pendant la perfusion par le rapport ASC014h/dose (proportions: 1,38; intervalle de confiance à 95% [IC]: 1,26–1,51). Après la fin de la perfusion, les concentrations de lévodopa ont diminué rapidement. La variabilité intrapatient des concentrations plasmatiques de lévodopa a été faible dans l'intervalle de 3 à 14 heures après le début de la perfusion de Lecigon (13,8%).
Un exemple pour le profil attendu de la concentration plasmatique en fonction du temps avec une dose d'entretien constante est représenté dans la figure 1. Au besoin, il est possible d'utiliser plusieurs doses d'entretien par jour/période de 24 heures (voir rubrique «Posologie/Mode d'emploi»).
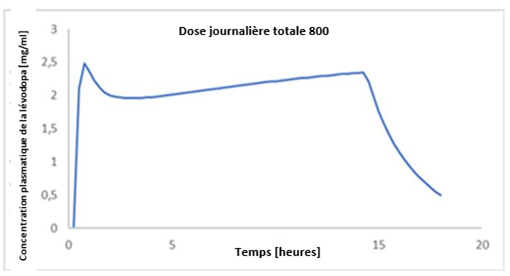
Figure 1: exemple de profil attendu de la concentration plasmatique de lévodopa en fonction du temps avec une dose journalière totale de 800 mg de lévodopa, une dose matinale (176 mg) et une dose d'entretien continue (45 mg/h) au cours de la journée. (Simulation avec un modèle de CP population)
Distribution
Le volume de distribution est relativement faible à l'état d'équilibre à la fois pour la lévodopa (0,36–1,6 l/kg) et pour l'entacapone (0,27 l/kg). Aucune donnée n'est disponible pour la carbidopa.
La lévodopa n'est liée aux protéines plasmatiques que dans une faible proportion (env. 10–30%). La carbidopa est liée à presque 36% aux protéines plasmatiques alors que l'entacapone est fortement liée aux protéines plasmatiques (env. 98%), essentiellement à l'albumine sérique. Aux concentrations thérapeutiques, l'entacapone ne déplace pas les autres molécules fortement liées (par ex. warfarine, acide salicylique, phénylbutazone ou diazépam) et n'est pas non plus significativement déplacée par ces médicaments à des concentrations thérapeutiques ou supérieures.
Métabolisme
La lévodopa est fortement métabolisée en différents métabolites, la décarboxylation par la dopadécarboxylase (DDC) et l'O-méthylation par la catéchol-O-méthyltransférase (COMT) étant les voies de métabolisation principales.
La carbidopa est métabolisée en deux métabolites principaux excrétés dans les urines sous forme de glucuronides et de molécules non conjuguées. La carbidopa non modifiée représente 30% de l'élimination totale dans les urines.
L'entacapone est presque totalement métabolisée avant l'élimination dans les urines (10–20%) ou la bile et les selles (80–90%). La principale voie de métabolisation est la glucuronidation de l'entacapone et de son métabolite actif, l'isomère cis, qui représente environ 5% de la quantité plasmatique totale.
Élimination
La clairance totale de la lévodopa se situe entre 0,55 et 1,38 l/kg/heure et celle de l'entacapone est de l'ordre de 070 l/kg/heure. La demi-vie est de 0,6-1-3 heures pour la lévodopa, 2-3 heures pour la carbidopa et 0,4–0,7 heure pour l'entacapone en utilisation séparée. La demi-vie moyenne estimée pour la lévodopa pendant le traitement par Lecigon est de 2,0 heures.
Induction/inhibition enzymatique
Les données issues des études in-vitro effectuées avec des microsomes hépatiques humains montrent que l'entacapone inhibe le cytochrome P450 2C9 (IC50 ~ 4 µM). L'entacapone a montré une inhibition faible ou nulle d'autres iso-enzymes du P450 (CYP1A2, CYP2A6, CYP2D6, CYP2E1, CYP3A et CYP2C19).
Cinétique pour certains groupes de patients
Troubles de la fonction hépatique
La métabolisation de l'entacapone est ralentie chez les patients souffrant d'insuffisance hépatique légère à modérée (classes A et B de Child-Pugh), ce qui entraîne une augmentation des concentrations plasmatiques de l'entacapone pendant la phase d'absorption et d'élimination (voir rubriques «Posologie/Mode d'emploi», «Contre-indications» et «Mises en garde et précautions»). Il n'existe pas d'étude pharmacocinétique spécifique sur la carbidopa et la lévodopa chez les patients présentant une insuffisance hépatique. Il est cependant recommandé d'être prudent lors de l'utilisation de Lecigon chez les patients avec une insuffisance hépatique légère à modérée. Lecigon ne doit pas être utilisé chez les patients avec insuffisance hépatique sévère; voir «Contre-indications».
Troubles de la fonction rénale
Une limitation de la fonction rénale n'influence pas la pharmacocinétique de l'entacapone. Il n'existe pas d'étude pharmacocinétique spécifique sur la carbidopa et la lévodopa chez les patients présentant un trouble de la fonction rénale. Une augmentation progressive de la dose (titration) doit donc être effectuée avec prudence chez les patients avec une insuffisance rénale sévère, y compris les patients traités par dialyse (voir rubrique «Posologie/Mode d'emploi»).
Patients âgés
Après utilisation de la lévodopa sans carbidopa ni entacapone, l'absorption de la lévodopa chez les patients âgés est plus importante et l'élimination est moins rapide que chez les patients jeunes. Après utilisation de la lévodopa en association avec la carbidopa cependant, l'absorption de la lévodopa chez les patients âgés est comparable à celle chez les jeunes patients, mais l'ASC reste 1,5 fois plus élevée chez les patients âgés que chez les patients jeunes en raison de la diminution de l'activité de la DDC due à l'âge et au ralentissement de la clairance. Il n'y a pas de différence significative entre l'ASC de la carbidopa et de l'entacapone chez les patients jeunes (45–64 ans) et âgés (65–75 ans).
Sexe
La biodisponibilité de la lévodopa est significativement plus élevée chez les femmes que chez les hommes, également lors de l'utilisation de l'entacapone. La différence est principalement due à la différence de poids corporelle. En termes de biodisponibilité de la carbidopa ou de l'entacapone, il n'existe pas de différence entre les deux sexes.
Données précliniquesLes études conventionnelles sur la pharmacologie de sécurité, la toxicité globale, la génotoxicité et la carcinogénicité ainsi que les données précliniques de la lévodopa, la carbidopa et l'entacapone (seules ou en association) n'ont pas permis de mettre en évidence un risque pour l'être humain.
Au cours des études sur la toxicité globale de l'entacapone en administration répétée, une anémie probablement due à la formation de chélates de l'entacapone avec du fer a été notée. Au cours d'études sur la toxicité sur la reproduction de l'entacapone chez le lapin en exposition systémique à des doses thérapeutiques, une diminution du poids des fœtus et un léger retard dans le développement du squelette ont été observés.
La lévodopa ainsi que les associations carbidopa/lévodopa ont conduit chez le lapin à des malformations viscérales et squelettiques.
L'hydrazine est un produit de dégradation de la carbidopa. Au cours des expérimentations animales, l'hydrazine a montré une toxicité systémique significative, surtout lors de l'exposition via les voies respiratoires. Ces études ont montré que l'hydrazine est hépatotoxique, qu'elle induit une toxicité sur le SNC (cependant non décrite après une prise orale) et qu'elle exerce des effets génotoxiques et carcinogènes (voir rubrique «Mises en garde et précautions»). Des études sur des cellules ganglionnaires spinales murines ont montré que l'hydrazine avait également un effet neurotoxique sur le système nerveux périphérique.
Remarques particulièresStabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l'emballage. La date de péremption se réfère au dernier jour du mois.
Stabilité après ouverture
Cartouches ouvertes: utiliser immédiatement. Après la sortie du réfrigérateur, le médicament peut être utilisé pendant 24 heures. La pompe doseuse contenant une cartouche installée peut être portée pendant 16 heures au maximum à proximité du corps. Pendant le traitement nocturne, la pompe ne doit pas être portée directement en contact avec le corps. Elle doit être posée à côté, par exemple sur une table de nuit. Jeter les quantités restantes inutilisées.
Les cartouches sont exclusivement destinées à un usage unique. Les cartouches ouvertes ne doivent pas être réutilisées.
Remarques particulières concernant le stockage
Cartouches encore fermées: conserver au réfrigérateur (2–8°C). À conserver à l'abri du gel.
Conserver dans l'emballage d'origine pour protéger le contenu de la lumière et hors de portée des enfants.
Remarques concernant la manipulation
Un mode d'emploi avec des instructions pour utiliser la pompe portable est fourni avec la pompe.
Numéro d’autorisation68360 (Swissmedic)
PrésentationBoîtes de 7 cartouches de 47 ml (B).
Titulaire de l’autorisationSpirig HealthCare SA, 4622 Egerkingen
Mise à jour de l’informationMars 2024
|

