Propriétés/EffetsCode ATC
S01LA09
Mécanisme d'action
Le faricimab est un anticorps bispécifique humanisé de type immunoglobuline G1 (IgG1) qui agit en inhibant deux voies de signalisation distinctes par neutralisation de l'Ang-2 (angiopoïétine-2) et du VEGF-A (facteur de croissance de l'endothélium vasculaire A). L'Ang-2 provoque une instabilité vasculaire en favorisant la déstabilisation de l'endothélium, la perte de péricytes et l'angiogenèse pathologique et en potentialisant ainsi les fuites vasculaires et les inflammations. En outre, elle sensibilise les vaisseaux sanguins à l'activité du VEGF-A, ce qui accroît encore la déstabilisation vasculaire. L'Ang-2 et le VEGF-A augmentent de manière synergique la perméabilité vasculaire et stimulent la néovascularisation. En inhibant l'Ang-2 et le VEGF-A, le faricimab réduit la perméabilité et l'inflammation vasculaires, inhibe l'angiogenèse pathologique et rétablit la stabilité vasculaire.
Pharmacodynamique
Une suppression des concentrations oculaires médianes d'Ang-2 libre et de VEGF-A libre par rapport à la valeur initiale a été observée à partir du 7e jour dans les six études de phase III décrites ci-dessous.
DMLAn
Les réductions de l'épaisseur moyenne du sous-champ central de la fovéa (Central Subfield Thickness, CST) entre l'inclusion et la semaine 48 étaient similaires lors de l'administration de Vabysmo et lors de celle de l'aflibercept. Dans les études TENAYA et LUCERNE, la réduction moyenne de la CST entre l'inclusion et les visites visant à examiner le critère d'évaluation principal (moyenne des semaines 40, 44 et 48) était respectivement de -137 μm et -137 μm lors de l'utilisation de Vabysmo à des intervalles de 8 (q8w), 12 (q12w) et 16 semaines (q16w), contre -129 μm et -131 μm lors de l'utilisation de l'aflibercept. Ces réductions moyennes de la CST se sont maintenues tout au long de la 2e année. Vabysmo et l'aflibercept ont eu un effet comparable sur la réduction du liquide intrarétinien (LIR), du liquide sous-rétinien (LSR) et du décollement de l'épithélium pigmentaire (DEP). Lors des visites visant à examiner le critère d'évaluation principal, les pourcentages de patients sans LIR dans les études TENAYA et LUCERNE étaient respectivement de 76% à 82% et de 78% à 85% sous le traitement par Vabysmo contre 74% à 85% et 78% à 84% sous le traitement par l'aflibercept. Les pourcentages de patients sans LSR dans les deux études étaient respectivement de 70% à 79% et de 66% à 78% sous le traitement par Vabysmo contre 66% à 78% et 62% à 76% sous le traitement par l'aflibercept. Les pourcentages de patients sans DEP dans les deux études étaient respectivement de 3% à 8% et de 3% à 6% sous le traitement par Vabysmo contre 8% à 10% et 7% à 9% sous le traitement par l'aflibercept. Ces réductions du LIR, du LSR et du DEP se sont maintenues durant la 2e année (semaines 104 à 108).
Dans les deux études, les modifications de la surface totale des lésions liées à une néovascularisation choroïdienne (NVC) et les diminutions de la surface de NVC avec fuites de sang et de liquide entre l'inclusion et la semaine 48 étaient comparables chez les patients traités par Vabysmo et chez les patients traités par l'aflibercept.
OMD
Dans les deux études YOSEMITE et RHINE, la réduction de la CST moyenne par rapport à la valeur initiale entre la semaine 4 et la semaine 100 a été numériquement plus élevée chez les patients traités par Vabysmo toutes les 8 semaines (q8w) et chez ceux ayant reçu Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w, que chez les patients traités par l'aflibercept q8w. Dans les deux études, le pourcentage de patients sans LIR et sans OMD (défini comme l'obtention d'une CST inférieure à 325 µm, mesurée par OCT) au cours du temps était plus élevé dans les bras sous Vabysmo que dans le bras sous aflibercept. Dans les deux études, les réductions du LSR observées au cours du temps ont été similaires dans les bras sous Vabysmo et dans le bras sous aflibercept. Dans l'étude YOSEMITE, la réduction moyenne de la CST entre l'inclusion et les visites visant à examiner le critère d'évaluation principal (moyenne des semaines 48, 52 et 56) était de 207 µm chez les patients traités par Vabysmo q8w et de 197 µm chez ceux ayant reçu Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w, contre 170 µm chez les patients traités par l'aflibercept q8w; dans l'étude RHINE, les chiffres correspondants étaient de 196 µm, 188 µm et 170 µm. Ces réductions moyennes de la CST se sont maintenues tout au long de la 2e année. Dans l'étude YOSEMITE, le pourcentage de patients sans OMD lors des visites visant à examiner le critère d'évaluation principal (min.-max.) était de 77% à 87% chez les patients traités par Vabysmo q8w et de 80% à 82% chez ceux ayant reçu Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w, contre 64% à 71% chez les patients traités par l'aflibercept q8w; dans l'étude RHINE, les chiffres correspondants étaient de 85% à 90%, 83% à 87% et 71% à 77%. Les résultats se sont maintenus tout au long de la 2e année.
Dans l'étude YOSEMITE, les pourcentages de patients sans LIR lors des visites visant à examiner le critère d'évaluation principal (moyenne des semaines 48, 52 et 56) étaient de 42% à 48% chez les patients traités par Vabysmo q8w et de 34% à 43% chez ceux ayant reçu Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w, contre 22% à 25% chez les patients traités par l'aflibercept q8w; dans l'étude RHINE, les chiffres correspondants étaient de 39% à 43%, 33% à 41% et de 23% à 29%. Ces résultats se sont maintenus tout au long de la 2e année.
OBVR et OVCR
Dans les études de phase III menées chez des patients atteints d'une occlusion d'une branche veineuse rétinienne (OBVR; BALATON) et d'une occlusion de la veine centrale de la rétine/occlusion veineuse hémicentrale (OVCR/OVHC; COMINO), des réductions de la CST moyenne ont été observées entre l'inclusion et la semaine 24 lors de l'administration de Vabysmo toutes les 4 semaines (q4w) et étaient comparables à celles observées sous aflibercept q4w. La réduction moyenne de la CST entre l'inclusion et la semaine 24 était de 311,4 μm sous Vabysmo q4w contre 304,4 μm sous aflibercept q4w dans l'étude BALATON et de 461,6 μm sous Vabysmo q4w contre 448,8 μm sous aflibercept q4w dans l'étude COMINO. Ces réductions de la CST se sont maintenues jusqu'à la semaine 72 comprise, lorsque les patients sont passés à un schéma de traitement par Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w.
Dans les deux études, le pourcentage de patients sans LIR, sans LSR et sans œdème maculaire (défini comme l'obtention d'une CST inférieure à 325 µm) au cours du temps était comparable dans le bras sous Vabysmo et dans le bras sous aflibercept jusqu'à la semaine 24 comprise. Ces résultats se sont maintenus jusqu'à la semaine 72 comprise, lorsque les patients sont passés à un schéma de traitement par Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w.
Dans l'étude BALATON, le pourcentage de patients sans œdème maculaire à la semaine 24 a été de 95,3% dans le bras sous Vabysmo q4w contre 93,9% dans le bras sous aflibercept q4w; le pourcentage de patients sans LIR a été de 72,5% dans le bras sous Vabysmo q4w contre 66% dans le bras sous aflibercept q4w. Le pourcentage de patients sans LSR a été de 91,3% dans le bras sous Vabysmo q4w contre 90,3% dans le bras sous aflibercept q4w.
Dans l'étude COMINO, le pourcentage de patients sans œdème maculaire à la semaine 24 a été de 93,7% dans le bras sous Vabysmo q4w contre 92,0% dans le bras sous aflibercept q4w. Le pourcentage de patients sans LIR a été de 76,2% dans le bras sous Vabysmo q4w contre 70,8% dans le bras sous aflibercept q4w; le pourcentage de patients sans LSR a été de 96,4% dans le bras sous Vabysmo q4w contre 93,4% dans le bras sous aflibercept q4w.
Efficacité clinique
Traitement de la forme néovasculaire de la dégénérescence maculaire liée à l'âge (DMLAn)
La sécurité et l'efficacité du faricimab ont été évaluées dans deux études (TENAYA et LUCERNE) à 2 bras, randomisées (1:1), multicentriques, en double aveugle, menées chez des patients atteints de DMLAn, en comparaison d'un traitement anti-VEGF. Le traitement (respectivement 6 mg de faricimab et 2 mg d'aflibercept) a été administré en injection intravitréenne, initialement toutes les 4 semaines. Dans le bras recevant l'aflibercept, après 3 injections initiales d'aflibercept, l'intervalle entre les injections était de 8 semaines (q8w) pour le reste de l'étude. Dans le bras recevant le faricimab, après 4 doses initiales, l'intervalle entre les injections était ajusté individuellement. L'intervalle entre les injections définitif (fixe) était de 8 semaines (q8w), de 12 semaines (q12w) ou au maximum de 16 semaines (q16w) en fonction de la variation définie selon le protocole de l'étude de la CST mesurée par SD-OCT et/ou de la variation de la MAVC mesurée à l'aide du score en lettres ETDRS, et en fonction de l'évaluation clinique de la présence/absence d'hémorragie maculaire par le médecin traitant aux semaines 20 et 24. À partir de la semaine 60, les patients du bras sous Vabysmo sont passés à un schéma thérapeutique extensible dans lequel l'intervalle entre les injections pouvait à chaque fois être augmenté par paliers de 4 semaines au maximum (jusqu'à q16w) ou diminué par paliers de 8 semaines au maximum (jusqu'à q8w), sur la base d'une évaluation objective automatisée de critères visuels et anatomiques prédéfinis pour l'activité de la maladie. Les patients du bras recevant l'aflibercept conservaient l'intervalle q8w pendant toute la durée de l'étude. Les deux études avaient une durée respective de 112 semaines.
Les études ont inclus au total 1329 patients naïfs de traitement, dont 1135 (85%) ont participé sans interruption aux études jusqu'à la semaine 112. Au total, 1326 patients ont reçu au moins une dose (664 patients dans le bras recevant le faricimab). L'âge moyen [intervalle] de la population étudiée était de 75,9 ans [de 50 à 99 ans].Le critère principal d'évaluation de l'efficacité était la variation moyenne de la MAVC par rapport à la valeur initiale au cours de la première année (sur la base de la moyenne des semaines 40, 44 et 48), laquelle a été déterminée à l'aide du tableau de lettres de l'Early Treatment Diabetic Retinopathy Study (ETDRS) à une distance de 4 mètres. L'hypothèse primaire (non-infériorité) a été confirmée dans les deux études: les patients traités par Vabysmo avec un intervalle entre les injections allant jusqu'à q16w et les patients traités par l'aflibercept q8w présentaient lors de la 1re année une variation moyenne comparable de la MAVC par rapport à leur valeur initiale respective. Dans les deux bras de traitement, de nettes améliorations de la vision par rapport à la valeur initiale ont été observées jusqu'à la semaine 112. Les résultats détaillés des deux études sont présentés ci-dessous dans les tableaux 2 et 3 ainsi que dans la figure 1.
Pourcentage de patients dans les groupes avec un intervalle de traitement personnalisé à la semaine 48 dans les études TENAYA et LUCERNE:
·q16w: 46%, 45%
·q12w: 34%, 33%
·q8w: 20%, 22%
Pourcentage de patients dans les groupes avec un intervalle de traitement personnalisé à la semaine 112 dans les études TENAYA et LUCERNE:
• q16w: 59%, 67%
• q12w: 15%, 14%
·q8w: 26%, 19%
Tableau 2: Résultats d'efficacité lors des visites visant à examiner le critère d'évaluation principala ainsi qu'à 2 ansb dans l'étude TENAYA
|
Résultats d'efficacité
|
TENAYA
| |
Année 1
|
Année 2
| |
Vabysmo avec un intervalle allant jusqu'à q16w
N = 334
|
Aflibercept q8w
N = 337
|
Vabysmo avec intervalle allant jusqu'à q16w
N = 334
|
Aflibercept q8w
N = 337
| |
Variation moyenne de la MAVC par rapport à la valeur initiale, mesurée à l'aide du score en lettres ETDRS (IC à 95%)
|
5,8
(4,6, 7,1)
|
5,1
(3,9, 6,4)
|
3,7
(2,1, 5,4)
|
3,3
(1,7, 4,9)
| |
Pourcentage de patients avec un gain de ≥15 lettres par rapport à la valeur initiale (pourcentage pondéré selon le test CMH, IC à 95%)
|
20,0%
(15,6%, 24,4%)
|
15,7%
(11,9%, 19,6%)
|
22,5%
(17,8%, 27,2%)
|
16,9%
(12,7%, 21,1%)
| |
Pourcentage de patients ayant évité une perte de ≥15 lettres par rapport à la valeur initiale (pourcentage pondéré selon le test CMH, IC à 95%)
|
95,4%
(93,0%, 97,7%)
|
94,1%
(91,5%, 96,7%)
|
92,1%
(89,1%, 95,1%)
|
88,6%
(85,1%, 92,2%)
|
a Moyenne des semaines 40, 44 et 48. b Moyenne des semaines 104, 108, 112.
MAVC: meilleure acuité visuelle corrigée.
ETDRS: Early Treatment Diabetic Retinopathy Study.
IC: intervalle de confiance.
CMH: méthode de Cochran–Mantel–Haenszel; test statistique qui génère l'estimation d'une association avec un résultat binaire et qui est utilisé pour analyser des variables catégorielles.
Tableau 3: Résultats d'efficacité lors des visites visant à examiner le critère d'évaluation principala ainsi qu'à 2 ansb dans l'étude LUCERNE
|
Résultats d'efficacité
|
LUCERNE
| |
Année 1
|
Année 2
| |
Vabysmo avec un intervalle allant jusqu'à q16w
N = 331
|
Aflibercept q8w
N = 327
|
Vabysmo avec un intervalle allant jusqu'à q16w
N = 331
|
Aflibercept q8w
N = 327
| |
Variation moyenne de la MAVC par rapport à la valeur initiale, mesurée à l'aide du score en lettres ETDRS (IC à 95%)
|
6,6
(5,3, 7,1)
|
6,6
(5,3, 7,8)
|
5,0
(3,4, 6,6)
|
5,2
(3,6, 6,8)
| |
Pourcentage de patients avec un gain de ≥15 lettres par rapport à la valeur initiale (pourcentage pondéré selon le test CMH, IC à 95%)
|
20,2%
(15,9%, 24,6%)
|
22,2%
(17,7%, 26,8%)
|
22,4%
(17,8%, 27,1%)
|
21,3%
(16,8%, 25,9%)
| |
Pourcentage de patients ayant évité une perte de ≥15 lettres par rapport à la valeur initiale (pourcentage pondéré selon le test CMH, IC à 95%)
|
95,8%
(93,6%, 98,0%)
|
97,3%
(95,5%, 99,1%)
|
92,9%
(90,1%, 95,8%)
|
93,2%
(90,2%, 96,2%)
|
a Moyenne des semaines 40, 44 et 48. b Moyenne des semaines 104, 108, 112.
MAVC: meilleure acuité visuelle corrigée.
ETDRS: Early Treatment Diabetic Retinopathy Study.
IC: intervalle de confiance.
CMH: méthode de Cochran–Mantel–Haenszel; test statistique qui génère l'estimation d'une association avec un résultat binaire et qui est utilisé pour analyser des variables catégorielles.
Figure 1: Études de phase III regroupées dans la DMLAn (TENAYA et LUCERNE): courbe de variation de la MAVC dans l'œil étudié entre l'inclusion et la semaine 112: méthode MMRM (évaluation primaire) (population en ITT)
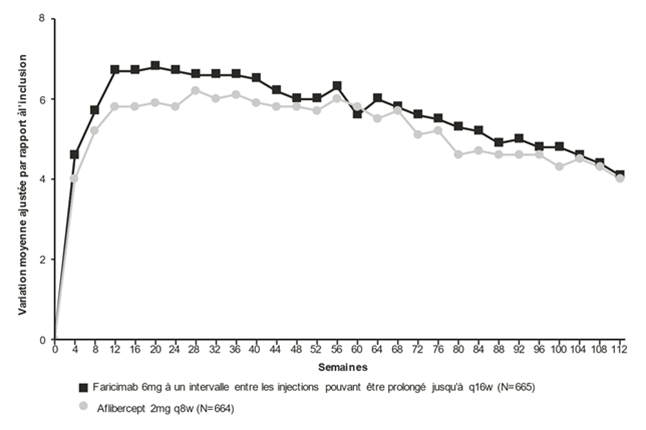
Dans les deux études TENAYA et LUCERNE, les améliorations de la MAVC et de la CST à la semaine 60 par rapport à l'inclusion étaient comparables dans les deux bras de traitement et concordaient avec celles observées à la semaine 48.
Les résultats d'efficacité dans tous les sous-groupes évaluables (p.ex. définis en fonction de l'âge, du sexe, de l'ethnie, de l'acuité visuelle à l'inclusion, du type de lésion, de la taille de la lésion) de chaque étude ainsi que de l'analyse regroupée correspondaient aux résultats observés dans la population globale.
Dans les deux études, l'administration de Vabysmo à un intervalle allant jusqu'à q16w a entraîné des améliorations cliniquement significatives s'agissant du résultat combiné du questionnaire sur la fonction visuelle du National Eye Institute (National Eye Institute Visual Function Questionnaire ou NEI VFQ-25) entre l'inclusion et la semaine 48, lesquelles étaient comparables à celles observées lors de l'administration d'aflibercept q8w. À la semaine 48, les patients inclus dans les bras sous Vabysmo des études TENAYA et LUCERNE ont obtenu une amélioration du résultat combiné du NEI VFQ-25 de ≥4 points par rapport à la valeur initiale.
Traitement de l'œdème maculaire diabétique (OMD)
La sécurité et l'efficacité du faricimab ont été évaluées sur une période de 2 ans dans deux études (YOSEMITE et RHINE) à 3 bras, randomisées (1:1:1), multicentriques, en double aveugle, menées chez des patients atteints d'OMD, en comparaison d'un traitement anti-VEGF. Les patients des trois bras de l'étude ont reçu des injections intravitréennes de 6 mg de faricimab q8w (après 6 injections mensuelles au début du traitement), de 6 mg de faricimab à un intervalle personnalisé entre les injections d'au maximum q16w (après 4 injections mensuelles au début du traitement) ou de 2 mg d'aflibercept q8w (après 5 injections mensuelles au début du traitement). Dans le bras recevant le faricimab à un intervalle entre les injections pouvant être prolongé jusqu'à q16w, le traitement a été administré selon un schéma standardisé T&E. Selon la variation de la CST mesurée par OCT et/ou la variation de la MAVC mesurée à l'aide du score en lettres ETDRS, l'intervalle personnalisé entre les injections dans le groupe recevant le faricimab a pu être prolongé de 4 semaines à chaque rendez-vous pour l'administration de la préparation à l'étude, ou être raccourci de 4 ou 8 semaines (voir «Posologie/Mode d'emploi»).
Les études ont inclus au total 1891 patients (dont environ 94% atteints de diabète sucré de type 2), parmi lesquels 1622 patients (85,8%) ont terminé complètement les études (jusqu'à la semaine 100). Au total, 1887 patients ont été traités avec au moins une dose jusqu'à la fin de la semaine 56 (1262 par Vabysmo). L'âge moyen [intervalle] des patients examinés était de 62,2 ans [de 24 à 91 ans]. La population de l'étude a englobé des patients naïfs d'anti-VEGF (78%) et des patients ayant déjà reçu un traitement anti-VEGF (22%).Le critère principal d'évaluation de l'efficacité était la variation moyenne de la MAVC entre l'inclusion et la fin de la première année (moyenne des semaines 48, 52 et 56), laquelle a été déterminée à l'aide du tableau de lettres de l'Early Treatment Diabetic Retinopathy Study (ETDRS) à une distance de 4 mètres. Dans les deux études, l'hypothèse primaire (non-infériorité) a été confirmée dans les deux bras de traitement: les patients traités par Vabysmo q8w ou par Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w et les patients traités par l'aflibercept q8w présentaient à 1 an une variation moyenne comparable de la MAVC par rapport à leur valeur initiale respective. Ces améliorations de la vision se sont maintenues tout au long de la 2e année.
Après 4 doses mensuelles initiales, les patients du bras sous Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w pouvaient avoir reçu au total au moins 6 et au plus 21 injections jusqu'à la semaine 96 comprise. Dans les études YOSEMITE et RHINE, à la semaine 52, respectivement 74% et 71% des patients des bras sous Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w avaient atteint un intervalle entre les injections de q16w ou q12w (q16w chez 53% et 51%, q12w chez 21% et 20%). Respectivement 75% et 84% des patients inclus dans les études YOSEMITE et RHINE ont conservé un intervalle entre les injections ≥ q12w sans raccourcissement inférieur à q12w jusqu'à la semaine 96 comprise; respectivement 70% et 82% des patients traités avec un intervalle entre les injections de q16w à la semaine 52 ont conservé l'intervalle q16w sans raccourcissement jusqu'à la semaine 96 comprise. À la semaine 96, 78% des patients des bras sous Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w avaient atteint un intervalle entre les injections de q16w ou q12w dans les deux études (q16w chez 60% et 65%, q12w chez 18% et 14%). Chez respectivement 4% et 6% des patients inclus dans les études YOSEMITE et RHINE, l'intervalle a été prolongé à q8w et les patients ont conservé un intervalle entre les injections ≤ q8w jusqu'à la semaine 96 comprise; respectivement 3% et 5% n'ont conservé qu'un intervalle q4w jusqu'à la fin de la semaine 96.
Les tableaux 4, 5, 6, 7 et la figure 2 ci-dessous présentent les résultats détaillés des analyses des études YOSEMITE et RHINE.
Tableau 4: Résultats d'efficacité lors des visites à 1 ana et à 2 ansb visant à examiner le critère d'évaluation principal dans l'étude YOSEMITE
|
Résultats d'efficacité
|
YOSEMITE
| |
Année 1
|
Année 2
| |
Vabysmo
q8w
N = 315
|
Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w
N = 313
|
Aflibercept q8w
N = 312
|
Vabysmo
q8w
N = 315
|
Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w
N = 313
|
Aflibercept
q8w
N = 312
| |
Variation moyenne de la MAVC mesurée à l'aide du score en lettres ETDRS par rapport à la valeur initiale (IC à 97,5% durant l'année 1 et à 95% durant l'année 2)
|
10,7
(9,4, 12,0)
|
11,6
(10,3, 12,9)
|
10,9
(9,6, 12,2)
|
10,7
(9,4, 12,1)
|
10,7
(9,4, 12,1)
|
11,4
(10,0, 12,7)
| |
Pourcentage de patients avec un gain en termes de MAVC d'au moins 15 lettres par rapport à la valeur initiale (pourcentage pondéré selon le test CMH, IC à 95% durant les années 1 et 2)
|
29,2%
(23,9%, 34,5%)
|
35,5%
(30,1%, 40,9%)
|
31,8%
(26,6%, 37,0%)
|
37,2%
(31,4%, 42,9%)
|
38,2%
(32,8%, 43,7%)
|
37,4%
(31,7%, 43,0%)
| |
Pourcentage de patients ayant évité une perte en termes de MAVC d'au moins 15 lettres par rapport à la valeur initiale (pourcentage pondéré selon le test CMH, IC à 95% durant les années 1 et 2)
|
98,1%
(96,5%, 99,7%)
|
98,6%
(97,2%, 100,0%)
|
98,9%
(97,6%, 100,0%)
|
97,6%
(95,7%, 99,5%)
|
97,8%
(96,1%, 99,5%)
|
98,0%
(96,2%, 99,7%)
|
a Moyenne des semaines 48, 52, 56. b Moyenne des semaines 92, 96, 100.
MAVC: meilleure acuité visuelle corrigée.
ETDRS: Early Treatment Diabetic Retinopathy Study.
IC: intervalle de confiance.
CMH: méthode de Cochran–Mantel–Haenszel; test statistique qui génère l'estimation d'une association avec un résultat binaire et qui est utilisé pour analyser des variables catégorielles.
Remarque: les données présentées relatives au pourcentage pondéré selon le test CMH pour le bras recevant l'aflibercept se rapportent à la comparaison entre Vabysmo q8w et l'aflibercept. Les données correspondantes relatives au pourcentage pondéré selon le test CMH pour la comparaison entre Vabysmo avec un intervalle entre les injections pouvant être prolongé et l'aflibercept sont cependant similaires à celles présentées ci-dessus.
ETDRS-DRSS: Early Treatment Diabetic Retinopathy Study Diabetic Retinopathy Severity Scale (échelle d'évaluation d'une rétinopathie diabétique issue de l'Early Treatment Diabetic Retinopathy Study).
Tableau 5: Pourcentage de patients avec une amélioration du score à l'ETDRS-DRSS de ≥2 niveaux par rapport à la valeur initiale à la semaine 52 et à la semaine 96 dans l'étude YOSEMITE (population évaluable pour la RD)
|
Résultats d'efficacité
|
YOSEMITE
| |
52 semaines
|
96 semaines
| |
Vabysmo q8w
N = 237
|
Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w
N = 242
|
Aflibercept q8w
N = 229
|
Vabysmo q8w
N = 220
|
Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w
N = 234
|
Aflibercept q8w
N = 221
| |
Pourcentage de patients avec une amélioration du score à l'ETDRS-DRSS de ≥2 niveaux par rapport à la valeur initiale (pourcentage pondéré selon le test CMH)
|
46,0%
|
42,5%
|
35,8%
|
51,4%
|
42,8%
|
42,2%
|
ETDRS-DRSS: Early Treatment Diabetic Retinopathy Study Diabetic Retinopathy Severity Scale.
IC: intervalle de confiance.
CMH: méthode de Cochran–Mantel–Haenszel; test statistique qui génère l'estimation d'une association avec un résultat binaire et qui est utilisé pour analyser des variables catégorielles.
Remarque: les données présentées relatives au pourcentage pondéré selon le test CMH pour le bras recevant l'aflibercept se rapportent à la comparaison entre Vabysmo q8w et l'aflibercept. Les données correspondantes relatives au pourcentage pondéré selon le test CMH pour la comparaison entre le faricimab avec un intervalle entre les injections pouvant être prolongé et l'aflibercept sont cependant similaires à celles présentées ci-dessus.
Tableau 6: Résultats d'efficacité lors des visites à 1 ana et à 2 ansb visant à examiner le critère d'évaluation principal dans l'étude RHINE
|
Résultats d'efficacité
|
RHINE
| |
Année 1
|
Année 2
| |
Vabysmo q8w
N = 317
|
Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w
N = 319
|
Aflibercept q8w
N = 315
|
Vabysmo q8w
N = 317
|
Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w
N = 319
|
Aflibercept q8w
N = 315
| |
Variation moyenne de la MAVC mesurée à l'aide du score en lettres ETDRS par rapport à la valeur initiale (IC à 97,5% durant l'année 1 et à 95% durant l'année 2)
|
11,8
(10,6, 13,0)
|
10,8
(9,6, 11,9)
|
10,3
(9,1, 11,4)
|
10,9
(9,5, 12,3)
|
10,1
(8,7, 11,5)
|
9,4
(7,9, 10,8)
| |
Pourcentage de patients avec un gain en termes de MAVC d'au moins 15 lettres par rapport à la valeur initiale (pourcentage pondéré selon le test CMH, IC à 95% durant les années 1 et 2)
|
33,8%
(28,4%, 39,2%)
|
28,5%
(23,6%, 33,3%)
|
30,3%
(25,0%, 35,5%)
|
39,8%
(34,0%, 45,6%)
|
31,1%
(26,1%, 36,1%)
|
39,0%
(33,2%, 44,8%)
| |
Pourcentage de patients ayant évité une perte en termes de MAVC d'au moins 15 lettres par rapport à la valeur initiale (pourcentage pondéré selon le test CMH, IC à 95% durant les années 1 et 2)
|
98,9%
(97,6%, 100,0%)
|
98,7%
(97,4%, 100,0%)
|
98,6%
(97,2%, 99,9%)
|
96,6%
(94,4%, 98,8%)
|
96,8%
(94,8%, 98,9%)
|
97,6%
(95,7%, 99,5%)
|
a Moyenne des semaines 48, 52, 56. b Moyenne des semaines 92, 96, 100.
MAVC: meilleure acuité visuelle corrigée.
ETDRS: Early Treatment Diabetic Retinopathy Study.
IC: intervalle de confiance.
CMH: méthode de Cochran–Mantel–Haenszel; test statistique qui génère l'estimation d'une association avec un résultat binaire et qui est utilisé pour analyser des variables catégorielles.
Remarque: les données présentées relatives au pourcentage pondéré selon le test CMH pour le bras recevant l'aflibercept se rapportent à la comparaison entre Vabysmo q8w et l'aflibercept. Les données correspondantes relatives au pourcentage pondéré selon le test CMH pour la comparaison entre Vabysmo avec un intervalle entre les injections pouvant être prolongé et l'aflibercept sont cependant similaires à celles présentées ci-dessus.
ETDRS-DRSS: Early Treatment Diabetic Retinopathy Study Diabetic Retinopathy Severity Scale (échelle d'évaluation d'une rétinopathie diabétique issue de l'Early Treatment Diabetic Retinopathy Study).
Tableau 7: Pourcentage de patients avec une amélioration du score à l'ETDRS-DRSS de ≥2 niveaux par rapport à la valeur initiale à la semaine 52 et à la semaine 96 dans l'étude RHINE (population évaluable pour la RD)
|
Résultats d'efficacité
|
RHINE
| |
52 semaines
|
96 semaines
| |
Vabysmo q8w
N = 231
|
Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w
N = 251
|
Aflibercept q8w
N = 238
|
Vabysmo q8w
N = 214
|
Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w
N = 228
|
Aflibercept q8w
N = 203
| |
Pourcentage de patients avec une amélioration du score à l'ETDRS-DRSS de ≥2 niveaux par rapport à la valeur initiale (pourcentage pondéré selon le test CMH)
|
44,2%
|
43,7%
|
46,8%
|
53,5%
|
44,3%
|
43,8%
|
ETDRS-DRSS: Early Treatment Diabetic Retinopathy Study Diabetic Retinopathy Severity Scale.
IC: intervalle de confiance.
CMH: méthode de Cochran–Mantel–Haenszel; test statistique qui génère l'estimation d'une association avec un résultat binaire et qui est utilisé pour analyser des variables catégorielles.
Remarque: les données présentées relatives au pourcentage pondéré selon le test CMH pour le bras recevant l'aflibercept se rapportent à la comparaison entre Vabysmo q8w et l'aflibercept. Les données correspondantes relatives au pourcentage pondéré selon le test CMH pour la comparaison entre Vabysmo avec un intervalle entre les injections pouvant être prolongé et l'aflibercept sont cependant similaires à celles présentées ci-dessus.
Figure 2: Études de phase III regroupées dans l'OMD (YOSEMITE et RHINE): courbe de variation de la MAVC dans l'œil étudié entre l'inclusion et la semaine 100: méthode MMRM (évaluation primaire) (population en ITT)
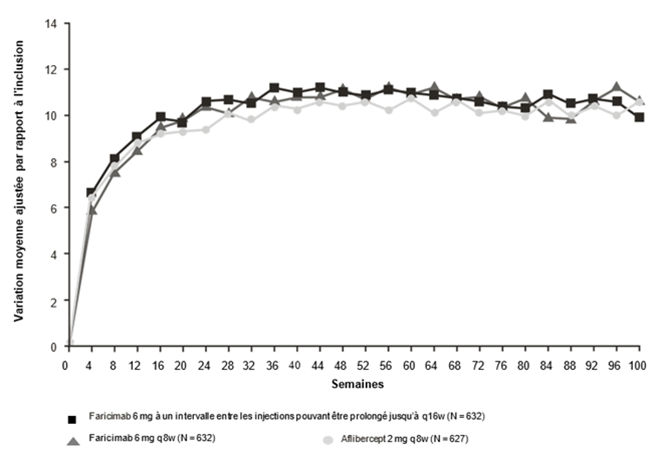
Les résultats d'efficacité chez les patients naïfs de traitement anti-VEGF avant l'inclusion dans l'étude ainsi que dans tous les autres sous-groupes évaluables (p.ex. définis en fonction de l'âge, du sexe, de l'ethnie, du taux d'HbA1c à l'inclusion, de l'acuité visuelle à l'inclusion) de chaque étude correspondaient aux résultats observés dans la population globale respective.
L'efficacité thérapeutique ne dépendait pas du contrôle glycémique. Les résultats obtenus sous le traitement par le faricimab étaient comparables chez les patients dont le taux d'HbA1c s'est amélioré ou détérioré de > 0,5% ou est resté dans les limites de 0,5% de la valeur initiale au cours du temps.
Traitement d'un œdème maculaire secondaire à une OBVR ou à une OVCR
La sécurité et l'efficacité du faricimab ont été évaluées dans deux études multicentriques, menées chez des patients atteints d'œdème maculaire secondaire à une OBVR (BALATON) ou une OVCR/OVHC (COMINO). Ces deux études comprenaient une phase initiale de traitement, de 24 semaines, randomisée (1:1) et contrôlée contre traitement actif (aflibercept). Tous les patients (y compris ceux traités initialement par l'aflibercept) ont ensuite été traités par le faricimab selon un schéma d'administration personnalisé jusqu'à la semaine 68 (dernière visite lors de la semaine 72). Sur la base de l'activité de la maladie (estimée à l'aide d'une évaluation objective et automatisée de critères visuels et anatomiques prédéfinis), l'intervalle entre les injections pouvait à chaque fois être augmenté par paliers de 4 semaines jusqu'à q16w au maximum ou au besoin (détérioration de la CST et/ou de l'acuité visuelle) diminué à nouveau par paliers de 4, 8 ou 12 semaines. Chez les patients pour lesquels une réduction de l'intervalle de traitement avait été nécessaire, cet intervalle n'était pas à nouveau prolongé après stabilisation de l'activité de la maladie, à l'exception des patients pour lesquels l'intervalle entre les injections était minimal (4 semaines).
Au total, 1282 patients (553 dans l'étude BALATON et 729 dans l'étude COMINO) ont été inclus dans les deux études et 1276 patients ont été traités par au moins une dose jusqu'à la semaine 24 incluse (641 par Vabysmo).
Les deux études ont démontré l'efficacité du traitement concernant le critère principal d'évaluation défini comme la variation de la MAVC entre l'inclusion et la semaine 24 et mesuré à l'aide du score en lettres ETDRS. Dans les deux études, les patients traités par Vabysmo q4w ont présenté à la semaine 24 une variation moyenne de la MAVC par rapport à la valeur initiale non inférieure à celle observée chez les patients traités par l'aflibercept q4w et ces améliorations de la vision se sont maintenues jusqu'à la semaine 72 comprise, lorsque les patients sont passés à un schéma de traitement par Vabysmo avec un intervalle entre les injections pouvant être prolongé jusqu'à q16w.
Entre la semaine 24 et la semaine 68, 81,5% des patients inclus dans l'étude BALATON et 74,0% des patients inclus dans l'étude COMINO ayant reçu Vabysmo 6 mg à un intervalle pouvant être prolongé jusqu'à q16w ont atteint un intervalle entre les injections de q16w ou de q12w. Parmi ces patients, 72,1% de ceux inclus dans l'étude BALATON et 61,6% de ceux inclus dans l'étude COMINO ont terminé au moins un cycle avec un intervalle entre les injections de q12w et ont conservé un intervalle entre les injections de q16w ou de q12w sans raccourcissement de l'intervalle inférieur à q12w jusqu'à la semaine 68 comprise; 1,2% des patients inclus dans l'étude BALATON et 2,5% des patients inclus dans l'étude COMINO n'ont conservé qu'un intervalle q4w jusqu'à la semaine 68 comprise.
Les tableaux 8 et 9, la figure 3 et la figure 4 ci-dessous présentent les résultats détaillés de ces deux études.
Tableau 8: Résultats d'efficacité concernant le critère principal d'évaluation à la semaine 24 ainsi qu'à la fin de l'étude BALATON
|
Résultats d'efficacité
|
BALATON
| |
24 semaines
|
72 semainesa
| |
Vabysmo
N = 276
|
Aflibercept
N = 277
|
Passage de Vabysmo q4w à Vabysmo avec un intervalle entre les injections pouvant être prolongé
N = 276
|
Passage de l'aflibercept q4w à Vabysmo avec un intervalle entre les injections pouvant être prolongé
N = 277
| |
Variation moyenne de la MAVC mesurée à l'aide du score en lettres ETDRS par rapport à la valeur initiale (IC à 95%)
|
16,9
(15,7, 18,1)
|
17,5
(16,3, 18,6)
|
18,1
(16,9, 19,4)
|
18,8
(17,5, 20,0)
| |
Pourcentage de patients avec un gain en termes de MAVC d'au moins 15 lettres par rapport à la valeur initiale (pourcentage pondéré selon le test CMH, IC à 95%)
|
56,1%
(50,4%, 61,9%)
|
60,4%
(54,7%, 66,0%)
|
61,5%
(56,0%, 67,0%)
|
65,8%
(60,3%, 71,2%)
|
a Moyenne des semaines 64, 68, 72.
MAVC: meilleure acuité visuelle corrigée.
ETDRS: Early Treatment Diabetic Retinopathy Study.
IC: intervalle de confiance.
CMH: méthode de Cochran–Mantel–Haenszel; test statistique qui génère l'estimation d'une association avec un résultat binaire et qui est utilisé pour analyser des variables catégorielles.
Tableau 9: Résultats d'efficacité concernant le critère principal d'évaluation à la semaine 24 ainsi qu'à la fin de l'étude COMINO
|
Résultats d'efficacité
|
COMINO
| |
24 semaines
|
72 semainesa
| |
Vabysmo
N = 366
|
Aflibercept
N = 363
|
Passage de Vabysmo q4w à Vabysmo avec un intervalle entre les injections pouvant être prolongé
N = 366
|
Passage de l'aflibercept q4w à Vabysmo avec un intervalle entre les injections pouvant être prolongé
N = 363
| |
Variation moyenne de la MAVC mesurée à l'aide du score en lettres ETDRS par rapport à la valeur initiale (IC à 95%)
|
16,9
(15,4, 18,3)
|
17,3
(15,9, 18,8)
|
16,9
(15,2, 18,6)
|
17,1
(15,4, 18,8)
| |
Pourcentage de patients avec un gain en termes de MAVC d'au moins 15 lettres par rapport à la valeur initiale (pourcentage pondéré selon le test CMH, IC à 95%)
|
56,6%
(51,7%, 61,5%)
|
58,1%
(53,3%, 62,9%)
|
57,6%
(52,8%, 62,5%)
|
59,5%
(54,7%, 64,3%)
|
a Moyenne des semaines 64, 68, 72.
MAVC: meilleure acuité visuelle corrigée.
ETDRS: Early Treatment Diabetic Retinopathy Study.
IC: intervalle de confiance.
CMH: méthode de Cochran–Mantel–Haenszel; test statistique qui génère l'estimation d'une association avec un résultat binaire et qui est utilisé pour analyser des variables catégorielles.
Figure 3: Étude de phase III BALATON: courbe de variation de la MAVC entre l'inclusion et la semaine 72: méthode MMRM (évaluation primaire) (population en ITT)
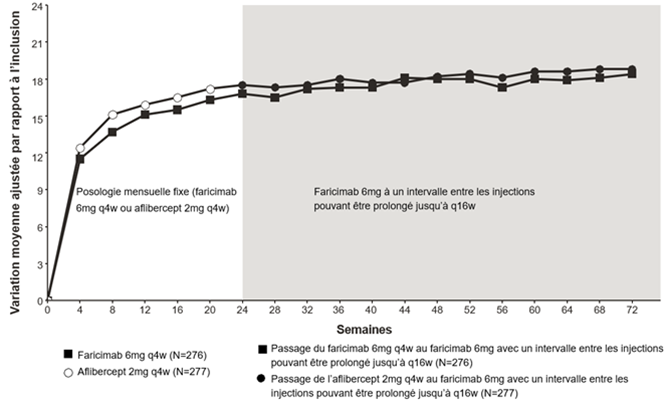
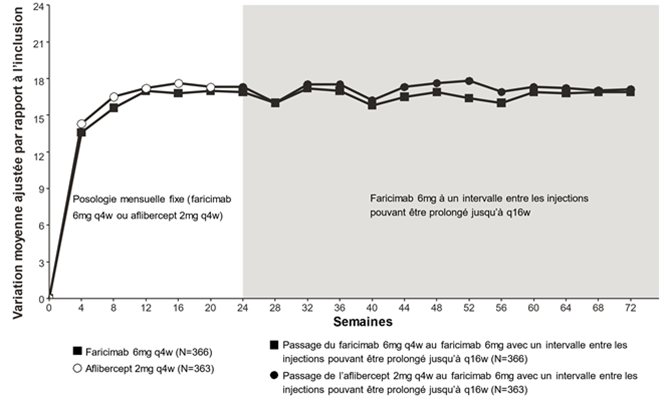
Figure 4: Étude de phase III COMINO: courbe de variation de la MAVC entre l'inclusion et la semaine 72: méthode MMRM (évaluation primaire) (population en ITT)
Patients âgés
Dans les six études cliniques de phase III, environ 58% des patients (1496/2571) ayant reçu un traitement par Vabysmo après la randomisation étaient âgés de ≥65 ans. L'analyse pharmacocinétique de population a montré un effet de l'âge sur la pharmacocinétique oculaire du faricimab, qui n'a pas été considéré comme cliniquement significatif (voir «Posologie/Mode d'emploi, Patients âgés» et «Pharmacocinétique, Patients âgés»).
Pédiatrie
La sécurité et l'efficacité de Vabysmo n'ont pas été évaluées chez les patients pédiatriques.
Informations complémentaires
Immunogénicité
Les patients traités par Vabysmo peuvent présenter une réaction immunitaire (voir «Mises en garde et précautions»).
Après une administration de Vabysmo allant jusqu'à 112 (DMLAn), 100 (OMD) et 72 (OBVR/OVCR) semaines, des anticorps anti-faricimab liés au traitement ont été mis en évidence chez environ 13,8%, 9,6% et 14,4% des patients atteints de DMLAn, d'OMD ou d'OBVR/OVCR qui avaient reçu du faricimab après la randomisation. La signification clinique des anticorps anti-faricimab en termes de sécurité n'est pas élucidée à l'heure actuelle. Une incidence accrue d'effets indésirables s'accompagnant d'une inflammation intraoculaire a été observée chez les patients présentant des anticorps anti-faricimab. Toutefois, l'incidence globale de la positivité des anticorps anti-faricimab et des inflammations intraoculaires est d'environ 1% dans la population totale des études. Les anticorps anti-faricimab n'ont pas été associés à des effets sur l'efficacité clinique ou la pharmacocinétique systémique.
|




