Propriétés/EffetsCode ATC
N02CD07
Mécanisme d'action/pharmacodynamie
L'atogépant est un antagoniste du récepteur du peptide lié au gène de la calcitonine (CGRP) qui bloque la liaison du CGRP au récepteur et s'oppose à la fonction du récepteur du CGRP. Le CGRP est un neuropeptide qui a été associé à la pathophysiologie de la migraine. Dans le système trigéminovasculaire, le CGRP module la signalisation nociceptive et l'inflammation et agit en outre comme un vasodilatateur.
Électrophysiologie cardiaque
À une dose 5 fois supérieure à la dose quotidienne maximale recommandée, AQUIPTA ne prolonge pas l'intervalle QT.
Efficacité clinique
AQUIPTA a été évalué dans deux études d'homologation pour la prophylaxie de la migraine sur l'ensemble du spectre de la migraine chronique et épisodique. Dans l'étude sur la migraine épisodique (ADVANCE) les patients qui répondaient aux critères International Classification of Headache Disorders (ICHD) pour le diagnostic de migraine avec ou sans aura ont été inclus. L'étude sur la migraine chronique (PROGRESS) a inclus des patients qui répondaient également aux critères ICHD de migraine chronique. Les patients ayant des antécédents d'infarctus du myocarde, d'accident vasculaire cérébral ou d'accident ischémique transitoire survenus au cours des six mois précédant la sélection ont été exclus des deux études.
Migraine épisodique
AQUIPTA a été évalué pour la prophylaxie de la migraine épisodique (4 à 14 jours de migraine par mois) dans une étude multicentrique randomisée en double aveugle, contrôlée contre placebo (ADVANCE). Les patients ont été randomisés pour recevoir AQUIPTA 60 mg (N = 235) ou le placebo (N = 223) une fois par jour pendant 12 semaines. Le traitement aigu des céphalées (c'est-à-dire les triptans, les dérivés de l'ergotamine, les AINS, le paracétamol et les opioïdes) était autorisé pour les patients.
Au total, 88 % des patients ont terminé la période d'étude en double aveugle de 12 semaines. L'âge moyen des patients était de 42 ans (entre 18 et 73 ans); 89 % étaient de sexe féminin et 83 % étaient caucasiens. La fréquence moyenne des jours de migraine lors de l'inclusion était d'environ 8 jours de migraine par mois et était comparable dans les deux groupes de traitement.
Le critère d'évaluation principal de l'efficacité était la variation par rapport à l'inclusion du nombre moyen de jours de migraine par mois (JMM) pendant la période de traitement de 12 semaines.
Le traitement par AQUIPTA a démontré des améliorations statistiquement significatives des résultats d'efficacité primaires et secondaires contrôlés par multiplicité dans l'étude ADVANCE par rapport au placebo, comme résumé dans le tableau 4.
Tableau 4. Critères d'efficacité dans l'étude ADVANCE
|
|
AQUIPTA 60 mg
n = 226
|
Placebo
n = 216
| |
Nombre de jours de migraine par mois (JMM) pendant 12 semaines
| |
Inclusion
|
7,8
|
7,5
| |
Variation moyenne par rapport à l'inclusion
|
-4,1
|
-2,5
| |
Différence par rapport au placebo
|
-1,7
|
| |
Valeur p
|
< 0,001
|
| |
Nombre de jours de céphalées par mois pendant 12 semaines
| |
Inclusion
|
9,0
|
8,5
| |
Variation moyenne par rapport à l'inclusion
|
-4,2
|
-2,5
| |
Différence par rapport au placebo
|
-1,7
|
| |
Valeur p
|
< 0,001
|
| |
Nombre de jours d'utilisation d'un traitement de crise par mois pendant 12 semaines
| |
Inclusion
|
6,9
|
6,5
| |
Variation moyenne par rapport à l'inclusion
|
-3,8
|
-2,3
| |
Différence par rapport au placebo
|
-1,4
|
| |
Valeur p
|
< 0,001
|
| |
Répondeurs ayant obtenu une réduction ≥50 % du nombre de JMM pendant 12 semaines
| |
Répondeurs (%)
|
59
|
29
| |
Odds Ratio (IC à 95 %)
|
3,55 (2,39; 5,28)
|
| |
Valeur p
|
< 0,001
|
| |
MSQ v.2.1 RFRa à la semaine 12
| |
Inclusion
|
46,6
|
46,6
| |
Variation moyenne par rapport à l'inclusion
|
31,0
|
20,0
| |
Différence par rapport au placebo
|
11,0
|
| |
Valeur p
|
< 0,001
|
|
aScore sur le Questionnaire Migraine Specific Quality of Life (Qualité de vie spécifique à la migraine) version 2.1 dans la section Role Function Restrictive
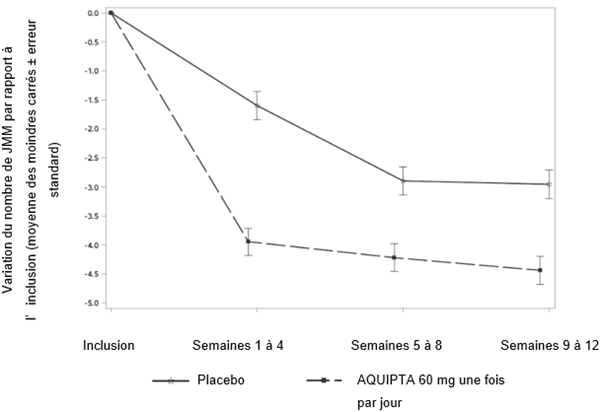
La figure 1 présente la variation moyenne du nombre de jours de migraine par mois (JMM) par rapport à l'inclusion dans l'étude ADVANCE. Comparativement aux patients qui recevaient le placebo, il a été observé chez les patients traités par AQUIPTA 60 mg une fois par jour une diminution moyenne plus importante du nombre de jours de migraine par mois par rapport à l'inclusion pendant la période de traitement de 12 semaines. Comparativement au placebo, AQUIPTA 60 mg, pris une fois par jour, a induit une diminution moyenne plus importante du nombre de jours de migraine par mois par rapport à l'inclusion pendant le premier mois du traitement.
Figure 1: Variation du nombre de jours de migraine par mois (JMM) par rapport à l'inclusion dans l'étude ADVANCE
Efficacité à long terme
Dans une étude en ouvert dans laquelle des patients présentant une migraine épisodique ont reçu AQUIPTA 60 mg une fois par jour, l'efficacité a été maintenue jusqu'à un an. 68,4 % des patients ont terminé la période de traitement. La réduction du nombre moyen de jours de migraine par mois (méthode des moindres carrés) pendant le premier mois (semaines 1 à 4) était de 3,8 jours, avec une amélioration jusqu'à une réduction moyenne (méthode des moindres carrés) de 5,2 jours pendant le dernier mois (semaines 49 à 52). Environ 84 %, 70 % et 48% des patients ont mentionné une réduction ≥50%, ≥75 % et de 100 % respectivement du nombre de jours de migraine par mois aux semaines 49 à 52.
Patients chez lesquels des traitements prophylactiques oraux par des médicaments de deux à quatre classes différentes ont précédemment échoué
Dans l'étude ELEVATE, 315 patients adultes souffrant de migraine épisodique qui n'avaient pas répondu précédemment à des traitements prophylactiques oraux par des médicaments de deux à quatre classes différentes (p.ex. topiramate, antidépresseurs tricycliques, bêtabloquants) en termes d'efficacité et/ou de tolérance ont été randomisés (1:1) pour recevoir soit de l'atogépant à raison de 60 mg (n = 157) soit un placebo (n = 158) pendant douze semaines. Les résultats de cette étude étaient cohérents avec les principaux résultats d'études précédentes sur l'efficacité en cas de migraine épisodique et étaient statistiquement significatifs s'agissant des critères principaux et secondaires d'évaluation de l'efficacité, y compris plusieurs questionnaires destinés aux patients pour évaluer les capacités fonctionnelles. Le nombre de jours de migraine par mois (JMM) a baissé de 4,2 jours sous atogépant alors qu'il a diminué de 1,9 jours sous placebo (p < 0,001). Au total, 50,6 % (78/154) des patients du groupe sous atogépant ont obtenu une réduction du nombre de JMM d'au moins 50 % par rapport à la valeur initiale, contre 18,1 % (28/155) des patients sous placebo (odds ratio [IC à 95 %]: 4,82 [2,85; 8,14]; p < 0,001).
Migraine chronique
AQUIPTA a été évalué pour la prophylaxie de la migraine chronique (15 jours ou plus de céphalées par mois avec au moins 8 jours de migraine) dans une étude multicentrique, randomisée en double aveugle, contrôlée contre placebo (PROGRESS). Les patients ont été randomisés pour recevoir AQUIPTA 60 mg (N = 262) ou le placebo (N = 259) une fois par jour pendant 12 semaines L'utilisation concomitante d'un médicament pour la prophylaxie de la migraine (par exemple, amitriptyline, propranolol, topiramate) était autorisée dans un sous-groupe de patients (11 %). Le traitement aigu des céphalées (c'est-à-dire les triptans, les dérivés de l'ergotamine, les AINS, le paracétamol et les opioïdes) était autorisé pour les patients. Ont également été inclus des patients présentant une utilisation excessive de médicaments de la médication aiguë et des céphalées dues à l'utilisation excessive de médicaments..
Au total, 463 patients (89 %) ont terminé la période d'étude en double aveugle de 12 semaines. L'âge moyen des patients était de 42 ans (entre 18 et 74 ans); 87 % étaient de sexe féminin et 59 % étaient caucasiens. La fréquence moyenne des jours de migraine lors de l'inclusion était d'environ 19 jours de migraine par mois et était comparable dans les deux groupes de traitement.
Le critère d'évaluation principal de l'efficacité était la variation par rapport à l'inclusion du nombre moyen de jours de migraine par mois (JMM) par rapport à l'inclusion pendant la période de traitement de 12 semaines.
Le traitement par AQUIPTA a démontré une amélioration statistiquement significative des résultats d'efficacité primaires et secondaires contrôlés par multiplicité dans l'étude PROGRESS par rapport au placebo, comme résumé dans le tableau 5.
Tableau 5. Critères d'efficacité dans l'étude PROGRESS
|
|
AQUIPTA 60 mg
n = 257
|
Placebo
n = 249
| |
Nombre de jours de migraine par mois (JMM) pendant 12 semaines
| |
Inclusion
|
19,2
|
19,0
| |
Variation moyenne par rapport à l'inclusion
|
-6,8
|
-5,1
| |
Différence par rapport au placebo
|
-1,7
|
| |
Valeur p
|
0,002
|
| |
Nombre de jours de céphalées par mois pendant 12 semaines
| |
Inclusion
|
21,5
|
21,4
| |
Variation moyenne par rapport à l'inclusion
|
-6,9
|
-5,2
| |
Différence par rapport au placebo
|
-1,7
|
| |
Valeur p
|
0,002
|
| |
Nombre de jours d'utilisation d'un traitement de crise par mois pendant 12 semaines
| |
Inclusion
|
15,5
|
15,3
| |
Variation moyenne par rapport à l'inclusion
|
-6,2
|
-4,1
| |
Différence par rapport au placebo
|
-2,1
|
| |
Valeur p
|
0,002
|
| |
Répondeurs ayant obtenu une réduction ≥50 % du nombre de JMM pendant 12 semaines
| |
Répondeurs (%)
|
40
|
27
| |
Différence par rapport au placebo (%)
|
14
|
| |
Valeur p
|
0,002
|
| |
MSQ v.2.1 RFRa à la semaine 12
| |
Inclusion
|
43,3
|
44,1
| |
Variation moyenne par rapport à l'inclusion
|
23,1
|
17,3
| |
Différence par rapport au placebo
|
5,8
|
| |
Valeur p
|
0,002
|
|
aScore sur le Questionnaire Migraine Specific Quality of Life (Qualité de vie spécifique à la migraine) version 2.1 dans la section Role Function Restrictive
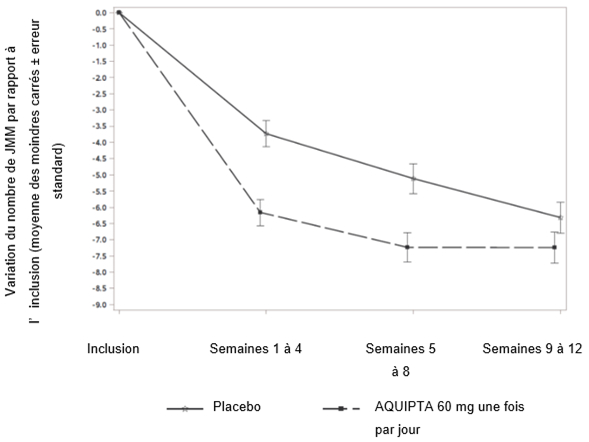
La figure 2 présente la variation moyenne du nombre de jours de migraine par mois (JMM) par rapport à l'inclusion dans l'étude PROGRESS. Les patients traités par AQUIPTA 60 mg une fois par jour ont présenté une réduction moyenne plus importante du nombre de jours de migraine par mois par rapport à l'inclusion pendant la période de traitement de 12 semaines, par rapport aux patients ayant reçu un placebo.
Figure 2: Variation du nombre de jours de migraine par mois (JMM) par rapport à l'inclusion dans l'étude PROGRESS
Pédiatrie
Il n'existe pas de données sur l'utilisation chez les enfants et les adolescents de moins de 18 ans.
|


