Propriétés/EffetsCode ATC
C02KX06
Mécanisme d'action
Le sotatercept, protéine de fusion recombinante du récepteur de l'activine de type IIA-Fc (ActRIIA-Fc), est un inhibiteur de la voie de signalisation de l'activine, qui se lie à l'activine A et d'autres ligands de la superfamille des TGF-β. En conséquence, le sotatercept améliore l'équilibre entre la signalisation pro-proliférative (médiée par ActRIIA/Smad2/3) et antiproliférative (médiée par BMPRII/Smad1/5/8) pour moduler la prolifération vasculaire.
Pharmacodynamique
Une étude clinique de phase II a évalué les résistances vasculaires pulmonaires (RVP) chez des patients atteints d'HTAP après 24 semaines de traitement par le sotatercept. La diminution des RVP par rapport à l'inclusion était significativement plus importante dans les groupes sotatercept 0,7 mg/kg et 0,3 mg/kg que dans le groupe placebo. La différence moyenne des moindres carrés (MC) ajustée au placebo par rapport à l'inclusion était de -269,4 dynes•s/cm5 (IC à 95%: -365,8; -173,0) pour le groupe sotatercept 0,7 mg/kg et de -151,1 dynes•s/cm5 (IC à 95%: -249,6; -52,6) pour le groupe sotatercept 0,3 mg/kg. Dans l'étude STELLAR, la diminution des RVP par rapport à l'inclusion était également significativement plus importante dans le groupe sotatercept 0,7 mg/kg que dans le groupe placebo (voir «Efficacité clinique»).
Dans des modèles d'HTAP chez le rat, un analogue du sotatercept a réduit l'expression des marqueurs pro-inflammatoires au niveau de la paroi artérielle pulmonaire, a réduit le recrutement de leucocytes, a inhibé la prolifération des cellules endothéliales et des cellules musculaires lisses et a favorisé leur apoptose dans le système vasculaire affecté. Ces modifications cellulaires étaient associées à un amincissement de la paroi des vaisseaux, à une inversion du remodelage artériel et ventriculaire droit et à une amélioration de l'hémodynamique.
Efficacité clinique
L'efficacité de Winrevair a été évaluée chez des patients adultes atteints d'HTAP dans l'étude STELLAR. STELLAR était une étude clinique mondiale, en double aveugle, contrôlée contre placebo, multicentrique et en groupes parallèles, dans laquelle 323 adultes atteints d'HTAP (groupe 1 de l'OMS, classe fonctionnelle II ou III) ont été randomisés selon un rapport de 1/1 pour recevoir Winrevair (dose cible de 0,7 mg/kg) (n = 163) ou le placebo (n = 160) administré par voie sous-cutanée une fois toutes les 3 semaines.
Les caractéristiques initiales démographiques et cliniques étaient généralement comparables entre le groupe Winrevair et le groupe placebo. Les personnes participant à l'étude étaient des adultes d'un âge médian de 48,0 ans (intervalle:18 à 82 ans); leur poids médian était de 68 kg (intervalle: 38,0 à 141,3 kg); 89,2% de ces personnes étaient blanches et 79,3% n'étaient ni hispaniques, ni latino-américaines; 79,3% étaient des femmes. Les étiologies les plus fréquentes de l'HTAP étaient: HTAP idiopathique (58,5%), HTAP héritable (18,3%) et HTAP associée à une connectivite (14,9%). La durée médiane entre le diagnostic d'HTAP et la sélection était de 8,76 ans. La plupart des participants recevaient un traitement de fond en trithérapie (61,3%) ou en bithérapie (34,7%). Plus d'un tiers (39,9%) recevaient des perfusions de prostacycline. Le pourcentage de participants ayant une HTAP et se trouvant en classe fonctionnelle II de l'OMS (48,6%) ou en classe fonctionnelle III de l'OMS (51,4%) était similaire dans les deux groupes. L'étude STELLAR a exclu les patients avec un diagnostic d'HTAP associée au virus de l'immunodéficience humaine (VIH), d'HTAP associée à une hypertension portale, d'HTAP associée à une schistosomiase et de maladie veino-occlusive pulmonaire.
Le critère principal d'évaluation de l'efficacité était la comparaison entre la distance parcourue au test de marche de 6 minutes (6MWD) à l'inclusion et à la semaine 24. Dans le groupe traité par Winrevair, la variation médiane de la distance parcourue au 6MWD ajustée au placebo entre l'inclusion et la semaine 24 était de 40,8 mètres (IC à 95%: 27,5; 54,1; p<0,001). La variation médiane de la distance parcourue au 6MWD ajustée au placebo entre l'inclusion et la semaine 24 a également été évaluée dans des sous-groupes (voir Figure 1).
Figure 1: Variation de la distance parcourue au test de marche de 6 minutes (en mètres) entre l'inclusion et la semaine 24 dans les sous-groupes
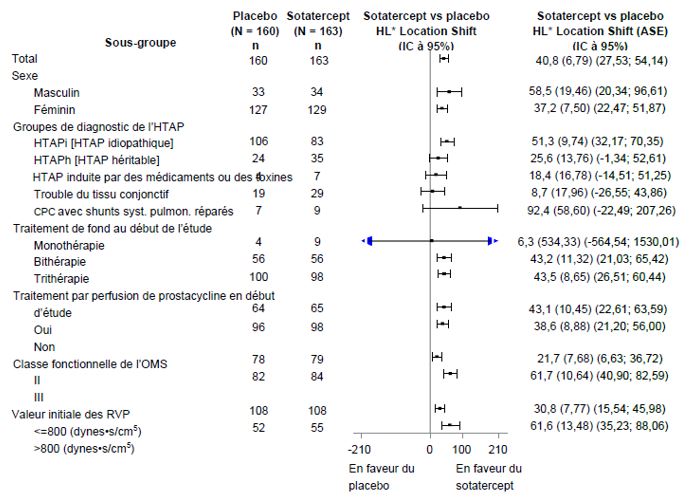
CPC = cardiopathie congénitale
* Estimation du changement de localisation de Hodges-Lehmann par rapport au placebo (médiane de toutes les différences appariées). ASE= asymptomatic standard error (erreur type asymptomatique). Pour les participants qui sont décédés, une valeur allant jusqu’à -2000 mètres a été attribuée à la variation de la distance parcourue au 6MWD à la semaine 24 par rapport à la valeur initiale, afin d’obtenir le plus mauvais rang. Pour les participants dont les données sont manquantes en raison d’une aggravation clinique non fatale, une valeur allant jusqu’à -1000 mètres a été attribuée à la variation de la distance parcourue au 6MWD à la semaine 24 par rapport à la valeur initiale, afin d’obtenir le deuxième plus mauvais rang.
L'amélioration clinique était un critère d'évaluation prédéfini, qui a été mesuré grâce au pourcentage de patients qui remplissaient les trois critères suivants à la semaine 24 par rapport à la situation initiale: amélioration de la distance parcourue au 6MWD (augmentation ≥30 m), amélioration du taux de peptides natriurétiques de type pro-B N-terminal (NT-proBNP) (réduction du NT-proBNP de ≥30% ou maintien/atteinte d'un taux de NT-proBNP <300 ng/l, et amélioration de la classe fonctionnelle de l'OMS ou maintien en classe fonctionnelle II. La progression de la maladie a été mesurée en tant que délai jusqu'au décès ou jusqu'à la survenue du premier événement d'aggravation clinique. Événements d'aggravation clinique: inscription sur liste d'attente de transplantation pulmonaire et/ou cardiaque liée à une aggravation, nécessité de débuter un traitement de secours par un traitement de référence de l'HTAP approuvé ou nécessité d'augmenter la dose de la perfusion de prostacycline de ≥10%, nécessité d'une septostomie atriale, hospitalisation liée à une aggravation de l'HTAP (≥24 h), ou aggravation de l'HTAP (dégradation de la classe fonctionnelle de l'OMS et diminution de la distance parcourue au 6MWD de ≥15% par rapport à l'inclusion, ces deux événements pouvant se produire simultanément ou à des moments différents). Les événements d'aggravation clinique et les cas de décès ont été recensés jusqu'à ce que le dernier patient termine les visites en semaines 24 (données obtenues jusqu'à la date limite; durée médiane d'exposition de 33,6 semaines).
Chez les patients traités par Winrevair, par rapport aux patients du groupe placebo, on a observé une amélioration clinique statistiquement significative, une amélioration de la classe fonctionnelle de l'OMS et une progression retardée de la maladie comprenant un risque moindre de décès et d'hospitalisation (voir Tableau 4 et Figure 2).
En semaine 24, 38,9% des patients sous sotatercept ont présenté une amélioration du MCI contre 10,1% dans le groupe placebo (p<0,001). La différence médiane de traitement des RVP entre le groupe sotatercept et le groupe placebo était de -234,6 dynes*s/cm5 (IC à 95%: -288,4; -180,8; p<0,001). La différence médiane de traitement des NT-proBNP entre le groupe sotatercept et le groupe placebo était de -441,6 pg/ml (IC à 95%: -573,54; -309,61; p<0,001). Une amélioration de la classe fonctionnelle par rapport à la valeur initiale est survenue chez 29% des patients du groupe sotatercept contre 13,8% dans le groupe placebo (p<0,001).
Tableau 4: Décès ou événements d'aggravation clinique
|
|
Placebo
(N = 160)
|
Winrevair
(N = 163)
| |
Nombre total de patients qui sont décédés ou qui ont souffert d'au moins un événement d'aggravation clinique, n (%)
|
42 (26,3)
|
9 (5,5)
| |
Évaluation du décès ou de la survenue du premier événement d'aggravation clinique*, n (%)
|
|
| |
Décès
|
6 (3,8)
|
2 (1,2)
| |
Inscription sur liste d'attente de transplantation pulmonaire et/ou cardiaque liée
à une aggravation
|
1 (0,6)
|
1 (0,6)
| |
Nécessité de débuter un traitement de secours par un traitement de référence
de l'HTAP approuvé ou nécessité d'augmenter la dose de la perfusion de
prostacycline de ≥10%
|
17 (10,6)
|
2 (1,2)
| |
Nécessité d'une septostomie atriale
|
0 (0,0)
|
0 (0,0)
| |
Hospitalisation spécifiquement liée à l'HTAP (≥24 h)
|
7 (4,4)
|
0 (0,0)
| |
Aggravation de l'HTAP†
|
15 (9,4)
|
4 (2,5)
| |
* Pour un même patient, plus d'une évaluation peut être documentée pour le premier événement d'aggravation clinique. Chez 3 patients sous placebo et 0 patient sous sotatercept, plus d'une évaluation a été documentée pour leur premier événement d'aggravation clinique.
† La détérioration de l'HTAP est définie par la survenue des deux événements suivants à tout moment, même s'ils se sont produits à des moments différents, par rapport à leurs valeurs à l'inclusion: (a) aggravation de la classe fonctionnelle de l'OMS (II à III, III à IV, II à IV, etc.); et (b) diminution de la distance parcourue au 6MWD de ≥15% (confirmée par deux tests de marche de 6 minutes à au moins 4 heures d'intervalle, mais sans dépasser une semaine).
N = nombre de patients dans la population FAS; n = nombre de patients dans la catégorie. Les pourcentages sont calculés sous forme de (n/N)•100.
|
Figure 2: Courbe de Kaplan-Meier du délai jusqu'au décès ou jusqu'à la survenue du premier événement d'aggravation clinique
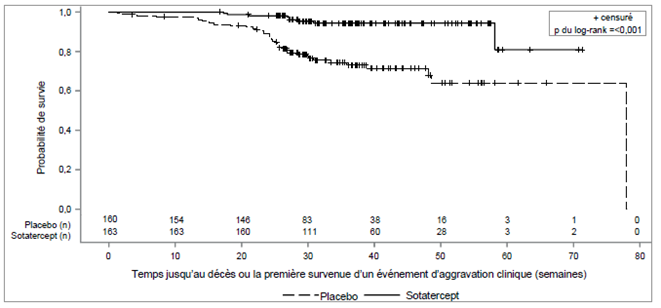
n = nombre de sujets à risque
|


