Dosierung/AnwendungMetalyse sollte so früh wie möglich nach Symptombeginn verabreicht werden.
Metalyse wird körpergewichtsbezogen verabreicht, mit einer maximalen Dosis von 10'000 U. Das Injektionsvolumen zur Verabreichung der richtigen Dosis kann mittels des folgenden Schemas ermittelt werden:
|
Körpergewicht des Patienten (kg)
|
Tenecteplase
(U)
|
Tenecteplase
(mg)
|
Volumen der gebrauchsfertigen Lösung (ml)
| |
< 60
|
6'000
|
30
|
6
| |
≥ 60 bis < 70
|
7'000
|
35
|
7
| |
≥ 70 bis < 80
|
8'000
|
40
|
8
| |
≥ 80 bis < 90
|
9'000
|
45
|
9
| |
≥ 90
|
10'000
|
50
|
10
|
Herstellung der Injektionslösung: siehe «Korrekte Art der Anwendung».
Begleittherapie
Es wird empfohlen, die antithrombotische Begleittherapie entsprechend den derzeitigen internationalen Richtlinien zur Behandlung von Myokardinfarkt mit ST-Hebung durchzuführen.
Für eine primäre perkutane koronare Intervention (PCI) siehe «Warnhinweise und Vorsichtsmassnahmen».
Zur Kombination von Metalyse mit Enoxaparin bzw. mit Abciximab siehe ASSENT-3-Studie in Kapitel «Eigenschaften/Wirkungen».
Spezielle Dosierungsanweisungen
Kinder und Jugendliche
Die Anwendung und Sicherheit von Metalyse, Injektionspräparat bei Kindern und Jugendlichen unter 18 Jahren ist bisher nicht geprüft worden.
Korrekte Art der Anwendung
Die rekonstituierte Lösung sollte intravenös verabreicht werden und ist zum sofortigen Gebrauch bestimmt.
Die erforderliche Dosis ist als intravenöser Einfach-Bolus innerhalb von 5-10 Sekunden zu verabreichen.
Zubereitung der Injektionslösung:
Die Herstellung der Metalyse-Lösung erfolgt durch Zugabe der gesamten Menge Wasser für Injektionszwecke aus der Fertigspritze in die Durchstechflasche mit dem Pulver.
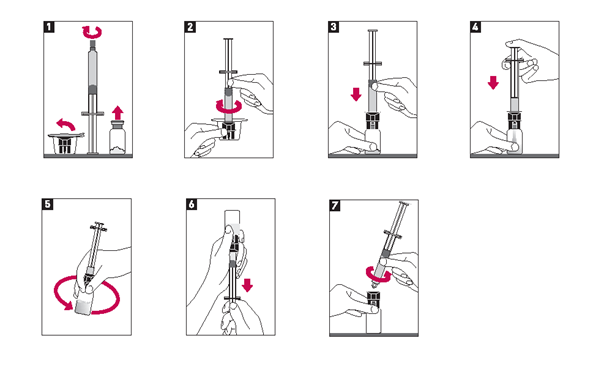
1.Prüfen Sie die Unversehrtheit der Verschlusskappe der Durchstechflasche und entfernen Sie die Verschlusskappe (Abbildung 1).
2.Entfernen Sie ebenfalls die Verschlusskappe der Fertigspritze (Abbildung 1).
3.Schrauben Sie unverzüglich die Fertigspritze auf den Adapter (Abbildung 2) und durchstechen Sie den Verschluss der Durchstechflasche mit Hilfe der Adapterspitze (Abbildung 3).
4.Injizieren Sie das Wasser in die Durchstechflasche durch langsames Niederdrücken des Spritzenstempels, um Schäumen zu vermeiden (Abbildung 4).
5.Lassen Sie die Fertigspritze am Adapter befestigt und lösen Sie das Pulver durch leichtes Schwenken (Abbildung 5).
6.Die rekonstituierte Lösung ist farblos bis schwach gelblich und klar. Nur klare, partikelfreie Lösungen verwenden.
7.Drehen Sie die Durchstechflasche samt Spritze unmittelbar vor Gabe der Lösung um, so dass sich nun die Spritze unten befindet (Abbildung 6).
8.Ziehen Sie das erforderliche Volumen Metalyse-Lösung in die Spritze auf, entsprechend dem Körpergewicht des Patienten (Abbildung 6) (siehe auch die entsprechende Tabelle unter «Dosierung/Anwendung»).
9.Schrauben Sie die Spritze vom Adapter ab (Abbildung 7).
10.Ein bereits vorhandener intravenöser Zugang, der ausschliesslich der Gabe von 0,9%iger Natriumchloridlösung diente, kann für die Verabreichung von Metalyse verwendet werden. Metalyse darf nicht mit anderen Arzneimitteln gemischt werden, weder in derselben Durchstechflasche noch über denselben intravenösen Zugang (auch nicht mit Heparin). Die Lösung nicht über eine Infusionsleitung geben, die Glukose enthält, da Metalyse mit Glukoselösung inkompatibel ist.
11.Metalyse wird intravenös innerhalb von 5-10 Sekunden verabreicht.
12.Der Zugang sollte nach der Metalyse-Injektion mit 0.9%iger Natriumchloridlösung durchgespült werden, um eine einwandfreie Abgabe zu gewährleisten.
13.Nicht verbrauchte Lösung sollte verworfen werden.
Alternativ kann die Zubereitung der Injektionslösung mit einer Injektionsnadel anstelle des mitgelieferten Adapters erfolgen.
Rückverfolgbarkeit
Um die Rückverfolgbarkeit von biotechnologisch hergestellten Arzneimitteln sicherzustellen, wird empfohlen Handelsname und Chargennummer bei jeder Behandlung zu dokumentieren.
| 
