Eigenschaften/WirkungenATC-Code
S01XA27
Wirkungsmechanismus
Luxturna wurde entwickelt, um eine normale Kopie des Gens, das für das menschliche retinale Pigmentepithel-spezifische 65-Kilodalton-Protein (RPE65) kodiert, an Zellen der Netzhaut bei Personen mit reduziertem oder fehlendem Gehalt an biologisch aktivem RPE65 zu liefern. RPE65 wird in den retinalen Pigmentepithelzellen (RPE) produziert und wandelt all-trans-Retinol in 11-cis-Retinol um, das anschliessend während des Sehzyklus (Retinoidzyklus) zum Chromophor 11-cis-Retinal umgewandelt wird. Der Sehzyklus ist entscheidend bei der Phototransduktion, d.h. die biologische Umwandlung eines Lichtphotons in ein elektrisches Signal in der Netzhaut. Mutationen im RPE65-Gen führen zu einer verminderten oder fehlenden Aktivität der RPE65-Isomerohydrolase, was den Sehzyklus blockiert. Im Laufe der Zeit führt die Akkumulation von toxischen Zwischenprodukten zum Absterben der Zellen des retinalen Pigmentepithels und in der Folge zum fortschreitenden Zelltod der Photorezeptoren, und somit zu einer Beeinträchtigung des Sehvermögens und letztlich zu einer vollständigen Erblindung.
Pharmakodynamik
Die Injektion von Luxturna in den Subretinalraum führt zur Transduktion von retinalen Pigmentepithelzellen mit cDNA, die für das normale humane RPE65-Protein kodiert und somit das Potential zur Wiederherstellung des Sehzyklus bietet.
Klinische Wirksamkeit
Klinische Studien: Studie 301
Die Wirksamkeit von Luxturna bei pädiatrischen und erwachsenen Patienten wurde in einer offenen, zweizentrischen, randomisierten Studie untersucht (Studie 301).
Von den 31 in die Studie eingeschlossenen Patienten (13 männlich, 18 weiblich) wurden 21 randomisiert, um eine subretinale Injektion mit Luxturna zu erhalten. DNA-Tests auf das Vorhandensein von biallelischen RPE65-Mutationen und Mutationstypen wurden in einem US-CLIA-zertifizierten Labor unter Verwendung der Sanger-Sequenzierungsmethode durchgeführt. Das Vorhandensein von ausreichend lebensfähigen Retinazellen (ein retinaler Bereich innerhalb des hinteren Pols von > 100 Mikrometer Dicke, bestimmt mittels optischer Kohärenztomographie [OCT]) wurden bei allen Patienten festgestellt. Die Sehschärfe (logMAR) des ersten Auges dieser Patienten betrug zu Studienbeginn im Mittel 1.18 (0.14 Standardfehler). Ein Patient wurde vor der Behandlung aus der Studie ausgeschlossen. 10 Patienten wurden in die Kontrollgruppe (ohne Intervention) randomisiert. Ein Patient der Kontrollgruppe zog seine Einwilligung zur Studienteilnahme zurück und wurde daraufhin aus der Studie ausgeschlossen. Die neun Patienten, die in die Kontrollgruppe randomisiert worden waren, wechselten nach einem Jahr Beobachtung in die Interventionsgruppe, um eine subretinale Injektion mit Luxturna zu erhalten. Das Durchschnittsalter der 31 randomisierten Patienten betrug 15 Jahre (Altersbereich 4 bis 44 Jahre), darunter 64% pädiatrische Patienten (n=20, Alter 4 bis 17 Jahre) und 36% Erwachsene (n=11). Bilaterale subretinale Injektionen mit Luxturna wurden nacheinander in zwei separaten chirurgischen Verfahren durchgeführt, wobei der Zeitintervall zwischen den Injektionen 6 bis 18 Tage betrug.
Der primäre Endpunkt der Phase-3-Studie mass die mittlere Veränderung ab Studienbeginn bis zu einem Jahr mittels Multi-Luminanz-Mobilitätstest (multi-luminance mobility testing, MLMT) an beiden Augen zwischen der Interventions- und der Kontrollgruppe.Der MLMT war dafür ausgelegt, Veränderungen im funktionalen Sehen zu messen, speziell die Fähigkeit eines Patienten, einen Parcours präzise und in akzeptabler Geschwindigkeit bei unterschiedlich heller Umgebungsbeleuchtung zu absolvieren. Diese Fähigkeit ist von der Sehschärfe, dem Gesichtsfeld und dem Grad der Nyktalopie (verminderte Wahrnehmungsfähigkeit und / oder Sehfähigkeit bei schwachem Licht) des Patienten abhängig, wobei jede dieser Funktionen spezifisch durch die RPE65-Mutation-assoziierte Netzhauterkrankung betroffen ist.
Die MLMT wurde mit beiden Augen (binokulares Sehen) und jedem Auge separat bei einer oder mehreren von sieben Helligkeitsstufen bewertet, die von 400 Lux (entsprechend zum Beispiel einem hell beleuchteten Büro) bis 1 Lux (entsprechend zum Beispiel einer mondlosen Sommernacht) reichten. Jeder Helligkeitsstufe wurde ein Score im Bereich von 0 bis 6 zugeordnet. Ein höherer Score gibt dabei an, dass ein Patient in der Lage war, den MLMT bei geringerer Helligkeit zu bestehen. Der MLMT jedes einzelnen Patienten wurde per Video aufgezeichnet und von unabhängigen Prüfern mit einer definierten Kombination aus Geschwindigkeits- und Genauigkeitswerten beurteilt. Der MLMT-Score wurde durch die niedrigste Helligkeitsstufe bestimmt, bei der der Patient den MLMT bestand. Die Veränderung des MLMT-Scores war definiert als die Differenz zwischen dem Score zu Studienbeginn (Baseline) und nach einem Jahr. Eine positive Veränderung im Score von Studienbeginn (Baseline) bis Jahr 1 gibt an, dass der Patient in der Lage war, den MLMT bei geringerer Helligkeit zu bestehen, dabei steht ein Lux-Score von 6 für die maximal mögliche MLMT-Verbesserung.
Zudem wurden drei sekundäre Endpunkte überprüft: ein Vollfeld-Lichtempfindlichkeits-Schwellenwert-Test (full-field light sensitivity threshold, FST) bei Weisslicht, die Änderung des MLMT-Scores für das zuerst behandelte Auge und ein Sehschärfetest (visual acuity, VA).
In Tabelle 2 ist die durchschnittliche Veränderung des MLMT-Scores von Studienbeginn (Baseline) bis Jahr 1 in der Luxturna-Behandlungsgruppe im Vergleich zur Kontrollgruppe zusammengefasst. Zu Studienbeginn bestanden die Patienten den Mobilitätstest bei Beleuchtungsstärken zwischen 4 und 400 Lux.
Tabelle 2: Veränderungen des MLMT-Scores: Jahr 1 im Vergleich zu Studienbeginn (Baseline) (ITT-Population: n=21 Intervention; n=10 Kontrolle)
|
Veränderung des MLMT-Scores
|
Differenz
(95%-KI)
Intervention/Kontrolle
|
p-Wert
| |
Mit beiden Augen
|
1.6 (0.72; 2.41)
|
0.001
| |
Nur mit dem zuerst behandelten Auge
|
1.7 (0.89; 2.52)
|
0.001
| |
Nur mit dem als zweites behandelten Auge
|
2.0 (1.14; 2.85)
|
< 0.001
|
Die Analyse des bilateralen MLMT-Änderungsscores für die Intention-to-Treat-Population (ITT) ergab einen statistisch signifikanten Behandlungseffekt mit einer mittleren Gruppendifferenz (95% Konfidenzintervall [CI]) von 1,6 (0.72, 2.41; p = 0.001).
Die Veränderung des monokularen MLMT-Scores verbesserte sich in der Behandlungsgruppe signifikant und war ähnlich den binokularen MLMT-Ergebnissen (siehe Tabelle 2).
Tabelle 3 zeigt die Anzahl und den Prozentsatz der Patienten mit unterschiedlichem Ausmass der Veränderungen des MLMT-Scores mit beiden Augen im Jahr 1. Elf der 21 (52%) Patienten in der Luxturna-Behandlungsgruppe wiesen eine Veränderung des MLMT-Scores von zwei oder mehr auf, während einer der zehn (10%) Patienten in der Kontrollgruppe eine Veränderung des MLMT-Scores von zwei aufwies.
Dabei ist zu beachten, dass 8 Patienten (38%) in der Luxturna Gruppe eine Veränderung des MLMT-Scores von eins aufwiesen, während 3 Patienten der Kontrollgruppe (30%) ebenfalls eine Verbesserung des MLMT-Scores von eins aufwiesen. Daher könnte die Verbesserung um 1 MLMT-Score auch als tagesabhängige Schwankung interpretierbar sein.
Tabelle 3: Ausmass der Veränderung des MLMT-Scores mit beiden Augen im Jahr 1
|
Veränderung des Scores
|
Luxturna
(n=21)
|
Kontrolle
(n=10)
| |
-1
|
0
|
3 (30%)
| |
0
|
2 (10%)
|
3 (30%)
| |
1
|
8 (38%)
|
3 (30%)
| |
2
|
5 (24%)
|
1 (10%)
| |
3
|
5 (24%)
|
0
| |
4
|
1 (4%)
|
0
|
Abbildung 1 zeigt die MLMT-Ergebnisse einzelner Patienten mit beiden Augen zu Studienbeginn (Baseline) und im Jahr 1.
Abbildung: 1 Binokularer MLMT-Score zu Studienbeginn und nach einem Jahr für einzelne Patienten

Hinweis zur Abbildung 1: *Patienten, die aus der Studie ausgeschlossen wurden oder diese abbrachen. Die nicht ausgefüllten Kreise sind die Scores bei Studienbeginn (Baseline). Die ausgefüllten Kreise sind die Scores nach 1 Jahr. Die Zahlen neben dem ausgefüllten Kreis entsprechen den Veränderungen des Scores im Jahr 1 dar. Die horizontalen Linien mit Pfeilen stellen das Ausmass der Veränderung und die Richtung dar. Pfeile, die nach rechts zeigen, stellen eine Verbesserung dar. Der obere Abschnitt zeigt die Ergebnisse der 21 Patienten in der Behandlungsgruppe. Der untere Abschnitt zeigt die Ergebnisse der 10 Patienten in der Kontrollgruppe. Die Patienten in jeder Gruppe sind chronologisch nach Alter geordnet, wobei der jüngste Patient oben und der älteste unten aufgeführt ist.
Abbildung 2 zeigt die Wirkung des Arzneimittels über den 3-Jahres-Zeitraum in der Voretigen Neparvovec-Behandlungsgruppe sowie die Wirkung in der Kontrollgruppe nach dem Wechsel in die Interventionsgruppe und dem Erhalt subretinaler Injektionen mit Voretigen Neparvovec. An Tag 30 wurden für die Voretigen Neparvovec-Behandlungsgruppe signifikante Unterschiede in den binokularen MLMT-Ergebnissen festgestellt, die über die verbleibenden Nachbeobachtungstermine im gesamten Dreijahreszeitraum aufrechterhalten werden konnten, im Vergleich zur Kontrollgruppe, in der es zu keiner Veränderung kam. Nach dem Wechsel in die Interventionsgruppe und dem Erhalt subretinaler Injektionen mit Voretigen Neparvovec zeigten die Patienten der Kontrollgruppe jedoch ein ähnliches Ansprechen auf Voretigen Neparvovec wie die Patienten der Voretigen Neparvovec-Behandlungsgruppe.
Abbildung 2: Veränderung des MLMT-Scores mit beiden Augen vs. der Zeit vor/nach Exposition mit Voretigen Neparvovec
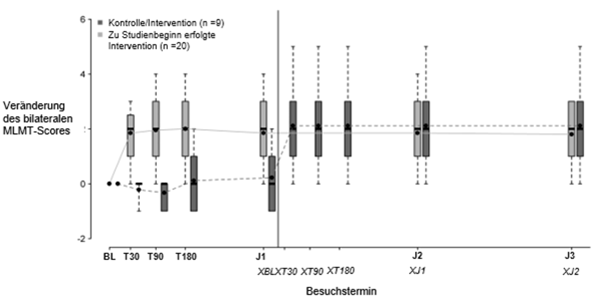
Hinweis zu Abbildung 2: Jede Box stellt die mittleren 50% der Verteilung der MLMT-Score-Veränderungen dar. Die vertikal gestrichelten Linien stellen die weiteren 25% oberhalb und unterhalb der Box dar. Der horizontale Balken innerhalb jeder Box stellt den Median dar. Der Punkt innerhalb jeder Box stellt den Mittelwert dar. Die durchgezogene Linie verbindet die mittleren MLMT-Score-Veränderungen über die Besuchstermine der Behandlungsgruppe hinweg. Die gestrichelte Linie verbindet die mittleren MLMT-Score-Veränderungen über die Besuchstermine der Kontrollgruppe hinweg, einschliesslich der fünf Besuchstermine im ersten Jahr ohne Voretigen Neparvovec-Behandlung. Der Kontrollgruppe wurde nach einem Jahr Beobachtung Voretigen Neparvovec verabreicht.
BL: Baseline;
T30, T90, T180: 30, 90 und 180 Tage nach Studienbeginn;
J1, J2, J3: ein, zwei und drei Jahre nach Studienbeginn;
XBL; XT30; XT90; XT180: Baseline, 30, 90 und 180 Tage nach Studienbeginn für die Kontrollgruppe nach dem Wechsel in die Interventionsgruppe;
XJ1; XJ2: ein und zwei Jahre nach Studienbeginn für die Kontrollgruppe nach dem Wechsel in die Interventionsgruppe.
Der Vollfeld-Lichtempfindlichkeits-Schwellenwert-Test (FST-Test) ist ein globales Mass für die retinale Lichtempfindlichkeit, wobei die Log10(cd.s/m2)-Werte eine bessere Empfindlichkeit anzeigen, je negativer sie sind. Die Ergebnisse des Vollfeld-Lichtempfindlichkeits-Schwellenwert-Tests (FST) bei Weisslicht im ersten Studienjahr [Log10(cd.s/m2)] sind nachstehend in Tabelle 4 aufgeführt.
Tabelle 4: Vollfeld-Lichtempfindlichkeits-Schwellenwert-Test
|
Vollfeld-Lichtempfindlichkeits-Schwellenwert-Test – mit dem zuerst behandelten Auge (ITT)
| |
|
Intervention, N = 21
| |
Studienbeginn (Baseline)
|
Jahr 1
|
Veränderung
| |
N
|
20
|
20
|
19
| |
Mittelwert (Standardfehler)
|
-1.23 (0.10)
|
-3.44 (0.30)
|
-2.21 (0.30)
| |
|
Kontrolle, N = 10
| |
N
|
9
|
9
|
9
| |
Mittelwert (Standardfehler)
|
-1.65 (0.14)
|
-1.54 (0.44)
|
0.12 (0.45)
| |
|
Differenz (95%-KI) (Intervention-Kontrolle)
-2.33 (-3.44; -1.22), p < 0.001
| |
Vollfeld-Lichtempfindlichkeits-Schwellenwert-Test – mit dem als zweites behandelten Auge (ITT)
| |
|
Intervention, N = 21
| |
Studienbeginn (Baseline)
|
Jahr 1
|
Veränderung
| |
N
|
20
|
20
|
19
| |
Mittelwert (Standardfehler)
|
-1.35 (0.09)
|
-3.28 (0.29)
|
-1.93 (0.31)
| |
|
Kontrolle, N = 10
| |
N
|
9
|
9
|
9
| |
Mittelwert (Standardfehler)
|
-1.64 (0.14)
|
-1.69 (0.44)
|
0.04 (0.46)
| |
|
Differenz (95%-KI) (Intervention-Kontrolle)
-1.89 (-3.03; -0.75), p=0.002
| |
Durchschnittswert des Vollfeld-Lichtempfindlichkeits-Schwellenwert-Tests für beide Augen (ITT)
Differenz (95 %-KI) (Intervention-Kontrolle): -2.11 (-3.19; -1.04), p < 0.001
|
Patienten in der Kontrollgruppe zeigten nach dem Wechsel in die Interventionsgruppe in Jahr 1 und dem Erhalt von Voretigen Neparvovec ein ähnliches Ansprechen auf Voretigen Neparvovec wie Patienten in der ursprünglichen Interventionsgruppe. In beiden Behandlungsgruppen betrug die Verbesserung der FST-Ergebnisse nach der Vektorverabreichung mehr als 2 Log-Einheiten, was mehr als einer 100-fachen Verbesserung der Lichtempfindlichkeit entspricht. Die Verbesserung in der Vollfeld-Lichtempfindlichkeit wurde für bis zu 3 Jahre nach Verabreichung von Voretigen Neparvovec aufrechterhalten.
Eine unterstützende Analyse zeigte, dass die linearen Beziehungen zwischen den experimentellen MLMT-Scores und den klinisch gebräulichen FST in dieser Studie im Allgemeinen gut bis stark waren, was darauf hindeutet, dass Patienten mit einer Verbesserung der Mobilitätstests im Jahr 1 tendenziell niedrigere (d.h. bessere) FST-Ergebnisse im Jahr 1 hatten.
Ein Jahr nach der Exposition gegenüber Voretigen Neparvovec betrug die mittlere Veränderung der Sehschärfe gegenüber Baseline für beide Augen unter Verwendung der Holladay-Skala -0.16 LogMAR für die Interventionsgruppe und 0.01 LogMAR für die unbehandelte Kontrollgruppe. Dies spiegelte eine durchschnittliche Verbesserung um 8 Buchstaben auf der ETDRS-Tafel für Patienten der Interventionsgruppe wider, verglichen mit einem durchschnittlichen Verlust von 0.5 Buchstaben bei Patienten der Kontrollgruppe, wobei dieser Unterschied zwischen den Gruppen nicht statistisch signifikant war.
|


