CompositionPrincipes actifs
Acidum penteticum (DTPA)
Excipients
Stannosi(II) chloridum dihydricum, Acidum gentisicum, Calcii chloridum dihydricum, Acidum hydrochloridum concentratum, Natrii hydroxidum.
Le lyophilisat du produit contient 4.72 mg de sodium par flacon-ampoule.
Après la reconstitution avec 10 ml d’une solution de pertechnétate de sodium, le produit contient 4.01mg/ml de sodium.
Mécanisme de réaction
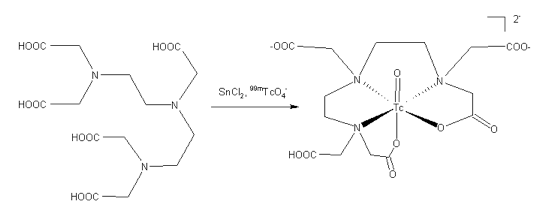
DTPA 99mTc - DTPA
Spécifications du produit marqué
Solution aqueuse, exempte d’endotoxines, stérile, apyrogène, claire à légèrement opalescente, incolore pour administration intraveineuse ou pour inhalation après fabrication d’un aérosol,
pH: 4,0 - 5,0;
Rendement de marquage: ≥ 95%.
Forme pharmaceutique et quantité de principe actif par unitéTrousse de marquage, pour la préparation d'une solution d’acide pentétique (DTPA) marqué au 99mTc. Un flacon contient 20,8 mg d’acide pentétique (DTPA).
Indications/Possibilités d’emploiTechneScan DTPA est une préparation radiodiagnostique, qui est indiquée, après reconstitution à l’aide du pertechnétate [99mTc] de sodium, pour:
-Scintigraphie rénale
-Scintigraphie cérébrale
-Scintigraphie pulmonaire de ventilation après préparation d’un aérosol adapté à son inhalation.
Posologie/Mode d’emploiLe 99mTc-DTPA est administré par injection unique, intraveineuse ou par inhalation au moyen d’un générateur d’aérosol. Le contenu marqué d'un flacon de TechneScan DTPA est destiné à l'examen de plusieurs patients. Dans certaines conditions particulières, on peut aussi administrer à un seul patient tout un flacon dont le contenu est marqué avec une activité adéquate.
Le produit ne doit pas être administré au patient sous forme non marquée.
Posologie pour un adulte
-Scintigraphie rénale: 40 - 400 MBq
-Scintigraphie cérébrale: 200 - 750 MBq
-Etude de ventilation pulmonaire: 50-100 MBq se déposent dans les poumons, 500 -1000 MBq dans le générateur aérosol en fonction de l’appareil.
Posologie chez les enfants et les adolescents :
Scintigraphie rénale :
L’utilisation chez les enfants et les adolescents doit être soigneusement reconsidérée et doit dépendre de la nécessité clinique ainsi que du rapport bénéfice/risque dans cette population. Les activités à administrer par voie intraveineuse chez les enfants et les adolescents peuvent être calculées selon les recommandations de la "Paediatric Dosage Card" de l’EANM (European Association of Nuclear Medicine) de 2016. Pour ce faire, il convient de choisir les formules pour chaque indication et le facteur de correction pertinent en fonction du poids corporel du jeune patient.
Administration de pentétate de technétium (99mTc) en cas d’insuffisance rénale:
Activité administrée [MBq] = activité initiale [MBq] x multiplicateur (pour une activité initiale de 14,0)
Tableau 1
Masse corporelle Facteur de multiplic Masse corporelle Facteur de multiplic Masse corporelle Facteur de multiplic
ation ation ation
3 kg 1 22 kg 5,29 42 kg 9,14
4 kg 1,14 24 kg 5,71 44 kg 9,57
6 kg 1,71 26 kg 6,14 46 kg 10,00
8 kg 2,14 28 kg 6,43 48 kg 10,29
10 kg 2,71 30 kg 6,86 50 kg 10,71
12 kg 3,14 32 kg 7,29 52-54 kg 11,29
14 kg 3,57 34 kg 7,72 56-58 kg 12,00
16 kg 4,00 36 kg 8,00 60-62 kg 12,71
18 kg 4,43 38 kg 8,43 64-66 kg 13,43
20 kg 4,86 40 kg 8,86 68 kg 14,00
Administration de pentétate de technétium (99mTc) en cas de fonction rénale normale:
Activité administrée [MBq] = activité initiale [MBq] x multiplicateur (pour une activité initiale de 34,0)
Tableau 2
Masse corporelle Facteur de multiplic Masse corporelle Facteur de multiplic Masse corporelle Facteur de multiplic
ation ation ation
3 kg 1 22 kg 3,06 42 kg 4,41
4 kg 1,12 24 kg 3,18 44 kg 4,53
6 kg 1,47 26 kg 3,35 46 kg 4,65
8 kg 1,71 28 kg 3,47 48 kg 4,77
10 kg 1,94 30 kg 3,65 50 kg 4,88
12 kg 2,18 32 kg 3,77 52-54 kg 5,00
14 kg 2,35 34 kg 3,88 56-58 kg 5,24
16 kg 2,53 36 kg 4,00 60-62 kg 5,47
18 kg 2,71 38 kg 4,18 64-66 kg 5,65
20 kg 2,88 40 kg 4,29 68 kg 5,77
Chez les enfants jusqu’à 1 an, lors de l’emploi de TechneScan DTPA marqué au 99mTc une dose minimale de 20 MBq est nécessaire afin d’obtenir des images de qualité suffisante.
Scintigraphie pulmonaire:
-Scintigraphie pulmonaire de ventilation: 10 MBq se déposent dans les poumons, 500–1000 MBq dans le générateur d’aérosol.
Acquisition d'images
-Perfusion rénale: l'examen est effectué par imagerie dynamique au cours de la première minute suivant l'injection. Le moment optimal pour l’imagerie statique est 1 heure après l’injection. En cas de scintigraphie rénale avec test au captopril (IEC), le captopril est administré par voie intraveineuse avant l’administration du pentétate de technétium (99mTc). L’enregistrement de la fonction de chaque rein est réalisée par imagerie dynamique après l’injection. Si l’un ou les deux reins ne se sont pas vidés correctement dans les 20 premières minutes, une charge de furosémide est effectuée. L’imagerie dynamique doit être poursuivie 15 minutes après l’administration du diurétique. Les clichés statiques peuvent être réalisés 1 heure après l'injection.
-Scintigraphie cérébrale: l'examen doit commencer immédiatement après l'injection par des acquisitions dynamiques. Les images statiques sont prises 1 heure et, si nécessaire, plusieurs heures après l’injection.
-Scintigraphie pulmonaire de ventilation: les images des poumons sont prises dans les 180 minutes. Pour la scintigraphie pulmonaire de ventilation, un générateur d’aérosol est nécessaire, en dosant en fonction du type d'appareil (consulter le mode d'emploi correspondant).
Répétition de l'examen
On peut envisager de répéter l'examen avec le TechneScan DTPA 48 heures au plus tôt (8 demi-vies de 99mTc) après la première administration de la préparation.
Posologie spéciale
Lors de limitation de la fonction rénale, la dose irradiée peut être accrue, ce dont il faut tenir compte lors du calcul de la dose.
Exposition aux rayonnements
Le technétium (99mTc) est préparé à l'aide d'un générateur (99Mo/99mTc) et se désintègre avec émission de rayons gamma ayant une énergie de 140 keV et une demi-vie de 6,01 heures en technétium (99Tc), qui peut être considéré comme quasi stable en raison de sa longue demi-vie de 2,13 x 105 ans.
Les données figurant dans le tableau proviennent de l’ICRP 128 et ont été calculées selon les hypothèses suivantes:
-L’injection intraveineuse de pentétate de technétium (99mTc) entraîne une distribution initiale dans le liquide extracellulaire. Après cette distribution initiale, la substance est éliminée uniquement par les reins. En cas de fonction rénale normale, la rétention corporelle totale peut être décrite comme une fonction biexponentielle avec des demi-vies pour les composants de 100 minutes (0,99) et 7 jours (0,01). La fraction excrétée par le rein est de 1,0 (1,0). Le débit rénal est de 5 minutes. En cas d’insuffisance rénale, on estime que la demi-vie de rétention du composant principal s'élève à 1000 minutes et le débit rénal est porté à 20 minutes.
Selon l’ICRP publication No. 128 les doses suivantes absorbées sont indiquées pour les patients avec fonction rénale normale:
Dose estimée absorbée par unité (mGy/MBq) d'activité administrée
Organ Adulte 15 ans 10 ans 5 ans 1 an
Surrénales 0,0014 0,0018 0,0027 0,004 0,0072
Surface osseuse 0,0024 0,0029 0,0043 0,0061 0,010
Cerveau 0,00086 0,0011 0,0017 0,0028 0,0049
Sein 0,00072 0,00092 0,0013 0,0022 0,0041
Paroi de la vésicule biliaire 0,0015 0,0021 0,0038 0,005 0,0061
Tractus gastro-intestinal
Paroi stomacale 0,0013 0,0017 0,0028 0,0040 0,0068
Paroi de l’intestin grêle 0,0025 0,0031 0,0049 0,0070 0,010
Paroi du côlon 0,0031 0,0039 0,0060 0,0081 0,011
Paroi du côlon ascendant 0,0021 0,0028 0,0043 0,0065 0,0092
Paroi du côlon descendant 0,0043 0,0054 0,0082 0,010 0,013
Paroi cardiaque 0,0012 0,0015 0,0022 0,0033 0,0059
Reins 0,0044 0,0053 0,0075 0,011 0,018
Foie 0,0012 0,0016 0,0025 0,0038 0,0064
Poumons 0,001 0,0013 0,002 0,003 0,0055
Muscles 0,0016 0,002 0,003 0,0043 0,0068
Œsophage 0,001 0,0013 0,0019 0,003 0,0054
Ovaires 0,0042 0,0053 0,0077 0,01 0,013
Pancréas 0,0014 0,0018 0,0028 0,0043 0,0074
Moelle osseuse rouge 0,0015 0,0018 0,0027 0,0037 0,0057
Peau 0,00087 0,001 0,0017 0,0026 0,0044
Rate 0,0013 0,0016 0,0026 0,0039 0,0068
Testicules 0,0029 0,004 0,0068 0,0094 0,013
Thymus 0,001 0,0013 0,0019 0,0030 0,0054
Thyroïde 0,001 0,0013 0,0021 0,0033 0,006
Paroi vésicale 0,062 0,078 0,11 0,15 0,17
Utérus 0,0079 0,0096 0,015 0,018 0,022
Autres tissus 0,0017 0,0021 0,0030 0,0042 0,0066
Dose efficace (mSv/MBq) 0,0049 0,0063 0,0094 0,012 0,016
La dose efficace d’irradiation est d’environ 3,6 mSv lorsque l’activité maximale recommandée de 740 MBq est administrée chez les adultes ayant un poids corporel de 70 kg.
Pour une activité administrée de 740 MBq, l’exposition aux rayonnements typique de l’organe cible (reins) est de 3,3 mGy et l’exposition aux rayonnements typique de l’organe critique (paroi de la vessie) est de 46 mGy.
Les valeurs suivantes sont valables selon l’ICRP 128 pour les patients avec fonction rénale limitée:
Dose estimée absorbée par unité (mGy/MBq) d'activité administrée
Organ Adulte 15 ans 10 ans 5 ans 1 an
Surrénales 0,0041 0,0051 0,0076 0,011 0,021
Surface osseuse 0,006 0,0071 0,011 0,015 0,028
Cerveau 0,0028 0,0035 0,0057 0,0091 0,016
Sein 0,0023 0,003 0,0042 0,0068 0,013
Paroi de la vésicule biliaire 0,0042 0,0057 0,0092 0,013 0,016
Tractus gastro-intestinal
Paroi stomacale 0,0038 0,005 0,0079 0,011 0,019
Paroi de l’intestin grêle 0,0045 0,0056 0,0085 0,013 0,022
Paroi du côlon 0,0045 0,0058 0,0087 0,013 0,022
Paroi du côlon ascendant 0,0043 0,0056 0,0081 0,013 0,021
Paroi du côlon descendant 0,0049 0,0061 0,0095 0,013 0,023
Paroi cardiaque 0,0037 0,0047 0,007 0,01 0,018
Reins 0,0077 0,0092 0,013 0,019 0,032
Foie 0,0037 0,0046 0,0071 0,011 0,019
Poumons 0,0033 0,0042 0,0062 0,0095 0,017
Muscles 0,0032 0,004 0,0061 0,0091 0,017
Œsophage 0,0033 0,0042 0,0062 0,0096 0,017
Ovaires 0,005 0,0062 0,0092 0,014 0,023
Pancréas 0,0043 0,0053 0,008 0,012 0,021
Moelle osseuse rouge 0,0034 0,0042 0,0064 0,0093 0,016
Peau 0,0022 0,0026 0,0042 0,0067 0,012
Rate 0,0038 0,0047 0,0073 0,011 0,019
Testicules 0,0035 0,0045 0,0069 0,01 0,018
Thymus 0,0033 0,0042 0,0062 0,0096 0,017
Thyroïde 0,0034 0,0042 0,0067 0,011 0,019
Paroi vésicale 0,021 0,027 0,039 0,05 0,066
Utérus 0,0061 0,0074 0,011 0,016 0,025
Autres tissus 0,0033 0,0041 0,0063 0,0097 0,017
Dose efficace (mSv/MBq) 0,0046 0,0058 0,0087 0,013 0,021
La demi-vie physique de (99mTc) est de 6,01 heures.
La paroi de la vessie contribue à jusqu’à 57% de la dose efficace.
Les données ci-dessous proviennent de l’ICRP 53 et ont été calculées selon les hypothèses suivantes:
-Inhalation de pentétate de technétium (99mTc):
l’inhalation d’aérosols composés de particules de diamètre inférieur à 2–3 micromètres entraîne des dépôts principalement dans les alvéoles pulmonaires. Les particules sont rapidement éliminées des poumons par la circulation sanguine. La demi-vie biologique du pentétate de technétium (99mTc) dans les poumons est de 60 à 80 minutes chez les non-fumeurs normaux; elle est raccourcie chez les fumeurs et chez la plupart des patients souffrant de maladies pulmonaires. Une valeur de 60 min est reprise ci-dessous. La substance qui pénètre dans le sang est éliminée selon le modèle du pentétate de technétium (99mTc) administré par voie intraveineuse.
En cas d’administration de DTPA marqué au 99mTc sous forme d’aérosol, les valeurs suivantes sont valables selon l’ICRP 53:
Dose estimée absorbée par unité (mGy/MBq) d'activité administrée
Organ Adulte 15 ans 10 ans 5 ans 1 an
Surrénales 0.0021 0.0029 0.0044 0.0067 0.012
Paroi de la vésicule biliaire 0.047 0.058 0.084 0.12 0.23
Surface osseuse 0.0019 0.0024 0.0035 0.0053 0.0098
Seins 0.0019 0.0019 0.0033 0.0048 0.0078
Tractus gastro-intestinal
Paroi stomacale 0.0017 0.0022 0.0035 0.0051 0.0089
Paroi de l’intestin grêle 0.0021 0.0026 0.0041 0.0063 0.011
Paroi du côlon ascendant 0.0019 0.0024 0.0038 0.0061 0.01
Paroi du côlon descendant 0.0032 0.0042 0.0063 0.0088 0.015
Reins 0.0041 0.0051 0.0072 0.011 0.019
Foie 0.0019 0.0025 0.0037 0.0055 0.0097
Poumons 0.017 0.026 0.036 0.054 0.1
Ovaires 0.0033 0.0041 0.0061 0.0089 0.015
Pancréas 0.0021 0.0026 0.004 0.0061 0.011
Moelle osseuse rouge 0.0027 0.0034 0.0047 0.0062 0.0096
Rate 0.0019 0.0024 0.0036 0.0056 0.0099
Testicules 0.0021 0.0031 0.0052 0.0079 0.015
Thyroïde 0.00099 0.0017 0.0027 0.0044 0.0078
Utérus 0.0059 0.0072 0.011 0.016 0.027
Autres tissus 0.0018 0.0022 0.0032 0.0049 0.0086
Dose efficace (mSv/MSq) 0.007 0.0091 0.013 0.02 0.036
Contre-indicationsHypersensibilité avérée au DTPA non marqué, au 99mTc-DTPA ou à un des autres composants contenu dans la préparation.
-Grossesse.
-Pendant l’allaitement.
-Administration intra-thécale.
Mises en garde et précautionsRéactions d’hypersensibilité ou anaphylactiques potentielles
Si des réactions d’hypersensibilité ou anaphylactiques surviennent, l'utilisation du médicament doit être interrompue et un traitement par voie intraveineuse doit être instauré si nécessaire. Afin de pouvoir réagir rapidement en cas d’urgence, des médicaments et des instruments d’urgence appropriés (par ex. tube trachéal, respirateur) doivent être disponibles.
Évaluation individuelle des bénéfices et des risques
Pour chaque patient, l’exposition aux rayonnements doit être justifiée par le bénéfice potentiel. Dans tous les cas, l’activité administrée doit être aussi faible que possible pour obtenir le résultat diagnostique souhaité.
Troubles de la fonction rénale/hépatique
L’activité à administrer doit être soigneusement reconsidérée car une exposition accrue aux rayonnements peut être observée dans cette population de patients.
Enfants et adolescents
Pour plus d’informations sur l’utilisation chez les enfants et les adolescents, voir rubrique "Posologie/Mode d’emploi" .
L’indication doit être posée de manière particulièrement stricte car la dose efficace par MBq est plus élevée que chez l’adulte (voir rubrique "Exposition aux rayonnements" ).
Préparation du patient
Il faut veiller à ce que le patient soit suffisamment hydraté avant l'examen. Afin de réduire le plus possible l'exposition aux rayonnements, les patients doivent être invités à vider la vessie le plus souvent possible pendant les premières heures suivant l'examen.
Mises en garde particulières
La solution injectable de Technescan DTPA ne doit pas être injectée dans l’espace subarachnoïdien et n’est pas adaptée à la scintigraphie du flux de la moelle épinière.
Selon l’heure à laquelle vous administrez l’injection, la teneur en sodium administrée au patient peut, dans certains cas, être supérieure à 1 mmol. Ceci doit être pris en compte chez les patients suivant un régime hyposodé.
InteractionsScintigraphie rénale
Dans certains cas, lors des tests pharmacologiques, l'administration unique d'un diurétique ou d'un IEC est utilisée pour permettre un diagnostic différentiel de troubles néphrologiques et urologiques.
-Les IEC diminuent la circulation sanguine dans les reins.
-Le diclofénac, le furosémide et d’autres diurétiques tels que l’hydrochlorothiazide peuvent modifier la sécrétion rénale et donc la clairance du pentétate de technétium (99mTc).
-Les agents néphrotoxiques tels que les aminoglycosides, le cisplatine et les produits de contraste administrés peuvent réduire l’excrétion rénale et affecter ainsi la clairance du pentétate de technétium (99mTc).
Scintigraphie cérébrale
Les médicaments psychotropes augmentent la perfusion sanguine dans la région de l’artère carotide externe. Cela peut entraîner une captation rapide de 99mTc-DTPA par le rhinopharynx.
Afin d’assurer une qualité de scintigraphie optimale, il vaut mieux ne pas administrer cette ou d'autres substances pendant un examen par TechneScan DTPA, ni les administrer dans un intervalle proche, sauf si le but d’examen implique un tel procédé. Dans tous les cas, l'évaluation des scintigrammes doit tenir en compte des médicaments pris par le patient au moment de l’examen.
Grossesse, AllaitementFemmes en âge de procréer
Si l’utilisation d’un produit radiopharmaceutique est envisagée chez une femme en âge de procréer, il est impératif de déterminer si une grossesse est en cours. Tant que le contraire n’a pas été démontré, une grossesse doit être présumée en l'absence de règles. En cas de doute (absence de règles, règles très irrégulières, etc.), il convient de proposer à la patiente d'autres méthodes d'examen ne recourant pas aux rayonnements ionisants (si de telles méthodes sont disponibles).
Grossesse
Les examens au moyen de radionucléides chez la femme enceinte entraînent également une irradiation du fœtus. Par conséquent, seuls les examens essentiels dont le bénéfice attendu est largement supérieur au risque encouru par la mère et le fœtus doivent être réalisés pendant la grossesse.
Allaitement
Avant l’administration d’un produit radiopharmaceutique pendant l’allaitement, il convient d’envisager la possibilité de reporter l’administration du radionucléide après la fin de l’allaitement et de tenir compte également de l’excrétion de la radioactivité dans le lait maternel lors du choix du produit radiopharmaceutique le plus approprié. Si l’administration est jugée nécessaire, l’allaitement doit être interrompu pendant au moins 12 heures et le lait tiré pendant cette période doit être éliminé.
Fertilité
Aucune étude de fertilité n’a été réalisée.
Effet sur l’aptitude à la conduite et l’utilisation de machinesLe pentétate de technétium (99mTc) n’a aucune influence ou a une influence négligeable sur l’aptitude à la conduite ou l'utilisation de machines.
Effets indésirablesLes effets indésirables présentés dans le tableau ci-dessous sont résumés par classe de systèmes d’organes. Leur fréquence est inconnue (la fréquence ne peut être estimée sur la base des données disponibles).
Classe de systèmes d’organes Symptôme Fréquence
Affections du système nerveux Sensations vertigineuses Fréquence inconnue
Affections respiratoires, thoraciques et Dyspnée Fréquence inconnue
médiastinales
Affections de la peau et du tissu sous-cutané Urticaire, prurit Fréquence inconnue
Affections vasculaires Hypotension, bouffées Fréquence inconnue
vasomotrices
Les rayonnements ionisants peuvent provoquer des cancers et des modifications du patrimoine génétique. La dose efficace étant de 3,6 mSv lorsque l’activité maximale recommandée de 740 MBq est administrée, ces effets sont peu probables.
Dans de cas rares, particulièrement chez des patients avec une allergie contre l'aspirine, on a observé des réactions anaphylactiques dues à l’acide gentisique (acide dihydroxy-benzoique) contenue dans TechneScan DTPA comme excipient. Des telles réactions peuvent être traitées par l’emploi d’antihistaminiques ou l’administration parentérale de stéroïdes.
L’annonce d’effets secondaires présumés après l’autorisation est d’une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d’effet secondaire nouveau ou grave via le portail d’annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageEn respectant les consignes d'utilisation, aucun surdosage n'est à envisager. En cas de surdosage accidentel de 99mTc-DTPA, l'importante dose absorbée qui en résulte diminue rapidement en raison de la courte demi-vie du 99mTc (6,02 heures). L'élimination devrait si possible être accélérée par une diurèse forcée et en demandant au patient de vider aussi souvent que possible sa vessie.
Propriétés/EffetsCode ATC
V09CA01
Mécanisme d’action
-Comme l’inuline, le pentétate de technétium (99mTc) circule dans la circulation sanguine avec une liaison négligeable aux protéines plasmatiques. Il est filtré par la membrane glomérulaire et ne subit ni sécrétion tubulaire ni réabsorption. Il ne traverse pas la barrière hémato-encéphalique (BHE) normale.
-Le pentétate de technétium (99mTc) est aérosolisé en particules ayant une taille de 1,2 à 2 micromètres à partir d'une solution aqueuse. Après l'inhalation, les gouttelettes d'aérosol sont distribuées et déposées dans les voies respiratoires et les alvéoles en fonction de leurs propriétés aérodynamiques, en particulier leur diamètre aérodynamique moyen.
Pharmacodynamique
Aux activités recommandées pour la scintigraphie et aux quantités administrées, on ne peut s'attendre à aucun effet pharmacodynamique particulier du 99mTc-DTPA.
Efficacité clinique
Les propriétés du 99mTc-DTPA qui sont importantes pour les examens de diagnostic reposent sur sa clearance plasmatique prolongée lors de maladies rénales, sa accumulation dans les lésions intracrâniennes et – après administration comme aérosol – sur sa distribution dans les poumons.
PharmacocinétiqueAprès injection intraveineuse le 99mTc-DTPA se distribue rapidement dans l’espace liquidien extra-cellulaire et il est rapidement excrété hors de l’organisme par filtration glomérulaire.
Le chélate n’est guère lié par le parenchyme rénal. Les protéines sériques lient le 99mTc-DTPA, en cas d’injection unique, jusqu’à env. 4% et, lors de perfusion prolongée, jusqu’à env. 10%. Bien que le chélate fournisse des indications utiles concernant le taux de filtration glomérulaire, cette fraction liée au plasma entraîne des taux de filtration glomérulaires plus faibles que, par exemple, ceux attendus lors de clearance à l’inuline.
Puisque le 99mTc-DTPA est excrété par filtration glomérulaire, la scintigraphie met en évidence, au cours des premières minutes après injection, le système vasculaire rénal. Les prises ultérieures montrent l’activité urinaire, tout comme celle des tubules collecteurs et du bassinet.
Le 99mTc-DTPA s’accumule dans les lésions intra-crâniennes, mais pas dans le plexus choroïde.
Après inhalation dans le cadre d’une scintigraphie de ventilation pulmonaire, le 99mTc-DTPA diffuse rapidement (avec une demi-vie biologique de 60 minutes environ) via la membrane alvéolaire dans le sang, où il se comporte comme mentionné plus haut après injection i.v., et d’où il est rapidement excrété par voie rénale.
Absorption
Voir "Pharmacocinétique" .
Distribution
Voir "Pharmacocinétique" .
Métabolisme
Non disponible.
Élimination
Voir "Pharmacocinétique" .
Cinétique pour certains groupes de patients
Lors de maladies rénales, la clearance plasmatique du 99mTc-DTPA peut être prolongée.
Lors des lésions intra-crâniennes associées à une néo-vascularisation excessive ou à une modification de la perméabilité de la barrière hémato-encéphalique, l’accumulation de 99mTc-DTPA est élevée. En cas des troubles de ventilation pulmonaire, les régions mal- ou non-ventilées s’imposent comme zones avec peu ou sans activité.
Données précliniquesLes études animales effectuées avec l’acide pentétique non marqué (DTPA) n’ont montré, à des doses comprises entre 5 et 50 mg/kg i.v., aucun signe de toxicité aiguë. Même les résultats d’autopsie 14 jours après administration répétée se sont avérés négatifs. La dose maximale pour les patients est de 20,8 mg d’acide pentétique (0,30 mg/kg), ce qui est 2 grandeurs d’ordre ou moins au dessous des doses utilisées pendant les études précliniques.
On ne dispose d'aucune donnée sur le 99mTc-DTPA quant à son potentiel mutagène, carcinogène ou toxique pour la reproduction. Les dangers potentiels des rayons ionisants sont toutefois connus.
Le produit n’est pas destiné à être administré de manière fréquente ou régulière.
Remarques particulièresIncompatibilités
Aucune incompatibilité n’est connue. Il est toutefois recommandé de ne pas administrer le 99mTc-DTPA en même temps que d’autres médicaments.
Stabilité
Stabilité du TechneScan DTPA non marqué
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention "EXP" sur l’emballage.
Stabilité du produit marqué
La préparation marquée peut être conservée dans le flacon d'origine pendant 8 heures après le marquage - ensuite, le produit n'est plus utilisable.
Remarques particulières concernant le stockage
Stockage du TechneScan DTPA non marqué
Le TechneScan DTPA non marqué doit être conservé à l’abri de la lumière, pas en dessus de 25 ºC.
Stockage du produit marqué
La préparation marquée doit être conservée pas en dessus de 25 °C, dans un conteneur de plomb d’épaisseur appropriée. Ne pas congeler.
Remarques concernant la manipulation
Le contenu d'un flacon de TechneScan DTPA est reconstitué à l'aide du [99mTc]pertechnétate de sodium en 99mTc-pentétate de calcium trisodique marqué (99mTc-DTPA), qui est le véritable agent diagnostique. Le marquage doit être effectué par du personnel qualifié, dans des conditions aseptiques strictes, sans air et en tenant compte des mesures de radioprotection (travail en conteneur ou derrière un écran de plomb).
Marquage
1.Oter le couvercle de fermeture flip-off du flacon TechneScan DTPA, désinfecter le bouchon en caoutchouc avec de l'alcool et mettre le flacon dans un conteneur en plomb.
2.Selon le nombre d'examens prévus, introduire dans le flacon l'activité correspondante à 110 MBq - 10 GBq de solution de [99mTc]pertechnétate de sodium dans un volume de 2 - 10 ml au moyen d'une seringue à injection stérile et protégée des radiations, sans bulle d'air et sans utiliser de seringue d'évacuation d'air. Ensuite, au moyen de la même seringue, prélever un volume équivalent de gaz afin de supprimer la surpression dans le flacon.
3.Recouvrir le flacon dans le conteneur en plomb par un couvercle en plomb et le retourner plusieurs fois ou le secouer légèrement sur un dispositif prévu à cet usage jusqu'à ce que la substance sèche soit entièrement dissoute.
4.Laisser reposer encore 15 à 30 minutes à température ambiante. Après cet intervalle de réaction le marquage est complet. La préparation est prête pour l’injection i.v. ou pour administration par inhalation au moyen d’un générateur d’aérosol.
5.Mesurer la radioactivité de la préparation marquée dans un activimètre adéquat. Remplir l'étiquette de précaution/protocole en indiquant l'activité totale, le volume, la concentration, l’heure et la date de mesure, puis affixer l’étiquette au flacon.
Le produit marqué doit être utilisé en l'espace de 8 heures. Dans ce laps de temps, le produit peut être conservé au-dessous de 25 °C et ne pas congeler – en tenant compte des mesures de protection envers les radiations.
Avant administration il faut déterminer le rendement de marquage.
Remarques concernant le marquage
Pour le marquage, il convient de n'utiliser que des éluats de 99mTc-pertechnétate produits avec des générateurs enregistrés et autorisés en Suisse. Les caractéristiques des éluats doivent correspondre aux exigences de la Ph. Eur., les éluats doivent en particulier ne pas contenir d'oxydants et doivent contenir moins de 5ppm d'aluminium. Pour garantir un rendement de marquage nécessaire d'au moins 95%, les éluats ne devraient plus être utilisés 6 heures après élution.
En cas d'activité trop importante, la solution de 99mTc-DTPA peut être diluée au moyen d'une solution de chlorure de sodium physiologique. La solution de chlorure de sodium physiologique choisie doit être stérile et exempte d’endotoxines, elle ne doit contenir ni bactériostatiques ni agents de conservations et elle devrait provenir d'un conteneur en verre (une ampoule) et non de conteneurs en plastique.
Contrôle de qualité
Le rendement du marquage et la pureté radiochimique sont déterminés à l'aide de la radiochromatographie. Cet examen peut être effectué à l'aide de deux chromatographies sur couche mince (A et B). La première chromatographie est destinée à la détection d'impuretés dues au pertechnétate libre et la seconde à la détection d'impuretés dues au technétium réduit, hydrolysé.
Les deux chromatographies permettent d'obtenir la somme des impuretés et de déterminer le rendement de marquage et la pureté radiochimique de la préparation marquée.
A: Détermination de pertechnétate libre (99mTcO4¯) par chromatographie sur couche mince:
Matériel nécessaire
Cuve à chromatographie
Gel de silice sur fibre de verre – Gelman ITLC-SG
Méthyl Ethyl Cétone
Seringue à 1 ml avec canule
Réalisation de la chromatographie
Direction du processus: ascendante
Durée du processus: environ 5 min
Le pertechnétate libre (99mTcO4
|

