CompositionPrincipe actifs
Losartanum kalicum, hydrochlorothiazidum.
Excipients
Co-Losartan Sandoz 50/12,5 mg:
Lactosum monohydricum, cellulosum microcristallinum, amylum pregelificatum, magnesii stearas, silica colloidalis anhydrica.
Film:
Hypromellosum, hydroxypropylcellulosum, ferri oxidum (E172), titanii dioxidum (E171).
1 comprimé pelliculé contient 26,9 mg de lactose monohydraté.
Co-Losartan Sandoz 100 /12,5 mg:
Silicified cellulosum microcristallinum, carmellosum natricum conexum, silica colloidalis, silica colloidalis anhydrica, magnesii stearas.
Film:
Hypromellosum, hydroxypropylcellulosum, titanii dioxidum (E171).
1 comprimé pelliculé contient 0,23 mg de sodium.
Co-Losartan Sandoz 100/25 mg:
Lactosum monohydricum, cellulosum microcristallinum, amylum pregelificatum, magnesii stearas, silica colloidalis anhydrica.
Film:
Hypromellosum, hydroxypropylcellulosum, ferri oxidum flavum (E172), titanii dioxidum (E171), macrogolum 400, talcum.
1 comprimé pelliculé contient 53,8 mg de lactose monohydraté.
Forme pharmaceutique et quantité de principe actif par unitéCo-Losartan Sandoz 50/12,5: comprimé pelliculé, contient 50 mg de losartan potassique et 12,5 mg d'hydrochlorothiazide.
Co-Losartan Sandoz 100/12,5: comprimé pelliculé, contient 100 mg de losartan potassique et 12,5 mg d'hydrochlorothiazide.
Co-Losartan Sandoz 100/25: comprimé pelliculé, contient 100 mg de losartan potassique et 25 mg d'hydrochlorothiazide.
Indications/Possibilités d’emploiHypertension artérielle
Co-Losartan Sandoz est indiqué chez les patients hypertendus dont le cas nécessite un traitement par association médicamenteuse.
Hypertension artérielle avec hypertrophie ventriculaire gauche
Réduction du risque d'accident vasculaire cérébral chez les patients hypertendus atteints d'hypertrophie ventriculaire gauche (voir sous "Propriétés/Effets" , "Étude LIFE, Patients de peau noire" ).
Posologie/Mode d’emploiPosologie usuelle
Hypertension artérielle
La dose initiale et d'entretien habituelle est de 1 comprimé pelliculé de Co-Losartan Sandoz 50 mg/12,5 mg par jour.
Pour les patients ne répondant pas de manière suffisante à Co-Losartan Sandoz 50 mg/12,5 mg, la dose peut être portée à 1 comprimé pelliculé de Co-Losartan Sandoz 100 mg/25 mg une fois par jour ou à 2 comprimés pelliculés de Co-Losartan Sandoz 50 mg/12,5 mg une fois par jour. La posologie maximale est de 1 comprimé pelliculé de Co-Losartan Sandoz 100 mg/25 mg une fois par jour ou de 2 comprimés pelliculés de Co-Losartan Sandoz 50 mg/12,5 mg une fois par jour. L'effet antihypertenseur est généralement atteint en l'espace de 3 semaines après le début du traitement. Co-Losartan Sandoz 100 mg/12,5 mg est destiné aux patients dont le traitement est déjà ajusté avec Losartan Sandoz 100 mg et qui nécessitent un contrôle supplémentaire de la pression artérielle.
Hypertension artérielle avec hypertrophie ventriculaire gauche
La posologie initiale normale est de 50 mg de losartan une fois par jour. Lorsque la pression artérielle visée ne peut pas être atteinte avec losartan 50 mg, le traitement devrait être adapté par l'association de losartan avec une dose faible d'hydrochlorothiazide (12,5 mg). Si nécessaire, la dose peut ensuite être portée à 100 mg de losartan/12,5 mg d'hydrochlorothiazide une fois par jour, ou à 100 mg de losartan/25 mg d'hydrochlorothiazide une fois par jour. Co-Losartan Sandoz est une formulation alternative adaptée aux patients qui seraient sinon traités au losartan et à l'hydrochlorothiazide en même temps.
Instructions posologiques particulières
Hypovolémie
Co-Losartan Sandoz ne devrait pas être utilisé chez les patients présentant une déplétion du volume intravasculaire (p.ex. les patients traités avec des hautes doses de diurétiques).
Patients présentant des troubles de la fonction rénale ou hépatique
L'utilisation de Co-Losartan Sandoz est déconseillée chez les patients souffrant d'une insuffisance grave de la fonction hépatique ou rénale (clairance de la créatinine ≤30 ml/min).
Patients âgés
Chez les patients âgés, aucune adaptation initiale de la dose de Co-Losartan Sandoz 50/12,5 n'est nécessaire. Co-Losartan Sandoz 100/12,5 et Co-Losartan Sandoz 100/25 ne devraient pas être utilisés pour le traitement initial chez les patients âgés.
Enfants et adolescents
Co-Losartan Sandoz ne devrait pas être utilisé chez les enfants et les adolescents, car la sécurité et l'efficacité chez les enfants et les adolescents n'ont pas été étudiées.
Co-Losartan Sandoz peut être également pris en association avec d'autres antihypertenseurs.
Co-Losartan Sandoz peut être pris avant, pendant ou après un repas.
Contre-indicationsCo-Losartan Sandoz est contre-indiqué:
chez les patients présentant une hypersensibilité à l'un des principes actifs ou à l'un des composants de la préparation;
chez les patients souffrant d'anurie;
chez les patients présentant une hypersensibilité à d'autres dérivés de sulfonamides;
pendant la grossesse (voir sous "Grossesse, Allaitement" );
chez les patients souffrant d'une grave insuffisance hépatique ou rénale (clairance de la créatinine ≤30 ml/min);
-Co-Losartan Sandoz est en outre contre-indiqué chez les patients présentant un angiœdème héréditaire ou chez ceux ayant développé un œdème de Quincke lors d'un traitement antérieur par un inhibiteur de l'ECA ou par un antagoniste du récepteur de l'angiotensine II.
L'utilisation concomitante de Co-Losartan Sandoz et de médicaments contenant de l'aliskirène est contre-indiquée chez les patients souffrant de diabète ou d'insuffisance rénale (DFG <60 ml/min/1,73 m2).
Mises en garde et précautionsLosartan – hydrochlorothiazide
Toxicité fœtale
Au cours du deuxième et du troisième trimestre de la grossesse, l'utilisation de médicaments agissant sur le système rénine-angiotensine tels que par exemple Co-Losartan Sandoz est associée à une réduction de la fonction rénale du fœtus et à une augmentation de la morbi-mortalité fœtale et néonatale. Un oligohydramnios dû au médicament peut être associé à une hypoplasie pulmonaire fœtale et à une déformation du squelette. Les effets indésirables potentiels chez le nouveau-né englobent une hypoplasie crânienne, une anurie, une hypotension, une défaillance rénale et la mort. L'administration de Co-Losartan Sandoz doit donc être arrêtée le plus rapidement possible dès qu'une grossesse est constatée (voir "Grossesse, Allaitement" ).
Hypersensibilité
Angiœdème – voir sous "Effets indésirables" .
Angiœdème intestinal
Des angiœdèmes intestinaux ont été rapportés chez des patients traités par des antagonistes des récepteurs de l'angiotensine II, y compris losartan (voir "Effets indésirables" ). Ces patients présentaient des douleurs abdominales, des nausées, des vomissements et de la diarrhée. Les symptômes se sont résolus après l'arrêt des antagonistes des récepteurs de l'angiotensine II. Si un angiœdème intestinal est diagnostiqué, losartan doit être arrêté et une surveillance appropriée doit être mise en oeuvre jusqu'à disparition complète des symptômes.
Les interactions potentielles de Co-Losartan Sandoz avec des anticoagulants oraux n'ont pas été étudiées.
Losartan
Insuffisance rénale
Chez certains patients, on a rapporté des modifications de la fonction rénale, y compris des défaillances rénales, consécutives à l'inhibition du système rénine-angiotensine; ces changements peuvent être réversibles après arrêt du médicament.
Lors de sténose de l'artère rénale, il est possible que l'usage du médicament ait pour conséquence une baisse massive de la pression artérielle.
D'autres médicaments agissant sur le système rénine-angiotensine peuvent augmenter les valeurs d'urémie et de créatinine sérique chez les patients atteints d'une sténose de l'artère rénale, bilatérale ou sur un seul rein. Des effets semblables ont été rapportés pour le losartan; ces altérations de la fonction rénale peuvent être réversibles après arrêt du médicament.
Chez les patients présentant une hypovolémie (p.ex. après un traitement par des hautes doses de diurétiques), il faut s'attendre à une chute symptomatique de la pression artérielle. Co-Losartan Sandoz ne doit pas être utilisé chez les patients présentant une déplétion du volume intravasculaire.
Élévation du potassium sérique
L'emploi simultané d'autres médicaments susceptibles d'augmenter le potassium sérique peut entraîner une hyperkaliémie (voir "Interactions" ).
Insuffisance hépatique
Des données pharmacocinétiques ont montré une augmentation significative des concentrations plasmatiques de losartan chez les patients cirrhotiques. C'est pourquoi il convient d'envisager une posologie initiale réduite chez les patients dont l'anamnèse révèle des troubles de la fonction hépatique (voir sous "Posologie/Mode d'emploi" et "Pharmacocinétique" ).
"Double blocage" du système rénine-angiotensine-aldostérone
Voir sous "Interactions" .
Hydrochlorothiazide
Hypotension et troubles de l'équilibre hydro-électrolytique
Comme pour tout autre traitement antihypertenseur, une hypotension symptomatique peut survenir chez certains patients. Cet effet secondaire, rarement observé chez les patients hypertendus ne présentant pas de complication, est en revanche plus probable en cas de déséquilibre hydrique et électrolytique. L'apparition d'éventuels signes cliniques de troubles de l'équilibre hydro-électrolytique, p.ex. un déficit volumique, une hyponatrémie, une alcalose hypochlorémique, une hypomagnésiémie ou une hypokaliémie, pouvant apparaître durant une diarrhée ou des vomissements, doit être surveillée. C'est pourquoi des déterminations périodiques des électrolytes sériques devraient être réalisées chez les patients sous traitement diurétique.
Effets métaboliques et endocriniens
Les thiazides peuvent diminuer la tolérance au glucose. Une adaptation du traitement antidiabétique, y compris par l'insuline, peut donc être nécessaire (voir sous "Interactions" ).
Les thiazides peuvent diminuer l'excrétion rénale du calcium et entraîner une augmentation légère et passagère du calcium sérique. Une hypercalcémie prononcée peut être le signe d'une hyperparathyroïdie cachée. Les thiazides doivent donc être arrêtés avant des tests de la fonction parathyroïdienne.
Un traitement diurétique avec des thiazides peut conduire à une augmentation des valeurs de cholestérol et de triglycérides.
Les thiazides peuvent provoquer une hyperuricémie et/ou un accès de goutte chez les patients prédisposés. Étant donné que le losartan fait baisser le taux d'acide urique, l'association losartan-hydrochlorothiazide diminue le risque d'une hyperuricémie induite par le diurétique.
Épanchement choroïdien, myopie aiguë et glaucome secondaire à angle fermé
Les sulfonamides et leurs dérivés peuvent provoquer une réaction idiosyncrasique susceptible d'entraîner un épanchement choroïdien avec dégradation du champ visuel, une myopie transitoire et un glaucome aigu à angle fermé. Les symptômes incluent une perte visuelle d'apparition brutale ou des douleurs oculaires et surviennent typiquement dans les heures, voire les semaines qui suivent le début du traitement. En l'absence de traitement, le glaucome à angle fermé peut provoquer une perte de vision permanente. Le traitement primaire consiste à arrêter immédiatement le médicament. Si la pression intra-oculaire reste accrue, un traitement médical immédiat ou une opération chirurgicale doivent être envisagés. Les facteurs de risque de développement d'un glaucome à angle fermé peuvent être un antécédent d'allergie à des sulfonamides ou à la pénicilline.
Toxicité respiratoire aiguë
Des très rares cas graves de toxicité respiratoire aiguë, y compris de syndrome de détresse respiratoire aiguë (SDRA) ont été signalés après la prise d'hydrochlorothiazide. Un œdème pulmonaire se développe typiquement dans les minutes ou les heures suivant la prise d'hydrochlorothiazide. Au début, les symptômes comprennent une dyspnée, de la fièvre, une aggravation de la fonction pulmonaire et une hypotension. En cas de suspicion de SDRA, il faut arrêter la prise de Co-Losartan Sandoz et instaurer un traitement adapté. L'hydrochlorothiazide ne doit pas être utilisé chez les patients qui ont déjà connu un SDRA après la prise d'hydrochlorothiazide.
Autres
Des patients avec ou sans anamnèse d'allergie ou d'asthme bronchique peuvent manifester des réactions d'hypersensibilité lors d'un traitement avec des thiazides. Une exacerbation ou l'apparition d'un lupus érythémateux systémique a été observée sous traitement avec des thiazides.
Cancers de la peau de type non mélanocytaire
Dans le cadre de deux études épidémiologiques fondées sur le registre national danois du cancer, un risque accru de cancers de la peau de type non mélanocytaire sous forme de carcinome basocellulaire (CBC) et de carcinome épidermoïde (CE) a été observé lors de l'exposition à des doses cumulées croissantes d'hydrochlorothiazide. L'effet photosensibilisant de l'hydrochlorothiazide pourrait constituer un mécanisme potentiel impliqué dans le développement du cancer de la peau non mélanocytaire.
Les patients qui prennent de l'hydrochlorothiazide doivent être informés du risque de cancer de la peau non mélanocytaire, et de la nécessité de contrôler régulièrement leur peau à la recherche de nouvelles lésions et de signaler immédiatement toute modification cutanée suspecte. Afin de minimiser le risque de cancer de la peau, il sera conseillé aux patients, à titre préventif, de limiter l'exposition au soleil et aux rayons UV et d'utiliser une protection solaire adéquate en cas d'exposition. Les modifications cutanées suspectes doivent être examinées rapidement, si nécessaire au moyen d'un examen histologique de biopsies. Chez les patients ayant des antécédents de cancer de la peau non mélanocytaire, il peut être nécessaire de reconsidérer l'utilisation d'hydrochlorothiazide (voir aussi la rubrique "Effets indésirables" ).
Enfants et adolescents
L'efficacité et la sécurité du médicament n'ont pas été étudiées chez les enfants et les adolescents.
Nouveau-nés ayant une anamnèse d'exposition à Co-Losartan Sandoz in utero
En présence d'une oligurie ou d'une hypotension, il faut veiller au soutien de la tension artérielle et de la circulation rénale. Une exsanguino-transfusion ou une dialyse peut être nécessaire pour corriger une hypotension et/ou substituer la fonction rénale insuffisante.
Utilisation chez les patients âgés
Des études cliniques ont montré l'absence d'effets liés à l'âge en ce qui concerne l'efficacité ou de la sécurité d'un traitement par Co-Losartan Sandoz.
Lactose
Co-Losartan Sandoz 50/12,5 mg et Co-Losartan Sandoz 100/25 mg contiennent du lactose. Les patients présentant une intolérance au galactose, un déficit total en lactase ou un syndrome de malabsorption du glucose et du galactose (maladies héréditaires rares) ne doivent pas prendre ce médicament.
Sodium
Co-Losartan Sandoz 100/12,5 mg contient moins de 1 mmol (23 mg) de sodium par comprimé pelliculé, c.-à-d. qu'il est essentiellement "sans sodium" .
InteractionsLosartan
Dans le cadre d'études pharmacocinétiques cliniques, aucune interaction cliniquement significative avec les substances ci-après n'a été observée: hydrochlorothiazide, digoxine, warfarine, (voir plus bas: hydrochlorothiazide, alcool, barbituriques ou narcotiques), kétoconazole et érythromycine. Le phénobarbital a, en tant qu'inducteur enzymatique, entraîné une diminution d'env. 20% de l'AUC du losartan et de son métabolite actif. La cimétidine, un inhibiteur enzymatique, a conduit à une augmentation de 18% de l'AUC du losartan, mais non de son métabolite actif. Ces effets ne sont pas considérés comme cliniquement significatifs. Pour la rifampicine et le fluconazole, des réductions du taux du métabolite actif ont été rapportées. Les conséquences cliniques de ces interactions n'ont pas été évaluées.
Comme avec d'autres médicaments qui bloquent l'angiotensine II ou ses effets, l'emploi simultané de diurétiques d'épargne potassique (p.ex. la spironolactone, le triamtérène, l'amiloride), de suppléments potassiques, de sels de régime contenant du potassium ou d'autres médicaments susceptibles d'augmenter le potassium sérique (tels que les médicaments contenant du triméthoprime) peuvent provoquer une hausse des taux sériques de potassium.
Comme avec d'autres médicaments qui influencent l'excrétion de sodium, l'excrétion du lithium peut diminuer. C'est pourquoi les taux sériques de lithium doivent faire l'objet d'une surveillance étroite lorsque des sels de lithium sont administrés en même temps que des antagonistes du récepteur de l'angiotensine II.
Les interactions potentielles du Co-Losartan Sandoz avec des anticoagulants oraux n'ont pas été étudiées.
Des études d'interaction entre Co-Losartan Sandoz et l'acénocoumarol et la phenprocoumone n'ont pas été effectuées.
Les anti-inflammatoires non stéroïdiens (AINS), y compris les inhibiteurs sélectifs de la cyclo-oxygénase-2 (inhibiteurs de la COX-2), peuvent diminuer l'effet des diurétiques et d'autres médicaments antihypertenseurs. C'est pourquoi l'effet hypotenseur des antagonistes du récepteur de l'angiotensine II ou des inhibiteurs de l'ECA peut diminuer sous l'effet des AINS, y compris des inhibiteurs sélectifs de la COX-2.
Chez les patients présentant une fonction rénale diminuée (par exemple patients âgés ou hypovolémiques, y compris patients sous diurétiques) et traités aux anti-inflammatoires non stéroïdiens, y compris des inhibiteurs sélectifs de la cyclo-oxygénase 2, l'administration simultanée d'antagonistes du récepteur de l'angiotensine II ou d'inhibiteurs de l'ECA peut provoquer une aggravation supplémentaire de la fonction rénale pouvant aller jusqu'à une éventuelle défaillance rénale aiguë. Ces effets sont habituellement réversibles. Par conséquent, ces associations seront administrées avec prudence chez des patients présentant une fonction rénale diminuée.
Double blocage du système rénine-angiotensine-aldostérone (SRAA)
Il existe des données indiquant que l'utilisation concomitante d'inhibiteurs de l'ECA, d'antagonistes des récepteurs de l'angiotensine II ou de l'aliskirène augmente le risque d'hypotension, d'hyperkaliémie et de diminution de la fonction rénale (y compris d'une défaillance rénale aiguë). C'est pour cette raison qu'un double blocage du SRAA par l'utilisation concomitante d'inhibiteurs de l'ECA, d'antagonistes des récepteurs de l'angiotensine II ou de l'aliskirène n'est pas recommandé.
Si le traitement par double blocage est considéré comme absolument nécessaire, celui-ci doit avoir lieu exclusivement sous la supervision d'un spécialiste et sous contrôle étroit de la fonction rénale, des valeurs électrolytiques et de la pression artérielle.
Les inhibiteurs de l'ECA et les antagonistes des récepteurs de l'angiotensine II ne doivent pas être utilisés simultanément chez des patients souffrant de néphropathie diabétique.
Le jus de pamplemousse contient des éléments inhibant des enzymes du CYP 450 et susceptibles de diminuer la concentration du métabolite actif de Co-Losartan Sandoz, ce qui peut amoindrir l'effet thérapeutique. La consommation de jus de pamplemousse doit être évitée pendant la prise de Co-Losartan Sandoz.
Hydrochlorothiazide
Les substances suivantes peuvent conduire à des interactions si elles sont administrées simultanément:
Alcool, barbituriques, narcotiques: renforcement de l'hypotension orthostatique.
Antidiabétiques: (substances orales et insuline): une adaptation de la dose des médicaments antidiabétiques peut être nécessaire.
Autres antihypertenseurs: effet additif.
Colestyramine et colestipol, résines échangeuses d'ions: l'absorption de l'hydrochlorothiazide est diminuée par les résines échangeuses d'anions. Des doses isolées de cholestyramine et de colestipol lient l'hydrochlorothiazide et réduisent son absorption gastro-intestinale dans des proportions pouvant atteindre respectivement 85% et 43%.
Corticostéroïdes, ACTH, ou glycyrrhizine (une substance contenue dans la réglisse), amphotéricine, carbénoxolone: renforcent la carence électrolytique, en particulier l'hypokaliémie.
Catécholamines (p.ex. adrénaline): une diminution de l'action des vasopresseurs est possible, ce qui n'interdit cependant pas leur utilisation.
Myorelaxants non dépolarisants (p.ex. tubocurarine): un renforcement de l'action de ces myorelaxants est possible.
Lithium: les diurétiques diminuent l'excrétion rénale du lithium et augmentent le risque d'une intoxication au lithium. Un traitement simultané est donc déconseillé. Les notices d'emballage accompagnant les préparations de lithium doivent être consultées avant l'utilisation de celles-ci.
Antirhumatismaux non stéroïdiens, y compris inhibiteurs de la cyclo-oxygénase 2: l'administration d'antirhumatismaux non-stéroïdiens, y compris d'inhibiteurs sélectifs de la cyclo-oxygénase 2, peut diminuer l'effet diurétique, natriurétique et antihypertenseur des diurétiques.
Chez les patients présentant une fonction rénale diminuée (p.ex. patients âgés ou hypovolémiques, y compris patients sous diurétiques) et traités avec des anti-inflammatoires non stéroïdiens, y compris des inhibiteurs sélectifs de la cyclo-oxygénase 2, l'administration simultanée d'antagonistes du récepteur de l'angiotensine II ou d'inhibiteurs de l'ECA peut provoquer une aggravation supplémentaire de la fonction rénale pouvant aller jusqu'à une éventuelle défaillance rénale aiguë. Ces effets sont habituellement réversibles. Par conséquent, ces traitements seront associés avec prudence chez des patients présentant une fonction rénale diminuée.
Allopurinol: augmentation de la fréquence des réactions d'hypersensibilité à l'allopurinol.
Cytostatiques (p.ex. méthotrexate, cyclophosphamide): diminution de l'excrétion rénale des cytostatiques.
Amantadine: augmentation du risque d'effets indésirables de l'amantadine.
Anticholinergiques (p.ex. atropine, bipéridène): augmentation de la biodisponibilité des diurétiques de type thiazide.
Vitamine D: renforcement de l'augmentation du calcium sérique.
Ciclosporine: augmentation du risque d'une hyperuricémie et de ses complications (goutte).
Sels calciques: les diurétiques de type thiazide peuvent provoquer une hypercalcémie par augmentation de la réabsorption tubulaire du calcium.
Diazoxide: renforcement de l'effet hyperglycémique du diazoxide.
Interactions médicamenteuses/Examens de laboratoire
En raison de leur action sur le métabolisme calcique, les thiazides peuvent influer sur les méthodes d'analyse de la fonction des glandes parathyroïdes (voir sous "Mises en garde et précautions" ).
Grossesse, allaitementGrossesse
Co-Losartan Sandoz est contre-indiqué pendant la grossesse (voir sous "Contre-indications" ). L'administration de Co-Losartan Sandoz doit être arrêtée le plus rapidement possible dès qu'une grossesse est constatée.
Premier trimestre
On ne dispose pas de données épidémiologiques définitives concernant le risque tératogène après une exposition aux inhibiteurs de l'ECA au cours du premier trimestre de la grossesse; une légère augmentation du risque ne peut cependant pas être exclue. Bien qu'il n'existe pas de données épidémiologiques contrôlées sur le risque associé aux antagonistes des récepteurs de l'angiotensine II (ARA II), un risque comparable pourrait exister avec cette classe de médicaments. À moins que le traitement par ARA II soit considéré comme nécessaire, les patientes qui envisagent une grossesse doivent passer à un traitement antihypertenseur alternatif offrant un profil de sécurité approprié pour la femme enceinte. Si une grossesse est constatée, il faut immédiatement arrêter le traitement par ARA II et commencer au besoin un traitement alternatif (voir "Mises en garde et précautions" ).
Les enfants ayant une anamnèse d'exposition à Co-Losartan Sandoz in utero doivent être surveillés étroitement à la recherche d'une hypotension, d'une oligurie et d'une hyperkaliémie.
Deuxième et troisième trimestres
On sait qu'un traitement aux ARA II pendant les deuxième et troisième trimestres de la grossesse entraîne des effets fœtotoxiques (diminution de la fonction rénale, oligohydramnios, retard d'ossification des os du crâne) et une toxicité chez le nouveau-né (défaillance rénale, hypotension, hyperkaliémie) (voir "Données précliniques" ).
En cas d'exposition à Co-Losartan Sandoz à partir du deuxième trimestre de la grossesse, il est vivement recommandé de contrôler la fonction rénale et le crâne par des examens échographiques.
Ces effets indésirables sont normalement associés à l'utilisation de ce type de médicaments au cours du deuxième et du troisième trimestre de la grossesse. La plupart des études épidémiologiques ayant examiné les anomalies fœtales à la suite d'un traitement antihypertenseur administré pendant le premier trimestre de la grossesse n'ont révélé aucune différence entre les antihypertenseurs agissant sur le système rénine-angiotensine et les autres types d'antihypertenseurs. Le traitement approprié d'une hypertension chez la femme enceinte est important pour optimiser les résultats aussi bien chez la mère que chez le fœtus.
L'hydrochlorothiazide traverse la barrière placentaire. Le mécanisme d'action pharmacologique de l'hydrochlorothiazide peut provoquer une perturbation de la circulation fœto-placentaire et entraîner chez le nouveau-né des effets indésirables tels qu'un ictère, un dérèglement de l'équilibre électrolytique et une thrombocytopénie.
Compte tenu des risques d'un volume plasmatique réduit et d'une ischémie placentaire sans effets bénéfiques sur l'évolution de la maladie, l'administration d'hydrochlorothiazide doit être évitée en cas d'œdèmes gestationnels, d'hypertension gestationnelle ou de pré-éclampsie.
Allaitement
Vu l'absence d'informations disponibles sur l'utilisation de Co-Losartan Sandoz dans la période d'allaitement et le fait que l'hydrochlorothiazide passe dans le lait maternel, Co-Losartan Sandoz est déconseillé. Il est préférable d'utiliser un traitement antihypertenseur alternatif offrant un profil de sécurité approprié pour la femme qui allaite, surtout dans le cas d'un enfant nouveau-né ou prématuré.
Effet sur l’aptitude à la conduite et l’utilisation de machinesLorsque le patient prend part au trafic routier ou conduit des machines, la prudence est de rigueur.
Effets indésirablesRésumé du profil de sécurité
Les études cliniques sur le traitement avec le losartan potassique en association avec l'hydrochlorothiazide n'ont révélé aucun effet indésirable nouveau. Les effets indésirables ont été limités à ceux déjà constatés au cours des études précédentes sur le losartan et/ou l'hydrochlorothiazide. La fréquence des événements indésirables sous association des deux médicaments a été comparable à celle enregistrée sous placebo. De même, le pourcentage des arrêts de traitement a été comparable à celui observé pour le placebo. Dans la plupart des cas, les effets indésirables ont été légers et passagers et n'ont pas nécessité l'arrêt du traitement.
Liste des effets indésirables
Les effets indésirables sont rangés par classe de système d'organes de la classification MedDRA et par fréquence selon la convention suivante: Très fréquents (≥1/10), fréquents (≥1/100, <1/10), occasionnels (≥1/1000, <1/100), rares (≥1/10'000, <1/1000) et très rares (<1/10'000), y compris des cas isolés rapportés.
Au cours d'études cliniques avec le losartan potassique/hydrochlorothiazide chez des patients atteints d'hypertension essentielle et d'hypertension avec hypertrophie du ventricule gauche, les effets indésirables ci-après ont été observés:
Affections du système nerveux
Fréquents: étourdissements.
Affections de l'oreille et du labyrinthe
Fréquents: vertige.
Affections de la peau et du tissu sous-cutané
Rares: éruption cutanée.
Troubles généraux et anomalies au site d'administration
Fréquents: sensation de faiblesse, fatigue.
Effets indésirables identifiés après la mise sur le marché
Les autres effets indésirables ci-après ont été observés pour Co-Losartan Sandoz après l'introduction sur le marché et/ou dans des études cliniques, ou observés pour les monosubstances indépendamment l'une de l'autre après l'introduction sur le marché (les catégories de fréquence ne peuvent pas être indiquées pour les rapports post-commercialisation):
Infections et infestations
Fréquents: infections des voies respiratoires supérieures.
Tumeurs bénignes, malignes et non précisées (incl. kystes et polypes)
Cancers de la peau de type non mélanocytaire [CPNM] (carcinome basocellulaire [CBC] et carcinome épidermoïde [CE]).
Affections hématologiques et du système lymphatique
Rares: purpura.
Très rares, y compris les cas isolés: agranulocytose, myélodépression et anémie hémolytique, leucopénie.
Anémie, thrombocytopénie.
Affections du système immunitaire
Très rares, y compris les cas isolés: réactions d'hypersensibilité.
De rares cas de réactions anaphylactiques, d'angiœdèmes y compris de gonflements du larynx et de la glotte (à l'origine d'une obstruction des voies respiratoires) et/ou des gonflements du visage, des lèvres, du pharynx et/ou de la langue ont été rapportés chez des patients sous traitement de losartan; quelques-uns de ces patients avaient présenté dans le passé un angiœdème sous d'autres médicaments, y compris des inhibiteurs de l'ECA.
Troubles du métabolisme et de la nutrition
Fréquents: hyperkaliémie, hypokaliémie.
Occasionnels: perte d'appétit, hyperuricémie, hyponatrémie, hypomagnésémie.
Rares: hypercalcémie, hyperglycémie, aggravation d'un état métabolique diabétique.
Très rares, y compris les cas isolés: alcalose hypochlorémique.
Affections psychiatriques
Fréquents: insomnie, agitation.
Rares: dépressions.
Affections du système nerveux
Très fréquents: céphalées.
Rares: vertiges ou étourdissements, paresthésies.
Dysgueusie, migraine.
Au cours d'études contrôlées, menées en double aveugle chez des patients atteints d'hypertension artérielle essentielle, des céphalées ont été observées chez 14,1% des patients traités avec le losartan, par rapport à 17,2% des patients dans le groupe sous placebo.
Affections oculaires
Troubles de la vision, surtout dans les premières semaines du traitement.
Épanchement choroïdien (fréquence inconnue).
Affections cardiaques
Fréquents: hypotension artérielle, palpitations, tachycardie.
Occasionnels: problèmes orthostatiques dépendants de la dose, hypotension orthostatique, pouvant être renforcée par l'alcool, les anesthésiques ou les sédatifs.
Rares: arythmies cardiaques.
Affections vasculaires
Rares: vascularite y compris de Henoch-Schoenlein.
Très rares, y compris les cas isolés: vascularite nécrosante.
Affections respiratoires, thoraciques et médiastinales
Fréquents: nez bouché, toux, pharyngite, troubles des sinus.
Très rares, y compris les cas isolés: troubles respiratoires y compris pneumopathie et œdème pulmonaire, syndrome de détresse respiratoire aiguë (SDRA) (voir "Mises en garde et précautions" ).
Affections gastro-intestinales
Fréquents: douleurs abdominales, dyspepsie, nausées, vomissements.
Rares: troubles abdominaux, constipation, troubles gastro-intestinaux, angiœdème intestinal.
Très rares, y compris les cas isolés: pancréatite.
Diarrhée.
Affections hépatobiliaires
Rares: hépatite, cholestase intra-hépatique ou ictère.
Affections de la peau et du tissu sous-cutané
Occasionnels: urticaire, autres éruptions cutanées.
Très rares, y compris les cas isolés: épidermolyse aiguë toxique, réactions rappelant un lupus érythémateux et réactivation d'un lupus érythémateux.
Érythrodermie, photosensibilité, prurit.
Affections musculosquelettiques et du tissu conjonctif
Fréquents: douleurs dorsales, crampes musculaires.
Arthralgie, myalgie.
Affections du rein et des voies urinaires
Rares: glycosurie.
Affections des organes de reproduction et du sein
Rares: impuissance.
Dysfonction érectile.
Troubles généraux et anomalies au site d'administration
Fréquents: douleurs thoraciques, œdèmes/tuméfaction.
Malaise.
Investigations
Fréquents: augmentation du taux d'ALAT, protéinurie.
Insuffisance hépatique.
Description d'effets indésirables sélectionnés
Cancers de la peau de type non mélanocytaire (CBC et CE): sur la base des données disponibles provenant d'études épidémiologiques, une relation cumulative dose-dépendante entre l'exposition à l'hydrochlorothiazide et des cancers de la peau de type non mélanocytaire a été observée (voir aussi les rubriques "Mises en garde et précautions" et "Propriétés/Effets" ).
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageIl n'existe pas d'informations spécifiques concernant le traitement d'un surdosage de Co-Losartan Sandoz. Le traitement avec Co-Losartan Sandoz doit être arrêté et le patient devra être attentivement surveillé. Au cas où la dose excessive a été prise depuis peu, induire le vomissement et corriger pertes de liquide, déséquilibres électrolytiques, coma hépatique et hypotension par des mesures appropriées.
Losartan
Les données dont on dispose sur le surdosage du losartan chez l'être humain sont limitées. Les signes les plus probables d'un surdosage devraient être une chute de la pression artérielle et une tachycardie. Une bradycardie pourrait survenir consécutivement à une stimulation du système parasympathique (stimulation vagale). En cas d'hypotension symptomatique, un traitement de soutien approprié pour stimuler la circulation devrait être administré.
Ni le losartan ni son métabolite actif ne peuvent être éliminés par hémodialyse.
Hydrochlorothiazide
Les principaux symptômes et les résultats d'analyse qui permettent de conclure à un surdosage sont des déséquilibres électrolytiques (hypokaliémie, hypochlorémie, hyponatrémie) et une déshydratation, consécutifs à une diurèse excessive. S'il y a prise simultanée de digitaliques, l'hypokaliémie peut renforcer les arythmies cardiaques.
On ignore dans quelle mesure l'hydrochlorothiazide est éliminé par hémodialyse.
Propriétés/EffetsCode ATC
C09DA01
Mécanisme d'action
Losartan
Le losartan est un antagoniste oral du récepteur de l'angiotensine II (type AT1). L'angiotensine II se lie au récepteur AT1 que l'on trouve dans de nombreux tissus du corps humain (p.ex. la musculature lisse des vaisseaux, les glandes surrénales, les reins et le cœur) où elle produit divers effets biologiques importants comprenant la vasoconstriction et la sécrétion d'aldostérone. L'angiotensine II stimule également la prolifération des cellules musculaires lisses. Des expérimentations biologiques et pharmacologiques ont montré que le losartan se lie sélectivement au récepteur AT1. Le losartan et son métabolite pharmacologiquement actif sous forme d'acide carboxylique (E-3174) bloquent aussi bien in vivo qu'in vitro tous les effets physiologiques significatifs de l'angiotensine II, indépendamment de son origine ou de son mode de synthèse.
Hydrochlorothiazide
Le mécanisme de l'effet antihypertenseur des thiazides n'est pas connu. Chez les sujets normotendus, les thiazides n'entraînent pas de diminution de la pression artérielle.
L'hydrochlorothiazide est un diurétique et un antihypertenseur. Il agit sur la réabsorption des électrolytes au niveau du tube contourné distal du rein. L'hydrochlorothiazide augmente l'excrétion du sodium et du chlorure environ dans les mêmes proportions. La natriurèse peut être accompagnée d'une légère perte en potassium et en bicarbonates.
La diurèse débute dans les 2 heures qui suivent la prise par voie orale, atteint un maximum après 4 heures environ, puis persiste durant 6–12 heures environ.
Losartan – hydrochlorothiazide
Les deux composants de Co-Losartan Sandoz ont un effet additif qui est supérieur à celui de chaque composant individuel sur la diminution de la pression artérielle. On présume que cet effet additif résulte d'une action complémentaire des deux substances. En conséquence de l'effet diurétique, l'hydrochlorothiazide augmente l'activité de la rénine plasmatique, la sécrétion d'aldostérone et les taux plasmatiques d'angiotensine II, et diminue le potassium sérique. L'administration de losartan bloque toutes les actions de l'angiotensine II importantes du point de vue physiologique. En outre, la déplétion potassique induite par les diurétiques pourrait être diminuée par un blocage de l'aldostérone.
Pharmacodynamique
Lors de l'administration du losartan, l'inhibition du rétrocontrôle négatif de l'angiotensine II sur la sécrétion de rénine conduit à une augmentation de l'activité de la rénine dans le plasma. L'accroissement de l'activité de la rénine plasmatique entraîne une augmentation de l'angiotensine II dans le plasma. En dépit de cette augmentation, l'effet hypotenseur et la diminution de la concentration d'aldostérone dans le plasma sont conservés, ce qui témoigne d'un blocage effectif des récepteurs de l'angiotensine II.
Le losartan se lie sélectivement aux récepteurs AT1; toutefois il ne se lie pas à - ou ne bloque pas – d'autres récepteurs hormonaux ou canaux ioniques qui jouent un rôle important dans la régulation cardiovasculaire. L'enzyme de conversion de l'angiotensine (kininase II) qui dégrade la bradykinine n'est pas inhibée par le losartan. Par conséquent, les effets qui ne reposent pas directement sur le blocage des récepteurs AT1, tels que l'augmentation des effets dus à la bradykinine ou la formation d'œdèmes (losartan 1,7%, placebo 1,9%) ne doivent pas être attribués au losartan.
On a montré que le losartan présente un effet uricosurique léger et passager. Une augmentation modérée de l'acide urique a été observée sous hydrochlorothiazide. L'association de losartan et d'hydrochlorothiazide tend à diminuer l'hyperuricémie induite par les diurétiques.
Efficacité clinique
Dans les études cliniques, l'administration d'une dose journalière unique de losartan à des patients présentant une hypertension essentielle légère à modérée, a induit une baisse statistiquement significative de la pression artérielle systolique et diastolique. Dans des études cliniques, cet effet hypotenseur a pu être maintenu durant une période se prolongeant jusqu'à un an. Les mesures de la pression artérielle au terme de l'intervalle posologique (24 heures après la prise) ont montré, comparativement à l'effet maximum (après 5–6 heures), un contrôle stable de la pression au cours des 24 heures. L'effet antihypertenseur correspondait au rythme journalier naturel. L'abaissement de la pression au terme de l'intervalle posologique se maintenait encore à des valeurs correspondant à 70–80% de la baisse obtenue après 5–6 heures. Une interruption du traitement avec le losartan n'a pas entraîné de montée brutale de la pression artérielle. En dépit d'une baisse notable de la pression artérielle, le losartan n'a pas exercé d'effet cliniquement significatif sur la fréquence cardiaque.
Chez des patients non diabétiques présentant une hypertension avec protéinurie, le losartan diminue de façon statistiquement significative la protéinurie et l'excrétion fractionnelle d'albumine et d'IgG. Le losartan maintient la filtration glomérulaire et réduit la fraction filtrée. Le losartan a entraîné une légère diminution des taux d'urémie, même pendant les traitements prolongés.
Chez des patients présentant une insuffisance cardiaque gauche, des doses de 25 à 50 mg de losartan ont provoqué des réactions hémodynamiques et neuro-hormonales positives, telles que l'élévation de l'index cardiaque et l'abaissement de la pression pulmonaire capillaire, de la résistance vasculaire systémique, de la pression artérielle moyenne, de la fréquence cardiaque et des taux sanguins d'aldostérone et de noradrénaline. Chez ces patients insuffisants cardiaques, la survenue d'une hypotension était dépendante de la dose administrée de losartan.
Le losartan présente une efficacité comparable chez l'homme et la femme, ainsi que chez les hypertendus jeunes (moins de 65 ans) et âgés (plus de 65 ans). L'efficacité du losartan était cependant plus faible chez les patients de couleur de peau noire que chez les Caucasiens.
L'expérience dont on dispose dans l'utilisation de Co-Losartan Sandoz chez les patients atteints d'autres affections cardiovasculaires (p.ex. insuffisance cardiaque, coronaropathie) est limitée.
Lorsque Co-Losartan Sandoz est administré en association avec des diurétiques du type thiazide, on peut s'attendre à un effet additif sur la baisse de la pression artérielle.
Cancers de la peau de type non mélanocytaire (CPNM): sur la base des données disponibles provenant d'études épidémiologiques, une relation cumulative dose-dépendante entre l'exposition à l'hydrochlorothiazide (HCTZ) et le développement de CPNM a été observée. Une des études a inclus une population composée de 71'553 cas de CBC et de 8629 cas de CE, appariés respectivement à 1'430'883 et 172'462 cas témoins. Une forte exposition à l'HCTZ (dose cumulative ≥50'000 mg) a été associée à un rapport de cotes (RC) ajusté de 1,29 (IC à 95%: 1,23-1,35) pour le CBC et de 3,98 (IC à 95%: 3,68-4,31) pour le CE. Une relation dose-effet cumulative claire a été observée à la fois pour le CBC et pour le CE. Une autre étude a montré le lien possible entre l'exposition à l'HCTZ et le carcinome des lèvres (CE): 633 cas de carcinome des lèvres ont été comparés avec 63'067 cas témoins, à l'aide d'une stratégie d'échantillonnage axée sur les risques ( "risk set sampling" ). Une relation dose-effet cumulative a été démontrée avec une augmentation du RC ajusté de 2,1 (IC à 95%: 1,7-2,6) à 3,9 (IC à 95%: 3,0-4,9) à la dose cumulative élevée (≥25'000 mg) et à 7,7 (IC à 95%: 5,7-10,5) à la dose cumulative la plus élevée (≥100'000 mg). (Voir également la rubrique "Mises en garde et précautions" ).
L'effet antihypertenseur de Co-Losartan Sandoz est maintenu pendant 24 heures. Cet effet antihypertenseur a persisté dans des études cliniques s'étendant sur une année au moins. En dépit d'une diminution significative de la pression artérielle, le traitement avec le losartan potassique/hydrochlorothiazide n'a pas entraîné d'effets cliniques mesurables sur la fréquence cardiaque. Dans des études cliniques, on a observé à la fin de l'intervalle de prise une diminution pouvant atteindre en moyenne 13,2 mmHg de la pression diastolique mesurée en position assise, au terme d'un traitement de douze semaines avec losartan 50 mg/hydrochlorothiazide 12,5 mg.
Dans une étude où l'on a testé en parallèle les deux associations losartan 50 mg/hydrochlorothiazide 12,5 mg et captopril 50 mg/hydrochlorothiazide 25 mg chez des patients hypertendus jeunes (<65 ans) et âgés (≥65 ans), on n'a pu mettre en évidence aucune différence entre les deux groupes de traitement ou les deux groupes d'âge.
Étude LIFE
L'étude interventionnelle avec le losartan sur la réduction des critères d'évaluation lors d'hypertension artérielle (Losartan Intervention for Endpoint Reduction in Hypertension, LIFE), était une vaste étude multinationale, randomisée, menée en triple aveugle et contrôlée activement, incluant 9193 patients hypertendus âgés entre 55 et 80 ans (moyenne: 67 ans) présentant une hypertrophie ventriculaire gauche documentée par ECG. Parmi les patients inclus au début de l'étude, 1195 (13%) présentaient un diabète sucré, 1326 (14%) une hypertension systolique isolée, 1468 (17%) une cardiopathie coronarienne et 728 (8%) une affection cérébrovasculaire.
L'objectif de l'étude était de démontrer l'existence d'un effet protecteur cardiovasculaire du losartan par rapport à l'aténolol, dépassant l'effet protecteur obtenu grâce à la baisse de la pression artérielle. La pression artérielle a été mesurée 24 heures après l'administration de la dernière dose. Selon la conception de l'étude, une réduction comparable de la pression artérielle devait être obtenue à cette fin dans les deux groupes de traitement. Les patients ont reçu, de manière randomisée, soit le losartan 50 mg, soit l'aténolol 50 mg une fois par jour. Lorsque la pression artérielle visée (<140/90 mm Hg) n'avait pas été atteinte, de l'hydrochlorothiazide (12,5 mg) était ajouté en premier, puis, le cas échéant, la dose de losartan ou d'aténolol était portée à 100 mg une fois par jour. Si nécessaire, d'autres antihypertenseurs (p.ex. augmentation de la dose d'hydrochlorothiazide à 25 mg ou adjonction d'autres diurétiques, d'antagonistes du calcium, d'alphabloquants, d'antihypertenseurs à action centrale, mais non d'inhibiteurs de l'ECA, d'antagonistes de l'angiotensine II ou de β-bloquants) ont été administrés en plus afin d'atteindre la pression artérielle visée. L'objectif étant de contrôler la pression artérielle, les patients des deux bras de l'étude LIFE ont reçu en plus de l'hydrochlorothiazide durant la majeure partie de la période pendant laquelle ils ont également été traités avec la médication d'étude (73,9% ou 72,4% des jours dans le groupe losartan ou aténolol).
Dans les deux groupes de traitement, la pression artérielle a été réduite de manière significative jusqu'à des valeurs comparables, et une fraction comparativement importante de patients a atteint la pression artérielle visée. La durée moyenne d'observation était de 4,8 ans.
Le critère d'évaluation principal était la combinaison des cas de morbidité et de mortalité cardiovasculaires et il était mesuré en termes de réduction des événements cardiovasculaires combinés de décès cardiovasculaire, d'accident vasculaire cérébral et d'infarctus du myocarde. Les résultats ont montré que le traitement par le losartan a permis, par rapport à l'aténolol, une réduction du risque de 13% (p=0,021) pour le critère d'évaluation principal combiné (voir le graphique 1).
La significativité statistique a été démontrée pour la réduction du nombre d'accidents vasculaires cérébraux, alors que les critères d'évaluation associés à la mortalité cardiovasculaire et aux infarctus du myocarde n'étaient pas statistiquement significatifs.
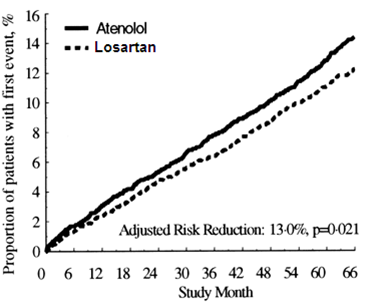
Graphique 1) Courbes de Kaplan-Meier décrivant le critère d'évaluation principal combiné (décès cardiovasculaire, accident vasculaire cérébral ou infarctus du myocarde) dans les groupes traités par le losartan et l'aténolol, ajustées au "Framingham Baseline Risk Score" et au degré de l'hypertrophie cardiaque gauche documentée par ECG.
Le traitement par le losartan a réduit le risque d'accident vasculaire cérébral par rapport à l'aténolol de 25% (p=0,001). Le taux des événements de mortalité cardiovasculaire et des infarctus du myocarde n'était pas significativement différent entre les groupes de traitement. L'effet du losartan sur le critère d'évaluation principal combiné semblait dépasser l'avantage obtenu grâce à la seule baisse de la pression artérielle (voir le tableau ci-dessous).
Critères d'évaluation de l'étude LIFE
Résultat Losartan (N=4605) n Taux* Aténolol (N=4588) n Taux* Réduction du risque* Valeur p
(%) (%) *
Critère d'évaluation 508 (11%) 23,8 588 (13%) 27,9 13% 0,021
combiné principal
Composantes du
critère d'évaluation
combiné principal
Mortalité cardiovasc 204 (4%) 9,2 234 (5%) 10,6 11% 0,206
ulaire
Accident vasculaire 232 (5%) 10,8 309 (7%) 14,5 25% 0,001
cérébral
Infarctus du myocard 198 (4%) 9,2 188 (4%) 8,7 -7% 0,491
e
* Par 1000 années-pa
tients de suivi. **
Ajusté au "Framingha
m Baseline Risk
Score" et aux
mesures de l'HVG
documentées par ECG.
D'autres critères d'évaluation cliniques de l'étude LIFE étaient: la mortalité totale, les hospitalisations en raison d'une insuffisance cardiaque ou d'une angine de poitrine, des mesures de revascularisation coronarienne ou périphérique ainsi qu'une réanimation après un arrêt cardiaque. Aucune différence significative en termes de fréquences de ces critères d'évaluation entre les groupes de traitement n'a été observée. Les patients traités par le losartan ont montré, par rapport aux patients traités par l'aténolol, une réduction significativement plus élevée des valeurs de l'HVG dans l'ECG.
L'effet du losartan par rapport à l'aténolol sur la morbidité et la mortalité cardiovasculaires a été étudié dans des sous-groupes chez des patients atteints de diabète sucré (n=1195) et présentant une hypertension systolique isolée (HSI) (n=1326) dans leurs antécédents. En ce qui concerne le critère d'évaluation principal combiné, les résultats de ces sous-groupes correspondaient au résultat favorable du traitement par le losartan de l'ensemble de la population étudiée: chez les diabétiques, une réduction de 24% du risque (p=0,03) et, chez les patients présentant une hypertension systolique isolée (HSI), une réduction de 25% du risque (p=0,06) ont été observées. Chez les patients atteints d'hypertension artérielle, avec hypertrophie ventriculaire gauche, Co-Losartan Sandoz est une formulation alternative adaptée aux patients qui seraient sinon traités en même temps avec le losartan et l'hydrochlorothiazide une fois par jour, afin de réduire la morbidité et la mortalité cardiovasculaires.
Différences concernant la couleur de peau
Les résultats favorables sur la morbidité et la mortalité cardiovasculaires du losartan par rapport à l'aténolol, observés au cours de l'étude LIFE, ne sont pas valables pour les patients de couleur de peau noire qui souffrent d'hypertension artérielle et d'hypertrophie ventriculaire gauche, bien que les deux traitements permettent des baisses efficaces de la pression artérielle chez les patients de couleur de peau noire.
En revanche, au cours de l'étude LIFE, le losartan a abaissé, par rapport à l'aténolol, le risque de morbidité et de mortalité cardiovasculaires chez les patients hypertendus non noirs souffrant d'hypertrophie ventriculaire gauche (n=8660) de manière significative (p=0,003) en ce qui concerne le critère d'évaluation principal composite (décès d'origine cardiovasculaire, accidents vasculaires cérébraux et infarctus du myocarde).
Il s'est avéré que les patients noirs traités par l'aténolol étaient exposés à un risque plus faible d'atteindre le critère d'évaluation principal combiné que les patients noirs traités par le losartan (p=0,03). Dans le sous-groupe de patients de couleur de peau noire (n=533; 6% des patients de l'étude LIFE), 29 événements du critère d'évaluation principal ont été observés parmi les 263 patients traités par l'aténolol (11%, 25,9 par 1000 années-patients) contre 46 parmi les 270 patients traités par le losartan (17%, 41,8 par 1000 années-patients).
Au cours de l'étude LIFE, une fréquence significativement plus faible des interruptions du traitement en raison d'effets secondaires indésirables a été observée sous le losartan, par rapport à l'aténolol.
PharmacocinétiqueAbsorption
Losartan
Après administration orale, le losartan est bien absorbé et subit un effet de premier passage, au cours duquel se forment un métabolite actif sous forme d'acide carboxylique et d'autres métabolites inactifs. La biodisponibilité des comprimés de losartan se situe aux environs de 33%. Les pics de concentration moyens du losartan sont atteints après 1 heure, ceux du métabolite actif après 3–4 heures. Lors de l'absorption simultanée d'un repas normal, on n'a pas constaté de variation cliniquement significative du profil des concentrations plasmatiques.
Hydrochlorothiazide
La biodisponibilité des comprimés d'hydrochlorothiazide est de 70% environ. Après absorption par voie orale d'une dose unique de 12,5, 25, 50 et 75 mg, des concentrations plasmatiques maximales moyennes de 70, 142, 260 et 376 ng/ml sont atteintes en moyenne au bout de deux heures. À l'intérieur de la fourchette des doses thérapeutiques, la disponibilité systémique de l'hydrochlorothiazide est proportionnelle à la dose.
Distribution
Losartan
Le losartan comme son métabolite actif sont liés aux protéines plasmatiques dans une proportion de 99% au moins, principalement à l'albumine. Le volume de distribution du losartan est de 34 litres. Des études chez le rat ont montré que le losartan ne traverse pratiquement pas la barrière hémato-encéphalique.
Hydrochlorothiazide
L'hydrochlorothiazide traverse le placenta, mais ne traverse pas la barrière hémato-encéphalique; il passe dans le lait maternel.
L'hydrochlorothiazide est lié pour environ 40–70% aux protéines du plasma. Le volume de distribution apparent est estimé à 5–6 l/kg.
Métabolisme
Losartan
Environ 14% d'une dose de losartan administrée per os sont transformés en métabolite actif. Des études in vitro montrent que les cytochromes P450 2C9 et 3A4 contribuent à la transformation du losartan en ses métabolites. Chez 1% des patients, cette transformation a été moins importante du fait d'un polymorphisme génétique concernant une enzyme particulière (moins de 1% de la dose en comparaison de 14% de la dose pour des patients normaux). Après administration orale de losartan marqué au 14C, la radioactivité circulant dans le plasma est due principalement au losartan et à son métabolite actif.
Outre le métabolite actif, des métabolites inactifs sont également formés, parmi lesquels deux principaux par hydroxylation de la chaîne latérale butyle et un autre métabolite, un glucuronide N-2 tétrazole.
Élimination
Losartan
La clairance plasmatique du losartan est de 600 ml/min, celle du métabolite actif de 50 ml/min. La clairance rénale du losartan est de 74 ml/min, respectivement de 26 ml/min pour le métabolite actif. Lors d'administration orale, 4% environ de la dose restent inchangés, environ 6% de la dose sont éliminés dans l'urine sous forme de métabolite actif. La pharmacocinétique du losartan et de son métabolite actif suit une évolution linéaire jusqu'à des doses de 200 mg.
Après administration orale, les concentrations plasmatiques de losartan et de son métabolite actif diminuent de manière polyexponentielle avec une demi-vie respective d'environ 2 et 6–9 heures. Avec une posologie journalière unique de 100 mg, on n'a pas observé de phénomène significatif d'accumulation du losartan ni de son métabolite actif dans le plasma.
L'élimination du losartan et de ses métabolites est assurée par les voies biliaire et rénale. Après administration orale de losartan marqué au 14C, on retrouve chez l'homme 35% de la radioactivité dans l'urine et 58% dans les selles.
Hydrochlorothiazide
Des études comprenant la mesure des taux plasmatiques sur au moins 24 heures ont révélé des demi-vies plasmatiques se situant entre 5,6 et 14,8 heures. Sur une dose administrée oralement, une part d'au moins 61% est éliminée dans les 24 heures par les reins, dont 95% sous forme inchangée et 4% sous forme d'hydrolysat 2-amino-4-chloro-m-benzènedisulfonamide. Jusqu'à 24% d'une dose orale peuvent être retrouvés dans les selles et une quantité insignifiante est excrétée par voie biliaire.
Cinétique pour certains groupes de patients
Losartan-hydrochlorothiazide
Pour le losartan (mais non pour le métabolite actif du losartan) et pour l'hydrochlorothiazide, l'aire sous la courbe (AUC) est plus élevée chez les patients âgés que chez les patients jeunes.
Losartan
Chez les patients atteints d'une cirrhose alcoolique légère à modérée, les concentrations plasmatiques de losartan et de son métabolite actif après prise per os se sont révélées respectivement 5 et 1,7 fois plus élevées que celles mesurées chez des hommes jeunes et sains.
Ni le losartan ni son métabolite actif ne peuvent être éliminés par hémodialyse.
Hydrochlorothiazide
Chez les patients âgés, la concentration plasmatique à l'état d'équilibre de l'hydrochlorothiazide est plus élevée et la clairance systémique considérablement ralentie par rapport aux patients jeunes.
En cas de troubles de la fonction rénale, les pics plasmatiques moyens et les valeurs d'AUC de l'hydrochlorothiazide sont augmentés. Chez les patients atteints d'insuffisance rénale (clairance de la créatinine comprise entre 30 et 70 ml/min), la demi-vie moyenne d'élimination est presque doublée.
Données précliniquesLes études précliniques – y compris les études conventionnelles concernant la pharmacologie générale, la génotoxicité et le potentiel cancérigène – n'ont révélé aucun risque particulier pour l'homme. Le potentiel toxique d'une association de losartan et d'hydrochlorothiazide en administration orale a été évalué chez des rats et des chiens dans des études de toxicité chronique d'une durée allant jusqu'à six mois. Les altérations observées sous l'association losartan-hydrochlorothiazide dans le cadre de ces études étaient dues essentiellement au losartan. L'administration de l'association losartan-hydrochlorothiazide a induit une réduction des paramètres érythrocytaires (taux de globules rouges, hémoglobine, hématocrite), une augmentation du taux sérique d'azote uréique, une réduction de la masse cardiaque (sans corrélat histologique) et des altérations gastro-intestinales (lésions des muqueuses, ulcères, érosions, hémorragies).
Aucun indice de tératogénicité n'a été trouvé chez le rat ou le lapin après l'administration de losartan-hydrochlorothiazide. Chez le rat, une toxicité fœtale se manifestant par une fréquence légèrement accrue de côtes surnuméraires dans la génération F1 a été observée lorsque les femelles étaient traitées avant et pendant la gestation. Ainsi qu'on l'a également constaté dans des études sur le losartan seul, une administration de losartan-hydrochlorothiazide à des rates en phase tardive de gestation et/ou allaitantes a été associée à des effets indésirables chez les fœtus et les animaux nouveau-nés, notamment une toxicité rénale ou la mort du fœtus.
Remarques particulièresStabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention "EXP" sur l'emballage.
Remarques particulières concernant le stockage
Conserver dans l'emballage original, à température ambiante (15-25°C) et hors de la portée des enfants.
Numéro d’autorisation57885 (Swissmedic)
PrésentationCo-Losartan Sandoz 50/12,5 mg: emballages de 28 et 98 comprimés pelliculés. [B]
Co-Losartan Sandoz 100/12,5 mg: emballages de 28 et 98 comprimés pelliculés. [B]
Co-Losartan Sandoz 100/25 mg: emballages de 28 et 98 comprimés pelliculés. [B]
Titulaire de l’autorisationSandoz Pharmaceuticals SA, Risch; domicile: Rotkreuz
Mise à jour de l’informationAvril 2025
|

