ZusammensetzungWirkstoffe:
Complexus toxini botulinici A et haemagglutinini
Hilfsstoffe
Albuminum humanum, Lactosum monohydricum
Darreichungsform und Wirkstoffmenge pro EinheitPulver zur Herstellung einer Injektionslösung.
Complexus toxini botulinici A et haemagglutinini 125 Speywood-Einheiten* pro Durchstechflasche.
* Eine Speywood Einheit ist definiert als mediane letale peritonale Dosis bei Mäusen (LD50)
Die Speywood-Einheiten von Azzalure sind für das Arzneimittel spezifisch und nicht auf andere Botulinumtoxin-Präparate übertragbar.
Indikationen/AnwendungsmöglichkeitenAzzalure wird angewendet zur vorübergehenden Verbesserung des Erscheinungsbildes von
mittelstarken bis starken Glabellafalten (vertikale Falten zwischen den Augenbrauen) beim Stirnrunzeln
mittelstarken bis starken Lateralen Augenfalten (Krähenfüsse) bei maximalem Lächeln
bei erwachsenen Patienten unter 65 Jahren, wenn das Ausmass dieser Falten eine erhebliche psychische Belastung für den Patienten darstellt.
Dosierung/AnwendungBotulinumtoxin-Einheiten sind je nach Arzneimittel verschieden. Die Speywood-Einheiten von Azzalure sind für das Arzneimittel spezifisch und nicht auf andere Botulinumtoxin-Präparate übertragbar.
Azzalure darf nur von Ärzten mit geeigneter Qualifikation angewendet werden, die die entsprechende Erfahrung mit dieser Behandlung haben und über die erforderliche Ausstattung verfügen.
Vor der Injektion muss das Arzneimittel rekonstituiert werden; die entsprechenden Anweisungen hierzu finden sich im Abschnitt "Sonstige Hinweise" .
Jedes Make-up ist zu entfernen, und die Haut ist mit einem Lokalantiseptikum zu desinfizieren.
Die intramuskulären Injektionen sollten mit einer sterilen 29-30 Gauge-Nadel vorgenommen werden.
Das Therapieintervall ist von dem festgestellten individuellen Ansprechen des jeweiligen Patienten abhängig
Das Therapieintervall mit Azzalure sollte nicht häufiger als alle 3 Monate sein.
Die empfohlenen Injektionspunkte für Glabellafalten und laterale Augenfalten sind unten beschrieben.
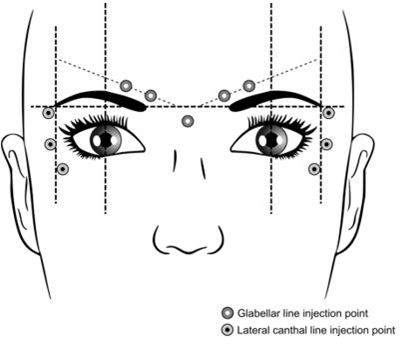
Übliche Dosierung
Glabellafalten:
Die empfohlene Dosis beträgt 50 Speywood-Einheiten (0,25 ml rekonstituierte Lösung) Azzalure, aufgeteilt auf 5 Injektionsstellen, d.h. es werden 10 Speywood-Einheiten (0,05 ml der rekonstituierten Lösung) intramuskulär im rechten Winkel an jeder der 5 Injektionsstellen angewendet: Zwei Injektionen in jeden M. corrugator und eine Injektion in den M. procerus in der Nähe des Nasofrontalwinkels, wie oben dargestellt.
Die anatomischen Orientierungspunkte können schneller ermittelt werden, wenn sie bei maximalem Stirnrunzeln beobachtet und palpiert werden. Vor der Injektion Daumen oder Zeigefinger fest unter den Augenhöhlenrand drücken, um eine Extravasation unter den Augenhöhlenrand zu verhindern. Die Nadel sollte während der Injektion nach superior und medial ausgerichtet sein. Um das Risiko einer Ptosis zu reduzieren, Injektionen in der Nähe des M. levator palpebrae superioris vermeiden, insbesondere bei Patienten mit grösseren Brauendepressorkomplexen (M. depressor supercilii). Injektionen in den M. corrugator dürfen nur im Mittelteil des Muskels, mindestens 1 cm über dem Augenhöhlenrand erfolgen.
In klinischen Studien wurde die optimale Wirkung bei Glabellafalten für bis zu 4 Monate nach Injektion nachgewiesen. Einige Patienten sprachen auch noch nach 5 Monaten auf die Therapie an (siehe Abschnitt "Eigenschaften/Wirkungen" ).
Laterale Augenfalten
Die empfohlene Dosis pro Seite beträgt 30 Speywood-Einheiten (60 Speywood-Einheiten für beide Seiten, 0,30 ml rekonstituierte Lösung) Azzalure, aufgeteilt auf 3 Injektionsstellen, d.h. es werden 10 Speywood-Einheiten (0,05 ml der rekonstituierten Lösung) intramuskular an jeder der Injektionsstellen verabreicht. Die Injektion sollte lateral (20 – 30° Winkel) zur Haut und sehr oberflächlich erfolgen. Alle Injektionsstellen sollten am äusseren Teil des Muskels Orbicularis oculi und ausreichend weit vom Orbitalrand entfernt (etwa 1 – 2 cm) liegen, wie oben dargestellt.
Die anatomischen Orientierungspunkte können schneller ermittelt werden, wenn sie bei maximalem Lächeln beobachtet und palpiert werden. Es muss darauf geachtet werden, Injektionen in die Muskeln Zygomaticus major/minor zu vermeiden, um einen seitlichen Mundabfall und ein asymmetrisches Lächeln zu vermeiden.
Allgemeine Informationen
Wenn die Behandlung fehlschlägt oder die Wirkung bei Wiederholungsinjektionen nachlässt, sollten alternative Behandlungsmethoden angewendet werden. Bei Fehlschlagen der Behandlung nach der ersten Anwendung können folgende Maßnahmen in Erwägung gezogen werden:
- Analyse der Gründe für das Therapieversagen, z.B. falsche Muskeln (in die injiziert wurde) oder ungeeignete Injektionstechnik, Bildung Toxin-neutralisierender Antikörper
- Erneute Überprüfung der Relevanz der Behandlung mit Botulinumtoxinum-A-Hämagglutininkomplex
Um die Rückverfolgbarkeit von biotechnologisch hergestellten Arzneimitteln sicherzustellen, wird empfohlen Handelsname und Chargennummer bei jeder Behandlung zu dokumentieren.
Therapiedauer
Sicherheit und Wirksamkeit von Wiederholungsinjektionen mit Azzalure wurden für Glabellafalten bis zu 24 Monaten und bis zu 8 wiederholten Behandlungszyklen sowie für laterale Augenfalten bis zu 12 Monaten und bis zu 5 wiederholten Behandlungszyklen überprüft
Ältere Patienten
Die Sicherheit und Wirksamkeit von Azzalure bei Personen über 65 Jahren wurde nicht nachgewiesen. Die Anwendung von Azzalure bei Personen über 65 Jahre wird nicht empfohlen
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von Azzalure bei Personen unter 18 Jahren wurde nicht nachgewiesen. Die Anwendung von Azzalure bei Personen unter 18 Jahren wird nicht empfohlen
KontraindikationenAzzalure darf nicht angewendet werden bei:
- Überempfindlichkeit gegenüber dem Wirkstoff oder einem der Hilfsstoffe gemäss Zusammensetzung.
- Infektionen an den vorgesehenen Injektionsstellen.
- Myasthenia gravis, Eaton-Lambert-Syndrom oder amyotropher Lateralsklerose.
Warnhinweise und VorsichtsmassnahmenEs sollte darauf geachtet werden, Azzalure nicht in ein Blutgefäss zu injizieren.
Bestehende neuromuskuläre Störungen
Azzalure ist bei Patienten mit einem Risiko für oder mit klinisch nachgewiesener gestörter neuromuskulärer Reizleitung mit Vorsicht anzuwenden. Solche Patienten haben möglicherweise eine erhöhte Empfindlichkeit gegen Arzneimittel wie Azzalure. Dies kann zu übermässiger Muskelschwäche führen.
Lokale und entfernte Ausbreitung der Toxin-Wirkung
Nebenwirkungen, die möglicherweise mit der Ausbreitung des Toxins an vom Applikationsort entfernte Stellen in Zusammenhang stehen, wurden bei Botulinumtoxin sehr selten berichtet. Bei Patienten, die mit therapeutischen Dosen behandelt wurden, kann eine übersteigerte Muskelschwäche auftreten. Schluck- und Atembeschwerden sind schwerwiegend und können zum Tod führen.
Bei Anwendung von Azzalure bei der Therapie von Glabellafalten und lateralen Augenfalten wurde über trockenes Auge berichtet (siehe "Unerwünschte Wirkungen" ). Es kann zur verringerten Tränenproduktion kommen, oder können verringertes Blinken oder Hornhauterkrankungen auftreten.
Die Injektion von Azzalure ist bei Patienten mit einer Vorgeschichte von Dysphagie und Aspiration nicht zu empfehlen.
Patienten oder pflegende Personen sollten darauf hingewiesen werden, dass sofort ein Arzt zu verständigen ist, wenn Schluck-, Sprech- oder Atemstörungen auftreten.
Die empfohlenen Dosierungen und die Häufigkeit der Anwendung von Azzalure dürfen nicht überschritten werden.
Es ist unbedingt erforderlich, dass sich der Arzt vor der Anwendung von Azzalure mit der Anatomie des Gesichts des Patienten vertraut macht. Gesichtsasymmetrien, Ptosis, übermässige Dermatochalasis, Vernarbungen und irgendwelche aufgrund früherer chirurgischer Eingriffe entstandene anatomische Veränderungen sollten berücksichtigt werden.
Azzalure sollte nur mit Vorsicht angewendet werden bei Entzündung der vorgesehenen Injektionsstelle(n) oder bei ausgeprägter Schwäche oder Atrophie des zu injizierenden Muskels.
Wie bei allen intramuskulären Injektionen wird eine Behandlung mit Azzalure bei Patienten mit verlängerter Blutgerinnungszeit nicht empfohlen.
Antikörperbildung
Injektionen in kürzeren Abständen oder mit zu hohen Dosierungen können das Risiko einer Antikörperbildung gegen Botulinumtoxin erhöhen. Klinisch kann die Bildung neutralisierender Antikörper die Wirksamkeit der nachfolgenden Behandlung verringern.
Botulinumtoxin-Einheiten sind nicht von einem Produkt zum anderen austauschbar. In Speywood-Einheiten empfohlene Dosen unterscheiden sich von anderen Botulinumtoxinpräparaten.
Azzalure darf nur zur Behandlung eines einzelnen Patienten bei einer Sitzung verwendet werden. Übrig gebliebenes, nicht verwendetes Arzneimittel muss, wie in Abschnitt "Sonstige Hinweise" näher beschrieben, entsorgt werden. Besondere Vorsicht ist bei der Zubereitung und Anwendung des Produkts sowie bei der Inaktivierung und Entsorgung der restlichen, nicht verwendeten Lösung erforderlich (siehe Abschnitt "Sonstige Hinweise" ).
InteraktionenDie gleichzeitige Behandlung mit Azzalure und Aminoglykosiden oder anderen Arzneimitteln, die auf die neuromuskuläre Reizleitung wirken (z.B. Curare-ähnliche Wirkstoffe), sollte nur mit Vorsicht erfolgen, da die Wirkung von Botulinumtoxinum-A-Hämagglutininkomplex potenziert werden kann.
Es wurden keine Wechselwirkungsstudien durchgeführt. Es wurden keine anderen Wechselwirkungen mit klinischer Relevanz berichtet
Schwangerschaft, StillzeitSchwangerschaft
Azzalure darf nicht in der Schwangerschaft angewendet werden. Es liegen keine hinreichenden Daten über die Anwendung von Clostridium botulinum Toxin Typ A bei schwangeren Frauen vor. In Studien an Tieren wurde bei hohen Dosierungen eine reproduktionstoxische Wirkung nachgewiesen (siehe Abschnitt "Präklinische Daten" ). Das potentielle Risiko für den Menschen ist nicht bekannt.
Stillzeit
Es ist nicht bekannt, ob Azzalure in die Muttermilch übergeht. Die Anwendung von Azzalure während der Stillzeit kann nicht empfohlen werden.
Fertilität
Es gibt keine klinischen Daten zu den Auswirkungen von Azzalure auf die Fertilität. In tierexperimentelle Studien gibt es keinen Nachweis einer direkten Auswirkung von Azzalure auf die Fertilität (siehe "Präklinische Daten" ).
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von MaschinenAzzalure hat einen geringen oder mässigen Einfluss auf die Fahrtüchtigkeit oder die Fähigkeit, Maschinen zu bedienen.
Es besteht ein potentielles Risiko für eine lokalisierte Muskelschwäche, Sehstörungen, Schwindel, eine generalisierte Asthenie oder Müdigkeit im Zusammenhang mit der Anwendung dieses Arzneimittels, die die Fähigkeit zum Führen eines Fahrzeugs oder zum Bedienen von Maschinen vorübergehend beeinträchtigen können (siehe "unerwünschte Wirkungen" ). Patienten sind auf dieses Risiko hinzuweisen.
Unerwünschte WirkungenMehr als 3800 Patienten erhielten Azzalure in den verschiedenen klinischen Studien.
Basierend auf placebokontrollierten klinischen Studien waren die beobachteten Nebenwirkungs-Raten nach der ersten Injektion von Azzalure 22,3 % bei der Behandlung der Glabellafalten (16,6 % für Placebo) und 6,2 % bei der Behandlung der lateralen Augenfalten (2,9 % für Placebo). Die meisten dieser Ereignisse hatten einen leichten bis mässigen Schweregrad und waren reversibel.
Die häufigsten Nebenwirkungen waren Kopfschmerzen und Reaktionen an der Injektionsstelle bei Glabellafalten sowie Kopfschmerzen, Reaktionen an der Injektionsstelle und Augenlidödem bei lateralen Augenfalten.
Im Allgemeinen traten Nebenwirkungen im Zusammenhang mit der Behandlung bzw. der Injektionstechnik innerhalb der ersten Woche nach Injektion auf und waren vorübergehend.
Die Inzidenz der Reaktionen, die mit der Behandlung bzw. mit der Injektionstechnik zusammenhingen, verringerte sich während der Wiederholungszyklen. Nebenwirkungen können mit dem Wirkstoff zusammenhängen, mit dem Injektionsverfahren oder einer Kombination von beidem.
„sehr häufig“ (≥1/10)
„häufig“ (≥1/100, <1/10)
„gelegentlich“ (≥1/1000, <1/100)
„selten“ (≥1/10'000, <1/1000)
„sehr selten“ (<1/10'000)
"nicht bekannt" (kann aus den verfügbaren Daten nicht abgeschätzt werden)
Erkrankungen des Immunsystems
Gelegentlich: Überempfindlichkeit*
Erkrankungen des Nervensystems
Sehr häufig: Kopfschmerzen (12.5%)**
Häufig: temporäre Fazialisparese (temporäre Parese der Gesichtsmuskeln proximal zu den Injektionsstellen, überwiegend wird Lidheberparese beschrieben)
Gelegentlich: Schwindel*
Augenerkrankungen
Häufig: Asthenopie* Ptosis, Lidödeme, vermehrter Tränenfluss*, trockenes Auge***, Muskelzucken* (Zucken der Muskeln in der Umgebung der Augen)
Gelegentlich: Sehstörungen*, Verschwommensehen*, Diplopie*
Selten: Störung der Augenbewegungen*
Erkrankungen der Haut und des Unterhautzellgewebes
Gelegentlich: Juckreiz*, Hautausschlag*
Selten: Urtikaria*
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort
Sehr häufig: Reaktionen an der Einstichstelle** (z.B. Hautrötung, Ödem, Reizung, Hautausschlag (Rash), Juckreiz, Parästhesien, Schmerzen, Beschwerden, Stechen und Bluterguss)
Über unerwünschte Wirkungen, für die eine sich von der Injektionsstelle ausbreitende Toxinwirkung verantwortlich gemacht wird (übermäßige Schwächung der Muskulatur, Dysphagie, Aspirationspneumonie, in einigen Fällen mit tödlichem Ausgang), wurde nach Anwendung von Botulinumtoxin sehr selten berichtet (siehe Abschnitt "Warnhinweise und Vorsichtsmassnahmen" ).
*unerwünschte Wirkungen nur beobachtet bei der Indikation "Glabellafalten"
**bei der Indikation "laterale Augenfalten" : "häufig"
***bei der Indikation "laterale Augenfalten" : "gelegentlich"
Unerwünschte Wirkungen nach Markteinführung
Erkrankungen des Nervensystems
nicht bekannt: Hypoästhesie
Erkrankungen des Immunsystems
Nicht bekannt: Überempfindlichkeit
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen
Nicht bekannt: Muskelatrophie
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort
Nicht bekannt: Asthenie, Müdigkeit, grippeähnliche Symptome
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
ÜberdosierungEs ist davon auszugehen, dass übermäßig hohe Dosen von Botulinumtoxin eine neuromuskuläre Schwäche mit einer Vielzahl von Symptomen hervorrufen. Bei Patienten, bei denen übermäßig hohe Dosen zu einer Lähmung der Atemmuskulatur führen, kann eine Beatmung erforderlich sein. Im Falle einer Überdosierung muss der Patient ärztlich auf Symptome einer übermäßigen Muskelschwäche oder einer Muskellähmung überwacht werden. Falls erforderlich, ist eine symptomorientierte Behandlung einzuleiten.
Es kann sein, dass Symptome einer Überdosierung nicht unmittelbar nach einer Injektion auftreten.
Eine Einweisung in ein Krankenhaus sollte bei Patienten erwogen werden, bei denen Symptome einer Vergiftung mit Botulinumtoxinum-A-Hämagglutininkomplex festgestellt werden (z.B. eine Kombination aus Muskelschwäche, Ptosis, Diplopie, Schluck- und Sprechstörungen oder Lähmung der Atemmuskulatur).
Eigenschaften/WirkungenATC-Code
M03AX01
Wirkungsmechanismus
Botulinumtoxin A blockiert selektiv die Übertragung an cholinergen Nervenendigungen durch Hemmung der Freisetzung von Acetylcholin. Die chemische Denervierung bewirkt am Skelettmuskel eine schlaffe Lähmung, an parasympathisch innervierten glatten Muskeln eine Atonie.
Die Wiederherstellung der Impulsübertragung erfolgt über neu gebildete Nervenendigungen und motorische Endplatten. Dieser Regenerationsprozess beginnt ca. 8 Wochen nach Toxinverabreichung.
Pharmakodynamik
Die wichtigste pharmakodynamische Wirkung von Botulinumtoxinum-A-Hämagglutininkomplex ist auf die chemische Denervierung des behandelten Muskels zurückzuführen, die zu einer messbaren Verringerung des Muskelsummenpotenzials führt, welche eine örtlich begrenzte Verringerung oder eine Lähmung der Muskelaktivität bewirkt.
Klinische Wirksamkeit
Während der klinischen Entwicklung von Azzalure wurden mehr als 4500 Patienten in die verschiedenen klinischen Studien einbezogen und etwa 3800 Patienten erhielten Azzalure.
Glabellafalten
2032 Patienten mit mittelstarken bis starken Glabellafalten wurden in klinischen Studien mit der empfohlenen Dosis von 50 Speywood-Einheiten behandelt. Von diesen Patienten wurden 305 mit 50 Einheiten in zwei zulassungsrelevanten, doppelblinden, placebokontrollierten Phase-III-Studien und 1'200 mit 50 Einheiten in einer offenen Phase-III-Langzeitstudie mit wiederholter Anwendung behandelt. Die übrigen Patienten wurden in supportiven Studien und Dosisfindungsstudien behandelt.
Die mediane Zeit bis zum Eintreten der Reaktion betrug 2 bis 3 Tage nach der Behandlung, wobei die maximale Wirkung am Tag 30 beobachtet wurde. In beiden zulassungsrelevanten, placebokontrollierten Phase-III-Studien verringerten die Azzalure-Injektionen signifikant den Schweregrad der Glabellafalten für bis zu 4 Monate. Die Wirkung war in einer der beiden zulassungsrelevanten Studien nach 5 Monaten noch signifikant.
30 Tage nach der Injektion hatten nach der Beurteilung der Prüfärzte 90 % (273/305) der Patienten auf die Behandlung angesprochen (d.h. sie wiesen keine oder nur leichte Glabellafalten bei maximalem Stirnrunzeln auf), dagegen nur 3 % (4/153) der mit Placebo behandelten Patienten. 5 Monate nach Injektion sprachen in der betroffenen Studie immer noch 17 % (32/190) der mit Azzalure behandelten Patienten auf die Therapie an, dagegen nur 1 % (1/92) der mit Placebo behandelten Patienten. Die Beurteilung der Patienten selbst ergab nach 30 Tagen und bei maximalem Stirnrunzeln eine Ansprechrate von 82 % (251/305) bei den mit Azzalure behandelten Patienten und von 6 % (9/153) bei den mit Placebo behandelten Patienten. Der Anteil der Patienten, die nach der Beurteilung der Prüfärzte bei maximalem Stirnrunzeln eine Verbesserung um zwei Schweregrade zeigte, betrug 77 % (79/103) in der einen zulassungsrelevanten Phase-III-Studie, in der diese Beurteilung vorgenommen wurde.
Eine Untergruppe von 177 Patienten hatte vor der Behandlung mittelstarke oder starke Glabellafalten im Ruhezustand. 30 Tage nach der Behandlung hatten nach der Beurteilung der Prüfärzte in diesem Kollektiv 71 % (125/177) der mit Azzalure behandelten Patienten auf die Behandlung angesprochen, verglichen mit 10 % (8/78) der mit Placebo behandelten Patienten.
Die offene Phase-III-Langzeitstudie mit wiederholter Anwendung ergab, dass die mediane Zeit von 3 Tagen bis zum Ansprechen über die Zyklen mit wiederholter Anwendung hinweg aufrechterhalten blieb. Die Ansprechrate bei maximalem Stirnrunzeln, die von den Prüfärzten nach 30 Tagen ermittelt wurde, wurde über die Zyklen mit wiederholter Anwendung hinweg aufrechterhalten und lag während der 5 Zyklen im Bereich von 80 % bis 91 %. Die Ansprechrate im Ruhezustand während der Zyklen mit wiederholter Anwendung war auch übereinstimmend mit der in den Einzeldosisstudien, 30 Tage nach der Behandlung und gemäss Beurteilung der Prüfärzte betrug diese 56 % bis 74 % bei den mit Azzalure behandelten Patienten.
Keiner der klinischen Endpunkte beinhaltete eine objektive Bewertung der psychischen Folgen.
Laterale Augenfalten
In doppelblinden klinischen Studien wurden 308 Patienten mit mittelstarken bis starken lateralen Augenfalten bei maximalem Lächeln mit der empfohlenen Dosis von 30 Speywood-Einheiten pro Seite behandelt. Von diesen Patienten wurden 252 in einer doppelblinden placebokontrollierten Phase III Studie und 56 Patienten in einer doppelblinden Phase II Dosisfindungsstudie behandelt.
Der primäre Wirksamkeitsendpunkt der Phase-III-Studie war 4 Wochen nach der Injektion: die Bewertung der Prüfer zeigte, dass 47,2 % (119/252) der Patienten auf die Behandlung angesprochen hatten (keine oder geringfügige laterale Augenfalten bei maximalem Lächeln), im Vergleich zu 7,2 % (6/83) der mit Placebo behandelten Patienten.
Azzalure-Injektionen reduzierten signifikant den Schweregrad von lateralen Augenfalten im Vergleich zu Placebo (p ≤0,001) nach 4, 8 und 12 Wochen (beurteilt durch die Prüfer bei maximalem Lächeln). Bei der Bewertung der Zufriedenheit der Probanden mit dem Erscheinungsbild ihrer lateralen Augenfalten gab es einen statistisch signifikanten Unterschied zwischen Azzalure und Placebo (p ≤0,010) zum Vorteil von Azzalure nach 4, 8 und 12 Wochen.
Insgesamt 315 Patienten traten in die offene Erweiterungsphase der Phase III Studie ein. Patienten, die in den doppelblinden und offenen Phasen der Phase III Studie mit Azzalure
behandelt wurden, erhielten im Mittel 3 Behandlungen der lateralen Augenfalten. Das mediane Intervall zwischen Injektionen der lateralen Augenfalten, das weitgehend durch das Protokolldesign bestimmt wurde, betrug zwischen 85 und 108 Tagen. Die Ergebnisse zeigten, dass die Wirksamkeit mit wiederholten Behandlungen über den Zeitraum von 1 Jahr erhalten bleibt.
Das Zufriedenheitsniveau der Patienten 4, 16 und 52 Wochen nach der ersten Behandlung mit Azzalure zeigt, dass 165/252 Patienten (65,5 %) entweder sehr zufrieden oder zufrieden mit dem Erscheinungsbild ihrer lateralen Augenfalten waren.
Nach 16 Wochen, d.h. 4 Wochen entweder nach der zweiten Behandlung mit Azzalure für Patienten, die in Teil A auf Azzalure randomisiert worden waren oder nach der ersten
Behandlung für Patienten, die auf Placebo randomisiert worden waren, lag der Anteil der Patienten, die sehr zufrieden oder zufrieden waren bei 233/262 (89,0 %). Nach 52 Wochen, wenn die Patienten bis zu fünf Behandlungen mit Azzalure erhalten haben konnten, mit der letzten Behandlung nach 48 Wochen, lag der Anteil der sehr zufriedenen/zufriedenen Patienten bei 255/288 (84,7 %).
Langzeitdaten
Auch nach über einem Jahr wiederholter Behandlungen mit Azzalure wurde kein Patient positiv auf Toxin-neutralisierende Antikörper getestet.
PharmakokinetikAbsorption
Nach i.m.-Injektion in der empfohlenen Dosierung ist nicht zu erwarten, dass Azzalure im peripheren Blut in messbarer Menge vorhanden ist. Daher wurden mit Azzalure keine pharmakokinetischen Studien durchgeführt.
Distribution
Keine Angaben
Metabolismus
Keine Angaben
Elimination
Keine Angaben
Präklinische DatenToxizität bei wiederholter Verabreichung
In einer an Ratten durchgeführten Langzeit-Toxizitätsstudie fanden sich keine Hinweise für eine systemische Toxizität in Dosierungen, die der 75-fachen bei Menschen empfohlenen Dosierung (50 Einheiten), bei gleichmäßiger Verteilung auf den rechten und linken M. glutaeus, entsprachen. Studien zur akuten Toxizität, Langzeit-Toxizität und lokalen Verträglichkeit an der Injektionsstelle ergaben bei klinisch relevanten Dosierungen keine ungewöhnlichen lokalen oder systemischen Nebenwirkungen
Mutagenität / Karzinogenität
Es wurden keine Studien zum genotoxischen oder kanzerogenen Potential von Azzalure durchgeführt.
Reproduktionstoxizität
In Reproduktionsstudien an Ratten und Kaninchen wurde bei hohen Dosierungen eine schwere maternale Toxizität mit Einnistungs- (Nidations-) Verlusten beobachtet. In Dosierungen, die dem 60- bis 100-fachen der empfohlenen Dosis beim Menschen (50 Einheiten) entsprechen, wurde bei Kaninchen bzw. Ratten keine embryofetale Toxizität beobachtet. Bei diesen Tierarten wurden keine teratogenen Effekte beobachtet. Bei Ratten wurde die Fruchtbarkeit von Männchen und Weibchen aufgrund der verminderten Paarungen, bedingt durch Muskellähmung unter hohen Dosierungen, verringert.
Sonstige HinweiseInkompatibilitäten
Das Arzneimittel darf nur mit den unter Hinweise für die Handhabung aufgeführten Arzneimitteln gemischt werden.
Haltbarkeit
Das Arzneimittel darf nur bis zu dem auf dem Behälter mit "EXP" bezeichneten Datum verwendet werden.
Haltbarkeit des Pulvers im unversehrten Behältnis: 24 Monate.
Haltbarkeit der rekonstituierten Lösung
Die gebrauchsfertige Lösung ist nicht konserviert. Die chemische und physikalische Stabilität der rekonstituierten Lösung wurde für 24 Stunden bei 2°C bis 8°C nachgewiesen.
Aus mikrobiologischen Gründen sollte die gebrauchsfertige Injektionslösung sofort, d.h. unmittelbar nach Rekonstitution, angewendet werden. Wenn die gebrauchsfertige Injektionslösung nicht sofort angewendet wird, ist der Anwender für die Dauer und die Bedingungen der Lagerung verantwortlich, die nicht länger als 24 Stunden bei 2-8°C betragen sollte. Nicht für eine weitere Anwendung einfrieren.
Besondere Lagerungshinweise
Im Kühlschrank (2-8°C) lagern.
In der Originalverpackung aufbewahren.
Ausser Reichweite von Kindern aufbewahren.
Hinweise für die Handhabung
Die Anweisungen zur Handhabung, Anwendung und Entsorgung müssen strikt eingehalten werden.
Zubereiten der Injektionslösung
Die Rekonstitution ist in Übereinstimmung mit den Regeln der guten Herstellungspraxis, insbesondere im Hinblick auf die Asepsis, durchzuführen.
Azzalure muss mit 0,63 ml Natriumchlorid 9 mg/ml (0,9 %)-Injektionslösung rekonstituiert werden. Dies ergibt eine klare und farblose Lösung, die 125 Speywood-Einheiten des Wirkstoffs bei einer Konzentration von 10 Einheiten pro 0,05 ml der rekonstituierten Lösung enthält.
Die genaue Abmessung von 0,63 ml kann mit 1 ml-Spritzen, wie für Insulin verwendet, vorgenommen werden: Diese sind bis 1 ml in Stufen von 0,1 ml und 0,01 ml unterteilt.
Empfehlungen für die Entsorgung von kontaminierten Materialien
Unmittelbar nach der Anwendung und vor der Entsorgung muss unbenutztes rekonstituiertes Azzalure (in der Durchstechflasche oder in der Spritze) mit 2 ml verdünnter Natriumhypochloritlösung (0,55 oder 1 %ig) (Bleichmittel) inaktiviert werden.
Gebrauchte Durchstechflaschen, Spritzen oder Materialien dürfen nicht entleert werden, sondern müssen in entsprechende Behälter geworfen und gemäss den lokalen Vorschriften entsorgt werden.
Empfehlungen bei Unfällen während des Umgangs mit Botulinumtoxin
- Jegliches verschüttetes Arzneimittel muss aufgewischt werden: Entweder - im Fall des Pulvers - mit einem saugfähigen Material, das mit einer Natriumhypochloritlösung (Bleichmittel) getränkt wurde oder - im Fall der rekonstituierten Lösung - mit einem trockenen saugfähigen Material.
- Kontaminierte Oberflächen müssen mit einem saugfähigen Material, das mit einer Natriumhypochloritlösung (Bleichmittel) getränkt wurde, gereinigt und anschließend trockengerieben werden.
- Wenn eine Durchstechflasche zerbricht, wie oben beschrieben vorgehen: Glassplitter vorsichtig aufsammeln und das Arzneimittel aufwischen, dabei Schnittverletzungen der Haut vermeiden.
- Wenn das Arzneimittel in Kontakt mit der Haut gelangt, den betroffenen Bezirk mit einer Natriumhypochloritlösung (Bleichmittel) waschen und anschließend gründlich mit reichlich Wasser abspülen.
- Wenn das Arzneimittel in Kontakt mit den Augen gelangt, die Augen gründlich mit reichlich Wasser oder einer Augenspüllösung ausspülen.
- Wenn das Arzneimittel in Kontakt mit einer Wunde, Schnittverletzung oder nicht-intakter Haut gelangt, gründlich mit reichlich Wasser spülen und die adäquaten medizinischen Massnahmen entsprechend der injizierten Dosis ergreifen.
Zulassungsnummer62780 (Swissmedic).
PackungenPackungen mit einer oder zwei Durchstechflasche(n) (A)
ZulassungsinhaberinIPSEN Pharma Schweiz GmbH, Zug
Stand der InformationMärz 2022
|

