| ||||||||||||||||
|
| Home - Ipro sur Trikafta |
| Information professionnelle sur Trikafta: | Vertex Pharmaceuticals (CH) GmbH |
Propriétés/EffetsCode ATC Tableau 7: liste des mutations du gène CFTR répondant à l'elexacaftor/teza caftor/ivacaftor Mutations répondant à Trikafta sur la base des données cliniques 2789+5G→A D1152H L997F P5L R1066H 3272-26A→G F508del L1077P R117C S945L 3849+10kbC→T G85E M1101K R347H T338I A455E L206W N1303K R347P V232D Mutations répondant à Trikafta sur la base des données in vitro 3141del9 E588V G970D L165S R117G S589N 546insCTA E822K G1061R L320V R117H S737F A46D F191V G1069R L346P R117L S912L A120T F311del G1244E L453S R117P S977F A234D F311L G1249R L967S R170H S1159F A349V F508C G1349D L1324P R258G S1159P A554E F508C;S1251N † H139R L1335P R334L S1251N A1006E F575Y H199Y L1480P R334Q S1255P A1067T F1016S H939R M152V R347L T1036N D110E F1052V H1054D M265R R352Q T1053I D110H F1074L H1085P M952I R352W V201M D192G F1099L H1085R M952T R553Q V456A D443Y G27R H1375P P67L R668C V456F D443Y;G576A; R668C † G126D I148T P205S R751L V562I D579G G178E I175V P574H R792G V754M D614G G178R I336K Q98R R933G V1153E D836Y G194R I502T Q237E R1070Q V1240G D924N G194V I601F Q237H R1070W V1293G D979V G314E I618T Q359R R1162L W361R D1270N G463V I807M Q1291R R1283M W1098C E56K G480C I980K R31L R1283S W1282R E60K G551D I1027T R74Q S13F Y109N E92K G551S I1139V R74W S341P Y161D E116K G576A I1269N R74W; D1270N † S364P Y161S E193K G576A;R668C † I1366N R74W;V201M † S492F Y563N E403D G622D K1060T R74W;V201M; D1270N † S549N Y1014C E474K G628R L15P R75Q S549R Y1032C Mutations répondant à Trikafta sur la base d'une extrapola tion de l'étude 445-124 711+3A→G E831X † Mutations complexe s/composées dans lesquelles un seul allèle du gène CFTR présente plusieurs mutations. Elles existent indépendamm ent des mutations présentes sur l'autre allèle. Tableau 8: Mutations CFTR appropriées répondant à l'elexac aftor/tezacaftor/iva caftor 2789+5G>A D1152H L997F R117C T338I 3272-26A>G G85E M1101K R347H V232D 3849+10kbC>T L1077P P5L R347P A455E L206W R1066H S945L Tableau 9: Analyses du critère
d'efficacité principal et des
principaux critères secondaires,
population complète d'analyse
(étude 445-102)
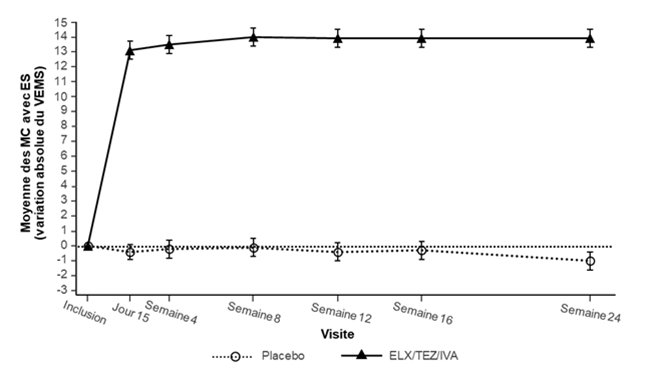
Analyse Statistique Placebo N = 203 Trikafta N = 200
Critère d'efficacité principal
Variation absolue du VEMS de Différence entre S/O S/O -0,4 (0,5) 14,3 (12,7; 15,8) P
l'inclusion jusqu'à la semaine 24 les traitements (IC < 0,0001 13,9 (0,6)
(%) à 95 %) Valeur de P
Variation intragroup
e (ES)
Principaux critères d'efficacité
secondaires
Variation absolue du VEMS à la Différence entre S/O S/O -0,2 (0,6) 13,7 (12,0; 15,3)
semaine 4 par rapport à la valeur les traitements (IC P < 0,0001 13,5
initiale (%) à 95 %) Valeur de P (0,6)
Variation intragroup
e (ES)
Nombre d'exacerbations Nombre d'événements 113 (0,98) S/O S/O 41 (0,37) 0,37
pulmonaires de l'inclusion (taux d'événements (0,25; 0,55) P <
jusqu'à la semaine 24‡ annuel††) Rapport 0,0001
des taux (RR) (IC à
95 %) Valeur de P
Variation absolue du taux de Différence entre S/O S/O -0,4 (0,9) -41,8 (-44,4;
chlorure sudoral par rapport à la les traitements (IC -39,3) P < 0,0001
valeur initiale jusqu'à la à 95 %) Valeur de P -42,2 (0,9)
semaine 24 (mmol/l) Variation intragroup
e (ES)
Variation absolue du score du Différence entre S/O S/O -2,7 (1,0) 20,2 (17,5; 23,0) P
domaine respiratoire CFQ-R de les traitements (IC < 0,0001 17,5 (1,0)
l'inclusion jusqu'à la semaine 24 à 95 %) Valeur de P
(points) Variation intragroup
e (ES)
Variation absolue de l'IMC à la Différence entre S/O S/O 0,09 (0,07) 1,04 (0,85; 1,23) P
semaine 24 par rapport à la les traitements (IC < 0,0001 1,13 (0,07)
valeur initiale (kg/m2) à 95 %) Valeur de P
Variation intragroup
e (ES)
Variation absolue du taux de Différence entre S/O S/O 0,1 (1,0) -41,2 (-44,0;
chlorure sudoral à la semaine 4 les traitements (IC -38,5) P < 0,0001
par rapport à la valeur initiale à 95 %) Valeur de P -41,2 (1,0)
(mmol/l) Variation intragroup
e (ES)
Variation absolue du score du Différence entre S/O S/O -1,9 (1,1) 20,1 (16,9; 23,2) P
domaine respiratoire CFQ-R à la les traitements (IC < 0,0001 18,1 (1,1)
semaine 4 par rapport au score à 95 %) Valeur de P
initial (points) Variation intragroup
e (ES)
VEMS: volume expiratoire maximum
par seconde exprimé en
pourcentage de la valeur
théorique; IC: intervalle de
confiance; ES: erreur standard;
S/O: sans objet; CFQ-R: Cystic
Fibrosis Questionnaire Revised,
(questionnaire révisé spécifique
de la mucoviscidose), IMC: indice
de masse corporelle. ‡ Une
exacerbation pulmonaire était
définie comme une modification de
l'antibiothérapie (intraveineuse,
inhalée ou orale) en raison de la
présence d'au moins 4 des 12
signes/symptômes sino-pulmonaires
prédéfinis. †† Taux annuel
d'événements estimé calculé sur
la base de 48 semaines par an.
ES: erreur standard; ELX/TEZ/IVA: elexacaftor/tezacaftor/ivacaftor. Tableau 10: Analyses du critère
d’efficacité principal et des
principaux critères secondaires,
population complète d’analyse
(étude 445-103)
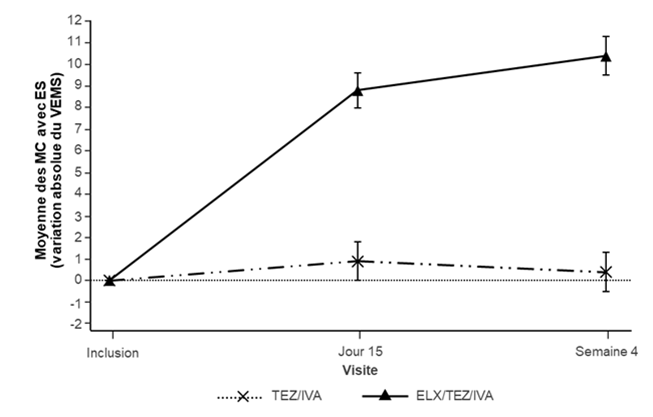
Analyse* Statistique Tezacaftor/ ivacafto Trikafta N = 55
r# N = 52
Critère d’efficacité principal
Variation absolue du VEMS à la Différence entre S/O S/O 0,4 (0,9) 10,0 (7,4 ; 12,6) P
semaine 4 par rapport à la valeur les traitements (IC < 0,0001 10,4 (0,9)
initiale (%) à 95 %) Valeur de P
Variation intragroup
e (ES)
Principaux critères d’efficacité
secondaires
Variation absolue du taux de Différence entre S/O S/O 1,7 (1,8) -45,1 (-50,1 ;
chlorure sudoral à la semaine 4 les traitements (IC -40,1) P < 0,0001
par rapport à la valeur initiale à 95 %) Valeur de P -43,4 (1,7)
(mmol/l) Variation intragroup
e (ES)
Variation absolue du score du Différence entre S/O S/O -1,4 (2,0) 17,4 (11,8 ; 23,0)
domaine respiratoire CFQ-R à la les traitements (IC P < 0,0001 16,0
semaine 4 par rapport au score à 95 %) Valeur de P (2,0)
initial (points) Variation intragroup
e (ES)
VEMS : volume expiratoire maximum
par seconde exprimé en
pourcentage de la valeur
théorique ; IC : intervalle de
confiance ; ES : erreur standard
; S/O : sans objet ; CFQ-R :
Cystic Fibrosis Questionnaire
Revised, (questionnaire révisé
spécifique de la mucoviscidose).
* La valeur initiale pour le
critère principal et les
principaux critères secondaires
est définie comme la valeur à la
fin de la période de pré-inclusion
de 4 semaines sous tezacaftor/iva
caftor et ivacaftor. # Traitement
par tezacaftor/ivacaftor et
ivacaftor.
ES: erreur standard; TEZ/IVA: tezacaftor/ivacaftor; ELX/TEZ/IVA: elexacaftor/tezacaftor/ivacaftor
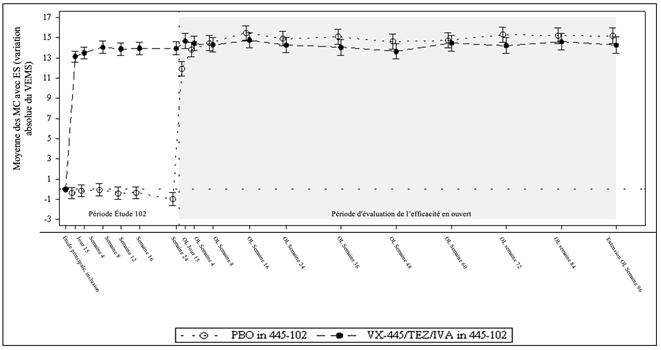
VEMS = volume expiratoire maximum par seconde (VEMS) exprimé en pourcentage de la valeur théorique; moyenne des MC = moyenne calculée par la méthode des moindres carrés; ES = erreur standard; OL = en ouvert.
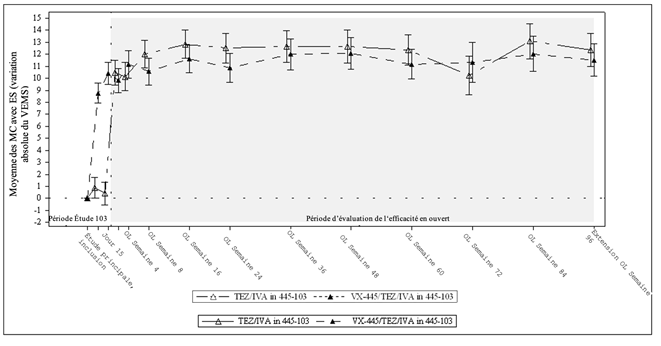
VEMS = volume expiratoire maximum par seconde exprimé en pourcentage de la valeur théorique; moyenne des MC = moyenne calculée par la méthode des moindres carrés; ES = erreur standard; OL = en ouvert. Tableau 11: Étude
445-105 Analyse en
ouvert des critères
d'efficacité seconda
ires, population
complète d'analyse
(patients porteurs
du génotype F/MF ou
F/F)
Analyse Statistique À la semaine 192 de
l'étude 445-105
PBO dans l'étude ELX/TEZ/IVA dans TEZ/IVA dans l'étude ELX/TEZ/IVA dans
445-102 N = 203 l'étude 445-102 N = 445-103 N = 52 l'étude 445-103 N =
196 55
Variation absoluedu n 136 133 32 36
VEMS parrapport à
la valeurinitiale*
(%)
Moyenne des MC 15,3 13,8 10,9 10,7
IC à 95 % (13,7; 16,8) (12,3; 15,4) (8,2; 13,6) (8,1; 13,3)
Variation absoluedu n 133 128 31 38
taux dechlorure
sudoral par rapport
àla valeur initiale*
(mmol/)
Moyenne des MC -47,0 -45,3 -48,2 -48,2
IC à 95 % (-50,1; -43,9) (-48,5; -42,2) (-55,8; -40,7) (-55,1; -41,3)
Nombrede PExpendant Nombre d'événe-ments 385 71
la périoded'évaluati
on del'efficacité
cumuléede la triplea
ssociation†
Taux annueld'événe-m 0,21 (0,17; 0,25) 0,18 (0,12; 0,25)
entsestimé (IC à95
%)
VEMS = volume
expiratoire maximum
par seconde exprimé
en pourcentage de
la valeur théorique;
PEx = exacerbation
pulmonaire; moyenne
LS = moyenne calculé
e selon la méthode
des moindres carrés;
IC intervalle de
confiance; PBO =
placebo. * Valeur
initiale = valeur
initiale de l'étude
principale. † Pour
les patients randomi
sés dans le groupe
ELX/TEZ/IVA, la
période d'évaluation
de l'efficacité
cumulée de la
triple association
inclut les données
des études principal
es jusqu'à la
semaine 192 de
traitement dans
l'étude 445-105 (N
= 255, dont 4
patients qui ne
sont pas entrés
dans l'étude 445-105
). Pour les patients
randomisés dans le
groupe placebo ou
TEZ/IVA, la période
d'évaluation de
l'efficacité cumulée
de la triple
association inclut
uniquement les
données jusqu'à la
semaine 192 de
traitement dans
l'étude 445-105 (N
= 255).
Tableau 12: Analyses du critère
d'efficacité principal et des
principaux critères secondaires,
population complète d'analyse
(étude 445-104)
Analyse* Statistique Groupe contrôle# N Groupe Trikafta N =
= 126 132
Critère principal
Variation absolue du VEMS de Variation intragroup 0,2 (-0,7; 1,1) 3,7 (2,8; 4,6)
l'inclusion jusqu'à la semaine 8 e (IC à 95 %)
(%)
Valeur de P S/O P < 0,0001
Principaux critères secondaires
et autres critères secondaires
Variation absolue du taux de Variation intragroup 0,7 (-1,4; 2,8) -22,3 (-24,5; -20,2)
chlorure sudoral de l'inclusion e (IC à 95 %)
jusqu'à la semaine 8 (mmol/l)
Valeur de P S/O P < 0,0001
Variation absolue du VEMS jusqu'à Différence entre S/O 3,5 (2,2; 4,7)
la semaine 8 par rapport à la les traitements (IC
valeur initiale comparativement à 95 %)
au groupe contrôle (%)
Valeur de P S/O P < 0,0001
Variation absolue du taux de Différence entre S/O -23,1 (-26,1; -20,1)
chlorure sudoral jusqu'à la les traitements (IC
semaine 8 par rapport à la valeur à 95 %)
initiale comparativement au
groupe contrôle (mmol/l)
Valeur de P S/O P < 0,0001
Variation absolue du score du Variation intragroup 1,6 (-0,8; 4,1) 10,3 (8,0; 12,7)
domaine respiratoire CFQ-R de e (IC à 95 %)
l'inclusion jusqu'à la semaine 8
(points) ±
Variation absolue du score du Différence entre S/O 8,7 (5,3; 12,1)
domaine respiratoire CFQ-R les traitements (IC
jusqu'à la semaine 8 par rapport à 95 %)
au score initial comparativement
au groupe contrôle (points) ±
VEMS: volume expiratoire maximum
par seconde exprimé en
pourcentage de la valeur
théorique; IC: intervalle de
confiance; S/O: sans objet;
CFQ-R: Cystic Fibrosis
Questionnaire-Revised,
(questionnaire révisé spécifique
de la mucoviscidose). * La valeur
initiale pour le critère
principal et les critères
secondaires est définie comme la
valeur à la fin de la période de
préinclusion de 4 semaines sous
ivacaftor ou tezacaftor/ivacaftor.
# Groupe ivacaftor ou groupe
tezacaftor/ivacaftor. ± Il n'a
pas été effectué d'ajustement
pour multiplicité des scores du
domaine respiratoire CFQ-R selon
la procédure de tests
hiérarchisés.
Tableau 13: Analyses des critères secondaires d'évaluation de l'efficacité,
population complète d'analyse sur 24 semaines (étude 445-106, partie B)
Analyse Variation intragroup
e (IC à 95 %) pour
Trikafta N=66
Variation absolue du VEMS de l'inclusion jusqu'à la semaine 24 (%) 10,2 (7,9; 12,6)
Variation absolue du taux de chlorure sudoral de l'inclusion jusqu'à la -60,9 (-63,7; -58,2)
semaine 24 (mmol/l)
Nombre d'exacerbations pulmonaires jusqu'à la semaine 24‡ 4 (0,12) ††
IC: intervalle de confiance: VEMS: volume expiratoire maximum par seconde en
pourcentage de la valeur théorique. ‡ Une exacerbation pulmonaire était
définie comme une modification de l'antibiothérapie (intraveineuse, inhalée
ou orale) en raison de la présence d'au moins 4 des 12 signes/symptômes
sino-pulmonaires prédéfinis. †† Nombre d'événements et taux annuel
d'événements estimé déterminé sur la base de 48 semaines par an.
Tableau 14: Analyses des critères
secondaires d'évaluation de
l'efficacité, population complète
d'analyse (N = 64) (étude 445-107)
Analyse Statistique Variation absolue à Variation absolue à
la semaine 96 par la semaine 192 par
rapport à la valeur rapport à la valeur
initiale initiale*
VEMS (%) n 45 27
Moyenne des MC 11,2 9,6
IC à 95 % (8,3; 14,2) (5,4; 13,7)
Taux de chlorure sudoral (mmol/l) n 56 35
Moyenne des MC -62,3 -57,9
IC à 95 % (-65,9; -58,8) (-63,3; -52,5)
Nombre de PEx pendant la période Nombre d'événements 7 11
d'évaluation de l'efficacité
cumulée de la triple association†
Taux annuel d'événements observé 0,04 0,045
VEMS = volume expiratoire maximum
par seconde exprimé en
pourcentage de la valeur
théorique; PEx = exacerbation
pulmonaire; MC = moindres carrés;
IC = intervalle de confiance. MC
= moindres carrés; IC =
intervalle de confiance. * Valeur
initiale = valeur initiale dans
l'étude principale. † La période
d'évaluation de l'efficacité
cumulée de la triple association
inclut les données des 66
patients ayant été inclus et qui
avaient reçu au moins une dose du
traitement dans l'étude
principale (étude 445-106 partie
B) et/ou qui ont reçu au moins
une dose pendant l'étude 445-107.
Tableau 15: Analyses des critères secondaires
d'évaluation de l'efficacité, population complète
d'analyse (étude 445-111)
Analyse Statistique TrikaftaVariation
intra-groupe (IC à
95 %)
Variation absolue du taux de chlorure sudoral jusqu'à N* Moyenne des MC 75 -57,9 (-61,3;
la semaine 24 par rapport à la valeur initiale (mmol/l) (IC à 95 %) -54,6)
Variation absolue de l'ICP2,5 jusqu'à la semaine 24 par N Moyenne des MC 63‡ -0,83 (-1,01;
rapport à la valeur initiale (IC à 95 %) -0,66)
Nombre d'exacerbations pulmonaires jusqu'à la semaine N Nombre d'événement 75 12 (0; 32) ††
24** s (taux annuel
d'événements estimé)
IC: intervalle de confiance; ICP: index de clairance
pulmonaire. * N est le nombre de patients dans la
population complète d'analyse correspondante. ‡ ICP
évalué uniquement chez les patients âgés de 3 ans et
plus lors de la sélection. ** Des définitions
spécifiques à l'âge d'une exacerbation pulmonaire sont
utilisées pour les patients âgés de 2 à 5 ans et de 6
ans et plus. †† Nombre d'événements et taux annuel
d'événements estimé déterminé sur la base de 48
semaines par an.
Tableau 16: Analyses d'efficacité
principale et secondaires,
population d'analyse complète
(étude 445-124)
Analyse Paramètres statistiq Placebo N = 102 ELX/TEZ/IVA N = 205
ues
Analyse principale
Variation absolue du VEMS à la Différence entre S/O 9,2 (7,2; 11,3)
semaine 24 par rapport à la les traitements (IC
valeur initiale (en pourcentage) à 95 %)
Valeur de p S/O p<0,0001
Variation intragroupe (ES) -0,4 (0,8) 8,9 (0,6)
Analyses secondaires
Variation absolue du taux de Différence entre S/O -28,3 (-32,1, -24,5)
chlorure sudoral à la semaine 24 les traitements (IC
par rapport à la valeur initiale à 95 %)
(mmol/l)
Valeur de p S/O p<0,0001
Variation intragroupe (ES) 0,5 (1,6) -27,8 (1,1)
Variation absolue du score du Différence entre S/O 19,5 (15,5; 23,5)
domaine respiratoire du CFQ-R à les traitements (IC
la semaine 24 par rapport à la à 95 %)
valeur initiale (points)
Valeur de p S/O p<0,0001
Variation intragroupe (ES) -2,0 (1,6) 17,5 (1,2)
Variation absolue de l'IMC à la Différence entre S/O 0,47 (0,24; 0,69)
semaine 24 par rapport à la les traitements (IC
valeur initiale (kg/m2) à 95 %)
Valeur de p S/O p<0,0001
Variation intragroupe (ES) 0,35 (0,09) 0,81 (0,07)
Variation absolue du poids à la Différence entre S/O 1,3 (0,6; 1,9)
semaine 24 par rapport à la les traitements (IC
valeur initiale (kg) à 95 %)
Valeur de p S/O p<0,0001
Variation intragroupe (ES) 1,2 (0,3) 2,4 (0,2)
Nombre de PEx jusqu'à la semaine Rapport des taux S/O 0,28 (0,15; 0,51)
24 incluse (IC à 95 %)
Valeur de p S/O p<0,0001
Nombre d'événements 40 21
Taux annuel d'événements estimé 0,63 0,17
CFQ-R RD: Cystic Fibrosis
Questionnaire-Revised Respiratory
Domain (questionnaire révisé
spécifique de la mucoviscidose,
domaine respiratoire); ELX:
elexacaftor; ES: erreur standard;
IMC: indice de masse corporelle;
IVA: ivacaftor; N: taille de
l'échantillon total; p:
probabilité; PEx: exacerbation
pulmonaire; TEZ: tezacaftor;
VEMS: volume expiratoire maximum
par seconde exprimé en
pourcentage de la valeur
théorique.
| |
| ||||||||||||
|
|