Propriétés/EffetsCode ATC
M05BX06
Mécanisme d'action/Pharmacodynamique
Le romosozumab est un anticorps monoclonal humanisé (IgG2) qui se lie à la sclérostine pour l'inhiber. Le romosozumab a une double action sur les os: Il augmente l'ossification et diminue la résorption osseuse. Le romosozumab augmente la masse osseuse trabéculaire et corticale, tout en améliorant la structure et la solidité des os.
Le rosomozumab entraîne une augmentation de l'ossification et une diminution de la résorption osseuse. Chez la femme post-ménopausée atteinte d'ostéoporose, le romosozumab a augmenté le marqueur d'ossification, à savoir le propeptide N-Terminal du procollagène de type 1 (P1NP), en début de traitement, l'augmentation maximale d'environ 145% par rapport au placebo ayant été atteinte 2 semaines après le début du traitement; puis, les valeurs sont revenues au niveau du placebo au bout de 9 mois et ont chuté à 15% environ au-dessous du niveau du placebo après 12 mois. Le romosozumab a diminué le marqueur de résorption osseuse, à savoir le télopeptide C-Terminal du collagène de type 1 (CTX), la réduction maximale d'environ 55% par rapport au placebo étant intervenue 2 semaines après le début du traitement. Les taux de CTX sont restés sous le niveau du placebo et étaient environ 25% inférieurs à ceux du placebo au bout de 12 mois.
Après l'arrêt du romosozumab chez la femme post-ménopausée atteinte d'ostéoporose, les taux de P1NP sont revenus aux valeurs de départ en l'espace de 12 mois; en 3 mois, le taux de CTX est passé au-dessus des valeurs de départ, puis est revenu aux taux de départ au bout de 12 mois, ce qui signifie que l'effet est réversible. Le renouvellement du traitement par romosozumab (chez un nombre limité de patientes) après une pause thérapeutique de 12 mois a entraîné une hausse du taux de P1NP et une baisse de CTX dues au romosozumab dans des proportions similaires à celles observées pendant le premier traitement.
Chez les femmes qui avaient antérieurement pris de l'alendronate par voie orale, le romosozumab a également entraîné une augmentation de l'ossification et une baisse de la résorption osseuse.
Efficacité clinique
Chez la femme post-ménopausée atteinte d'ostéoporose, EVENITY réduit le risque de fractures vertébrales et cliniques d'une part et non vertébrales d'autre part. EVENITY augmente la masse osseuse chez la femme post-ménopausée atteinte d'ostéoporose.
Traitement de l'ostéoporose chez la femme post-ménopausée
L'efficacité et la sécurité d'EVENITY ont été contrôlées dans deux études pivots, l'une contrôlée par alendronate (ARCH) et l'autre contrôlée par placebo (FRAME).
Etude 20110142 (ARCH)
L'efficacité et la sécurité d'EVENITY dans le traitement de l'ostéoporose chez la femme post-ménopausée ont été démontrées dans une étude de supériorité multicentrique, internationale, randomisée, en double aveugle, contrôlée par alendronate sur 4093 femmes post-ménopausées ayant entre 55 et 90 ans (âge moyen de 74,3 ans).
Les femmes incluses avaient soit un score DMO-T ≤ −2,50 au niveau de la hanche totale ou du col du fémur et au moins 1 fracture vertébrale modérément sévère ou sévère, soit un score DMO-T ≤ -2,00 au niveau de la hanche totale ou du col du fémur et au moins 2 fractures vertébrales modérément sévères ou sévères, soit elles avaient subi une fracture du fémur proximal 3 à 24 mois avant la randomisation.
Au début de l'étude, les scores DMO-T moyens étaient respectivement de -2,6, -2,80 et -2,90 au niveau du rachis lombaire, de la hanche totale et du col du fémur; 96,1% des femmes présentaient une fracture vertébrale au début de l'étude et 99% avaient déjà subi une fracture ostéoporotique. Les femmes ont été randomisées (1:1) pour recevoir un traitement de 12 mois en double aveugle par injections sous-cutanées mensuelles d'EVENITY ou par alendronate administré par voie orale une fois par semaine. Suite à la phase d'étude de 12 mois en double aveugle, les femmes ont reçu de l'alendronate dans les deux groupes, sans lever le caractère aveugle du traitement initial. L'analyse principale a été effectuée après que toutes les femmes ont achevé la visite de l'étude du 24è mois; des fractures cliniques ont été confirmées chez au moins 330 femmes et sont survenues après une période de suivi médiane de 33 mois d'étude. Les femmes ont reçu une supplémentation quotidienne en calcium et vitamine D.
Les principaux critères d'évaluation de l'efficacité étaient l'incidence des nouvelles fractures vertébrales jusqu'au 24è mois et l'incidence des fractures cliniques (fractures non vertébrales ou cliniques et vertébrales) au moment de l'analyse principale.
Effet sur les nouvelles fractures vertébrales et cliniques
Comme indiqué dans le tableau 1, EVENITY entraîne une baisse significative de l'incidence des nouvelles fractures vertébrales jusqu'au mois 24 et de l'incidence des fractures cliniques jusqu'au moment de l'analyse principale par rapport au traitement par alendronate seul. Le risque de subir les deux types de fractures était déjà réduit au bout de 12 mois.
Tableau 1. Effet d'EVENITY sur l'incidence et le risque de nouvelles fractures vertébrales et cliniques chez des femmes post-ménopausées atteintes d'ostéoporose
|
|
Taux de femmes présentant une fracture
|
Réduction du risque absolu
(%) (IC à 95%)
|
Réduction du risque relatif
(%) (IC à 95%)
|
Valeur P nominale
|
Valeur P
ajustéea
| |
Alendronate/
Alendronate
(%)
|
Romosozumab/
Alendronate
(%)
| |
Nouvelles fractures vertébrales
| |
Jusqu'au mois 12 b
|
85/1703
(5,0)
|
55/1696
(3,2)
|
1,84
(0,51; 3,17)
|
36
(11; 54)
|
0,008
|
NAc
| |
Jusqu'au mois 24b
|
147/1834 (8,0)
|
74/1825
(4,1)
|
4,03
(2,50; 5,57)
|
50
(34; 62)
|
< 0,001
|
< 0,001
| |
Fractures cliniquesd
| |
Analyse principale
Suivi médian d'environ 33 mois
|
266/2047 (13,0)
|
198/2046
(9,7)
|
NAe
|
27
(12; 39)
|
< 0,001
|
< 0,001
| |
Jusqu'au mois 12
|
110/2047 (5,4)
|
79/2046
(3,9)
|
1,8
(0,5; 3,1)
|
28
(4; 46)
|
0,027
|
NAc
| |
Jusqu'au mois 24
|
197/2047 (9,6)
|
146/2046
(7,1)
|
2,7
(0,8; 4,5)
|
26
(9; 41)
|
0,005
|
NAc
|
a Les valeurs P ajustées reposent sur la procédure d'Höchberg et doivent être comparées avec un niveau de signification de 0,05.
b La réduction du risque absolu et la réduction du risque relatif reposent sur la méthode de Mantel-Haenszel ajustée pour Altersstrata, le score DMO-T au niveau de la hanche totale au début de l'étude (≤2,5, > -2,5) et la présence de fractures vertébrales sévères au début de l'étude. La comparaison des traitements repose sur un modèle de régression logistique ajusté pour Altersstrata, le score DMO-T au niveau de la hanche totale au début de l'étude et la présence de fractures vertébrales sévères au début de l'étude.
NAc: Le critère d'évaluation ne faisant pas partie du test séquentiel, l'ajustement de la valeur P n'est pas applicable.
d Toutes les fractures symptomatiques, y compris les fractures non vertébrales et vertébrales douloureuses, font partie des fractures cliniques. La comparaison entre les traitements repose sur un modèle à risque proportionnel (régression de Cox) ajusté pour Altersstrata, le score DMO-T au niveau de la hanche totale au début de l'étude et la présence de fractures vertébrales sévères au début de l'étude.
e NA: Non disponible, car l'exposition au moment de l'analyse principale était différente parmi les participantes de l'étude.
Effet sur d'autres types/groupes de fractures
Tableau 2. Effet d'EVENITY sur l'incidence et le risque d'autres types/groupes de fractures jusqu'à l'analyse principale (suivi médian de 33 mois environ) chez des femmes post-ménopausées atteintes d'ostéoporose
|
|
Taux de femmes présentant une fracture
|
Réduction du risque relatif
(%) (IC à 95%)
|
Valeur P nominalea
|
Valeur P
ajustée
| |
Alendronate/
Alendronate
(%)
|
Romosozumab/
Alendronate
(%)
| |
Non vertébrale
|
217/2047 (10,6)
|
178/2046 (8,7)
|
19 (1; 34)
|
0,019d
|
0,040c
| |
Hanche
|
66/2047 (3,2)
|
41/2046 (2,0)
|
38 (8; 58)
|
0,015
|
NAe
| |
Ostéoporotique majeure f
|
209/2047 (10,2)
|
146/2046 (7,1)
|
32 (16; 45)
|
< 0,001
|
NAe
| |
Non vertébrale majeureg
|
196/2047 (9,6)
|
146/2046 (7,1)
|
27 (10; 41)
|
0,004
|
NAe
|
a Les valeurs P nominales reposent sur un modèle à risque proportionnel (régression de Cox) ajusté pour Altersstrata, le score DMO-T au niveau de la hanche totale au début de l'étude et la présence de fractures vertébrales sévères au début de l'étude.
b Les valeurs P ajustées reposent sur une association des méthodes suivantes: Procédure d'Höchberg, procédure de test avec hypothèses posées a priori et procédure de test séquentielle par groupes; elles doivent être comparées avec un niveau de signification de 0.05.
c Bilatérale
d Unilatérale
NAe: Le critère d'évaluation ne faisant pas partie du test séquentiel, l'ajustement de la valeur P n'est pas applicable.
f Fractures de la hanche, de l'avant-bras ou du haut du bras sans lien avec une fracture pathologique, quelle que soit la sévérité du traumatisme, et fractures cliniques vertébrales
g Fractures du bassin, du fémur distal, du tibia proximal, des côtes, du haut du bras proximal, de l'avant-bras et fractures de la hanche
En outre, EVENITY a réduit l'incidence des fractures non vertébrales majeures (major nonvertebral) après 12 mois seulement par rapport à l'alendronate.
Effet sur la densité minérale osseuse (DMO)
Chez les femmes post-ménopausées atteintes d'ostéoporose, EVENITY a entraîné une hausse significative de la DMO au niveau du rachis lombaire, de la hanche totale et du col du fémur au bout de 12 mois seulement par rapport à l'alendronate. Suite à la phase en double aveugle, la DMO a augmenté chez les patientes qui étaient passées d'EVENITY à l'alendronate par rapport aux patientes qui avaient continué à être traitées par alendronate jusqu'au mois 24 (voir tableau 3 et illustration 2).
Au bout de 12 mois de traitement, le romosozumab a augmenté la DMO au niveau du rachis lombaire par rapport aux valeurs de départ chez 98% des femmes post-ménopausées. 91% des femmes traitées par romosozumab ont obtenu une hausse d'au moins 5% de la DMO au niveau du rachis lombaire et 68% ont obtenu une hausse d'au moins 10% par rapport aux valeurs de départ en l'espace de 12 mois.
Les valeurs de départ d'âge et de DMO, ainsi que la région géographique n'ont eu aucune influence sur la hausse constante observée de la densité minérale osseuse (DMO) au niveau du rachis lombaire et de la hanche totale.
Tableau 3. Variation moyenne en pourcentage de la DMO entre le début de l'étude et les mois 12 et 24 chez des femmes post-ménopausées atteintes d'ostéoporose
|
|
Alendronate vs. Alendronate
Moyenne (IC à 95%)
N = 2047a
|
Romosozumab vs. Alendronate
Moyenne (IC à 95%)
N = 2046a
|
Différence entre les traitements pour l'Alendronate vs. Alendronate
| |
Après 12 mois
| |
Rachis lombaire
|
5,0 (4,73; 5,21)
|
13,7 (13,36; 13,99)
|
8,7b (8,31; 9,09)
| |
Hanche totale
|
2,8 (2,67; 3,02)
|
6,2 (5,94; 6,39)
|
3,3b (3,03; 3,60)
| |
Col du fémur
|
1,7 (1,46; 1,98)
|
4,9 (4,65; 5,23)
|
3,2b (2,90; 3,54)
| |
Après 24 mois
| |
Rachis lombaire
|
7,2 (6,90; 7,53)
|
15,3 (14,89; 15,69)
|
8,1b (7,58; 8,57)
| |
Hanche totale
|
3,5 (3,23; 3,68)
|
7,2 (6,95; 7,48)
|
3,8b (3,42; 4,10)
| |
Col du fémur
|
2,3 (1,96; 2,57)
|
6,0 (5,69; 6,37)
|
3,8b (3,40; 4,14)
|
a Nombre de femmes randomisées
b Valeur P <0,001 basée sur un modèle ANCOVA
Illustration 1. Modification en pourcentage de la DMO au niveau du rachis lombaire, de la hanche totale et du col du fémur à partir du début de l'étude, pendant 24 mois, chez des femmes post-ménopausées atteintes d'ostéoporose
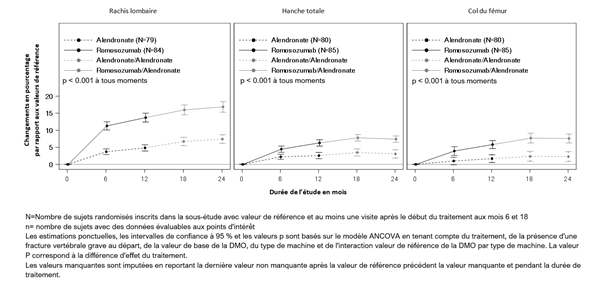
La différence significative obtenue au cours des 12 premiers mois en termes de densité minérale osseuse a perduré après le passage à l'aldendronate ou sa poursuite jusqu'au mois 36. Au mois 6, des différences entre les traitements ont été observées au niveau du rachis lombaire, de la hanche totale et du col du fémur.
Etude 20070337 (FRAME)
L'efficacité et la sécurité du romosozumab dans le traitement de l'ostéoporose chez la femme post-ménopausée ont été démontrées dans une étude à groupes parallèles multicentrique, internationale, randomisée, en double aveugle et contrôlée par placebo sur 7180 femmes post-ménopausées ayant entre 55 et 90 ans (âge moyen de 70,9 ans). 40,8% des femmes qui ont participé présentaient une ostéoporose sévère avec une fracture antérieure au départ.
Les femmes qui avaient un score T de densité minérale osseuse (DMO) ≤ -2,50 à > -3,5 au niveau de la hanche totale ou du col du fémur ont été incluses. Au début de l'étude, les scores T de DMO moyens étaient respectivement de -2,2, -2,47 et -2,75 au niveau du rachis lombaire, de la hanche totale et du col du fémur et 18,3% des femmes présentaient une fracture vertébrale au début de l'étude. Les femmes ont été randomisées pour recevoir un traitement de 12 mois en aveugle, soit par injections sous-cutanées de romosozumab, soit par placebo une fois par mois. Après la phase d'étude de 12 mois en double aveugle, les femmes sont passées à une étude ouverte, où 60 mg de dénosumab ont été administrés par voie sous-cutanée tous les 6 mois pendant une durée de 12 mois, tandis que le caractère aveugle du traitement de départ était maintenu. La dernière phase a été étendue à une étude ouverte de 12 mois supplémentaires sur le dénosumab. Les femmes ont reçu une supplémentation quotidienne en calcium et vitamine D.
Les co-critères d'évaluation principaux de l'efficacité étaient l'incidence des nouvelles fractures vertébrales jusqu'aux mois 12 et 24.
Effet sur les nouvelles fractures vertébrales, cliniques et non vertébrales
Le romosozumab a diminué significativement l'incidence des nouvelles fractures vertébrales jusqu'au mois 12 (p< 0,001), comme indiqué dans le tableau 4. En outre, chez les femmes qui avaient reçu du romosozumab la première année, le risque de fracture est resté réduit pendant toute la deuxième année lorsqu'elles sont passées du romosozumab au dénosumab par rapport à celles qui sont passées du placebo au dénosumab (mois 24; p < 0,001).
Le romosozumab a également réduit significativement l'incidence des fractures cliniques jusqu'au mois 12 (voir tableau 4). L'effet du romosozumab sur l'incidence et le risque de nouvelles fractures vertébrales, cliniques et non vertébrales jusqu'aux mois 12 et 24 est représenté dans le tableau 4.
Tableau 4. Effet du romosozumab sur l'incidence et le risque de nouvelles fractures vertébrales et cliniques et de nouvelles fractures non vertébrales jusqu'aux mois 12 et 24 chez des femmes post-ménopausées atteintes d'ostéoporose
|
|
Taux de femmes présentant une fracture
|
Réduction du risque absolu
(%) (IC à 95%)
|
Réduction du risque relatif
(%) (IC à 95%)
|
Valeur P nominale
|
Valeur P
ajustéea
| |
Placebo
(%)
|
Romosozumab
(%)
| |
Jusqu'au mois 12
| |
Nouvelle vertébraleb
|
59/3322 (1,8)
|
16/3321 (0,5)
|
1,30 (0,79; 1,80)
|
73 (53; 84)
|
< 0,001
|
< 0,001
| |
Cliniquec
|
90/3591 (2,5)
|
58/3589 (1,6)
|
1,2 (0,4; 1,9)
|
36 (11;54)
|
0,008
|
0,008
| |
Non vertébrale
|
75/3591 (2,1)
|
56/3589 (1,6)
|
0,8 (0,1; 1,4)
|
25 (−5; 47)
|
0,096
|
0,096
| |
|
Placebo vs. Dénosumab (%)
|
Romosozumab vs. Dénosumab (%)
|
| |
Jusqu'au mois 24
| |
Nouvelle vertébraleb
|
84/3327 (2,5)
|
21/3325 (0,6)
|
1,89 (1,30; 2,49)
|
75 (60; 84)
|
< 0,001
|
< 0,001
| |
Cliniquec,d
|
147/3591 (4,1)
|
99/3589 (2,8)
|
1,4 (0,5; 2,4)
|
33 (13; 48)
|
0,002
|
0,096
| |
Non vertébrale
|
129/3591 (3,6)
|
96/3589 (2,7)
|
1,0 (0,2; 1,9)
|
25 (3; 43)
|
0,029
|
0,057
|
a Les valeurs P ajustées reposent sur une procédure de test séquentielle et doivent être comparées avec un niveau de signification de 0,05.
b La réduction du risque absolu et du risque relatif repose sur la méthode de Mantel-Haenszel ajustée pour les facteur de stratification d'âge et de prévalence des fractures vertébrales. Les comparaisons entre les traitements reposent sur un modèle de régression logistique ajusté pour les facteurs de stratification.
c Toutes les fractures symptomatiques, y compris les fractures non vertébrales et vertébrales douloureuses, font partie des fractures cliniques. Les comparaisons entre les traitements reposent sur un modèle à risque proportionnel (régression de Cox) ajusté pour les facteurs de stratification d'âge et de prévalence des fractures vertébrales.
d Non significatif, car la signification statistique n'a pas été atteinte pour un critère d'évaluation qui se trouvait antérieurement dans la séquence de test; valeur-P nominale: 0,002.
Pour tous les types de fractures, la réduction du risque a été allongée jusqu'au mois 36.
Effet sur d'autres types/groupes de fractures
L'effet du romosozumab sur les autres types/groupes de fractures jusqu'au mois 24 est indiqué dans le tableau 5.
Tableau 5. Effet du romosozumab sur l'incidence et le risque d'autres types/groupes de fractures jusqu'aux mois 12 et 24 chez des femmes post-ménopausées atteintes d'ostéoporose
|
|
Taux de femmes présentant une fracture
|
Réduction du risque absolu
(%)
(IC à 95%)
|
Réduction du risque relatif
(%) (IC à 95%)
|
Valeur P nominalea
|
Valeur P
ajustée
| |
Placebo
(%)
|
Romosozumab (%)
| |
Jusqu'au mois 12
| |
Non vertébrale majeured
|
55/3591 (1,5)
|
37/3589 (1,0)
|
0,6
(0,1; 1,2)
|
33
(−2; 56)
|
0,060
|
0,096
| |
Vertébrale, nouvelle ou s'étant aggravée
|
59/3322 (1,8)
|
17/3321 (0,5)
|
1,3
(0,76; 1,77)
|
71
(51; 83)
|
< 0,001
|
0,096
| |
Hanche
|
13/3591 (0,4)
|
7/3589 (0,2)
|
0,3
(0,0; 0,6)
|
46
(-35; 78)
|
0,18
|
0,18
| |
Ostéoporotique majeuree
|
63/3591 (1,8)
|
38/3589 (1,1)
|
0,9
(0,3; 1,5)
|
40
(10; 60)
|
0,012
|
NAc
| |
Vertébrale, multiple, nouvelle/s'étant aggravée
|
9/3322 (0,3)
|
1/3321 (< 0,1)
|
0,24
(0,05; 0,43)
|
89
(13; 99)
|
0,011
|
NAc
| |
|
Placebo vs. Dénosumab
(%)
|
Romosozumab vs. Dénosumab
(%)
|
|
| |
Jusqu'au mois 24
| |
Non vertébrale majeured
|
101/3591 (2,8)
|
67/3589 (1,9)
|
1,1
(0,3; 1,8)
|
33
(9; 51)
|
0,009
|
0,096
| |
Vertébrale, nouvelle ou s'étant aggravée
|
84/3327 (2,5)
|
22/3325 (0,7)
|
1,86
(1,27; 2,46)
|
74
(58; 84)
|
< 0,001
|
0,096
| |
Hanche
|
22/3591 (0,6)
|
11/3589 (0,3)
|
0,4
(0,0; 0,7)
|
50
(-4; 76)
|
0,059
|
0,12
| |
Ostéoporotique majeuree
|
110/3591 (3,1)
|
68/3589 (1,9)
|
1,2
(0,5; 2,0)
|
38
(16; 54)
|
0,002
|
NAc
| |
Vertébrale, multiple, nouvelle/s'étant aggravée
|
17/3327 (0,5)
|
1/3325 (< 0,1)
|
0,48 (0,23; 0,73)
|
94
(56; 99)
|
< 0,001
|
NAc
|
a Les valeurs P nominales reposent sur un modèle de régression logistique (nouvelles fractures vertébrales ou fractures vertébrales s'aggravant et fractures vertébrales multiples nouvelles/s'aggravant) ou sur un modèle à risque proportionnel (régression de Cox) (fractures non vertébrales, non vertébrales majeures [major nonvertebral], de la hanche et ostéoporotiques majeures [major osteoporotic]) ajusté pour les facteurs de stratification d'âge et de prévalence des fractures vertébrales.
b Les valeurs P ajustées reposent sur une procédure de test séquentielle et doivent être comparées avec un niveau de signification de 0,05.
c NA: Le critère d'évaluation ne faisant pas partie du test séquentiel, l'ajustement de la valeur P n'est pas applicable.
d Bassin, fémur distal, tibia proximal, côtes, haut du bras proximal, avant-bras et hanche
e Fractures vertébrales cliniques et fractures de la hanche, de l'avant-bras et du haut du bras
Effet sur la densité minérale osseuse (DMO)
Chez les femmes post-ménopausées atteintes d'ostéoporose, le romosozumab a entraîné une hausse significative de la densité minérale osseuse au niveau du rachis lombaire, de la hanche totale et du col du fémur au bout de 6 et 12 mois par rapport au placebo (tableau 6). Au bout de 12 mois de traitement, le romosozumab a augmenté la DMO au niveau du rachis lombaire par rapport aux valeurs de départ chez 99% des femmes post-ménopausées. 92% des femmes traitées par romosozumab ont obtenu une hausse d'au moins 5% de la DMO au niveau du rachis lombaire et 68% ont obtenu une hausse d'au moins 10% par rapport aux valeurs de départ en l'espace de 12 mois. Cet effet a perduré après le passage à un autre traitement de l'ostéoporose: Suite au passage du romosozumab au dénosumab, la DMO a continué à augmenter jusqu'au mois 24. Chez les patientes qui sont passées du placebo au dénosumab, la DMO a également augmenté sous dénosumab. Chez les femmes qui ont reçu du romosozumab puis du dénosumab, la hausse de la DMO au niveau du rachis lombaire, de la hanche totale et du col du fémur était plus importante au bout de 24 mois que chez celles qui ont reçu un placebo puis du dénosumab (tableau 6). La modification en pourcentage de la DMO au niveau du rachis lombaire, de la hanche totale et du col du fémur à partir du début de l'étude et pendant une durée de 24 mois est représentée dans l'illustration 4.
Les valeurs de départ d'âge et de DMO, ainsi que la région géographique n'ont eu aucune influence sur la hausse constante observée de la densité minérale osseuse (DMO) au niveau du rachis lombaire et de la hanche totale.
Tableau 6. Variation moyenne en pourcentage de la DMO entre le début de l'étude et les mois 12 et 24 chez des femmes post-ménopausées atteintes d'ostéoporose
|
|
Placebo
Moyenne (IC à 95%)
N = 3591a
|
Placebo
Moyenne (IC à 95%)
N = 3589a
|
Différence entre les traitements vs. Placebo
Moyenne (IC à 95%)
| |
Après 12 mois
| |
Rachis lombaire
|
0,4 (0,2; 0,5)
|
13,1 (12,8; 13,3)
|
12,7b (12,4; 12,9)
| |
Hanche totale
|
0,3 (0,1; 0,4)
|
6,0 (5,9; 6,2)
|
5,8b (5,6; 6,0)
| |
Col du fémur
|
0,3 (0,1; 0,5)
|
5,5 (5,2; 5,7)
|
5,2b (4,9; 5,4)
| |
|
Placebo vs. Dénosumab
Moyenne (IC à 95%)
N = 3591 a
|
Romosozumab vs. Dénosumab
Moyenne (IC à 95%)
N = 3589 a
|
Différence entre les traitements pour le placebo vs. Dénosumab
| |
Après 24 mois
| |
Rachis lombaire
|
5,5 (5,3; 5,7)
|
16,6 (16,3; 16,8)
|
11,1b (10,8; 11,4)
| |
Hanche totale
|
3,2 (3,1; 3,3)
|
8,5 (8,3; 8,7)
|
5,3b (5,1; 5,5)
| |
Col du fémur
|
2,3 (2,1; 2,6)
|
7,3 (7,0; 7,5)
|
4,9b (4,7; 5,2)
|
a Nombre de femmes randomisées
b Valeur P <0,001 basée sur un modèle ANCOVA
Illustration 2. Modification en pourcentage de la DMO au niveau du rachis lombaire, de la hanche totale et du col du fémur à partir du début de l'étude, pendant la durée de 24 mois, chez des femmes post-ménopausées atteintes d'ostéoporose
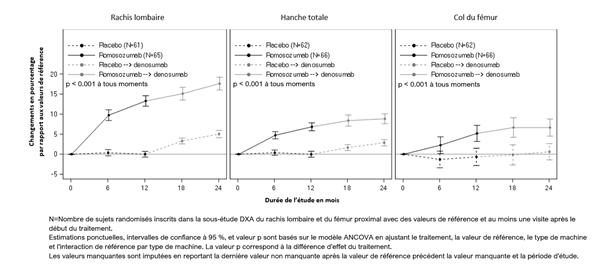
La différence significative obtenue au cours des 12 premiers mois en termes de densité minérale osseuse a perduré jusqu'au mois 36 après le passage au dénosumab.
Histologie osseuse et histomorphométrie
Au total, 139 femmes post-ménopausées atteintes d'ostéoporose se sont prêtées à 154 biopsies osseuses transiliaques au bout de 2, 12 et/ou 24 mois. Parmi les biopsies prélevées, 154 (100,0%) convenaient pour une analyse histologique qualitative et 138 (89,6%) pour une analyse histomorphométrique complète. Les analyses histologiques qualitatives des échantillons des femmes traitées par romosozumab ont démontré une architecture et une qualité osseuses normales à tous les points temporels. Il n'y a pas eu de signes d'os fibreux, de défauts de minéralisation ni de fibroses médullaires.
L'effet du romosozumab par rapport au placebo a été analysé par histomorphométrie sur des biopsies prélevées au bout de 2 et 12 mois. Chez les femmes traitées par romosozumab, les indices histomorphométriques ont montré une hausse de l'ossification et une baisse de la résorption osseuse au bout de 2 mois. Au bout de 12 mois, les indices indiquaient à la fois une diminution de l'ossification et de la résorption sous romosozumab, tandis que les volumes osseux et la densité trabéculaire augmentaient.
Femmes en transition d'une thérapie par bisphosphonates
Etude 20080289 (STRUCTURE)
Pour évaluer la sécurité et l'efficacité du romosozumab chez la femme post-ménopausée atteinte d'ostéoporose en transition d'un traitement par bisphosphonates, une étude multicentrique, randomisée et ouverte a été menée sur 436 femmes post-ménopausées ayant entre 56 et 90 ans (âge moyen de 71,5 ans). Dans cette étude, la sécurité et les évolutions de la DMO ont été évaluées par absorptiométrie biphotonique à rayons X (DXA) au bout de 12 mois de traitement par romosozumab par rapport à un traitement de 12 mois par tériparatide. L'étude a également porté sur la densité osseuse de la hanche pendant 12 mois, selon la méthode des éléments finis (FEM), en utilisant l'imagerie qualitative par tomodensitométrie.
Pour être incluses, les femmes devaient remplir les critères suivants au début de l'étude: score DMO-T ≤ -2,50 au niveau du rachis lombaire, de la hanche totale ou du col du fémur et anamnèse de fractures non vertébrales après l'âge de 50 ans ou de fractures vertébrales à un moment donné. Au début de l'étude, les scores DMO-T moyens étaient respectivement de -2,85, -2,24 et -2,46 au niveau du rachis lombaire, de la hanche totale et du col du fémur.
Au bout de 12 mois, la DMO atteinte sous romosozumab était 9,8% plus élevée que la valeur de départ au niveau du rachis lombaire (IC à 95%: 9,0; 10,5), 2,9% au niveau de la hanche totale (IC à 95%: 2,5; 3,4) et 3,2% au niveau du col du fémur (IC à 95%: 2,6; 3,8). Par rapport au tériparatide, les différences entre les traitements en termes de DMO au bout de 12 mois atteignaient 4,4% (IC à 95%: 3,4; 5,4) au niveau du rachis lombaire, 3,4% (IC à 95%: 2,8; 4,0) au niveau de la hanche totale et 3,4% au niveau du col du fémur (IC à 95%: 2,6; 4,2; valeur p < 0,0001 pour toutes les comparaisons). Des différences entre les traitements ont été observées au bout de 6 mois seulement.
Au bout de 12 mois, la densité osseuse estimée sous rosomozumab était 2.5% plus élevée que la valeur de départ au niveau de la hanche totale (IC à 95%: 1,7; 3,2). Par rapport au tériparatide, la différence entre les traitements en termes de densité osseuse estimée au niveau de la hanche totale au bout de 12 mois atteignait 3.2% (IC à 95%: 2,1; 4,3; valeur p < 0,0001). Les effets indésirables observés dans cette étude correspondaient généralement à ceux constatés chez les femmes qui n'avaient pas pris antérieurement de traitement par bisphosphonates (voir Effets indésirables).
|


