CompositionPrincipes actifs
Saxagliptine sous forme de chlorhydrate de saxagliptine, metformine sous forme de chlorhydrate de metformine.
Excipients
Kombiglyze XR 5 mg/500 mg: carmellose sodique (E466) équivalent à max. 4,75 mg de sodium, hypromellose (E464), stéarate de magnésium (E470b), cellulose microcristalline (E460i), poly(alcool vinylique) (E1203), dioxyde de titane (E171), macrogol 3350, talc (E553b), acide chlorhydrique, oxyde de fer rouge et jaune (E172), encre d'impression: gommes laques, indigotine (E132).
Kombiglyze XR 5 mg/1000 mg: carmellose sodique (E466) équivalent à max. 4,75 mg de sodium, hypromellose (E464), stéarate de magnésium (E470b), poly(alcool vinylique) (E1203), dioxyde de titane (E171), macrogol 3350, talc (E553b), acide chlorhydrique, oxyde de fer rouge (E172), encre d'impression: gommes laques, indigotine (E132).
Kombiglyze XR 2,5 mg/1000 mg: carmellose sodique (E466) équivalent à max. 4,75 mg de sodium, hypromellose (E464), stéarate de magnésium (E470b), poly(alcool vinylique) (E1203), dioxyde de titane (E171), macrogol 3350, talc (E553b), acide chlorhydrique, oxyde de fer jaune (E172), encre d'impression: gommes laques, indigotine (E132).
Forme pharmaceutique et quantité de principe actif par unitéComprimé à libération modifiée:
5 mg de saxagliptine et 500 mg de chlorhydrate de metformine ou
5 mg de saxagliptine et 1000 mg de chlorhydrate de metformine ou
2,5 mg de saxagliptine et 1000 mg de chlorhydrate de metformine.
Indications/Possibilités d’emploiKombiglyze XR est indiqué en plus d'un régime alimentaire et d'un exercice physique permettant d'améliorer le contrôle de la glycémie chez les patients adultes atteints de diabète de type 2 pour lesquels la metformine seule, à la dose maximale qu'ils tolèrent, ne suffit pas à un contrôle satisfaisant de la glycémie, ou qui sont déjà traités par une association de saxagliptine et de metformine administrées séparément.
Traitement adjuvant associé
Kombiglyze XR en association avec l'insuline est indiqué en cas de diabète de type 2 lorsque l'une des monothérapies, en plus d'un régime alimentaire et d'exercice physique accru, ne permet pas un contrôle suffisant de la glycémie.
Kombiglyze XR en association avec une sulfonylurée est indiqué en cas de diabète de type 2 lorsque la metformine et la sulfonylurée (en bithérapie orale à la dose maximale tolérée), en plus d'un régime alimentaire et d'exercice physique accru, ne permettent pas un contrôle suffisant de la glycémie.
Posologie/Mode d’emploiLa posologie de Kombiglyze XR se détermine de cas en cas en fonction du régime thérapeutique en cours ainsi que de l'efficacité et de la tolérance au traitement.
Chez les patients qui étaient traités jusque-là avec la metformine seule, on choisira une posologie de Kombiglyze XR apportant une dose journalière de metformine identique à la dose journalière de metformine administrée jusque-là ou aussi proche que possible de cette dose.
La dose de saxagliptine est déterminée individuellement.
La dose maximale de Kombiglyze XR est de 5 mg de saxagliptine/2000 mg de metformine à libération retardée; dans ce cas, la prise est de deux comprimés à 2,5 mg/1000 mg.
En principe, Kombiglyze XR est pris une fois par jour, avec le repas du soir.
Pour les patients insuffisamment contrôlés par une bithérapie associant de l'insuline et de la metformine ou pour les patients sous trithérapie associant de l'insuline à de la metformine et de la saxagliptine sous forme de comprimés séparés
La dose de saxagliptine est déterminée individuellement. Les comprimés pelliculés de Kombiglyze XR sont choisis selon la dose de metformine administrée jusque-là ou à une dose aussi proche que possible de celle-ci. Kombiglyze XR est pris une fois par jour avec le repas du soir. Si la dose journalière de metformine est de 2000 mg, la prise est de deux comprimés à 2,5 mg de saxagliptine/1000 mg de metformine XR le soir.
Lorsque Kombiglyze XR est utilisé en association avec de l'insuline, une dose plus faible d'insuline peut être initialement requise pour diminuer le risque d'hypoglycémie (voir "Mises en garde et précautions" ).
Pour les patients insuffisamment contrôlés par une bithérapie associant une sulfonylurée et la metformine ou pour les patients sous trithérapie associant la metformine et une sulfonylurée à la saxagliptine sous forme de comprimés séparés
La dose de saxagliptine est déterminée individuellement. Les comprimés pelliculés de Kombiglyze XR sont choisis selon la dose de metformine administrée jusque-là ou à une dose aussi proche que possible de celle-ci. Kombiglyze XR est pris une fois par jour avec le repas du soir. Si la dose journalière de metformine est de 2000 mg, la prise est de deux comprimés à 2,5 mg de saxagliptine/1000 mg de metformine XR le soir.
Lorsque Kombiglyze XR est utilisé en association avec une sulfonylurée, une dose plus faible de sulfonylurée peut être requise pour diminuer le risque d'hypoglycémie (voir "Mises en garde et précautions" ).
Chez les patients atteints de diabète de type 2, les modifications de traitement doivent toujours se faire avec prudence et sous surveillance adéquate, en raison d'éventuelles perturbations du contrôle glycémique. Ceci s'applique également lors d'un passage des comprimés de metformine à libération rapide à des comprimés à libération retardée, comme par exemple Kombiglyze XR, et lors d'une modification de l'horaire d'administration, par exemple prise de la saxagliptine le soir à la place du matin, notamment lorsque le traitement comprend de l'insuline ou une sulfonylurée.
Les patients doivent être instruits que les comprimés de Kombiglyze XR s'avalent sans être mâchés et ne doivent être ni broyés ni divisés. Occasionnellement, les composants non actifs de Kombiglyze XR sont éliminés dans les selles sous forme de masse gonflée dont l'aspect ressemble à celui du comprimé original.
Patients présentant des troubles de la fonction rénale
La fonction rénale doit être examinée avant le début du traitement par Kombiglyze XR et, ensuite, régulièrement (voir "Mises en garde et précautions" et "Propriétés pharmacocinétiques" ).
Patients atteints d'insuffisance rénale légère
Aucun ajustement de la dose n'est nécessaire pour les patients atteints d'insuffisance rénale légère (TFGe de 60–89 ml/min/1,73 m2, conformément à l'équation du TFGe pour le régime alimentaire modifié en cas d'affection rénale [Modified Diet in Renal Disease, MDRD]).
Patients atteints d'insuffisance rénale moyennement sévère
Un ajustement de la dose est nécessaire chez les patients atteints d'insuffisance rénale moyennement sévère 3a (TFGe de 45-59 ml/min/1,73 m2) et la posologie doit être limitée à 5 mg/1000 mg une fois par jour au maximum.
L'instauration d'un traitement par Kombiglyze XR n'est pas recommandée chez les patients présentant un TFGe de <45 ml/min/1,73 m2. Lorsque le TFGe baisse en permanence à des valeurs inférieures à 45 ml/min/1,73 m2 pendant le traitement, le bénéfice et le risque de la poursuite du traitement doivent être évalués et la dose maximale de Kombiglyze XR doit être limitée à 2,5 mg/1000 mg une fois par jour (voir "Mises en garde et précautions" ).
Patients atteints d'insuffisance rénale sévère
Kombiglyze XR ne doit pas être utilisé chez les patients atteints d'insuffisance rénale sévère (TFGe de <30 ml/min/1,73 m2) (voir "Contre-indications" , "Mises en garde et précautions" et "Pharmacocinétique" ).
Patients présentant des troubles de la fonction hépatique
Kombiglyze XR ne doit pas être utilisé chez les patients présentant une insuffisance hépatique (voir "Contre-indications" , "Mises en garde et précautions" et "Pharmacocinétique" ).
Patients âgés
La metformine et la saxagliptine étant éliminées par voie rénale, la prudence est de rigueur lors de l'utilisation de Kombiglyze XR chez des patients âgés. Une surveillance de la fonction rénale est nécessaire pour prévenir une acidose lactique due à la metformine, en particulier chez les sujets âgés (voir "Contre-indications" et "Mises en garde et précautions" ). On ne dispose que d'une expérience très limitée concernant l'utilisation de saxagliptine chez les patients de 75 ans ou plus âgés. La prudence est donc de rigueur en cas de traitement de ce groupe de patients (voir "Mises en garde et précautions" et "Pharmacocinétique" ).
Enfants et adolescents
La sécurité et l'efficacité de Kombiglyze XR n'ont pas été démontrées à ce jour chez des enfants ou des adolescents de moins de 18 ans. Par conséquent, Kombiglyze XR ne doit pas être utilisé chez les enfants ou adolescents de moins de 18 ans.
Contre-indicationsKombiglyze XR est contre-indiqué chez les patients en cas de:
-Hypersensibilité à l'un des deux principes actifs, aux deux ou à l'un des excipients de ce médicament;
-Acidocétose diabétique, précoma diabétique;
-Insuffisance rénale sévère (TFGe de <30 ml/min/1,73 m2) (voir "Mises en garde et précautions" );
-État clinique aigu susceptible d'altérer la fonction rénale tel que:
-Déshydratation
-Infection sévère
-Choc
-Administration intravasculaire de produits de contraste iodés (voir "Mises en garde et précautions" )
-Maladie aiguë ou chronique pouvant provoquer une hypoxie tissulaire telles que:
-Insuffisance cardiaque ou respiratoire
-Infarctus du myocarde survenu récemment
-Choc
-Insuffisance hépatique (voir "Posologie/Mode d'emploi" , "Mises en garde et précautions" et "Pharmacocinétique" );
-Intoxication éthylique aiguë, alcoolisme;
Mises en garde et précautionsÀ ce jour, aucune étude spécifique sur la sécurité et l'efficacité de Kombiglyze XR n'a été menée chez des patients qui avaient passé d'un précédent traitement avec d'autres antidiabétiques oraux, y compris la metformine à libération non retardée, à Kombiglyze XR.
Généralités
Kombiglyze XR ne doit pas être utilisé chez les patients souffrant d'un diabète de type 1 ou pour le traitement de l'acidocétose diabétique. L'utilisation de Kombiglyze XR en association avec l'insuline n'a pas été étudiée.
Kombiglyze XR n'est pas un substitut à l'insuline chez les patients requérant de l'insuline.
Acidose lactique
L'acidose lactique est une complication métabolique très rare mais sérieuse (mortalité élevée en l'absence d'un traitement immédiat) qui peut survenir lors d'une accumulation de metformine, l'un des composants de Kombiglyze XR. Les cas d'acidose lactique rapportés chez des patients sous metformine concernaient surtout des patients diabétiques présentant une insuffisance rénale très importante. L'incidence de l'acidose lactique peut être réduite par l'évaluation d'autres facteurs de risque tels que diabète mal contrôlé, cétose, carence alimentaire prolongée, consommation d'alcool excessive, insuffisance hépatique, déshydratation et tout état accompagné d'hypoxie ou entravant la fonction rénale.
Les patients et/ou les soignants doivent être informés sur le risque d'une acidose lactique. L'acidose lactique est caractérisée par des symptômes tels que dyspnée acidosique, douleurs abdominales et hypothermie, suivies d'un coma. Les analyses de laboratoire révèlent un pH sanguin réduit, un taux plasmatique de lactate supérieur à 5 mmol/l, un trou anionique augmenté et une valeur accrue du quotient lactates/pyruvates. En cas de suspicion d'acidose métabolique, le traitement par Kombiglyze XR doit être arrêté et le patient hospitalisé immédiatement (voir "Surdosage" ). Les symptômes précurseurs sont peu spécifiques; ils peuvent inclure des crampes musculaires accompagnées de symptômes gastro-intestinaux, de douleurs abdominales, d'une fréquence respiratoire accrue et d'une grande faiblesse. Ces symptômes doivent être pris au sérieux par le médecin traitant. De plus, le médecin doit informer les patients des signes possibles d'une acidose lactique.
Fonction rénale
Étant donné que la metformine est éliminée par les reins et que le risque d'une accumulation de metformine et d'une acidose lactique augmente avec l'augmentation du degré d'atteinte de la fonction rénale, la fonction rénale doit être examinée avant l'instauration du traitement par Kombiglyze XR et, ensuite, régulièrement:
au moins une fois par an chez les patients présentant une fonction rénale normale,
au moins tous les 3 à 6 mois chez les patients présentant un TFGe atteignant la limite inférieure du domaine normal, resp. entre 45 et 59 ml/min/1,73 m2 ainsi que chez les patients âgés,
au moins tous les 3 mois chez les patients présentant un TFGe entre 30 et 44 ml/min/1,73 m2.
L'instauration d'un traitement par Kombiglyze XR n'est pas recommandée chez les patients présentant un TFGe de <45 ml/min/1,73 m2.
Lorsque le TFGe baisse en permanence à des valeurs inférieures à 45 ml/min/1,73 m2 pendant le traitement, le bénéfice et le risque de la poursuite du traitement doivent être évalués et la dose maximale de Kombiglyze XR doit être limitée à 2,5 mg/1000 mg une fois par jour.
Chez les patients âgés, une réduction de la fonction rénale est fréquente et généralement sans symptôme. Une prudence particulière s'impose dans les situations faisant craindre une détérioration de la fonction rénale, par exemple lors de l'instauration d'un traitement antihypertenseur ou diurétique, ou lors d'un traitement avec un antiinflammatoire non stéroïdien (AINS).
Kombiglyze XR est contre-indiqué chez les patients atteints d'insuffisance rénale sévère (TFGe de <30 ml/min/1,73 m2) (voir "Contre-indications" ).
Affections aiguës associées à l'hypoxie ou à l'atteinte de la fonction rénale
Le collapsus cardiovasculaire (choc), l'insuffisance cardiaque congestive aiguë, l'infarctus du myocarde aigu et d'autres affections caractérisées par l'hypoxémie ont été associées à l'acidose lactique et peuvent provoquer en outre une azotémie pré-rénale. Des états aigus tels que la déshydratation, les infections graves et l'hypoperfusion peuvent porter atteinte à la fonction rénale. Dans ces situations, la metformine doit être arrêtée.
Insuffisance cardiaque
Dans l'étude SAVOR, une augmentation du taux d'hospitalisation pour insuffisance cardiaque a été observée dans le groupe des patients traités par la saxagliptine comparé au groupe placebo, bien qu'une relation de causalité n'ait pas été établie. La prudence est recommandée lorsque Kombiglyze XR est utilisé chez des patients qui ont des facteurs de risque connus d'hospitalisation pour insuffisance cardiaque, tel qu'un antécédent d'insuffisance cardiaque ou d'insuffisance rénale modérée à sévère. Les patients doivent être informés des symptômes caractéristiques d'une insuffisance cardiaque et signaler immédiatement de tels symptômes (voir "Propriétés/Effets" ).
Arthralgie
Des cas de douleurs articulaires, parfois sévères, ont été rapportés en post-commercialisation pour les inhibiteurs de la DPP4. L'arrêt du médicament a entraîné une amélioration des symptômes. Chez certains patients, les symptômes sont réapparus à la reprise du traitement par le même ou par un autre inhibiteur de la DPP4. Les symptômes peuvent survenir soit peu après le début du traitement, soit après une durée de traitement plus longue. Si un patient présente une douleur articulaire sévère, la poursuite du traitement par le médicament doit être évaluée pour chaque cas (voir "Effets indésirables" ).
Interventions chirurgicales
Kombiglyze XR contenant de la metformine, le traitement doit être suspendu 48 heures avant une intervention chirurgicale élective avec anesthésie générale, spinale ou épidurale. L'administration de Kombiglyze XR ne doit normalement pas être reprise avant 48 heures après l'intervention, et cela seulement si un nouveau contrôle montre que la fonction rénale est normale.
Administration de produits de contraste iodés
L'administration intravasculaire de produits de contraste iodés pour des examens radiologiques peut entraîner une insuffisance rénale. Chez des patients sous metformine, cette insuffisance rénale était associée à une acidose lactique. L'administration de Kombiglyze XR doit donc être arrêtée avant ou au moment de l'examen et ne pas être reprise avant 48 heures après l'examen, et cela seulement si un nouveau contrôle montre que la fonction rénale est normale (voir "Interactions" ).
Pemphigoide bulleuse
Après commercialisation, des cas de pemphigoïde bulleuse ont été rapportés chez des patients traités par un inhibiteur de la DPP-4. Les patients doivent être informés qu'ils doivent contacter leur médecin en cas d'apparition de bulles (cloques) ou d'érosions cutanées pendant le traitement par Kombiglyze XR. En cas de suspicion de pemphigoïde bulleuse, le traitement par Kombiglyze XR devrait être arrêté.
Maladies de peau
Dans les études toxicologiques non cliniques sur la saxagliptine, des lésions cutanées ulcéro-nécrotiques ont été rapportées chez des singes au niveau des extrémités (voir "Données précliniques" ). Bien qu'aucune augmentation de l'incidence des lésions cutanées n'ait été observée dans les études cliniques, l'expérience dont on dispose chez les patients présentant des complications cutanées diabétiques sont limitées. Des cas d'éruptions cutanées ont été rapportés post-commercialisation en rapport avec des médicaments appartenant à la classe des inhibiteurs de la DPP-4. Les éruptions cutanées font aussi partie des effets indésirables possibles de la saxagliptine (voir "Effets indésirables" ). On surveillera donc l'apparition éventuelle d'affections cutanées telles que des vésicules, des ulcérations ou une éruption cutanée, comme indiqué dans la prise en charge habituelle des patients diabétiques.
Réactions d'hypersensibilité
Kombiglyze XR contenant de la saxagliptine et de la metformine, il ne doit pas être utilisé chez les patients ayant déjà eu par le passé une réaction sévère d'hypersensibilité à la saxagliptine ou à la metformine.
Si une réaction sévère d'hypersensibilité est suspectée, il faut interrompre l'administration de Kombiglyze XR, évaluer les autres causes possibles d'une telle réaction et commencer un autre traitement antidiabétique. Comme on ne peut pas exclure avec certitude une réaction croisée avec d'autres inhibiteurs de la DPP-4, Kombiglyze XR ne doit pas être utilisé par les patients ayant déjà subi une réaction sévère d'hypersensibilité à un autre inhibiteur de la DPP-4.
Pancréatite
Dans le cadre de l'expérience post-commercialisation sur la saxagliptine, des cas spontanés de pancréatite aiguë ont été rapportés. Les patients seront informés des symptômes caractéristiques d'une pancréatite aiguë: douleurs abdominales sévères et persistantes. Au cas où une pancréatite serait supposée, on arrêtera le traitement par Kombiglyze XR.
Modification de l'état clinique chez les patients dont le diabète de type 2 était contrôlé auparavant
Kombiglyze XR contenant de la metformine, il faut rechercher immédiatement des signes d'acidocétose ou d'acidose lactique chez les patients diabétiques de type 2 précédemment bien contrôlés sous Kombiglyze XR qui développent des valeurs de laboratoire anormales ou des symptômes cliniques (en particulier des symptômes vagues et peu spécifiques). Les investigations doivent inclure les taux sériques d'électrolytes et des corps cétoniques, la glycémie et – si indiqué – le pH sanguin et les taux de lactates et de pyruvates. En présence d'une acidose de quelque forme que ce soit, il faut arrêter immédiatement l'administration de Kombiglyze XR et initier d'autres mesures médicales appropriées.
Patients âgés
L'expérience concernant l'utilisation de saxagliptine chez les patients de 75 ans ou plus âgés est très limitée. La prudence est donc de rigueur lors du traitement de ce groupe de patients (voir "Pharmacocinétique" )
Utilisation avec des inducteurs puissants du CYP3A4
L'utilisation d'inducteurs du CYP3A4 comme la carbamazépine, la dexaméthasone, le phénobarbital, la phénytoïne et la rifampicine peut réduire l'effet hypoglycémiant de la saxagliptine (voir "Interactions" ).
Utilisation avec des médicaments connus pour entraîner une hypoglycémie
Les antidiabétiques comme l'insuline et les sulfonylurées sont connus pour entraîner des hypoglycémies. C'est pourquoi une réduction de la dose d'insuline ou de sulfonylurée peut être nécessaire afin de diminuer le risque d'hypoglycémie, lors d'une utilisation en association à Kombiglyze XR.
Chez les patients atteints de diabète de type 2, les modifications de traitement doivent toujours se faire avec prudence et sous surveillance adéquate, en raison d'éventuelles perturbations du contrôle glycémique. Ceci s'applique également lors d'un passage des comprimés de metformine à libération rapide à des comprimés à libération retardée, comme par exemple Kombiglyze XR, et lors d'une modification de l'horaire d'administration, par exemple prise de la saxagliptine le soir à la place du matin, notamment lorsque le traitement comprend de l'insuline ou une sulfonylurée.
Myopathie/Rhabdomyolyse
Des cas de myopathie ont été rapportés dans le cadre de la prise de Kombiglyze XR et se manifestaient sous forme de douleurs musculaires, de faiblesse musculaire ou de sensibilité anormale des muscles, associées à une forte élévation de la créatine kinase (CK, dix fois la limite supérieure de la normale). Une myopathie peut parfois survenir sous forme d'une rhabdomyolyse associée ou non à une insuffisance rénale aiguë due à une myoglobinurie, avec une issue fatale dans de rares cas.
Kombiglyze XR doit être prescrit avec prudence chez les patients avec facteurs de prédisposition à la rhabdomyolyse. Le taux de créatine kinase doit être mesuré avant le début du traitement dans les situations suivantes:
-Atteinte de la fonction rénale
-Hypothyroïdie non contrôlée
-Antécédents personnels ou familiaux de troubles musculaires héréditaires
-Antécédents de toxicité musculaire avec des statines ou des fibrates
-Alcoolisme
-Personnes âgées (≥65 ans): la nécessité d'une telle mesure doit être évaluée en présence d'autres facteurs de prédisposition à la rhabdomyolyse
-Personnes de sexe féminin
Dans de telles situations, il convient d'évaluer le rapport bénéfice/risque du traitement.
Diminution de la vitamine B12/Carence en vitamine B12
Chlorhydrate de metformine
La metformine peut induire une diminution des taux sériques de vitamine B12. Le risque de diminution des taux de vitamine B12 augmente avec l'élévation de la dose de metformine, avec la prolongation de la durée du traitement et/ou chez les patients présentant des facteurs de risque connus de développement d'une carence en vitamine B12. En cas de suspicion de carence en vitamine B12 (par exemple en cas de survenue d'une anémie ou d'une neuropathie), le taux de vitamine B12 doit être surveillé. Des contrôles réguliers du taux de vitamine B12 peuvent être nécessaires chez les patients présentant des facteurs de risque de carence en vitamine B12. Le traitement par la metformine doit être poursuivi aussi longtemps qu'il est toléré et qu'il n'est pas contre-indiqué; en outre, un traitement correcteur adapté de la carence en vitamine B12 correspondant aux directives cliniques actuelles doit être doit être mis en œuvre.
Autres mesures de précaution
En principe, Kombiglyze XR doit être pris avec le repas du soir. Lors d'une prise en même temps que le repas, les effets secondaires gastro-intestinaux de la metformine peuvent être en partie réduits. Il faut en outre s'attendre à ce que la biodisponibilité de la metformine à libération retardée soit diminuée lors d'une prise à jeun. Cela pourrait rendre plus difficile le contrôle du diabète. Il faut tenir compte du fait que la biodisponibilité de la metformine à libération normale, c'est-à-dire non retardée, est réduite par la prise simultanée de nourriture - contrairement à ce qui se passe avec la metformine à libération retardée (voir ci-dessus).
Ce médicament contient moins de 1 mmol (23 mg) de sodium par comprimé pelliculé, c.-à-d. qu'il est essentiellement "sans sodium" .
InteractionsInteractions pharmacocinétiques
Aucune modification significative de la pharmacocinétique de la saxagliptine ou de la metformine n'a été observée chez des patients diabétiques de type 2 lors d'une co-administration de doses répétées de saxagliptine (2,5 mg deux fois par jour) et de metformine (1000 mg deux fois par jour).
Aucune étude d'interaction formelle n'a été conduite avec Kombiglyze XR. Les informations suivantes reposent sur les données disponibles des monosubstances.
Saxagliptine
Le métabolisme de la saxagliptine est principalement médié par le cytochrome P450 3A4/5 (CYP3A4/5). Au cours d'études in vitro, la saxagliptine et son principal métabolite n'ont pas eu d'effet inhibiteur sur le CYP1A2, 2A6, 2B6, 2C8, 2C9, 2C19, 2D6, 2E1 ou 3A4 ou d'effet inducteur sur le CYP1A2, 2B6, 2C9 ou 3A4. La saxagliptine est un substrat de la glycoprotéine P (P-gp), mais elle n'est pas un inhibiteur ou un inducteur significatif de la P-gp.
Effets de la saxagliptine sur d'autres médicaments
La saxagliptine n'a pas d'influence significative sur la pharmacocinétique de la metformine, du glibenclamide, de la pioglitazone, de la digoxine, de la simvastatine, du diltiazem, du kétoconazole ou des contraceptifs oraux de type œstroprogestatif (étudié pour une association d'éthinylestradiol et de norgestimate).
Effets d'autres médicaments sur saxagliptine
Dans des études cliniques réalisées auprès de volontaires sains, la pharmacocinétique de la saxagliptine et de son principal métabolite ainsi que l'exposition totale aux formes actives de la saxagliptine (substance mère et métabolite) n'a pas été modifiée de manière significative par la metformine, le glibenclamide, la pioglitazone, la digoxine, la simvastatine, l'oméprazole ou une association d'hydroxyde d'aluminium + hydroxyde de magnésium + siméticone ou famotidine.
Le kétoconazole et le diltiazem – des inhibiteurs du CYP3A4/5 – ont augmenté jusqu'à 2,5 fois l'exposition à la saxagliptine et réduit d'un pourcentage allant jusqu'à 88% l'exposition au métabolite actif. L'exposition à la totalité des formes actives de la saxagliptine n'a pas été influencée de façon significative par ces inhibiteurs du CYP3A4/5 (augmentation <22%).
La rifampicine – un inducteur du CYP3A4/5 – a réduit l'exposition à la saxagliptine de 76% et n'a pas eu d'influence significative sur l'exposition au métabolite actif. Les effets sur l'exposition à la totalité des formes actives de la saxagliptine ont été faibles, tout comme les effets sur l'activité plasmatique de la DPP-4 dans l'intervalle de dosage (réduction de 26% et de 6% respectivement). Aucun ajustement de la dose n'est nécessaire lors d'une administration de rifampicine en association avec la saxagliptine.
Les effets d'inducteurs du CYP3A4/5 sur la pharmacocinétique de la saxagliptine n'ont pas été étudiés. L'administration concomitante de saxagliptine et d'inducteurs du CYP3A4/5 tels que la carbamazépine, la dexaméthasone, le phénobarbital et la phénytoïne peut cependant entraîner une diminution des concentrations plasmatiques de saxagliptine et une augmentation des concentrations de son métabolite principal.
Les effets du tabagisme, du régime alimentaire, de produits de phytothérapie ou de l'alcool sur la pharmacocinétique de la saxagliptine n'ont pas été spécifiquement étudiés.
Metformine
Lorsque les médicaments nommés ci-après sont utilisés pendant un traitement par metformine ainsi qu'en cas d'arrêt de leur administration, la glycémie doit être surveillée de près. Les patients doivent être informés en conséquence. Si nécessaire, la dose du traitement hypoglycémiant doit être ajustée pendant la co-administration.
Interactions influençant les effets de la metformine
Réduction des effets hypoglycémiants
Les glucocorticoïdes (en utilisation systémique ou locale), les bêta-2 agonistes, les diurétiques, les phénothiazines (par exemple chlorpromazine), les hormones thyroïdiennes, les œstrogènes, les contraceptifs oraux, les médicaments utilisés dans les traitements hormonaux substitutifs, la phénytoïne, l'acide nicotinique, les inhibiteurs calciques, l'isoniazide et le tétracosactide peuvent faire augmenter la glycémie.
Augmentation des effets hypoglycémiants
Le furosémide provoque une augmentation de la concentration plasmatique de metformine (augmentation de la Cmax de 22% et de l'AUC de 15%) sans influencer significativement la clairance rénale.
La nifédipine provoque une augmentation de la concentration plasmatique de metformine (augmentation de la Cmax de 20% et de l'AUC de 9 à 20%), due à une absorption accrue de la metformine.
La cimétidine provoque une augmentation de 60% de la Cmax et de 40% de l'AUC de la metformine. La demi-vie d'élimination de la metformine n'est pas influencée. D'autres agents actifs (amiloride, digoxine, morphine, procaïnamide, quinidine, quinine, ranitidine, triamtérène, triméthoprime ou vancomycine), qui sont éliminés par voie rénale par sécrétion tubulaire active, peuvent potentiellement avoir des interactions avec la metformine. Les patients traités par ces médicaments doivent par conséquent être surveillés consciencieusement lors d'une association avec la metformine.
Les IEC peuvent faire baisser la glycémie.
La glycémie peut aussi être réduite par les bêtabloquants. Cette interaction est beaucoup plus faible avec les bêtabloquants de type cardiosélectif (β1-sélectifs) qu'avec les bêtabloquants non cardiosélectifs.
L'administration concomitante d'inhibiteurs de la MAO et d'hypoglycémiants oraux peut améliorer la tolérance au glucose et renforcer les effets hypoglycémiants.
La consommation d'alcool pendant le traitement peut entraîner une augmentation des effets hypoglycémiants de la metformine pouvant aller jusqu'à un coma hypoglycémique.
Augmentation ou réduction des effets hypoglycémiants de la metformine
Les antagonistes H2, la clonidine et la réserpine peuvent renforcer ou affaiblir les effets de la metformine.
Des perturbations du contrôle de la glycémie (y compris hyperglycémie ou hypoglycémie) ont été observées lors d'une co-administration de metformine et de quinolones.
Interactions renforçant les effets indésirables de la metformine
Diurétiques: une acidose lactique peut survenir suite à un trouble de la fonction rénale dû aux diurétiques (en particulier aux diurétiques de l'anse). De plus, les diurétiques ont des effets hyperglycémiants.
Substances de contraste iodées: au sujet des interactions avec les substances de contraste iodées et du risque d'acidose lactique associé à ces substances, voir "Mises en garde et précautions" .
Alcool: lors d'une intoxication éthylique aiguë, les patients sous metformine ont un risque accru d'acidose lactique, surtout après avoir jeûné, en cas d'alimentation carencée ou d'insuffisance hépatique.
Interactions influençant les effets d'autres substances
La metformine provoque une réduction des taux plasmatiques de furosémide (réduction de la Cmax de 33% et de l'AUC de 12%) et la demi-vie terminale est réduite de 32% sans modification de la clairance rénale du furosémide.
Les effets de la phenprocoumone peuvent être réduits du fait de l'élimination accélérée de cette substance en présence de metformine.
Les études d'interactions avec le glibenclamide, la nifédipine, l'ibuprofène ou le propranolol n'ont révélé aucun effet cliniquement significatif sur les paramètres pharmacocinétiques de ces substances.
Autres interactions
Sous l'influence d'agents sympatholytiques (par exemple bêtabloquants, clonidine, guanéthidine, réserpine), la perception des signes annonçant une hypoglycémie peut être altérée.
Grossesse, allaitementGrossesse
Un diabète incontrôlé pendant la grossesse (dû à la grossesse ou préexistant) est associé à un risque accru de malformations congénitales et de mortalité périnatale.
On ne dispose que d'expériences limitées sur l'utilisation de Kombiglyze XR chez la femme enceinte. Des études expérimentales sur des animaux ont montré une toxicité pour la reproduction chez le rat ou le lapin à doses élevées de saxagliptine seule ou en association à la metformine. Des études expérimentales sur des animaux portant sur la metformine seule n'ont pas révélé d'indices de toxicité pour la reproduction (voir "Données précliniques" ).
Dans la mesure du possible, le taux de glycémie doit être stabilisé à des valeurs normales par l'insuline afin de réduire le risque de malformations chez le fœtus. Kombiglyze XR ne doit pas être utilisé pendant la grossesse, sauf indication absolue.
Allaitement
La metformine est excrétée dans le lait maternel.
On ignore si la saxagliptine passe dans le lait maternel. Des études expérimentales sur des animaux ont montré que la saxagliptine et/ou des métabolites passent dans le lait (voir "Données précliniques" ).
Les données limitées disponibles n'excluent pas le risque théorique d'hypoglycémies chez l'enfant allaité.
La décision d'arrêter Kombiglyze XR ou d'arrêter l'allaitement doit être prise en tenant compte du bénéfice du médicament pour la mère et du risque potentiel pour l'enfant.
Effet sur l’aptitude à la conduite et l’utilisation de machinesAucune étude n'a été effectuée sur les effets de Kombiglyze XR ou de la saxagliptine sur l'aptitude à la conduite et à la manipulation de machines. Cependant, en cas de participation à la circulation routière ou d'utilisation de machines, il faut tenir compte du fait que des vertiges ont été rapportés lors de la prise de saxagliptine.
Effets indésirablesAucune étude clinique n'a été effectuée sur les comprimés de Kombiglyze XR, mais la bioéquivalence de Kombiglyze XR avec la saxagliptine et la metformine à libération retardée co-administrées a été démontrée (voir "Pharmacocinétique" ).
Les effets indésirables observés dans les études cliniques sous l'association saxagliptine-metformine à libération non retardée sont indiqués ci-dessous.
Les effets indésirables décrits sont ceux qui ont été observés chez ≥5% des patients sous saxagliptine 5 mg et plus fréquemment que chez les patients traités par placebo, ou qui ont été rapportés chez ≥2% des patients sous saxagliptine 5 mg avec une différence de ≥1% par rapport au placebo.
La fréquence doit être indiquée comme suit: "très fréquents" (≥1/10), "fréquents" (≥1/100, <1/10), "occasionnels" (≥1/1000, <1/100), "rares" (≥1/10 000, <1/1000), "très rares" (<1/10 000), Cas isolés (fréquence non estimable sur la base des données disponibles).
Infections et infestations
Fréquents: infection respiratoire supérieure, sinusite, rhinopharyngite, infection des voies urinaires, gastro-entérite.
Affections du système nerveux
Fréquents: céphalées.
Affections gastro-intestinales
Fréquents: vomissements.
Metformine
Les effets indésirables proviennent d'études cliniques et de données post-commercialisation. Les fréquences reposent sur les indications fournies dans l'information professionnelle suisse de Glucophage.
Affections hématologiques et du système lymphatique
Cas isolés: leucopénie, de thrombopénie et d'anémie hémolytique.
Troubles du métabolisme et de la nutrition
Fréquents: diminution de la vitamine B12/carence en vitamine B12.
Très rares: acidose lactique (incidence de 3 cas sur 100 000 patients-années, cf. "Mises en garde et précautions" ).
Affections du système nerveux
Fréquents: altération du goût.
Affections gastro-intestinales
Fréquents à très fréquents: troubles gastro-intestinaux (5 à 15%) comme par exemple nausées, vomissements, diarrhées, douleurs abdominales, pertes d'appétit.
Ces symptômes se manifestent le plus souvent au début du traitement et régressent en général spontanément par la suite.
Affections hépatobiliaires
Cas isolés: valeurs anormales dans les examens de la fonction hépatique, p.ex. taux de transaminases accrus ou hépatite (réversibles après l'arrêt du traitement par metformine).
Affections de la peau et du tissu sous-cutané
Très rares: réactions cutanées telles qu'urticaire, érythème, prurit.
Informations supplémentaires concernant les effets indésirables
Description de certains effets indésirables
Outre les effets indésirables décrits ci-dessus, les effets indésirables suivants ont été rapportés – indépendamment du lien causal avec le médicament – plus souvent chez les patients sous saxagliptine que chez ceux sous placebo: hypersensibilité (0,6% vs 0%) et éruption cutanée (1,4% vs 1,0%).
Les effets indésirables dont l'investigateur a jugé du moins possible qu'ils soient dus au médicament et qui ont été observés chez au moins 2 patients de plus du groupe sous saxagliptine 5 mg que du groupe de contrôle sont indiqués ci-dessous par régime de traitement.
Monothérapie: vertiges (fréquent) et épuisement (fréquent).
Association avec la metformine: dyspepsie (fréquente) et myalgie (fréquente), gastrite (fréquente), arthralgie (occasionnelle), myalgie (occasionnelle) et dysfonction érectile (occasionnelle).
Hypoglycémie
Les effets indésirables hypoglycémiques étaient basés sur tous les rapports d'hypoglycémies sans exiger en même temps un dosage de la glycémie. L'incidence des hypoglycémies rapportées a été de 3,4% à 7,8% chez les patients sous saxagliptine 2,5 mg et 5 mg en plus de la metformine, et de 3,8% à 5% sous metformine seule.
Lorsqu'utilisé en traitement adjuvant associé avec de l'insuline, l'incidence globale des cas d'hypoglycémie rapportés était de 18,4% pour la saxagliptine 5 mg et de 19,9% pour le placebo.
Lorsqu'utilisé en traitement adjuvant associé avec une sulfonylurée, l'incidence globale des cas d'hypoglycémie rapportés était de 10,1% pour la saxagliptine 5 mg et de 6,3% pour le placebo.
Thrombocytopénie
Un cas de thrombocytopénie correspondant à un diagnostic de purpura thrombocytopénique idiopathique a été rapporté dans le cadre du programme d'études cliniques. On ignore quel est le rapport de cet événement avec la saxagliptine.
Réactions d'hypersensibilité
Des événements en rapport avec des réactions d'hypersensibilité telles qu'une urticaire ou un œdème facial ont été rapportés dans une analyse cumulative des données de 24 semaines, issues de 5 études sur la saxagliptine. Ils ont été rapportés chez 1,5% des patients sous saxagliptine 2,5 mg, 1,5% des patients sous saxagliptine 5 mg et 0,4% des patients sous placebo. Aucun de ces événements survenus chez les patients sous saxagliptine n'a exigé une hospitalisation et aucun n'a été rapporté par l'investigateur comme un événement menaçant le pronostic vital. Dans l'analyse cumulative, un patient traité par saxagliptine a quitté l'étude prématurément à cause d'une urticaire généralisée et d'un œdème facial.
Effets indésirables après commercialisation
Après l'autorisation de la saxagliptine, on a observé des cas de pancréatite aiguë et de réactions d'hypersensibilité sévères avec anaphylaxie, angio-œdème, éruption cutanée et urticaire.
Affections hépatobiliaires
Occasionnels: cholélithiase et cholécystite.
Résultats de l'étude SAVOR (détails voir ci-dessous): L'étude SAVOR a inclus 8240 patients traités par saxagliptine 5 mg ou 2,5 mg une fois par jour et 8173 patients recevant un placebo. L'incidence des événements indésirables sous saxagliptine et sous placebo était de 72,5% contre 72,2%.
Une pancréatite a été observée chez 0,3% des patients sous saxagliptine et sous placebo.
L'incidence des réactions d'hypersensibilité a été de 1,1% chez les patients traités par saxagliptine et chez ceux sous placebo.
17,1% des sujets traités par saxagliptine et 14,8% des patients sous placebo ont eu des épisodes d'hypoglycémie. Le pourcentage de sujets ayant présenté des épisodes d'hypoglycémie majeure (définie comme un événement nécessitant l'assistance d'une autre personne) a été de 2,1% sous saxagliptine contre 1,6% sous placebo. L'augmentation du risque d'hypoglycémie a principalement touché les sujets traités par une sulfonylurée à l'inclusion, et non les sujets recevant de l'insuline ou de la metformine en monothérapie à l'inclusion; elle a été observée principalement chez les sujets présentant à l'inclusion une HbA1C <7%.
Tuberculose
Dans la banque de données d'une étude clinique contrôlée ouverte sur la saxagliptine, 6 (0,12%) cas de tuberculose parmi les 4959 patients traités ont été annoncés (1,1 pour 1000 patients-années), alors qu'aucun cas n'était annoncé parmi les 2868 patients traités avec la médication de référence. Deux de ces six cas ont été confirmés par des examens de laboratoire appropriés. Dans les autres cas, on ne disposait que d'informations lacunaires ou il s'agissait de diagnostics suspectés. Aucun des six cas ne s'est produit aux États-Unis ou en Europe occidentale. Un cas est survenu au Canada chez un patient originaire d'Indonésie qui avait qui s'était rendu dans son pays d'origine peu de temps auparavant. La durée du traitement par la saxagliptine jusqu'à l'annonce de la tuberculose a varié de 144 à 929 jours. Dans quatre cas, le nombre de leucocytes était largement à l'intérieur du domaine de référence après le traitement. Un patient présentait avant le début du traitement par la saxagliptine une lymphopénie, qui est restée stable pendant toute la durée du traitement par la saxagliptine. Chez le dernier patient, il y a eu, environ quatre mois avant le rapport de tuberculose, à une reprise un nombre de lymphocytes en-dessous du domaine normal. Il n'y a pas eu d'annonces spontanées de tuberculose en rapport avec l'utilisation de saxagliptine. Le lien de causalité n'a pas pu être démontré et, en raison du petit nombre de cas, il n'est pas possible de juger si la tuberculose est en lien avec l'utilisation de saxagliptine.
Pemphigoïde bulleuse
Fréquence inconnue.
Rhabdomyolyse
Observation provenant de données après commercialisation. Fréquence inconnue.
Investigations
Saxagliptine
Nombre absolu de lymphocytes: sous saxagliptine, on a observé une réduction moyenne du nombre absolu de lymphocytes en fonction de la dose utilisée. Dans une analyse cumulative de 5 études cliniques contrôlées versus placebo, au bout de 24 semaines les nombres absolus moyens de lymphocytes (d'environ 2200 cellules/μl initialement) avaient diminué en moyenne d'environ 100 cellules/μl sous saxagliptine 5 mg et de 120 cellules par/μl sous saxagliptine 10 mg par rapport au placebo. Des effets similaires ont été observés par rapport à un traitement par metformine seule lorsque la saxagliptine 5 mg était administrée initialement en association avec la metformine. Aucune différence n'a été constatée entre la saxagliptine 2,5 mg et le placebo. Les pourcentages de patients avec un nombre de lymphocytes ≤750 cellules/μl étaient de 0,5% (saxagliptine 2,5 mg), de 1,5% (saxagliptine 5 mg), de 1,4% (saxagliptine 10 mg) et de 0,4% (placebo). Chez la majorité des patients, cet événement ne s'est plus produit par la suite après l'exposition répétée à la saxagliptine. Certains patients ont cependant présenté à nouveau des réductions après une nouvelle exposition, ce qui a conduit à l'arrêt du traitement par saxagliptine. Ces réductions du nombre de lymphocytes n'ont pas été accompagnées de réactions cliniquement significatives.
Dans le cadre de l'étude SAVOR, une diminution du taux de lymphocytes a été rapportée chez 0,5% des patients sous saxagliptine et chez 0,4% des patients sous placebo; 0,3% des patients sous saxagliptine et 0,2% des patients sous placebo avaient ≤0,5 x 109 cellules/l.
La signification clinique de ce nombre réduit de lymphocytes est inconnue. Dans le cas d'une infection sortant de l'ordinaire ou d'une infection persistante, il faut procéder à une numération des lymphocytes. On ignore quelle est l'influence de la saxagliptine sur le nombre de lymphocytes chez les patients présentant des anomalies lymphocytaires (dues par exemple au virus de l'immunodéficience humaine).
Metformine
Cas isolés: valeurs anormales dans les examens de la fonction hépatique, p.ex. taux de transaminases accrus ou hépatite (réversibles après l'arrêt du traitement par metformine).
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageOn ne dispose pas de données concernant un surdosage par Kombiglyze XR.
Saxagliptine
À des doses allant jusqu'à 400 mg par jour (80 fois la dose recommandée chez l'homme) sur une période de deux semaines, aucun effet significatif sur l'intervalle QTc ou la fréquence cardiaque n'a été constaté.
Dans le cas d'un surdosage, il faut initier un traitement de soutien approprié en fonction de l'état clinique du patient. La saxagliptine et son principal métabolite peuvent être éliminés du sang par hémodialyse (23% de la dose en l'espace de 4 heures).
Metformine
Un surdosage important de metformine ou la présence d'un risque concomitant peut entraîner le développement d'une acidose lactique. Celle-ci constitue une urgence médicale et doit être traitée à l'hôpital. Le lactate et la metformine sont hémodialysables.
Propriétés/EffetsCode ATC
A10BD10
Mécanisme d'action
Saxagliptine
La saxagliptine est un inhibiteur compétitif de la DPP-4. Chez les patients diabétiques de type 2, l'administration de saxagliptine a entraîné une inhibition de l'activité de l'enzyme DPP-4 pendant 24 heures. Après une charge orale de glucose, cette inhibition de la DPP-4 a provoqué une augmentation d'un facteur 2 à 3 des taux circulants d'hormones incrétines actives telles que le glucagon like peptid 1, GLP-1 et le polypeptide insulinotropique dépendant du glucose, GIP, une réduction des concentrations de glucagon et une augmentation de la sécrétion glucose-dépendante d'insuline. L'augmentation de la libération d'insuline par les cellules bêta pancréatiques et la diminution de la libération de glucagon par les cellules alpha pancréatiques ont été associées à une réduction de la glycémie à jeun et à une moindre augmentation de la glycémie après une charge orale de glucose ou un repas.
Metformine
La metformine est un biguanide aux effets hypoglycémiants qui agissent à la fois sur la glycémie de base et la glycémie postprandiale. La metformine ne stimule pas la libération d'insuline et ne provoque donc pas d'hypoglycémie en monothérapie.
La metformine peut déployer ses effets par trois mécanismes:
-Réduction de la production hépatique de glucose par une inhibition de la néoglucogenèse et de la glycogénolyse;
-Augmentation modérée de la sensibilité du tissu musculaire à l'insuline, entraînant une amélioration de l'absorption et de l'utilisation du glucose en périphérie;
-Ralentissement de l'absorption intestinale du glucose.
La metformine stimule la synthèse intracellulaire de glycogène par ses effets sur le glycogène synthétase. La metformine a augmenté la capacité de transport de certains types de transporteurs membranaires du glucose (GLUT-1 et GLUT-4).
Chez l'homme, la metformine a des effets bénéfiques sur le métabolisme des lipides indépendamment de ses effets hypoglycémiants. Cet effet a été démontré dans des études cliniques contrôlées de moyenne et de longue durée avec des doses thérapeutiques. La metformine réduit les taux de cholestérol total, de LDL-C et de triglycérides.
Pharmacodynamique
Voir aussi sous "Mécanisme d'action" .
Efficacité clinique
Il n'a pas été effectué d'études sur l'efficacité et la sécurité clinique de Kombiglyze XR dans lesquelles l'effet sur la baisse de l'hémoglobine A1c (HbA1C) ait été caractérisé. La bioéquivalence de Kombiglyze XR avec l'administration concomitante de saxagliptine et de chlorhydrate de metformine sous forme de comprimés à libération retardée est démontrée; des études sur la comparaison de la biodisponibilité relative entre Kombiglyze XR et la co-administration de saxagliptine et de comprimés de chlorhydrate de metformine à libération non retardée n'ont toutefois pas été réalisées. L'absorption de chlorhydrate de metformine à partir de comprimés à libération retardée et de comprimés à libération non retardée est comparable (AUC), tandis que les concentrations plasmatiques maximales après la prise de comprimés à libération retardée sont environ 20% plus basses qu'après la prise de la même dose sous forme de comprimés à libération non retardée du principe actif.
L'administration concomitante de saxagliptine et de comprimés de metformine à libération non retardée du principe actif a été étudiée chez des patients adultes atteints de diabète de type 2 dont le contrôle glycémique était insuffisant sous monothérapie de metformine, ainsi que chez des patients naïfs de traitement dont la glycémie était insuffisamment contrôlée par un régime et l'exercice physique seuls. Dans ces deux études, l'administration matinale de comprimés de saxagliptine plus metformine à libération non retardée a entraîné des améliorations cliniquement importantes et statistiquement significatives de la valeur de HbA1C, du glucose plasmatique à jeun (FPG, fasting plasma glucose) et de la valeur du glucose postprandial (PPG) 2 heures après un test standard de tolérance au glucose (OGTT). La baisse de la valeur de HbA1C a pu être classée en sous-groupes (notamment en fonction du sexe, de l'âge, de l'origine ethnique et de la valeur initiale du BMI).
Dans ces deux études, la réduction du poids corporel dans les groupes de traitement qui ont reçu la saxagliptine et la metformine à libération non retardée, a été comparable à celle observée dans les groupes sous monothérapie de metformine à libération non retardée. Par rapport à la monothérapie de metformine, le traitement de saxagliptine plus metformine à libération non retardée a été associée à des variations non significatives des lipides sériques à jeun.
L'administration concomitante de saxagliptine et de comprimés de metformine à libération non retardée a été en outre comparée, dans une étude avec contrôle actif, à la saxagliptine comme traitement adjuvant et au glipizide chez 858 patients dont le contrôle glycémique était insuffisant sous monothérapie de metformine, ainsi que dans une étude avec contrôle de placebo, dans laquelle un sous-groupe de 314 patients dont le contrôle glycémique était insuffisant sous insuline plus metformine a reçu un traitement adjuvant de saxagliptine ou de placebo.
Dans une étude randomisée, en double aveugle, de 24 semaines, des patients qui avaient reçu 500 mg deux fois par jour de metformine à libération non retardée pendant une période d'au moins 8 semaines, ont été traités avec soit 500 mg deux fois par jour de metformine à libération non retardée soit de la metformine à libération retardée (1000 mg une fois par jour ou 1500 mg une fois par jour). La variation moyenne de la valeur de HbA1C entre le début de l'étude et la semaine 24 a été de 0,1% (intervalle de confiance à 95%: 0%; 0,3%) sous metformine à libération non retardée, de 0,3% (intervalle de confiance à 95%: 0,1%; 0,4%) sous 1000 mg de metformine à libération retardée et de 0,1% (intervalle de confiance à 95%: 0%; 0,3%) sous 1500 mg de metformine à libération retardée. Les résultats de cette étude suggèrent que, chez les patients qui reçoivent la metformine à libération non retardée, il est possible de passer en toute sécurité à la metformine à libération retardée une fois par jour, à la même dose journalière (jusqu'à 2000 mg une fois par jour). Après un passage de la metformine à libération non retardée à la metformine à libération retardée, on surveillera étroitement le contrôle glycémique et on procèdera éventuellement à des ajustements appropriés de la dose.
Administration de la saxagliptine le matin et le soir
Une étude de monothérapie sur 24 semaines a été réalisée pour évaluer divers schémas posologiques de la saxagliptine. Des patients naïfs de traitement dont le diabète était insuffisamment contrôlé (HbA1C ≥7% à 10%) ont été inclus dans une phase de lead-in sous placebo de 2 semaines en simple aveugle, avec régime et exercice physique. Au total, 365 patients ont été ensuite randomisés pour recevoir soit la saxagliptine 2,5 mg une fois par jour le matin, avec augmentation possible à 5 mg une fois par jour le matin ou 5 mg une fois par jour le soir, soit un placebo. Les patients qui n'atteignaient pas certaines valeurs déterminées de glycémie pendant l'étude ont reçu, outre le placebo ou la saxagliptine, un traitement de secours de metformine; le nombre de patients dans les divers groupes de traitement se situait entre 71 et 74.
Le traitement avec la saxagliptine 5 mg une fois par jour le matin ou 5 mg une fois par jour le soir a entraîné des améliorations significatives de la valeur de HbA1C par rapport au placebo (baisse moyenne, corrigée pour le placebo, respectivement de -0,4 et -0,3%).
Administration additionnelle de saxagliptine à la metformine à libération non retardée
Un total de 743 patients atteints de diabète de type 2 ont participé à une étude de 24 semaines, randomisée, contrôlée par placebo, en double aveugle, qui a évalué l'efficacité et la sécurité de la saxagliptine associée à la metformine chez des patients dont le contrôle glycémique était insuffisant (HbA1C ≥7% à ≤10%) sous monothérapie de metformine. Pour pouvoir participer à l'étude, les patients devaient avoir reçu de la metformine à un dosage stable (1500 - 2550 mg par jour) pendant au moins 8 semaines.
Les patients qui remplissaient les critères d'inclusion ont été inclus dans une phase de lead-in sous placebo, en simple aveugle, de 2 semaines, avec régime et exercice physique, au cours de laquelle ils ont pris de la metformine au même dosage qu'avant l'étude (jusqu'à 2500 mg par jour); ce traitement de metformine a été poursuivi sur toute la durée de l'étude. À la suite de la phase de lead-in, les patients qui remplissaient les critères d'inclusion ont été randomisés pour recevoir 2,5 mg, 5 mg ou 10 mg de saxagliptine ou un placebo en plus du traitement de metformine à un dosage inchangé (la dose maximale autorisée recommandée de saxagliptine est de 5 mg par jour; la dose de 10 mg par jour ne manifeste pas une efficacité supérieure à celle de la dose de 5 mg). Les patients qui n'atteignaient pas certaines valeurs cibles de glycémie pendant l'étude ont reçu, outre leur traitement de l'étude, de la pioglitazone comme traitement de secours. Les augmentations progressives de la dose de saxagliptine et de metformine n'étaient pas autorisées.
La saxagliptine 2,5 mg ou 5 mg ajoutée à la metformine a entraîné des améliorations significatives de HbA1C, FPG et PPG par rapport au placebo ajouté à la metformine (Tableau 1). Les variations moyennes de la valeur de HbA1C en fonction du temps, par rapport aux valeurs du début de l'étude, sont illustrées dans la Figure 1. Le pourcentage de patients qui ont arrêté le traitement ou reçu un traitement de secours en raison d'un contrôle glycémique insuffisant s'est élevé à 15% dans le groupe recevant 2,5 mg de saxagliptine en complément de la metformine, à 13% dans le groupe recevant 5 mg de saxagliptine en complément de la metformine et à 27% dans le groupe recevant le placebo en complément de la metformine.
Tableau 1: Paramètres du contrôle glycémique (semaine 24) dans une étude contrôlée par placebo avec la saxagliptine comme traitement adjuvant de la metformine à libération non retardée*
Paramètre d'efficacité Saxagliptine 2,5 mg + Saxagliptine 5 mg + Placebo + metformine
metformineN = 192 metformineN = 191 N = 179
Hémoglobine HbA1C (%) N = 186 N = 186 N = 175
Début de l'étude (moyenne) 8,1 8,1 8,1
Variation par rapport au début −0,6 −0,7 +0,1
de l'étude (moyenne ajustée†)
Différence par rapport au −0,7‡ −0,8‡
placebo (moyenne ajustée†)
Intervalle de confiance à 95% (−0,9, −0,5) (−1,0, −0,6)
Pourcentage de patients qui 37%§ (69/186) 44%§ (81/186) 17% (29/175)
ont atteint une HbA1C <7%
Glucose plasmatique à jeun N = 188 N = 187 N = 176
(mg/dl/mmol/l)
Début de l'étude (moyenne) 174 / 9,66 179 / 9,93 175 / 9,71
Variation par rapport au début -14 / -0,78 -22 / -1,22 +1 / +0,06
de l'étude (moyenne ajustée†)
Différence par rapport au −16 / -0,89§ −23 / 1,28§
placebo (moyenne ajustée†)
Intervalle de confiance à 95% (−23, −9) / (-1,28, (−30, −16) / (-1,67,
-0,50) -0,89)
Glucose postprandial à N = 155 N = 155 N = 135
2h(mg/dl/mmol/l)
Début de l'étude (moyenne) 294 / 16,32 296 / 16,43 295 / 16,37
Variation par rapport au début −62 / -3,44 −58 / -3,22 −18 / -1,00
de l'étude (moyenne ajustée†)
Différence par rapport au −44 / - 2,44§ −40 / - 2,22§
placebo (moyenne ajustée†)
Intervalle de confiance à 95% (−60, −27) / (-3,33, (−56, −24) / (-3,11,
-1.50) -1,33)
* Population Intent-to-treat (avec utilisation de la dernière valeur obtenue pendant l'étude ou de la dernière valeur obtenue avant un traitement de secours à la pioglitazone).
† Moyenne des moindres carrés, ajustée pour la valeur initiale au début de l'étude.
‡ p <0,0001 par rapport au placebo + metformine
§ p <0,05 par rapport au placebo + metformine
Figure 1: Variation moyenne de la valeur de HbA1C dans une étude contrôlée par placebo avec la saxagliptine comme traitement adjuvant de la metformine à libération non retardée*
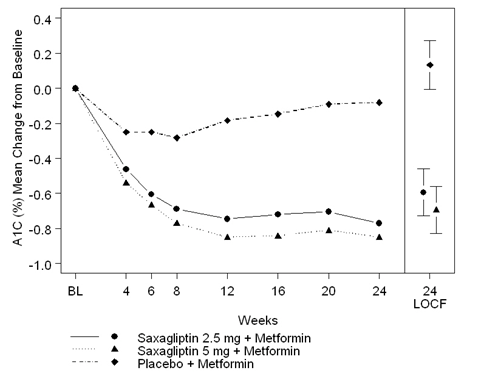
* Patients avec des valeurs aussi bien au début de l'étude qu'à la semaine 24.
Semaine 24 (LOCF) englobe la population Intent-to-treat avec utilisation de la dernière valeur obtenue avant un traitement de secours avec la pioglitazone. La variation moyenne par rapport au de l'étude est ajustée pour la valeur initiale.
La saxagliptine en traitement adjuvant de la metformine à libération non retardée versus le glipizide en traitement adjuvant de la metformine à libération non retardée
Dans cette étude de 52 semaines, contrôlée, randomisée, en double aveugle, 858 patients au total atteints de diabète de type 2 dont le contrôle glycémique était insuffisant (HbA1C >6,5% et ≤10%) ont été traités avec la saxagliptine ou le glipizide. Les patients devaient avoir reçu la metformine à une dose stable (au minimum 1500 mg par jour) depuis au moins 8 semaines avant leur inclusion dans l'étude.
Les patients qui remplissaient les critères d'inclusion ont été inclus dans une phase de lead-in sous placebo, en simple aveugle, de 2 semaines, avec régime et exercice physique, au cours de laquelle ils ont reçu de la metformine (1500 – 3000 mg, selon la dose utilisée avant l'étude). À la suite de la phase de lead-in, les patients ont été randomisés pour recevoir 5 mg de saxagliptine ou 5 mg de glipizide en complément de leur dose de metformine administrée de façon ouverte. Chez les patients du groupe sous glipizide plus metformine, un titrage en aveugle de la dose de glipizide a été effectué pendant les 18 premières semaines de l'étude, jusqu'à une dose maximale de 20 mg de glipizide par jour. Le titrage de la dose s'est fait jusqu'à l'obtention d'une valeur cible de FPG de ≤110 mg/dl / 6,11 mmol/l ou jusqu'à la plus haute dose tolérée de glipizide. Chez 50% des patients traités avec le glipizide, la dose a été augmentée à 20 mg par jour; à la fin du titrage de la dose, 21% des patients traités avec le glipizide recevaient une dose de glipizide de 5 mg ou moins par jour. En moyenne, la dose de glipizide après le titrage était de 15 mg.
Administrés en complément de la metformine, la saxagliptine et le glipizide ont induit au bout de 52 semaines de traitement une baisse moyenne comparable de HbA1C par rapport au début de l'étude (Tableau 2). Cette conclusion se limite probablement aux patients dont la valeur initiale de HbA1C se situe dans la zone des valeurs initiales décrites dans cette étude (91% des patients avaient une valeur de HbA1C <9% au début de l'étude).
Chez les patients traités avec la saxagliptine, on a constaté une perte pondérale moyenne significative de 1,1 kg par rapport au poids initial moyen de 89 kg mesuré au début de l'étude; en revanche, chez les patients traités au glipizide, une prise pondérale moyenne de 1,1 kg (p<0,0001) a été relevée.
Tableau 2: Paramètres du contrôle glycémique (semaine 52) dans une étude avec contrôle actif comparant la saxagliptine au glipizide associés à la metformine à libération non retardée *
Paramètre d'efficacité Saxagliptine 5 mg + Glipizide (titré) +
metformineN = 428 metformineN = 430
Hémoglobine HbA1C (%) N = 423 N = 423
Début de l'étude (moyenne) 7,7 7,6
Variation par rapport au début de l'étude −0,6 −0,7
(moyenne ajustée†)
Différence par rapport au glipizide + 0,1
metformine (moyenne ajustée†)
Intervalle de confiance à 95% (−0,02, 0,2)‡
Glucose plasmatique à jeun(mg/dl / mmol/l) N = 420 N = 420
Début de l'étude (moyenne) 162 / 8,99 161 / 8,94
Variation par rapport au début de l'étude −9 / -0,50 −16 / -0,89
(moyenne ajustée†)
Différence par rapport au glipizide + 6 / 0,33
metformine (moyenne ajustée†)
Intervalle de confiance à 95% (2, 11) / (0,11, 0,61)§
* Population Intent-to-treat (avec utilisation de la dernière valeur obtenue pendant l'étude ou de la dernière valeur obtenue avant un traitement de secours à la pioglitazone).
† Moyenne des moindres carrés, ajustée pour la valeur initiale au début de l'étude.
‡ Saxagliptine + metformine est considéré comme non inférieur à glipizide + metformine car la limite supérieure de cet intervalle de confiance se situe au-dessous de la limite préétablie de non infériorité de 0,35%.
§ Signification statistique non vérifiée.
Saxagliptine dans le traitement adjuvant associé avec de l'insuline
Un total de 455 patients atteints de diabète de type 2 et avec un contrôle insuffisant de la glycémie (HbA1C ≥7,5% et ≤11%) a participé à une étude randomisée de 24 semaines, en double aveugle, contrôlée versus placebo pour évaluer l'efficacité et la sécurité d'emploi de la saxagliptine 5 mg en association à une dose stable d'insuline (valeur de base moyenne: 54,2 unités/jour). Les patients étaient soit sous insuline seule (n=141) ou sous insuline associée à une dose stable de metformine (variation ≤20%) (libération rapide ou retardée) (n=314). La saxagliptine 5 mg était prise 1 fois par jour le matin. Comparativement au placebo, une amélioration significative des valeurs de l'HbA1C et de la glycémie postprandiale a été notée après 24 semaines. Par rapport au placebo, la réduction de l'HbA1C a été plus importante (env. 0,4%) chez les patients recevant de la saxagliptine en ajout à l'insuline, qu'ils utilisent de la metformine ou non. Cet effet s'est maintenu durant la phase d'extension de 28 semaines de cette étude. Durant les 24 premières semaines de l'étude, l'augmentation de la dose d'insuline requise a été plus faible chez les patients sous saxagliptine que chez ceux du groupe placebo (2 unités/jour versus 5 unités/jour). Une prise de poids minime a été enregistrée sur 24 semaines dans les deux bras de l'étude.
Saxagliptine dans le traitement adjuvant associé avec une sulfonylurée
Un total de 257 patients atteints de diabète de type 2 a participé à une étude randomisée de 24 semaines, en double aveugle, contrôlée versus placebo pour évaluer l'efficacité et la sécurité d'emploi de la saxagliptine en association à la metformine et à une sulfonylurée chez des patients avec un contrôle insuffisant de la glycémie (HbA1C ≥7% et ≤10%).
Associée à la metformine et à une sulfonylurée, la saxagliptine a entraîné une amélioration significative de l'HbA1C et du PPG comparativement au placebo associé à de la metformine et à une sulfonylurée. La modification de l'HbA1C pour la saxagliptine (n=127) comparée au placebo (n=128) était de -0,7% à la semaine 24.
Tableau 3: Principaux résultats des études d'efficacité contrôlées versus placebo d'associations avec la saxagliptine et la metformine
Début de l'étude Variation par Moyenne ajustée par
(moyenne) HbA1C (%) rapport au début de rapport au placebo
l'étude HbA1C (%) HbA1C (%) (IC 95%)
Etude de 24 semaines portant
sur le traitement adjuvant
associé avec de l'insuline
Saxagliptine 5 mg par 8,7 -0,7 -0,4 (-0,6, -0,2)1
jourEtude CV181057 (n=300)
Etude de 24 semaines portant
sur le traitement adjuvant
associé avec une sulfonylurée
Saxagliptine 5 mg par 8,4 -0,7 -0,7‡ (−0,9, −0,5)
jourEtude D180006 (n=257)
n=patients randomisés
1 p<0,0001 par rapport au placebo
‡ valeur de p <0,0001 par rapport au placebo + sulfonylurée
Etude SAVOR (Saxagliptin Assessment of Vascular Outcomes Recorded in Patients with Diabetes Mellitus-Thrombolysis in Myocardial Infarction)
L'étude SAVOR était une étude clinique contrôlée avec critères d'évaluation cardiovasculaires. 16 492 patients présentant une HbA1C ≥6,5% et <12% ont été traités. 12 959 d'entre eux présentaient un antécédent de maladie cardiovasculaire, 3533 avaient des facteurs de risque multiples pour une maladie cardiovasculaire. Les patients ont été randomisés pour recevoir la saxagliptine (n=8280) ou un placebo (n=8212), en complément des traitements antidiabétiques déjà en cours. 8561 patients étaient âgés de ≥65 ans, 2330 avaient ≥75 ans. 13 916 patients avaient une fonction rénale normale ou une altération légère de la fonction rénale, 2240 patients avaient une altération de la fonction rénale modérée et 336 une altération sévère.
Le critère d'évaluation principal (sécurité d'emploi et efficacité) était un paramètre composite regroupant les événements indésirables cardiovasculaires majeurs suivants (MACE: major adverse cardiovascular events): mortalité cardiovasculaire, infarctus du myocarde non fatal ou accident vasculaire cérébral ischémique non fatal. Le délai avant la survenue de l'un de ces événements a été analysé statistiquement (fonction de survie selon la méthode de Kaplan-Meier; modèle des risques proportionnels de Cox).
Après une durée moyenne de deux ans, l'étude a atteint son critère de sécurité d'emploi principal, démontrant ainsi que la saxagliptine en complément d'un traitement de fond en cours n'augmente pas le risque cardiovasculaire (MACE) chez des patients atteints de diabète de type 2 par rapport au placebo (HR 1,00; IC à 95%: [0,89; 1,12]; p=0,99 pour la supériorité; p<0,001 pour la non-infériorité).
Le critère d'efficacité principal n'a pas été atteint. La saxagliptine n'a conduit ni à une réduction ni à une augmentation du critère d'évaluation composite comprenant la mortalité pour causes cardiovasculaires, l'infarctus du myocarde et l'accident vasculaire cérébral.
Tableau 4: Critères d'évaluation clinique principaux et secondaires par groupe de traitement dans l'étude SAVOR**
(taux d'événements et pourcentages correspondent aux estimations selon Kaplan-Meier après 2 ans).
Critère d'évaluation Saxagliptine(N=8280) Placebo(N=8212) Hazard Ratio (IC
95%)†
Patients avec événementsn (%) Patients avec événementsn
(%)
Critère principal composite: 613(7,4) 609(7,4) 1,00(0,89;1,12)‡,§
MACE
Critère secondaire 1059(12,8) 1034(12,6) 1,02(0,94; 1,11)¶
composite: MACE plus&
Mortalité globale 420(5,1) 378(4,6) 1,11(0,96; 1,27)¶
* Population en intention de traiter (intent-to-treat-Population)
& MACE plus: mortalité cardiovasculaire, infarctus du myocarde non fatal, accident vasculaire cérébral ischémique non fatal, hospitalisation pour angine de poitrine instable, insuffisance cardiaque ou revascularisation coronaire.
† Hazard Ratio, ajusté selon la catégorie de fonction rénale initiale et la catégorie de risque de maladie cardiovasculaire.
‡ Valeur de p <0,001 pour la non-infériorité (basée sur un HR <1,3) par rapport au placebo.
§ Valeur de p = 0,99 pour la supériorité (basée sur un HR <1,0) par rapport au placebo.
¶ Signification statistique non testée.
Les hospitalisations pour insuffisance cardiaque sont survenues plus fréquemment dans le groupe saxagliptine (3,5%) par rapport au groupe placebo (2,8%) (HR = 1,27; [IC à 95%: 1,07, 1,51]). Aucun facteur clinique pertinent relié à l'augmentation du risque relatif d'insuffisance cardiaque sous saxagliptine n'a pu être identifié de manière certaine. Il n'y a pas eu d'augmentation du risque concernant les critères d'évaluation principaux et secondaires chez les patients avec antécédents d'insuffisance cardiaque par rapport au placebo.
** Saxagliptin and Cardiovascular Outcomes in Patients with Type 2 Diabetes Mellitus. Scirica B.M.et al. NEJM 2013;369:1317-26.
** The design and rationale of the Saxagliptin Assessment of Vascular Outcomes Recorded in Patients with Diabetes Mellitus- Thrombolysis in Myocardial Infarction (SAVOR-TIMI) 53 study. Scirica B.M.et al. Am Heart J 2011;162:818.e6-825.e6.
Sécurité et efficacité chez les patients âgés
Dans l'étude SAVOR, l'efficacité et la sécurité d'emploi dans les sous-groupes des tranches d'âge supérieures à 65 et à 75 ans ont été comparables à celles observées dans la population globale de l'étude.
PharmacocinétiqueLa bioéquivalence de Kombiglyze XR et l'effet de la prise d'aliments ont été étudiés après l'ingestion d'un repas pauvre en calories (324 kcal, 11,1% de protéines, 10,5% de graisses et 78,4% de glucides). Les résultats d'études de bioéquivalence menées chez des volontaires sains montrent que, lors d'une prise simultanée de nourriture, les comprimés de Kombiglyze XR sont bioéquivalents à la co-administration de doses correspondantes de saxagliptine et de chlorhydrate de metformine à libération retardée sous forme de comprimés séparés.
Saxagliptine
La pharmacocinétique de la saxagliptine et de son principal métabolite s'est révélée similaire chez les sujets sains et les diabétiques de type 2.
Absorption
La saxagliptine a été rapidement absorbée après administration orale à jeun, les concentrations plasmatiques maximales (Cmax) de saxagliptine et de son principal métabolite ont été atteintes en 2 et en 4 heures respectivement (Tmax). Les valeurs de la Cmax et de l'AUC de la saxagliptine et de son principal métabolite ont augmenté proportionnellement à l'augmentation de la dose de saxagliptine, et cette proportionnalité à la dose a été observée pour des doses allant de 2,5 mg à 400 mg. Après administration d'une dose orale unique de 5 mg de saxagliptine chez des sujets sains, les valeurs moyennes de l'AUC plasmatique de la saxagliptine et de son principal métabolite étaient de 78 ng•h/ml et de 214 ng•h/ml respectivement. Les valeurs correspondantes de la Cmax plasmatique ont été de 24 ng/ml et 47 ng/ml respectivement. Les coefficients de variation intra-individuelle pour la Cmax et l'AUC de la saxagliptine étaient inférieurs à 12%
Interactions avec les aliments: l'ingestion de nourriture a eu des effets relativement modestes sur la pharmacocinétique de la saxagliptine chez les sujets sains. Après administration en même temps que l'ingestion de nourriture (repas très riche en graisse), on n'a observé aucune modification de la Cmax de la saxagliptine, tandis que l'AUC était augmentée de 27% en comparaison avec l'administration à jeun. La prise avec un repas a prolongé d'environ 0,5 heure le temps nécessaire pour atteindre la Cmax de la saxagliptine (Tmax) par rapport à une administration à jeun. Ces modifications n'ont pas été considérées comme cliniquement significatives.
Distribution
La liaison in vitro de la saxagliptine et de son principal métabolite aux protéines du sérum humain est négligeable. En conséquence, des modifications des taux sanguins de protéines dans le cadre de certaines maladies (par exemple insuffisance rénale ou hépatique) ne devraient pas modifier la distribution de la saxagliptine.
Métabolisme
Biotransformation: la biotransformation de la saxagliptine est principalement médiée par le cytochrome P450 3A4/5 (CYP3A4/5). Les inhibiteurs et inducteurs puissants du CYP 3A4/5 influenceront par conséquent la pharmacocinétique de la saxagliptine et de son métabolite actif. Le principal métabolite de la saxagliptine est également un inhibiteur la DPP-4 présentant environ la moitié de la puissance de la saxagliptine.
Élimination
Les valeurs moyennes de demi-vie terminale (t½) plasmatique de la saxagliptine et de son principal métabolite sont de 2,5 heures et de 3,1 heures respectivement, et la valeur moyenne de t½ pour l'inhibition de la DPP-4 était de 26,9 heures. La saxagliptine est éliminée par voies rénale et hépatique. Après administration d'une dose unique de 50 mg de saxagliptine marquée au 14C, 24% de la dose ont été retrouvés dans l'urine sous forme de saxagliptine, 36% sous la forme de son principal métabolite et 75% sous la forme de radioactivité totale. La clairance rénale moyenne de la saxagliptine (~230 ml/min) était supérieure au taux moyen de filtration glomérulaire estimé (~120 ml/min), ce qui indique une certaine excrétion rénale active. Pour le métabolite principal, les valeurs de clairance rénale étaient comparables au taux de filtration glomérulaire estimé. Au total, 22% de la radioactivité administrée ont été retrouvés dans les selles, ce qui correspond à la fraction de la dose de saxagliptine excrétée dans la bile et/ou à la part non absorbée du médicament dans l'appareil digestif.
Linéarité
La Cmax et l'AUC de la saxagliptine et de son métabolite principal augmentaient de manière proportionnelle à la dose de saxagliptine. Il n'a pas été observé d'accumulation notable de saxagliptine ni de son métabolite principal lors d'une administration quotidienne répétée. Lors d'une administration quotidienne de saxagliptine à des doses comprises entre 2,5 mg et 400 mg pendant 14 jours, aucune dépendance à la dose ou au temps n'a été constatée pour la clairance de la saxagliptine et de son métabolite principal.
Cinétique pour certains groupes de patients
Troubles de la fonction rénale
La pharmacocinétique de la saxagliptine a été examinée dans une étude ouverte avec une dose unique de 10 mg chez des patients présentant une insuffisance rénale chronique de divers degrés par comparaison avec des volontaires présentant une fonction rénale normale.
Le degré de l'insuffisance rénale n'a pas influencé la Cmax de la saxagliptine ni de son métabolite principal.
Chez les volontaires présentant une ClCr 50 ml/min (correspondant à un TFGe de ≥45 ml/min/1,73 m2 selon l'équation du TFGe par MDRD), les valeurs ASC de la saxagliptine et de son métabolite principal étaient multipliées par un facteur 1,2, resp. 1,7 par rapport aux volontaires présentant une fonction rénale normale. Étant donné que les augmentations de cet ordre ne sont pas pertinentes sur le plan clinique, un ajustement de la dose n'est pas recommandé chez ces patients.
Chez les volontaires atteints d'insuffisance rénale avec une ClCr de ≤50 ml/min (correspondant à un TFGe de <45 ml/min/1,73 m2) ainsi que chez les patients atteints d'insuffisance rénale en phase terminale (ESRD) soumis à la dialyse, les valeurs ASC de la saxagliptine et de son métabolite principal étaient multipliées par un facteur 2,1, resp. 4,5 par rapport aux volontaires présentant une fonction rénale normale. Chez ces patients, la dose est de 2,5 mg une fois par jour (voir "Posologie/Mode d'emploi" et "Mises en garde et précautions" ).
Troubles de la fonction hépatique
Chez les sujets présentant une insuffisance hépatique légère (classe Child-Pugh A), modérée (classe Child-Pugh B) ou sévère (classe Child-Pugh C), les expositions à la saxagliptine étaient supérieures de 10%, 40% et 80% respectivement à celles observées chez les sujets sains, et l'exposition au BMS-510849 était réduite de 22%, 7% et 33%.
Sexe
Une adaptation de la dose en raison du sexe n'est pas recommandée. Aucune différence en termes de pharmacocinétique de la saxagliptine n'a été observée entre les hommes et les femmes. En comparaison avec les hommes, les femmes ont présenté une exposition au métabolite actif plus élevée d'environ 25% mais cette différence ne devrait toutefois pas revêtir une importance clinique. Dans l'analyse pharmacocinétique de population, le sexe ne s'est pas révélé être une covariable significative de la clairance apparente de la saxagliptine et de son métabolite actif.
Patients âgés
Les patients âgés (65 à 80 ans) ont une AUC de 60% supérieure à celle des patients plus jeunes (18 à 40 ans). Ceci n'est pas jugé cliniquement significatif. C'est pourquoi aucune adaptation de la dose de Kombiglyze XR n'est recommandée du fait de l'âge uniquement.
Enfants et adolescents
Il n'existe aucune étude sur la pharmacocinétique de la saxagliptine chez les enfants et adolescents de moins de 18 ans.
Body Mass Index
Une adaptation de la dose sur la base du Body Mass Index (BMI) n'est pas recommandée car, dans l'analyse pharmacocinétique de population, le BMI ne s'est pas révélé être une covariable significative de la clairance apparente de la saxagliptine et de son métabolite actif.
Origine ethnique
Une adaptation de la dose sur la base de l'origine ethnique n'est pas recommandée. Dans l'analyse pharmacocinétique de population, la pharmacocinétique de la saxagliptine et de son métabolite actif a été comparée chez 309 volontaires caucasiens et 105 volontaires non caucasiens (six différentes origines ethniques). Aucune différence significative en termes de pharmacocinétique de la saxagliptine et de son métabolite actif n'a été constatée entre ces deux populations.
Metformine
Absorption
Après administration d'une dose orale unique de metformine à libération retardée, la Cmax est atteinte en l'espace de 7 heures (médiane), avec une fourchette allant de 4 à 8 heures. Bien que l'importance de l'absorption (sur la base de l'AUC) de la metformine à partir de comprimés de metformine à libération retardée ait augmenté d'environ 50% lors d'une ingestion simultanée de nourriture, la prise de nourriture n'a pas eu de répercussions sur la Cmax ou la Tmax de la metformine. Des repas riches en graisses et pauvres en graisses ont eu le même effet sur la pharmacocinétique de la metformine à libération retardée. La prise de nourriture n'exerce pas de répercussions significatives sur la pharmacocinétique de la metformine lorsque cette dernière est administrée sous la forme de comprimés d'association Kombiglyze XR.
Distribution
Aucune étude n'a été réalisée sur la distribution de la metformine à libération retardée; le volume de distribution apparent (V/F) de la metformine après une administration orale unique de 850 mg de metformine à libération non retardée s'est élevé en moyenne à 654 ± 358 l. La metformine se lie en quantité négligeable aux protéines plasmatiques, contrairement aux sulfonylurées, dont la liaison aux protéines dépasse 90%. La metformine se distribue probablement, en fonction du temps, dans les érythrocytes. Comme la liaison de la metformine aux protéines est négligeable, des interactions avec des principes actifs fortement liés aux protéines tels que les salicylates, les sulfonamides, le chloramphénicol et le probénécide sont moins probables que dans le cas des sulfonylurées, qui se lient dans une forte proportion aux protéines sériques.
Métabolisme
Des études portant sur une administration veineuse unique à des volontaires en bonne santé montrent que la metformine est éliminée sous forme inchangée dans l'urine et ne subit ni un métabolisme hépatique (aucun métabolite n'a été trouvé chez l'homme) ni une excrétion biliaire.
Aucune étude sur le métabolisme de comprimés de metformine à libération retardée n'a été réalisée.
Élimination
La clairance rénale est environ 3,5 fois plus élevée que la clairance de la créatinine, ce qui suggère que la sécrétion tubulaire représente la voie principale d'élimination de la metformine. Après administration orale, environ 90% du principe actif absorbé sont éliminés par voie rénale en l'espace des 24 premières heures, avec une demi-vie d'élimination plasmatique de 6,2 heures environ. Dans le sang, la demi-vie d'élimination est d'environ 17,6 heures, ce qui fait supposer que la masse des érythrocytes constitue probablement un compartiment de distribution.
Cinétique pour certains groupes de patients
Troubles de la fonction rénale
Chez les patients souffrant d'insuffisance rénale (sur la base de la mesure de la clairance de la créatinine), la demi-vie de la metformine dans le plasma et le sang est allongée et la clairance rénale est réduite proportionnellement à la diminution de la clairance de la créatinine. L'utilisation de metformine chez des patients atteints d'insuffisance rénale augmente le risque d'acidose lactique. Comme Kombiglyze XR contient de la metformine, il est contre-indiqué chez les patients qui présentent une insuffisance rénale (TFGe de <30 ml/min/1,73 m2) (voir "Contre-indications" et "Mises en garde et précautions" ).
Troubles de la fonction hépatique
Aucune étude pharmacocinétique n'a été réalisée avec la metformine chez des patients atteints d'insuffisance hépatique. L'utilisation de metformine chez des patients atteints d'insuffisance hépatique a été associée dans quelques cas à une acidose lactique. Comme Kombiglyze XR contient de la metformine, il est contre-indiqué chez les patients qui présentent une insuffisance hépatique (voir "Contre-indications" et "Mises en garde et précautions" )
Sexe
Chez des volontaires sains et chez des patients atteints de diabète de type 2, les paramètres pharmacocinétiques de la metformine n'ont pas présenté de différences significatives liées au sexe (hommes = 19, femmes = 16). De même, l'effet anti-hyperglycémiant de la metformine a été comparable entre les hommes et les femmes dans des études cliniques contrôlées menées auprès de patients atteints de diabète de type 2.
Patients âgés
Des données limitées issues d'études pharmacocinétiques réalisées avec la metformine chez des volontaires âgés en bonne santé suggèrent que la clairance plasmatique globale de la metformine est diminuée par rapport à celle de volontaires jeunes en bonne santé, que la demi-vie est allongée et que la Cmax est augmentée. Ces données font supposer que la variation de la pharmacocinétique de la metformine avec l'âge est imputable avant tout à une modification de la fonction rénale.
Indépendamment de l'âge du patient, Kombiglyze XR ne sera administré qu'après qu'une mesure de la clairance de la créatinine aura montré que la fonction rénale est normale (voir "Mises en garde et précautions" ).
Enfants et adolescents
La sécurité et l'efficacité de Kombiglyze XR n'ont pas été démontrées chez l'enfant et l'adolescent.
Origine ethnique
Aucune étude pharmacocinétique avec la metformine n'a été réalisée à ce sujet. Dans des études cliniques contrôlées effectuées avec la metformine chez des patients atteints de diabète de type 2, l'effet antihyperglycémiant a été comparable chez des patients caucasiens (n = 249) et afro-américains (n = 51) ainsi que chez des patients d'origine hispanique (n = 24).
Données précliniquesCo-administration de saxagliptine et de metformine
Toxicité à long terme (ou toxicité en cas d'administration répétée)
Une étude de 3 mois sur des chiens a examiné les effets de la saxagliptine et de la metformine à des expositions (AUC) 68 et 1,5 fois supérieures à la dose maximale recommandée chez l'homme (MRHD). Aucune toxicité n'a été constatée.
Développement embryofœtal
La co-administration orale de saxagliptine et de metformine à des rates et à des lapines gravides à des doses de saxagliptine/metformine allant jusqu'à 25/600 mg/kg (rates) et 40/50 mg/kg (lapines) - produisant chez le rat des expositions systémiques (AUC) 100 et 10 fois supérieures respectivement à la dose maximale recommandée chez l'homme (la dose recommandée étant 5 mg de saxagliptine et 2000 mg de metformine) et, chez le lapin, des expositions 249 fois et 1,1 fois supérieures à la dose recommandée chez l'homme - n'a pas conduit chez l'une ou l'autre espèce à des effets embryolétaux ou tératogènes au cours de la phase d'organogenèse.
Des défauts congénitaux de la fermeture du tube neural ont été observés chez 2 fœtus de rats d'une mère. Ce constat n'a pas pu être reproduit avec des doses plus élevées.
Chez le rat, la toxicité mineure observée sur le développement s'est limitée à une survenue accrue de retards de l'ossification ( "côtes ondulées" ); la toxicité maternelle associée s'est limitée à des pertes de poids de 5 à 6% entre les jours 13 et 18 de la gestation et à des réductions de la prise alimentaire des mères. Chez le lapin, la co-administration a été mal tolérée par de nombreuses mères, avec mortalité, états moribonds et avortements. Toutefois, parmi les mères ayant survécu avec des portées évaluables, la toxicité maternelle s'est limitée à des réductions marginales du poids corporel entre les jours 21 et 29 de la gestation; et la toxicité sur le développement observée chez ces portées s'est limitée à des diminutions du poids corporel fœtal de 7% et à une faible incidence de retard de l'ossification au niveau de l'os hyoïde des fœtus.
Saxagliptine
Toxicité à long terme (ou toxicité en cas d'administration répétée)
Chez des singes cynomolgus, la saxagliptine a produit des lésions cutanées (croûtes, ulcérations et nécroses) au niveau des extrémités (queue, doigts, scrotum et/ou nez) à des doses ≥3 mg/kg/jour. Ces lésions étaient réversibles sous une dose ≤3 mg/kg/jour (correspondant environ à ≥7 fois l'exposition de l'être humain après utilisation de la dose recommandée de 5 mg par jour). Aux doses plus élevées, les lésions cutanées étaient irréversibles et nécrosantes).
La dose NOEL (no-effect-level, dose associée à l'absence d'effet) pour les lésions correspond à 1 et à 2 fois l'exposition humaine à la saxagliptine et à son métabolite principal avec la dose thérapeutique recommandée de 5 mg/jour.
La signification clinique des lésions cutanées n'est pas connue. Aucune manifestation cutanée correspondant à ces lésions chez le singe n'a été observée dans le cadre des études cliniques humaines.
Des constats immunologiques – d'hyperplasie lymphoïde non progressive minimale au niveau de la rate, de ganglions lymphatiques et de la moelle osseuse sans aucune séquelle – ont été faits chez toutes les espèces testées à des expositions correspondant à ≥7 fois la dose recommandée chez l'homme.
Les résultats des études précliniques font supposer que la saxagliptine présente un potentiel d'allergie de contact lors d'une utilisation par application sur la peau.
Chez le chien, la saxagliptine à doses élevées a causé une toxicité gastro-intestinale incluant des selles sanguinolentes/mucoïdes et une entéropathie. La dose NOEL (dose avec une absence d'effet) correspondait à une exposition à la saxagliptine et à son métabolite principal 4 fois et 2 fois supérieure respectivement à celle recommandée chez l'homme.
Mutagénicité et cancérogénicité
Dans une série d'études de génotoxicité conventionnelles in vitro et in vivo, la saxagliptine n'a présenté aucune génotoxicité. Dans des expérimentations de deux ans sur des souris et des rats examinant la cancérogénicité, aucun potentiel cancérogène n'a été observé.
Toxicologie sur la reproduction
Des effets sur la fertilité ont été observés chez des rats mâles et des rats femelles à des doses élevées produisant clairement des signes de toxicité. La saxagliptine n'a pas montré d'effet tératogène aux doses auxquelles elle a été évaluée chez le rat et le lapin. À des doses élevées chez le rat, la saxagliptine a entraîné un retard de l'ossification (retard de développement) du pelvis fœtal et une diminution du poids corporel du fœtus (en présence d'une toxicité maternelle), avec une exposition NOEL (sans effet) respectivement 303 fois et 30 fois supérieure à l'exposition humaine à la saxagliptine et à son métabolite principal à la dose recommandée chez l'homme. Chez le lapin, les effets de la saxagliptine se sont limités à des variations mineures du squelette observées uniquement à des doses toxiques pour la mère (avec une dose NOEL [dose sans effet] correspondant respectivement à 158 et à 224 fois l'exposition humaine à la saxagliptine et à son métabolite principal à la dose thérapeutique recommandée). Dans une étude sur le développement pré et postnatal chez le rat, la saxagliptine a causé des diminutions du poids de la progéniture à des doses toxiques pour la mère, avec une dose NOEL (dose sans effet) correspondant respectivement à 488 fois et à 45 fois l'exposition humaine à la saxagliptine et à son métabolite principal à la dose thérapeutique recommandée. Les effets sur le poids corporel de la progéniture ont été observés jusqu'au jour 92 après la naissance chez les femelles et jusqu'au jour 120 après la naissance chez les mâles.
Des études expérimentales sur des animaux ont montré que la saxagliptine et/ou son métabolite passent dans le lait.
Metformine
Les données précliniques sur la metformine – issues d'études conventionnelles de pharmacologie de sécurité, de toxicité en administration répétée, de toxicité de la reproduction et du développement, de génotoxicité et de cancérogénicité – n'ont pas révélé de risque particulier pour l'homme.
Remarques particulièresStabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention "EXP" sur le récipient.
Remarques particulières concernant le stockage
Ne pas conserver au-dessus de 30°C.
Conserver hors de la portée des enfants.
Numéro d’autorisation62598 (Swissmedic).
PrésentationComprimés pelliculés de 2,5/1000 mg: 56 et 196 comprimés. [B]
Comprimés pelliculés de 5/500 mg: 28 et 98 comprimés. [B]
Comprimés pelliculés de 5/1000 mg: 28 et 98 comprimés. [B]
Titulaire de l’autorisationAstraZeneca AG, 6340 Baar.
Mise à jour de l’informationSeptembre 2023
|

